常用磷酸钙盐峰值
城镇污水处理厂低浓度进水原因分析及提升措施

城镇污水处理厂低浓度进水原因分析及提升措施摘要:城镇污水处理厂是重要的市政基础设施,城镇污水处理也是水污染防治的关键环节。
对污水处理厂配套管网的调查、病害检测,同时全面系统地掌握和摸清配套管网的建设运行情况及质量状况,这将有利于系统治理、精准施策。
提出了完善排水管理体制机制、工业企业排水实行三管分设整改、细化管网渗漏的检测排查和有效修复、加强管网验收和质量监管、尽量降低管网水位等4项整治措施。
关键词:城镇;污水处理厂;低浓度;进水引言我国城市污水处理厂进水水量组成不仅有原生污水和工业废水,还有地下水、河水以及雨水等外来水。
采用水量平衡三角法、水量平衡三角法对城镇污水处理厂进水中地下水、河水及雨水混入比例进行了研究,提高城市污水处理厂进水水质浓度的首要前提是解析进水水量的组成情况,这一前提步骤直接关系到污水处理厂进水低COD或BOD问题原因的发现,对后续提出水质提升措施和解决排水系5统存在的问题至关重要。
1降雨对进水污染物浓度的影响1.1降雨对进水流量和pH的影响从最近4年每月的降雨频次可知,降雨在全年1月—12月均有分布。
从最近4年不同降雨量降雨的频次分布分析,降雨以累计降水量在1~10mm的小到中雨为主,占总降雨频次的85%。
降水量为6mm的典型中雨降水过程中,污水处理厂接收雨水后中线进水流量的变化曲线。
由于降雨影响,中线进厂水流量迅速上升,在5h后达到峰值,峰值流量为25.2m3/s,随后逐渐降低,并在22h后逐渐恢复正常流量。
雨水径流中含有的碳酸盐、硫酸盐、氮氧化物等酸性物质进入污水处理厂后,进厂污水的pH迅速下降,并在10h后达到最低值(6.15)。
因此,降雨对污水处理厂进厂水量和进水pH都会造成较大影响。
1.2降雨对进水COD浓度的影响进水CODCr浓度接收雨水后的0~3h和7~10h出现两个峰值,峰值CODCr浓度分别为280mg/L和277mg/L。
表明在降雨过程中,一些小分子的有机污染物如乙醇等,由于在雨水中的溶解度高,溶解于雨水后随雨水径流进入城镇污水处理系统,从而体现为污水处理厂进水COD浓度曲线上的第一个峰值。
【可编辑全文】磷化工概论—2

第三节磷酸钙盐磷酸钙盐是磷酸盐系列的重要品种,在磷酸盐工业中占有越来越来大的比列,估计在2000年生产的磷酸钙盐占无机磷酸盐的31%。
全世界1989年磷酸钙盐消费量达180万吨P2O5,我国磷酸钙盐1989年生产能力达13.49万吨(实物量),主要发展品种是饲料磷酸氢钙与脱氟磷酸钙。
一、磷酸钙盐品种和性质1、磷酸二氢钙磷酸二氢钙C a(H2PO4)2是无色或白色三斜晶体。
有一水合物和无水物两种形式。
溶于酸和水,水解时产生磷酸呈酸性(pH值为3)。
不溶于乙醇。
纯品无潮解性。
一水合物C a(H2PO4)2·H2O相对密度2.22,在1090C失去结晶水;在2030C时分解成偏磷酸盐。
C a(H2PO4)2·H2O 1090C C a(H2PO4)2 + H2OC a(H2PO4)2 2030C C a3(PO4)2 + 2H2O2、磷酸氢钙磷酸氢钙C a HPO4是白色单斜晶体。
有二水合物和无水物两种,常用的是二水合物C a HPO4·2H2O。
相对密度2.306。
稍溶于水(0.02%250C)。
溶于稀盐酸、硝酸、醋酸,不溶于乙醇。
在空气中稳定。
二水合物在115~1200C时失去两个结晶水。
加热至4000C以上时形成焦磷酸钙。
3、磷酸三钙磷酸三钙C a3(PO4)2是白色晶体或无定形粉末,无臭无味。
相对密度3.18。
熔点16700C易溶于稀盐酸和硝酸,不溶于乙醇,几乎不溶于水(0.0025g/100ml)。
已知磷酸三钙有β型(在11800C以下稳定,属三方斜晶系),α型(在1180~14300C稳定,属单斜晶系),及γ型(在14300C以上稳定)。
4、碱式磷酸钙(又称羟基磷灰石HAP)碱式磷酸钙C a10(PO4)6(OH)2,相对密度3.1~3.2。
干法反应时根据煅烧条件可分为致密物和多孔物。
致密物是半透明、乳白色;多孔物是白色的,具有一种隧道式结构,沿轴向易发生离子移动,易被多— 52 —种离子置换。
食品营养强化剂 甘油磷酸钙标准2023年

食品营养强化剂甘油磷酸钙1 范围本标准适用于以甘油磷酸和氢氧化钙或碳酸钙中和而得的食品营养强化剂甘油磷酸钙。
2 化学名称、分子式、结构式和相对分子质量2. 1 化学名称甘油磷酸钙2. 2 分子式C3H7Cao6P2. 3 结构式2. 4 相对分子质量210. 14(按2018年国际相对原子质量)3 技术要求3. 1 感官要求感官要求应符合表1的规定。
表1 感官要求3. 2 理化指标理化指标应符合表2的规定。
1表2 理化指标2附录A检验方法A. 1 一般规定本标准所用试剂和水在没有注明其他要求时,均指分析纯试剂和GB/T6682规定的三级水。
试验中所用标准溶液、杂质测定用标准溶液、制剂和制品,在没有注明其他要求时均按GB/T 601、GB/T602、GB/T603的规定制备。
试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。
A. 2 鉴别试验A. 2. 1 试剂和材料A. 2. 1. 1 硝酸。
A. 2. 1. 2 钥酸。
A. 2. 1. 3 氨水。
A. 2. 1. 4 盐酸溶液:3. 65g/L。
A. 2. 1. 5 稀硝酸溶液:吸取 105mL硝酸(A. 2. 1. 1),加水稀释至 1000mL。
A. 2. 1. 6 钥酸锁溶液:称取6. 5g钥酸(A. 2. 1. 2),加14mL水与14. 5mL氨水(A. 2. 1. 3),振摇使溶解,冷却,边搅拌边缓缓加入已冷却的32 mL稀硝酸溶液(A. 2. 1. 5)和40 mL水的混合液中,静置48h,过滤,取滤液。
A. 2. 2 仪器和设备A. 2. 2. 1 天平:感量为 0. 001g 。
A. 2. 2. 2 钳丝:1根。
A. 2. 3 鉴别方法A. 2. 3. 1 溶解性试验称取试样约1. 0g,加入三5节水10mL溶解,煮沸,有白色晶体析出。
A. 2. 3. 2 钥酸较鉴别称取0. 1g(精确至0. 001g)试样,用水和稀硝酸溶液(A. 2. 1. 5)各10mL溶解后,再加入钥酸锁溶液(A. 2. 1. 6)5mL,煮沸,即产生黄色沉淀。
磷酸盐

1基本简介磷酸盐(phosphorous salts)是几乎所有食物的天然成分之一,作为重要的食品配料和功能添加剂被广泛用于食品加工中。
天然存在的磷酸盐是磷矿石(含磷酸钙),用硫酸跟磷矿石反应,生成能被植物吸收的磷酸二氢钙和硫酸钙,可制得磷酸盐。
磷酸盐可分为正磷酸盐和缩聚磷酸盐:在食品加工中使用的磷酸盐通常为钠盐、钙盐、钾盐以及作为营养强化剂的铁盐和锌盐,常用的食品级磷酸盐的品种有三十多种,磷酸钠盐是国内食品磷酸盐的主要消费种类,随着食品加工技术的发展,磷酸钾盐的消费量也在逐年上升。
2化学特性在酸性溶液下磷酸官能团的结构式。
在碱性的溶液下,该官能团会释放两个氢原子,并离化磷酸盐带有-2的形式电荷。
[1]磷酸盐离子是一个多原子的离子,其实验式是PO43−,而分子量是94.97。
它包含一个磷原子,并由四个氧原子所包围,形成一个正四面体。
磷酸盐离子带有-3的形式电荷,且是磷酸氢盐离子(HPO42−)的共轭碱;磷酸氢盐离子则是磷酸二氢盐离子(H2PO4−)的共轭碱;而磷酸二氢盐离子又是磷酸(H3PO4)的共轭碱。
它是一个超价分子(磷原子在其价壳层有着10个电子)。
磷酸盐亦是一个有机磷化合物,其化学式为OP(OR)3。
除了一些碱金属外,大部份磷酸盐,在标准状态下,都是不可溶于水的。
在稀释的水溶液中,磷酸盐以四种形式存在。
在强碱环境下,磷酸盐离子(PO43−)会较多;而在弱碱的环境下,磷酸氢盐离子(HPO42−)则较多。
在弱酸的环境下,磷酸二氢盐离子(H2PO4−)较为普遍;而在强酸的环境下,则水溶的磷酸(H3PO4)是主要存在的形式。
3基本形式磷酸盐是元素磷自然产生的形态,在多种磷酸盐矿物中可以找到。
元素的磷或是磷化物是很难发现的(只有极少量在陨石中可以找到)。
在矿物学及地质学,磷酸盐是指含有磷酸盐离子的石或矿石。
在北美洲最大型的磷矿粉矿床位于美国的佛罗里达州中部、爱德荷州的索达斯普陵、北卡罗莱那州沿岸区域。
磷酸钙沉淀ph值

磷酸钙沉淀ph值全文共四篇示例,供读者参考第一篇示例:磷酸钙沉淀ph值是指当磷酸钙在水中发生沉淀反应时,溶液的PH值的变化规律。
磷酸钙是一种常见的无机盐,在很多领域都有广泛的应用,比如食品添加剂、医药制剂、建筑材料等。
磷酸钙在水中会发生不同程度的溶解和沉淀,其中的PH值对其沉淀行为起着重要的影响。
磷酸钙的化学式为Ca3(PO4)2,它具有很强的不溶性。
当磷酸钙溶解在水中时,会形成磷酸根离子(PO43-)和钙离子(Ca2+),这些离子在水溶液中的浓度会影响磷酸钙的溶解度和沉淀行为。
磷酸钙的溶解度与PH值之间存在着一定的关系,通常来说,PH值越高,磷酸钙的溶解度就越低。
当PH值适中时,磷酸钙的溶解度会达到最佳值。
一般来说,PH 值在6-7之间时,磷酸钙的溶解度较高,此时磷酸钙在水中呈现较好的稳定性。
而当PH值偏高或偏低时,磷酸钙的溶解度都会降低,容易发生沉淀反应。
磷酸钙沉淀ph值的具体变化规律取决于水质中其他溶质的种类和浓度。
当水质中存在碱性物质时,PH值会升高,磷酸钙的溶解度会降低,从而促进磷酸钙的沉淀。
而当水质中存在酸性物质时,PH值会降低,磷酸钙的溶解度会增加,从而减少磷酸钙的沉淀。
正确控制水质的PH值是磷酸钙在水中溶解和沉淀的关键。
磷酸钙在实际应用中有很多种不同的形式,比如磷酸钙粉、磷酸钙结晶、磷酸钙颗粒等。
不同形式的磷酸钙在水中的沉淀ph值也会有所差异。
一般来说,磷酸钙粉的PH值较低,容易形成沉淀,而磷酸钙颗粒的PH值相对较高,不容易发生沉淀。
在选择和应用磷酸钙时,需要根据具体情况来合理调节PH值,以获得最佳的效果。
磷酸钙沉淀ph值的研究在很多领域都有着重要的应用价值。
比如在食品工业中,磷酸钙常被用作食品添加剂,调节食品的硬度和口感。
在制药工业中,磷酸钙被用于制备钙片、钙粉等药品。
在环境保护领域,磷酸钙的溶解度和沉淀行为也对水质的净化和处理起着重要作用。
磷酸钙沉淀ph值是一个复杂而重要的研究课题,涉及到物质的溶解、沉淀、离子平衡等多个方面。
1536_7758-87-4_磷酸钙
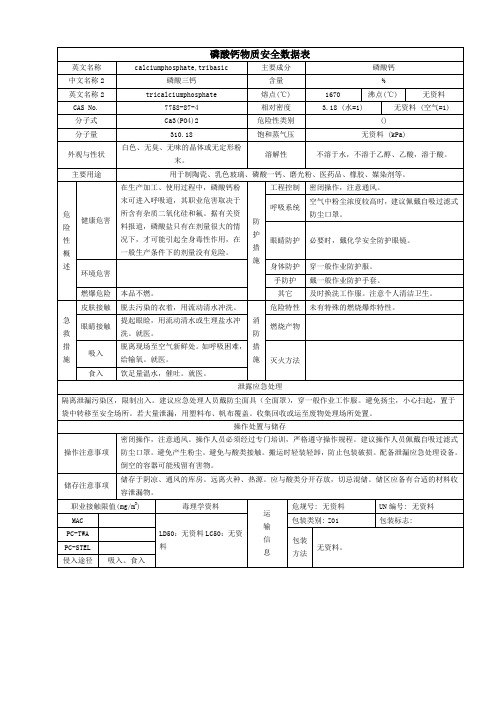
磷酸钙物质安全数据表英文名称calciumphosphate,tribasic 主要成分磷酸钙中文名称2 磷酸三钙含量%英文名称2 tricalciumphosphate 熔点(℃) 1670 沸点(℃) 无资料CAS No. 7758-87-4 相对密度 3.18 (水=1) 无资料 (空气=1) 分子式Ca3(PO4)2 危险性类别()分子量310.18 饱和蒸气压无资料 (kPa)外观与性状白色、无臭、无味的晶体或无定形粉末。
溶解性不溶于水,不溶于乙醇、乙酸,溶于酸。
主要用途用于制陶瓷、乳色玻璃、磷酸一钙、磨光粉、医药品、橡胶、媒染剂等。
危险性概述健康危害在生产加工、使用过程中,磷酸钙粉末可进入呼吸道,其职业危害取决于所含有杂质二氧化硅和氟。
据有关资料报道,磷酸盐只有在剂量很大的情况下,才可能引起全身毒性作用,在一般生产条件下的剂量没有危险。
防护措施工程控制密闭操作,注意通风。
呼吸系统空气中粉尘浓度较高时,建议佩戴自吸过滤式防尘口罩。
眼睛防护必要时,戴化学安全防护眼镜。
环境危害身体防护穿一般作业防护服。
手防护戴一般作业防护手套。
燃爆危险本品不燃。
其它及时换洗工作服。
注意个人清洁卫生。
急救措施皮肤接触脱去污染的衣着,用流动清水冲洗。
消防措施危险特性未有特殊的燃烧爆炸特性。
眼睛接触提起眼睑,用流动清水或生理盐水冲洗。
就医。
燃烧产物吸入脱离现场至空气新鲜处。
如呼吸困难,给输氧。
就医。
灭火方法食入饮足量温水,催吐。
就医。
泄露应急处理隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘面具(全面罩),穿一般作业工作服。
避免扬尘,小心扫起,置于袋中转移至安全场所。
若大量泄漏,用塑料布、帆布覆盖。
收集回收或运至废物处理场所处置。
操作处置与储存操作注意事项密闭操作,注意通风。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩。
避免产生粉尘。
避免与酸类接触。
搬运时轻装轻卸,防止包装破损。
骨盐量标准

骨盐量标准骨盐量是指骨骼中的矿物质含量,主要成分包括钙、磷等物质。
骨盐量的多少与骨骼的健康密切相关,因此对于人们的健康和生活来说十分重要。
现在,为了更好地保护人们的骨骼健康,各个国家和地区都制定了相应的骨盐量标准。
下面是我对骨盐量标准的一些介绍和解读。
一、骨盐量的意义骨盐是指骨骼中的无机物质,包括磷酸钙、碳酸钙、氟化物等。
骨盐的含量与骨骼的健康密切相关。
当骨盐量低于正常范围时,骨骼易于发生骨质疏松、骨折等问题,严重影响人们的生活质量。
保持健康的骨盐量对于身体健康至关重要。
骨盐量还与人体其他器官和系统的健康相互关系密切,如心血管、神经、肌肉等系统。
保持健康的骨盐量对于全身健康都有重要影响。
1.世界卫生组织(WHO)骨盐量标准WHO提出的骨盐量标准是最广泛应用的标准之一。
根据该标准,人类骨骼中的矿物质含量呈一个年龄递增的趋势。
女性的骨盐量一般要低于男性,而在女性更年期前后,骨盐量会发生急剧下降。
由于不同年龄段的人体状况也不同,因此在不同年龄段以及不同性别和膳食结构下,骨盐量标准还需要做出相应的调整。
2.日本骨质疏松症学会(JOS)骨盐量标准日本骨质疏松症学会的骨盐量标准是另一种常用的标准。
该标准认为,成年女性和男性骨盐量应分别为1000毫克/翼椎和1400毫克/翼椎。
三、骨盐量的影响因素1.饮食人体从食物中摄取到的钙和磷可以促进骨盐的生成。
如果饮食中缺乏这些元素,会导致骨盐量下降,从而影响骨骼的健康。
保持合理的膳食结构和摄取足够的钙、磷等元素对于骨盐量非常重要。
2.运动适当的运动可以促进骨盐的代谢和吸收,并增强骨骼的密度和强度。
长期坚持运动可以有助于维持健康的骨盐量。
骨盐量的高低与人类的遗传基因密切相关。
一些人具有天生的高骨盐量,而另一些人则可能存在骨盐量缺乏等问题。
四、如何提高骨盐量饮食是最基本的保持骨盐量的途径之一。
保持均衡的膳食结构,适当增加钙、磷等元素的摄取量,可以有效预防骨盐量下降。
3.补钙补充剂对于骨盐量缺乏的患者,可以考虑补钙补充剂。
磷酸钙沉淀ph值

磷酸钙沉淀ph值全文共四篇示例,供读者参考第一篇示例:磷酸钙是一种常见的盐类化合物,化学式为Ca3(PO4)2。
磷酸钙在工业生产和实验室中都有广泛的应用,其中磷酸钙沉淀是其中一种常见的应用。
磷酸钙沉淀是指将磷酸根离子和钙离子在一定条件下混合反应而生成的固体沉淀物。
pH值是影响磷酸钙沉淀形成的重要因素之一。
pH值是表示溶液中氢离子浓度的指标,其数值范围为0-14,中性溶液的pH值为7,酸性溶液的pH值小于7,碱性溶液的pH值大于7。
在磷酸钙沉淀中,pH值对磷酸根离子和钙离子的溶解度和反应速率都有着重要的影响。
当pH值较高时,磷酸根离子在溶液中的溶解度会增加,而钙离子的溶解度会降低。
这样一来,磷酸根离子和钙离子在高pH值条件下更容易结合生成磷酸钙沉淀。
此时,磷酸钙沉淀的产生速率会加快,形成较大的颗粒。
在实际应用中,磷酸钙沉淀的pH值通常会通过控制酸碱度来进行调节。
在医药和食品工业中,磷酸钙常被用作添加剂,为了保证其质量和稳定性,需要控制沉淀时的pH值。
在环境保护和水处理领域,磷酸钙沉淀也被广泛应用,而pH值的调控也成为影响处理效果的重要因素之一。
磷酸钙沉淀的形成受到多种因素的影响,其中pH值是其中一个重要的调节参数。
通过合理控制溶液中的pH值,可以调节磷酸钙沉淀的形成速率和颗粒大小,从而实现对沉淀过程的有效控制。
随着科学技术的不断发展,对磷酸钙沉淀过程的研究也将变得更加深入,为其在各个领域的应用提供更多可能性。
第二篇示例:磷酸钙是一种常见的化合物,具有广泛的应用领域,包括医药、食品、农业等。
磷酸钙沉淀是指在溶液中由磷酸和钙离子反应生成的沉淀物,其pH值对沉淀的形成、稳定性和性质起着重要的影响。
本文将重点讨论磷酸钙沉淀的pH值及其影响因素。
1. 磷酸钙沉淀的生成过程磷酸钙沉淀的生成过程主要是通过磷酸和钙离子之间的化学反应产生沉淀物。
在一般情况下,当磷酸盐与钙离子在溶液中反应时,会生成沉淀:3Ca2+ + 2PO43- → Ca3(PO4)2↓这个反应是一个平衡反应,其平衡常数与pH值密切相关。
