第五章相图
第5章 相图

2.可逆与不可逆多晶转变
z 多晶转变相图 4个单相区
晶型II熔融曲线
晶型转变线 晶型I的升华曲线
熔体的蒸气压曲线
3相平衡点: 晶型II的升华曲线 晶型II、熔体和气相
3相平衡点: 晶型I、II和气相
z 多晶转变相图(介稳平衡态)
过热晶型I熔融曲线 过热晶型I的介稳单相区
过冷熔体的介稳单相区
硅钙石:不一致熔 各种高炉矿渣中
水泥熟料生产重要
9%体积效应
C2S:一致熔融化合物 具有复杂的多晶转变 C3S:不一致熔融化合物
2150℃ ~ 1250℃
IV. 三元系统相图
对于三元凝聚态系统, C=3,n=1(T)
相律:F = C-P + n = 4-P
Fmin = 0,Pmax = 4 Pmin = 1,Fmax = 3
z 自由度(F)
在温度、压力、组分浓度等可能影响系统平衡状态的变量中, 可以在一定范围内任意改变而不会引起旧相消失或新相产生的 独立变量数目.
z 组分及独立组分(C)
组分 系统中每个能独立分离出来,并能独立存在的化学纯物质. 独立组分 足以表示系统中各个相的组成所需的组分的最小数目.
C = 组分数-独立的化学反应数-独立的限制条件数
M’熔体的结晶路程
液相点
L M’
1
F=2
L→S F=1
3
L→S F=1
5
固相点
L→S 2
4 L→S
6S
M
⑦ 形成有限固溶体的二元相图
B在A中 形成的 固溶体
SA(B)的 溶解度 曲线
B在A中 的最大 固溶度
A在B中 的最大 固溶度
A在B中 形成的 固溶体
第五章 相图

材料科学基础材料科学基础-石德珂主编
第五章 材料的相结构及相图
电子浓度的定义是合金中各组成元素的价电子数总和与原子总数的比值 电子浓度的定义是合金中各组成元素的价电子数总和与原子总数的比值 ,记 作e/a e/a=VA(1-x)+VBx。 。 元素名称 Cu、Ag、Au 、 、 Be、Mg、Zn、Cd、Hg 、 、 、 、 Al、In、Ga 、 、 Sn、Si、Ge、Pb 、 、 、 As、Sb、Bi、P 、 、 、 Fe、Co、Ni 、 、 每个元素贡献的价电子 +1 +2 +3 +4 +5 0
性能:无论是置换固溶体还是间隙固溶体,均能引起固溶体的硬度、 性能:无论是置换固溶体还是间隙固溶体,均能引起固溶体的硬度、强度 硬度 升高。 升高。 对置换式固溶体,溶质原子与溶剂原子的尺寸差别越大, 对置换式固溶体,溶质原子与溶剂原子的尺寸差别越大,溶质原子的浓度 越高,其强化效果就越大。 越高,其强化效果就越大。这种由于溶质原子的固溶而引起的强化效应 , 称为固溶强化 称为固溶强化 。
材料科学基础材料科学基础-石德珂主编
第五章 材料的相结构及相图
3.陶瓷材料中的固溶方式 .
的方式溶入一些元素而形成固溶体, 无机非金属化合物也可以置换或间隙固溶 的方式溶入一些元素而形成固溶体,有些 甚至可以形成无限固溶体。 甚至可以形成无限固溶体。 如菱镁矿中的Mg 2+可以完全被 Fe 2+置换,形成如下系列矿物: 置换,形成如下系列矿物: 如菱镁矿中的 Mg[CO3]→(Mg, Fe) [CO3]→(Fe, Mg) [CO3 ]→Fe [CO3 ] 菱镁矿 含铁菱镁矿 含镁菱铁矿 菱铁矿
材料科学基础材料科学基础-石德珂主编
陶杰版材料科学基础--第5章 相图

90
10 20 30
40
II C% 50 60 70 80 90
90
80
70
60
50 ← A%
40
30
20
10
C
化学与化学工程系材料科学教研室
B 第五章 相图
课堂练习
1. 确定合金I、II、III、IV的成分 III 点:
70 80
90
10 20 30
A%=20% B%=20% C%=60%
60 B% 40 30 20 10
化学与化学工程系材料科学教研室
第五章 相图
意义
•
相图是反映物质在不同温度、成分和压力时,各种 相的平衡存在条件,以及相与相之间平衡关系的重要图 解,掌握相图对于了解物质在加热、冷却或压力改变时 的组织转变基本规律,以及物质的组织状态和预测物质 的性能,都具有重要意义。
•
研究多相系统的平衡在化学、化工的科研和生产中 有重要的意义,例如:溶解、蒸馏、重结晶、萃取、提 纯及金相分析等方面都要用到相平衡的知识
用一个温度坐标和一个压力坐标表示,这时的相图为一个二
维平面图。
化学与化学工程系材料科学教研室
第五章 相图
纯铁的相图
化学与化学工程系材料科学教研室
第五章 相图
二氧化碳相图示意图
B
p/Pa 固相
C
超临界 流体
临界点
液相
O
A
气相
T/K
纯净物质根据温度和压力的不同,会呈现出液体、气体、 固体等状态变化,如果 提高温度和压力,来观察状态的变化,那么会发现,如果达到特定的温度和压力,会 出现液体与气体界面消失的现象,该点被称为临界点。在临界点附近,会出现流体的 密度、粘度、溶解度、热容量、介电常数等所有流体的物性发生急剧变化的现象。 温度和压力均高于临界点时的流体,称为超临界流体。
第五章 相图
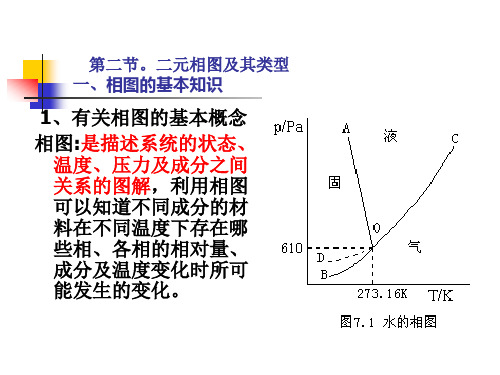
第三节 二元共晶相图及合金凝固
(2)共晶合金(分析要点) ① 凝固过程(冷却曲线、相变、组织示意图)。 ② 共晶线上两相的相对量计算。 ③ 室温组织(α+β)及其相对量计算。
2h
图4-28 Pb-Sn共晶合金平衡凝固过程示意图
1) 在液体中α 和β 同时具有析出条件,都可以析出。
2) 由于α 和β 析出过程在成分上可以互相补充和促进, 共同析出。
二元匀晶相图
一、匀晶相图及其分析 (1)匀晶转变:由液相直接结晶出单相固溶体的 转变。 (2)匀晶相图:具有匀晶转变特征的相图。 Cu-
Ni、 Cu-Au、 Au-Ag、Fe-Cr等
(3)相图分析(以Cu-Ni相图为例) 两点:纯组元的熔点; 两线:L, S相线; 三区:L, α, L+α。
固溶体合金的平衡结晶
金相法
膨胀法 电阻法
热分析法(以Cu-Ni系相图为例):
配制一系列成分不同的Cu-Ni合金; 测定上述合金的冷却曲线 找出各合金的临界点 以温度为纵坐标、以成分为横坐标的图中,将各临 界点连接起来即得到Cu-Ni合金相图
二.相图的建立
名称 晶格类型 熔点 合金1 合金2 合金3 …….. 合金9 合金10 合金11 A金属 fcc 高 100% 90% 80% …….. 20% 10% 0% B金属 fcc 低 0% 10% 20% ……. 80% 90% 100%
二、包晶体转变
过程
成分为P点合金的凝固 β 相的形核在α 相晶体和液体 的边界处,由于β 相的成分介于 液体和α 相之间,所以它是靠消 耗部分已有的α 相和部分液体来 实现。 β 相的生长在液体和α 相的交 界面处最有利,沿边界同时消耗 液体和α 相来长大,形成的β 相 包围在α 相外围,将α 相与液体 分隔开,所以把这种转变称为包 晶转变。
《材料科学基础》课件——第五章相平衡与相图第一节第二节第三节第四节

相和相平衡
Байду номын сангаас四、自由度与相律
1、自由度:平衡系统中独立可变的因素
自由度数:独立可变的强度变量的最大数目
(强度变量与广度变量的区别)
2、相律:自然规律
在平衡系统中由于受平衡条件的制约,系统内
存在的相数有一定限制。 组元数 相数P≥1
吉布斯相律:不可为负数
f=c-p+n
外界影 响因素
通常外界影响因素只考虑T、P,所以f=c-p+2
• 掌握匀晶,包晶,共晶相图的特点,进而了解二元合金的一些平衡凝固,固 相转变的规律。
• 重点难点: • 二元系相图的建立,杠杆定律 • 包晶相图,共晶相图,共晶合金 • 相图分析,各种液固,固相转变的判断
材料的性能决定于内部的组织结构,而组织结构
又由基本的相所组成。
相:均匀而具有物理特性的部分,并和体系的其他 部分有明显界面。
晶型转变过程都是在恒温下进行,并伴随有体 积、密度的变化。 2、SiO2系统相图 α-石英与β-石英相变相当慢, β-石英常因冷却过快而被保留 到室温,在常压下,低于573℃
单元系相图
β-石英很稳定,所以自然界或低温时最常见的是 β-石英。晶型转变时,体积效应特别显著。 Al2O3、ZrO2也具有多晶型转变。 3、聚合物相图 (1)状态由分子间作用力决定,分子间约束力弱
共晶相图,平衡凝固,共晶合金,包晶相图,形成化合物的相图,含有双液 共存区的相图,熔晶相图等 ,二元相图的几何规律 ,单相,双相及三相共 存区,相图特征 ,二元系相图的分析,分析的方法与步骤,分析举例。
• 教学目的: • 学习相平衡与相图的基本知识,了解相图在材料科学学习中的重要性,学会
相图的使用。
物理化学第5章相律与相图

第五章相律与相图5.1 相平衡相平衡是热力学在化学领域中的重要应用,也是化学热力学的主要内容之一。
在第三章中已经应用热力学原理研究了纯物质系统的两相平衡;在第四章中研究了多组分系统的两相平衡,其结果是用热力学公式表达相平衡的规律。
而本章则是应用热力学原理采用图解的方法来表达相平衡规律,特别是对多相系统的相平衡规律的研究,用图解的方法更显得方便和实用。
研究多相系统的相平衡状态随组成、温度、压力等变量的改变而发生变化,并用图形来表示系统相平衡状态的变化,这种图称为相图,相图形象而直观地表达出相平衡时系统的状态与温度、压力、组成的关系。
相律为多相平衡系统的研究建立了热力学基础,是物理化学中最具有普遍性的规律之一,它讨论平衡系统中相数、独立组分数与描述该平衡系统的变数之间的关系,并揭示了多相平衡系统中外界条件(温度、压力、组成等)对相变的影响。
虽然相律不能直接给出相平衡的具体数据,但它能帮助我们从实验数据正确地画出相图,可以帮助我们正确地阅读和应用相图。
本章首先介绍相律,然后介绍单组分、二组分和三组分系统的最基本的几种相图,其中着重介绍二组分气-液相图和液-固相图,介绍相图的制法和各种相图的意义以及它们和分离提纯方法之间的关系。
应用:a、水泥熟料的烧成过程,系统中有C3S(硅酸三钙)、C2S(硅酸二钙)、C3A(铝酸三钙)、C4AF(铁铝酸四钙)————固相,还有一定的液相,是一个多相的系统。
随着温度升高,这个多相系统中那些相能继续存在?那些相会消失?有没有新的相生成?各相组成如何?各相含量为多少?b、在化工生产中对原料和产品都要求有一定的纯度,因此常常对原料和产品进行分离和提纯。
常用的分离提纯的方法是结晶、蒸馏、萃取和吸收等等,这些过程的理论基础就是相平衡。
相图:根据多相平衡的实验结果,可以绘制成几何图形用来描述这些在平衡状态下的变化关系,这种图相成为相图。
现实意义:水泥、玻璃、陶瓷等形成过程均在多相系统中实现,都是将一定配比的原料经过锻烧而形成的,并且要经历多次相变过程。
材料科学基础I 第五章 (相图)
F = 0的含义是:在保持系统平衡状态不变的条件下,没有可以 的含义是:在保持系统平衡状态不变的条件下, 的含义是 独立变化的变量。 独立变化的变量。即,任何变量的变化都会造成系统平衡状态 的变化。 的变化。
纯水的PT相图: 纯水的 相图:在a点,水在 相图 点 水在1 大气压、 ℃ 条件下 保持液(水 条件下, 大气压、(0℃)条件下,保持液 水) –固(冰)二相平衡。温度升高,冰 二相平衡。 固 冰 二相平衡 温度升高, 溶化成水;温度降低, 溶化成水;温度降低,水结晶成 也就是说,此时水的液-固平 冰。也就是说,此时水的液 固平 衡转变是在恒温(0℃ 下进行的 下进行的。 衡转变是在恒温 ℃)下进行的。 b点是气 液二相平衡点,意义与 点是气–液二相平衡点 点是气 液二相平衡点,意义与a 点相似。 之间(0℃ 点相似。在a、b之间 ℃~100℃), 、 之间 ℃, 水是单一的液相(P =1),此时F =1, 水是单一的液相 ,此时 , 这说明在此范围内温度的变化不 会引起状态的改变。 会引起状态的改变。
二、相图的建立
建立相图的方法有两种: 建立相图的方法有两种: 利用已有的热力学参数,通过热力学计算和分析建立相图; 利用已有的热力学参数,通过热力学计算和分析建立相图; 依靠实验的方法建立相图。 依靠实验的方法建立相图。 目前计算法还在发展之中,实际使用的相图都是实验法建立的。 目前计算法还在发展之中,实际使用的相图都是实验法建立的。 实验法建立相图的原理和步骤: 实验法建立相图的原理和步骤: 二元合金相图的建立为例。 以A-B二元合金相图的建立为例。 二元合金相图的建立为例 首先, 首先,将A-B二元合金系分成 二元合金系分成 若干种不同成分的合金。 若干种不同成分的合金。 1) 合金成分间隔越小,合金数目 合金成分间隔越小, 越多,测得的相图越精确; 越多,测得的相图越精确; 2) 合金成分间隔不需要相等。 合金成分间隔不需要相等。
第五章 相图

相图
(2)∵150/500<70.0%∴当温度由共沸点刚有上升趋势时,系统处于气(G)与液(L1)两 相平衡设 L1 的质量为 x 则 x(150/500-0.087)=(500-x)(0.70-150/500) 解得 x=326g 气相质量为 174g。 6-10 为了将含非挥发性杂质的甲苯提纯,在 86.0kPa 压下用水蒸气蒸馏。已知:在此压力 下该系统的共沸点为 80℃,80℃时水的饱和蒸气压为 47.3kPa。试求: (1)气相组成(含甲苯的摩尔分数) ; (2)欲蒸出 100g 纯甲苯,需要消耗水蒸气多少千克? 86.0 47.3 100 / 92.140 解: y甲 0.45 y甲 解得 x=23.9kg 86.0 100 / 92.140 x / 18.02 6-14 低温时固态部分互溶、 高温时固态完全互溶且具有最低熔点的 A-B l 二组分凝聚系统相图如附图。指出各相区的相平衡关系及各条线所代表 T l+ 的意义。 解:上面的线为液相线或凝固点曲线;中间的线为固相线或熔点线;下 面的线为固相溶解度曲线 1+
A(l)+B(l) x(y) B
液态部分互溶
液态不互溶
5.常见的二组分固液相图(上述的气液相图中将气态变为液态,液态变为固态也是常 见的固液相图)
T
T l+A(s) l+B(s) A(s)+B(s) A x B l
T l l+s
T
l
l l+s ssl+s s源自x BAx
B
A
A
x
B
固态不互溶
固态完全互溶
54.22 0.4588 0.2523 98.54 p* x' (2) y’ y' A * ' A A * ' A=xA p A x A p B x B
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
• .马氏体相变没有一个特定的温度, 而是在一个温度范围内进行的。
18
五、 有序—无序转变
• 随温度升降而出现低温有序和 高温无序的可逆转变过程称为 有序—无序转变。
19
五、 有序—无序转变
完全有序时 为,完全
无序时 为。 如: 磁铁矿
• 有序参数 ( )( )
• 碰撞频率υ表示为:
原子或分子的跃迁频 率
• υυ(Δ/)
原子或分子跃迁新旧 界面的迁移活化能
38
一、晶核形成过程动力学 均匀成核( )
• 成核速率可以写成:
• υυ(Δ/)
•
(Δ/)
• (Δ/)
•
(Δ/)
•·
常数
受核化位垒影响 的成核率因子
受原子扩散影响 的成核率因子
39
、均匀成核( )
见图
•
,只有在合适的过冷度下,
υ有最大值。
40
图—
41
、非均匀成核( )
• 非均匀成核是指借助于表面、界 面、微粒裂纹、器壁以及各种催 化位置等而形成晶核的过程。
4
图—
5
一、按热力学分类二级相变
• 相变时两相化学势相等,其一级偏微商 也相等,但二级偏微商不等,即:
• µµ • ( µ )( µ ) • ( µ )( µ )
6
一、按热力学分类二级相变
• ( µ )≠( µ ) • ( µ )≠( µ ) • ( µ )≠( µ ) • 即 µµ ≠;≠ ≠ β≠β α≠α • 式中β和α分别为等温压缩系数和等
29
三、晶核()形成条件
新相的 体积
• Δ=ΔΔ=Δγ
新相总 表面积
单位体积中旧 相和新相之间 的自由能之差
新相界面能
30
三、晶核()形成条件
• 若假设生成的新相晶胚呈球形, 则
• Δπ··Δπ·γ
球形晶胚半径
单位体积中半径的 晶胚数
31
三、晶核()形成条件
• Δπ··ΔΔπ·γ
• 见 图 表示Δ与晶胚半径的关系
13
四、马氏体()
• .结晶学特征 • •图 所示()为一四方形的母相—一奥氏体
块。()是从母相中形成马氏体示意图。其中 和这两个把母相奥氏体和转变相马氏体之间 连接起来的平面称为习性平面。
• 结晶学特征是相变后存在习性平面和晶面的 定向关系。
14
图—
15
图—
16
图—
17
四、马氏体()
• .马氏体相变的另一特征是无扩散 性的位移式相变,其相对位移不超 过原子间距。
压膨胀系数。见图
7
图
8
一、按热力学分类二级相变
• 特点:无相变潜热,没有 体积的不连续变化 ,只 有热容量、热膨胀系数和 压缩系数的不连续变化。
9
一、按热力学分类二级相变
• 由于这类相变中 热容随温度的变 化在相变温度时 趋于无穷大,因 此可根据—曲线 具有 形状而称 二级相变为 相 变,其相变点可 称 点或居里点。 见图
10
二、按相变方式分类
• 成核—长大型相变():是由程度 大、但范围小的浓度起伏开始发生 相变,并形成新相核心的相变;
• 分解():由程度小、范围广的浓度 起伏连续地长大形成新相的相变。
11
三、按质点迁移特征分类
• 扩散型相变 • 无扩散型相变:如马氏体转变。
12
四、马氏体()
• 一个晶体在外加应力的作用下通 过晶体的一个分立体积的剪切作 用以极迅速的速率而进行相变称 为马氏体转变。
1
§— 相变的分类 §—
2
• 一、按热力学分类一级相变
体系由一相变为另一相时, 如两相的化学势相等但化学势的 一级偏微商(一级导数)不相等的 称为一级相变,即:
3
• 一、按热力学分类一级相变
µµ ( µ )≠( µ ) ( µ )≠( µ ) 由于( µ );( µ ) , 即≠;≠。因此在一级相变时熵()和体积() 有不连续变化,如图—示。 特点:相变时有相变潜热,并伴随有体 积改变。
25
二、相变过程推动力相变过程的温度条 件
• 在等温等压下,ΔΔΔ
• 在平衡条件下,Δ=,则ΔΔ
• 在任意一温度的不平衡条件下,
则相有变Δ热ΔΔ≠
相变的平衡温度
• 若Δ与Δ不随温度而变化,
• ΔΔΔΔ()
• ΔΔ
26
二、相变过程推动力相变过程的温度条 件
• Δ<,要使Δ<,须有Δ>,<,过冷;
• 相变过程吸热Δ>,要使Δ<,须有 Δ<,>,过热。
• 因此相平衡理论温度与系统实际 温度之差即为该相变过程的推动 力。
27
二、相变过程推动力相变过程的压力和浓度 条件
• 、气相,恒温下Δ 欲使Δ <,须> 即汽相过饱和。
• 、溶液, Δ 欲使Δ <,须> 即液相 过饱和 。
• 综上所述,相变过程的推动力应为
过冷度、过饱和浓度、过饱和蒸汽
压。即相变时系统温度、浓度和压
力与相平衡时温度、浓度和压力之
差值。
28
三、晶核()形成条件
• 当一个熔体(熔液)冷却发生相转变时,则系 统由一相变成两相,这就使体系在能量上出 现两个变化,一是系统中一部分原子(离子) 从高自由能状态(例如液态)转变为低自由能 的另一 状态(例如晶态),这就使系统的自由 能减少(Δ);另一是由于产生新相,形成了 新的界面(例如固—液界面),这就需要作功, 从而使系统的自由能增加(Δ)。因此系统在 整个相变过程中自由能的变化(Δ )应为此两 项的代数和。
35
§— 液—固相变过程动力学
§—
36
一、晶核形成过程动力学 、均匀成核( )
• 晶核从均匀的单相熔体中产生的过程。
成核速率,指单位时间、单 位体积中所生成的晶核数目, 其单位通常是晶核个数秒·厘
米
• υυ
临界晶核周界 上的原子或分
子数
单个原子或分 子同临界晶核 碰撞的频率
37
、均匀成核( )
32
图—
33
三、晶核()形成条件
• γΔΔγΔ
• 由此得出: • .愈小,新相愈易形成。 • .因为γ、均为正值,析晶放热过
程Δ<,所以 Δ>。
• .降低γ、增加Δ均有利于析晶。
34
三、晶核()形成条件
• .相应于时的自由能变化为:
• ΔπγΔπγΔ
•
(π γ Δ)
•
γ
• 、达晶胚数目: • (Δ)
原子占据应该占 据的位置数
原子占据不应占 据的位置数
20
图
21
§— 液—固相变过程热力学
§—
22
一、相变过程的不平衡状态及亚稳区 • 亚稳区 :理论上应发生相变而实 际上不能发生相转变的区域 • (如 见图 所示的阴影区)。 • 需过冷、过饱和才能相变。
23
图—
24
二、相变过程推动力
• 总的推动力:相变过程前后自由 能的差值
