飞行检查的工作程序
飞检小组管理制度

飞检小组管理制度第一章总则第一条为了规范和提高飞检小组的管理工作,保证飞检工作的顺利进行,制定本管理制度。
第二条飞检小组的任务是对航空器进行飞行前和飞行中的安全检查,以确保航空器完全适航,确保飞行安全。
第三条飞检小组的管理工作应该遵循“严格、细致、严谨、高效”的工作原则。
第四条飞检小组的管理制度适用于飞行检查小组的各个环节。
第二章飞检小组的组织架构第五条飞检小组由飞检小组长、副小组长、飞检员等组成。
第六条飞检小组长负责飞检小组的整体工作,协调各个部门之间的关系。
第七条飞检小组的副小组长协助小组长工作,并在小组长不在时履行小组长的职责。
第八条飞检员是飞检小组的核心成员,负责执行飞行前和飞行中的安全检查任务。
第九条飞检小组的组织架构应当合理,保证每个成员的职责明确,互相配合。
第十条飞检小组应当建立科学、严密的管理制度,保证飞行检查任务的完成。
第三章飞检小组的管理制度第十一条飞检小组应当建立起机动灵活的管理制度,以应对飞检工作的各种情况。
第十二条飞检小组应当建立起合理的值班制度,以保证24小时随时能够进行飞行检查工作。
第十三条飞检小组在进行飞检任务时,应当严格按照飞检计划执行,确保每个飞行检查任务的完成。
第十四条飞检小组应当建立起安全意识,保证在飞行检查过程中,不出现任何安全事故和隐患。
第十五条飞检小组应当建立起科学、严密的信息记录和汇报制度,确保对飞行检查任务的记录完整。
第十六条飞检小组应当建立起完善的训练和考核制度,以提高飞检员的业务水平和工作质量。
第四章飞检小组的管理工作第十七条飞检小组应当制定详细的飞行检查计划,包括飞行前和飞行中的安全检查内容和流程。
第十八条飞检小组应当建立起科学的飞行检查工具和设备,确保飞行检查任务的顺利进行。
第十九条飞检小组应当建立起完善的记录和报告制度,对每次飞行检查任务进行详细记录,及时向相关部门汇报。
第二十条飞检小组应当对飞行检查任务进行严格的审核,确保每次飞行检查任务的合格完成。
食品生产企业体系飞行检查工作记录(范本)
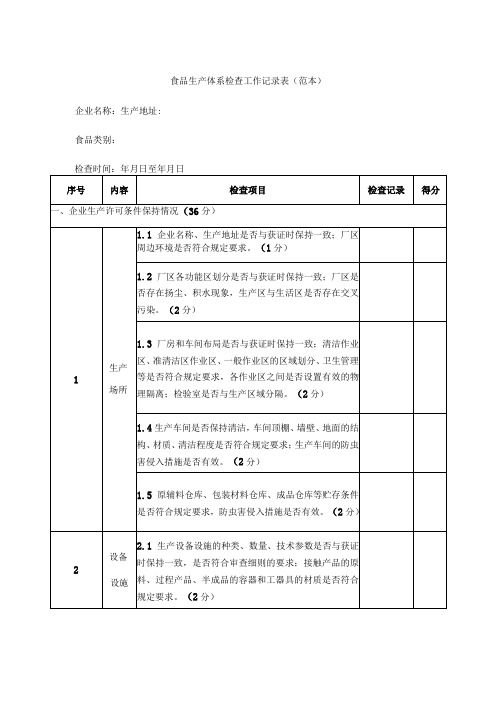
齐全、完整。(2分)
11.3是否存在使用不合格原辅材料以及利用回收
食品作为原料生产食品的行为。(2分)
12
食品
安全事故处置
12.1食品生产经营企业是否制定食品安全事故处置方案,是否定期检查本企业各项食品安全防范措施的落实情况,及时消除事故隐患。(2分)
13
2.本记录表包括生产许可条件保持情况、食品安全管理制度落实情况、不安全食品召回与处置、其他问题和重复扣分项等4方面内容,总分共IOO分;
3.每个检查项目根据重要性赋予不同的分值。如该项目检查未发现问题得满分,对检查发现的问题则根据问题的数量和严重程度进行扣分:
(1)按问题的严重程度扣分:一般性的问题扣项目分值的25%,较严重的问题扣项目分值的50%,严重的问题扣项目分值的75%—100%,扣完为止;例如:检查项目10.3,建立留样制度,但无保留样品,扣完1.5分;未建立制度也未进行留样,则扣完全部分值2分。
(2)按问题的数量扣分:如一个项目发现多个问题,按每个问题的扣分值累加,扣完为止。例如:检查项目1.1,分值1分,若此项发现两个问题,每个问题扣0.25分,则最后得分0.5分。
4.检查中发现的其他问题(除重大问题重复扣分项外),按每条扣1分;
5.重大问题重复扣分项要求:若发现存在违反《食品安全法》第122条至125条法律规定的情形,每项重复扣10分;违反《食品安全法》规定的其他情形,每项重复扣5分(配方标签管理一般问题按5.1内容进行扣分,如涉嫌重大欺诈消费者则以食品安全法进行扣分);发现存在食品安全标准、审查细则中明令禁止行为的情形,每项重复扣5分;
10.1是否建立并执行食品出厂检验记录制度,自行检验或委托具备相应资质的食品检验机构对原料和产品进行检验。(2分)
【规范】江苏省公路水运建设工程质量监督工作程序及标准

江苏省公路水运建设工程质量监督工作程序及标准(6月7日44次厅务会审议通过)第一章总则第一条为规范全省公路水运建设工程质量监督工作,实现质量监督工作标准化、程序化、规范化,进一步提高工程质量,根据《建设工程质量管理条例》、《公路工程质量监督规定》、《水运工程质量监督规定》等法规、规章,结合本省实际,制定本程序及标准。
第二条县级以上地方人民政府交通运输主管部门所属的质量监督机构(以下简称“质量监督机构”)应当按照本程序及标准对本省行政区域内公路水运建设工程(以下简称“建设工程”)进行质量监督。
第三条质量监督机构主要以抽查的方式对已受理质量监督申请的建设工程实施质量监督检查。
质量监督检查分为中间质量监督检查和竣(交)工质量监督鉴(评)定检查。
质量监督申请与受理是指建设单位或者项目法人(以下简称“建设单位”)在办理施工许可或者报备开工报告前,依法向质量监督机构申请工程质量监督,质量监督机构对所提交的资料进行审核,发出《质量监督通知书》,并建立建设工程质量监督档案的活动。
中间质量监督检查是指质量监督机构在建设工程施工过程中对有关责任主体的质量管理行为、施工工艺以及工程实体质量情况进行的除竣(交)工质量监督鉴(评)定检查之外的抽查活动。
竣(交)工质量监督鉴(评)定检查是指质量监督机构在建设工程竣(交)工验收环节进行的质量监督检查。
第四条本程序及标准适用于本省行政区域内四级及四级以上公路新建、改(扩)建、大修工程,除长江以外内河四级以上航道新建、改建工程,以及沿海、沿江万吨级以上泊位、内河500吨级以上泊位的港口(码头)工程的中间质量监督检查。
其他建设工程的中间质量监督检查可以根据实际情况,由市、县质量监督机构参照执行。
竣(交)工质量监督鉴(评)定检查工作程序及标准,按照交通运输部和省有关规定执行。
第二章质量监督申请与受理第五条建设单位应当按照国家和省有关规定向质量监督机构申请办理建设工程质量监督手续。
(一)建设单位应当在完成开工前各项准备工作之后,办理施工许可或者报备开工报告30日前申请办理质量监督手续。
学校食品安全飞行检查内容及标准

学校食品安全飞行检查内容及标准一.食堂食品安全管理1.食堂自主经营,不对外承包;严格落实学校食堂月度自查制度,查阅基层监管部门的季度检查情况;2.食品药品监管部门颁发的餐饮服务许可证在有效期内;从业人员均持有有效的健康合格证明上岗;3.积极参加“星级学校食堂”创建活动,各项管理规范,落实了食品安全责任制度,建立健全采购索证索票、进货验收、入(出)库登记、清洗消毒、食品留样、健康查体、规范管理、安全卫生、责任追究等一系列制度。
4.食堂布局流程规范,食品采购、加工、运输、储存等环节符合要求;5.严格执行领导陪餐制、周食谱制及食堂开放日制度;6.开展经常性食品安全工作检查并有记录;食品采购索证记录和消毒记录、食品留样记录规范;7.实行大宗物品集中定点采购,杜绝过期、变质、“三无”食品;8.不得经营“三无”食品和自制食品;9.食品添加剂使用符合国家有关规定;10.食堂消防用电管理规范,消防设施配备到位;11.食堂所用燃气设备设施应符合安全规定,并与供气单位签订安全责任书;812.学校自备水源应定期检查清洗消毒,桶装水、纯净水须有合格证明。
二、食堂卫生(一)环境和器械卫生1.厨房整体环境卫生整洁;杀菌、灭蝇、消毒等卫生设施配备齐全,并处于正常使用状态;2.各种炊事机械有专人负责、专人保养,器械干净,并用专用盖布盖好。
冰箱内无血水,东西码放有序,并定期除霜。
3.工作厨台、橱箱及厨房无垃圾死角,无遗留腐烂的菜屑、碎肉。
4.应装置抽油烟机,并定时清理油垢。
5.地面、天花板、墙壁、门窗应坚固美观,所有孔洞缝隙应予填实密封,并保持整洁,以免蟑螂、老鼠躲藏或出入。
6.应备置密盖污物桶、厨余桶,厨余最好当夜倒除,不在厨房内隔夜。
7.厨房清洁扫除工作,每日要做到数次,清洁完毕,清扫用具应集中放置。
8.杀菌剂和洗涤剂不得与杀虫剂等放在一起,有毒的物质要标明,放在固定场所及指定专人管理。
(二)食品和炊具卫生1.严格执行生熟、半成品分开存放。
飞行检查年终检查总结

飞行检查年终检查总结一、背景飞行检查是保障航空安全的重要手段,对提高航空公司的运营水平和保障旅客生命财产安全具有重要意义。
本总结对2024年飞行检查工作进行了回顾和总结,以期为今后的工作提供有益的参考和借鉴。
二、检查内容与目标2024年飞行检查工作重点围绕以下几个方面展开:1.飞行员资质与训练:检查飞行员是否具备相应的资质和训练水平,确保其具备执行航班任务的能力。
2.机组资源管理:评估机组人员之间的协作与沟通,确保航班运行过程中的高效协作。
3.飞机维护与检查:对飞机进行定期维护和检查,确保飞机处于适航状态。
4.安全管理与应急处置:评估航空公司的安全管理体系和应急处置能力,提高应对突发事件的能力。
通过以上内容的检查,旨在发现潜在问题、消除安全隐患、提高航空安全水平。
三、检查结果与问题分析在2024年的飞行检查中,共检查了XX家航空公司的XX个航班,发现以下问题:1.部分飞行员资质过期或训练不足,需加强培训和资质审核。
2.机组资源管理存在沟通不畅、协作不力的情况,需加强团队协作和沟通培训。
3.飞机维护与检查方面存在记录不规范、维护不到位等问题,需加强维护管理和监督。
4.安全管理与应急处置方面存在预案不完善、演练不充分等问题,需加强安全管理体系建设和应急演练。
针对以上问题,已要求相关航空公司采取措施进行整改和完善。
四、经验教训与改进措施在2024年的飞行检查工作中,我们认识到以下几点经验教训:1.检查工作需更加细致全面,不留死角。
2.加强与航空公司的沟通与协作,提高检查工作的透明度和有效性。
3.注重对航空安全新形势、新技术的研究和应用,提高检查工作的前瞻性和针对性。
为改进飞行检查工作,我们将采取以下措施:1.完善检查标准和程序,提高检查工作的规范性和科学性。
2.加强培训和学习,提高检查人员的专业素质和技能水平。
3.加大监督和处罚力度,对存在安全隐患的航空公司进行严格处理和督促整改。
4.加强国际合作与交流,借鉴国际先进经验和技术,提高我国飞行检查的整体水平。
飞行检查相关工作流程文件

飞行检查相关工作流程文件下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!一、飞行检查计划制定1. 确定检查目标和范围:明确飞行检查的目的,例如评估航空公司的安全管理、运营规范或服务质量等。
飞行检查的工作程序

省食品药品监督管理局关于印发药品GMP飞行检查工作程序的通知(鄂食药监文〔2007〕61号)发布时间:2007-11-22 来源:药品审评认证中心阅读次数:436 【字体:大中小】各市、州、直管市、神农架林区食品药品监督管理局:为加强药品GMP飞行检查管理,规范飞行检查工作程序,省局制定了《药品GMP飞行检查工作程序》,现印发给你们,请遵照执行。
二00七年八月十五日药品GMP飞行检查工作程序为加强药品GMP飞行检查管理,规范飞行检查工作程序,根据《湖北省药品GMP飞行检查暂行规定》,制定本工作程序。
一、省局药品审评认证中心(以下简称中心)受省局的委托,具体组织实施GMP飞行检查。
二、药品GMP飞行检查的企业名单及检查范围由省局药品安全监管处确定。
三、药品GMP飞行检查的具体时间由中心根据实际情况确定。
四、中心负责下发《药品GMP飞行检查通知》(附件1),一式两份,于检查组到达被检查企业后分别交给企业及所在地药监局。
五、中心负责制定《药品GMP飞行检查实施方案》(附件2),内容包括检查单位、检查范围、检查时间、检查程序、重点检查内容、需要核实的问题、检查组组成及分工等。
六、中心负责抽调检查员。
中心在抽调检查员时要告知检查员所在单位,检查员参加检查时要向所在单位报告。
各级食品药品监督管理局和药品检验所要全力支持检查员的工作。
中心要加强对检查员工作的考核,对不符合要求或不能参加现场检查工作的不再聘任。
七、检查组由2至3名药品GMP检查员、药品生产监督检查员和药检所技术人员组成,根据检查工作需要可以邀请有关专家参加检查。
对有举报、投诉或有违法案件线索的飞行检查,省局稽查分局须派人参加。
八、检查组成员应到中心指定的地点集中,到达时间由中心适时通知被检查企业所在地市(州)局,检查组适时将被检查企业告知所在地市(州)局。
市(州)局派一名观察员协助检查组工作并负责安排检查组的食宿、交通等,费用由中心按规定的标准统一承担。
浙江省食品药品监督管理局关于印发《医疗器械经营企业飞行检查工作程序》的通知

浙江省食品药品监督管理局关于印发《医疗器械经营企业飞行检查工作程序》的通知文章属性•【制定机关】浙江省食品药品监督管理局•【公布日期】2016.05.09•【字号】浙食药监规〔2016〕10号•【施行日期】2016.08.01•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】卫生医药计划生育正文浙江省食品药品监督管理局关于印发《医疗器械经营企业飞行检查工作程序》的通知浙食药监规〔2016〕10号各市市场监督管理局(食品药品监督管理局),省药品认证检查中心: 为加强医疗器械经营监督管理,规范医疗器械经营企业飞行检查,省局制定了《浙江省食品药品监督管理局医疗器械经营企业飞行检查工作程序》,现印发给你们,请遵照执行。
其中,飞行检查报告录入省局医疗器械GSP检查信息数据库的工作,待数据库建成后开展。
浙江省食品药品监督管理局2016年5月9日浙江省食品药品监督管理局医疗器械经营企业飞行检查工作程序第一条为加强医疗器械经营监督管理,根据《医疗器械经营监督管理办法》(国家食品药品监督管理总局令第8号)、《药品医疗器械飞行检查办法》(国家总局令第14号)、《医疗器械经营质量管理规范》(国家总局2014年第58号公告)、《医疗器械经营质量管理规范现场检查指导原则》(食药监械监〔2015〕239号)和省局《关于实施〈医疗器械经营质量管理规范〉有关事项的通知》(浙食药监规〔2015〕26号)等相关规定,制定本程序。
第二条医疗器械经营企业飞行检查(以下简称“飞行检查”)是指食品药品监督管理部门根据监管工作需要,对医疗器械经营企业实施不预先告知的监督检查。
第三条省、市、县(市、区)局分别负责辖区内医疗器械经营企业的飞行检查工作,包括被检查单位的确定、检查结果的审核及处理。
第四条浙江省药品认证检查中心(以下简称“省中心”)负责省局飞行检查的组织和实施,包括检查方案的制定、检查组的调派和检查报告的技术审查。
第五条省局根据上一年度全省医疗器械经营企业监管情况,抽取部分企业作为年度飞行检查对象;有下列情形之一的企业列为飞行检查对象:(一)投诉举报或其他来源的线索表明企业经营及产品质量可能存在安全风险的;(二)产品质量抽验发现存在质量问题的;(三)企业有严重不守信记录的;(四)其它省局认为需开展飞行检查情形的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
省食品药品监督管理局关于印发药品GMP飞行检查工作程序的通知(鄂食药监文〔2007〕61号)
发布时间:2007-11-22 来源:药品审评认证中心阅读次数:436 【字体:大中小】
各市、州、直管市、神农架林区食品药品监督管理局:
为加强药品GMP飞行检查管理,规范飞行检查工作程序,省局制定了《药品GMP飞行检查工作程序》,现印发给你们,请遵照执行。
二00七年八月十五日
药品GMP飞行检查工作程序
为加强药品GMP飞行检查管理,规范飞行检查工作程序,根据《湖北省药品GMP飞行检查暂行规定》,制定本工作程序。
一、省局药品审评认证中心(以下简称中心)受省局的委托,具体组织实施GMP飞行检查。
二、药品GMP飞行检查的企业名单及检查范围由省局药品安全监管处确定。
三、药品GMP飞行检查的具体时间由中心根据实际情况确定。
四、中心负责下发《药品GMP飞行检查通知》(附件1),一式两份,于检查组到达被检查企业后分别交给企业及所在地药监局。
五、中心负责制定《药品GMP飞行检查实施方案》(附件2),内容包括检查单位、检查范围、检查时间、检查程序、重点检查内容、需要核实的问题、检查组组成及分工等。
六、中心负责抽调检查员。
中心在抽调检查员时要告知检查员所在单位,检查员参加检查时要向所在单位报告。
各级食品药品监督管理局和药品检验所要全力支持检查员的工作。
中心要加强对检查员工作的考核,对不符合要求或不能参加现场检查工作的不再聘任。
七、检查组由2至3名药品GMP检查员、药品生产监督检查员和药检所技术人员组成,根据检查工作需要可以邀请有关专家参加检查。
对有举报、投诉或有违法案件线索的飞行检查,省局稽查分局须派人参加。
八、检查组成员应到中心指定的地点集中,到达时间由中心适时通知被检查企业所在地市(州)局,检查组适时将被检查企业告知所在地市(州)局。
市(州)局派一名观察员协助检查组工作并负责安排检查组的食宿、交通等,费用由中心按规定的标准统一承担。
九、检查组到达被检查企业后,及时召开首次会议,通报检查要求,签订《药品GMP
飞行检查纪律》(附件3)。
十、检查组在被检查企业显著位置张贴公告(附件4),公布检查事由和联系方式。
因企业被举报实施的飞行检查,应尽可能与举报人取得联系。
十一、检查组在现场检查过程中应注意及时取证,对不符合药品GMP的设施、设备、物料和现场情况进行拍摄和记录,对相关文件资料等进行复印,对有关人员进行调查询问。
必要时,通知当地药监局依法采取先行登记保存或查封扣押措施。
十二、在现场检查过程中。
检查员应及时做好《药品GMP飞行检查现场记录》(附件5)、详细记录检查时间、地点、现场状况、发现的问题、询问对象和内容等。
十三、检查组对有关问题的核实情况,如实填写《药品GMP飞行检查查实问题》(附件6)表,并经企业负责人和检查组全体人员签字。
企业拒绝签字的,检查组应予说明,由2名以上检查员签字。
十四、检查组撰写《药品GMP飞行检查报告》(附件7),检查报告包括检查过程及内容、核实的情况、缺陷项目、结论及处理建议等。
要求根据《药品GMP认证检查评定标准》,将检查过程中存在的问题与具体的缺陷项目条款号相对应。
十五、被检查企业负责人或相关负责人在《药品GMP飞行检查缺陷项目表》(附件8)上签字,双方各执一份,拒绝签字的,检查组应予说明,由2名以上检查员签字。
十六、召开末次会议,检查组向被检查企业通报检查情况,并将检查报告交企业。
被检查企业对检查结果有异议的,应提交书面说明。
十七、检查组在完成检查后及时将药品GMP飞行检查报告、药品GMP飞行检查缺陷项目表、药品GMP飞行检查查实问题、药品GMP飞行检查工作记录、企业的书面说明及相关证据资料等一并上交中心。
十八、中心对药品GMP飞行检查报告及有关资料进行审核,提出审核意见,报分管局领导审查同意后将所有资料一并转交省局药品安全监管处。
省局药品安全监管处负责对检查报告的综合审核和呈报。
十九、组织和实施飞行检查的有关人员应遵守工作纪律,不得泄漏飞行检查的有关情况和举报人信息,并对被检查单位提供的信息资料负保密责任。
二十、检查组不应向被检查企业摊派任何费用。
被检查企业所在地市(州)局应协助做好检查工作。
二十一、本办法自发布之日起实施。
