产品初始污染菌检测记录
初始污染菌数检测记录表

计算方法:菌数/件次=平均菌数×稀释倍数/件次
批准:检验:复核:
批准:检验:复核:
样品名称
规格型号
进货批号
检验日期
检验依据
GB15980-1995
报告日期
培养基名称
营养琼脂培养基
培养
温度
30℃-35℃
稀释
倍数
1:10
1:100
1:1000
阴性
对照
碟号
1
2
1
2
1
2
1
2
接种量(ml)
1
1
1
1
1
1
1
1
培养天数及结果
1
2
3
4
5
结论
细菌:
标准要求:
产品初始污染菌数:灭菌产品管道类内腔≤10cfu/件次;外部≤100 cfu/件次;非管道类≤100 cfu/件次;敷料类≤100 cfu/g
初始污染菌数检测
样品名称
一次性使用输液器带针
检测日期
检测数量
报告日期
检测依据
GB15980-1995
培养基
普通琼脂培养基
内腔
外部
标准
≤10cfu/件次
标准
≤100cfu/件次
序号
平皿上菌数菌数结果序号平皿上菌数菌数
结果
1#
2#
平均
1#
2#
平均
1
1
2
2
3
3
4
4
5
5
6
6
7
7
8
8
9
9
计算方法:菌数/件次=平均菌数×稀释倍数/件次
初始污染菌校正因子的测定报告

深圳市麦瑞科林科技有限公司初始污染菌校正因子确认报告文件编号:___________版本号:___________受控状态:___________分发编号:___________持有部门:___________2010-06-03发布2010-06-10实施编制:审核:批准:目录1 概述2确认依据4 确认过程3.1洗脱液的制备3.2 营养琼脂培养基的制备3.3 接种3.4 培养3.5 菌落计数5 校正因子的计算6 确认结论7 再确认1 概述公司制定的《初始污染菌检测作业指导书》是用于描述产品中的活微生物群体。
但准确地确定初始污染菌是不可能的,因此,在实践中,采用校正因子将活菌计数转换成产品中初始污染菌评估,此因子用于补偿洗脱效率。
2 确认依据ISO 11737.1-2006医疗器械的灭菌微生物方法第1部分:产品上微生物总数的测定方法进行测定。
3 确认过程3.1 洗脱液的制备:分别选取三支新制备的样品一次性使用采血针、宫颈采样拭子,在净化工作台上,用无菌剪刀将每支样品剪碎,称重,放入事先灭菌的具塞三角瓶中,加入约(样品重量×10)ml的pH7.0 氯化钠-蛋白胨灭菌洗脱液,加塞,充分震荡,使样品得到充分的洗脱,然后将洗脱液转移到另一个无菌的具塞三角瓶中,立即盖好备用。
3.2 营养琼脂培养基的制备:将市售的营养琼脂培养基产品按说明书要求进行配制,然后在121℃高压蒸气消毒器内灭菌15min,放入50℃左右的水浴中备用。
3.3 接种:在净化工作台上,用移液管吸取1ml上述制备的洗脱液注入经过灭菌的平皿内,将约15-20ml已融化的45℃左右的营养琼脂培养基倾注到平皿中,并立即旋摇平皿,使水样与培养基充分混匀。
同样方法每组洗脱液做12个平行试验,同时另用一个平皿只倾注1ml灭菌洗脱液于营养琼脂培养基内作为空白对照。
3.4 培养:待上述培养基冷却凝固后,翻转平皿,使低面朝上,置于36±1℃恒温箱中培养48±2h。
初始污染菌检测记录
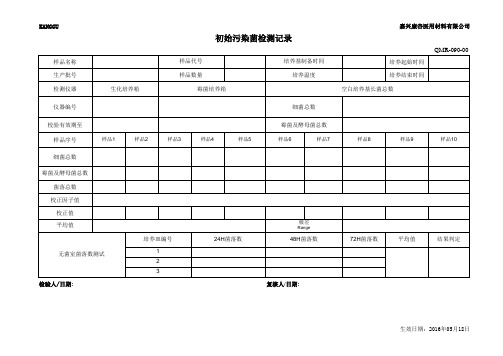
样品7
样品8
样品9
样品10
细菌总数 霉菌及酵母菌总数
菌落总数 校正因子值
校正值 平均值
无菌室菌落数测试
检验人/日期:
培养皿编号
1 2 3
24H菌落数
极差
Range
48H菌落数
72H菌落数
平均值
结果判定
复核人/日期:
生效日期:2016年05月18日
KANGGU
样品名称 生产批号 检测仪器
生化培养箱
初始污染菌检测记录
样品代号 样品数量
霉菌培养箱
培养基制备时间 培养温度
嘉兴康谷医用材料有限公司
QMR-090-00 培养起始时间 培养结束时间 空白培养基长菌总数
仪器编号
细菌总数
校验有效期至 样品序号
样品1
ห้องสมุดไป่ตู้
样品2
样品3
样品4
样品5
霉菌及酵母菌总数
样品6
医疗器械初始污染菌检验

起草人/日期 审核人/日期批准人/日期 分发部门 品质部1、目的检测产品灭菌前实际带菌(活的微生物群)的数目。
2、适用范围适用于本公司产品初始污染菌的检测。
3、职责由品管部负责执行实施。
4、检测程序4.1检验频次:车间生产的产品三个月做一次初始污染菌检验,至少抽取3个批次进行检测,对不同车间和材质的产品进行轮流循环抽样。
标准作业规程标准要求4.2取样方法4.3试验方法4.3.1配制洗脱液4.3.1.1称量4.3.1.2溶解4.3.1.3洗脱液分装用电子太平准确称取9gNaCl 。
用灭菌镊子于同一个批次三个大包装(三个以上员工的产品)中至少随机抽取90g 或抽取12个最小销售包装样品,1/3样品用于检测,1/3样品用于留样,另1/3样品(可就地封存)必要时用于复检。
装入无菌的塑料袋中,立即密封好(塑料袋上应标示产品的生产日期、定单编号、规格、生产车间、员工姓名、产品代号)并立即送检,送检中不得打开塑料袋,三分之一用于测试,三分之一用于留样,三分之一必要复试。
样品最小包装不应有破损,检验前不得开启。
将已称好9gNaCl 溶于1000ml 蒸馏水中,充分搅拌直至完全溶解。
4.3.1.4洗脱液灭菌4.3.2样品处理4.3.2.1样品制备4.3.2.2 样品混匀4.3.2.3吸取样液4.3.2.4平板倾注法称取9gNaCl溶于1000ml蒸馏水中,然后用锥形瓶分装,每瓶100ml(可以根据实验的需要分装不同体积的液体)。
在 100 级净化工作台条件下用无菌方法打开用于检测的至少3个包装,从每个包装中随机取样,准确称取l0g土1g样品.用灭菌剪刀和镊子把样品剪碎.样品剪碎后用灭菌镊子加入到100ml的洗脱溶液中,将装有样品的锥形瓶靠压在旋涡混合器上的施转垫上振荡(2800次/min)2min。
如被检样品是吸水量较高的材料而导致不能吸出足够样液时,洗脱液量可按每次50ml,递增,直至能吸出足够测试在无菌操作台中,待上述生理盐水样液自然沉降后取上清液,用灭菌移液管从锥形瓶中吸取1ml样品的洗脱液转移到无菌平皿。
初始污染回收率及检测记录
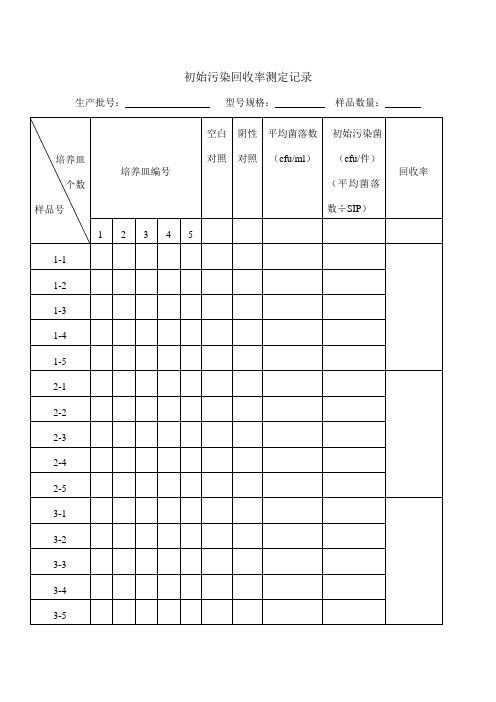
初始污染回收率测定记录生产批号:型号规格:样品数量:培养皿个数样品号培养皿编号空白对照阴性对照平均菌落数(cfu/ml)初始污染菌(cfu/件)(平均菌落数÷SIP)回收率1 2 3 4 51-1 1-2 1-3 1-4 1-5 2-1 2-2 2-3 2-4 2-5 3-1 3-2 3-3 3-4 3-54-14-24-34-44-55-15-25-35-45-5平均回收率修正系数初始污染菌检测原始记录生产批号:型号规格:样品数量:培养皿个数样品号培养皿编号阴性对照空白对照平均菌落数(cfu/SIP)初始污染菌(cfu/件)1 2 3 4 51 2 3 4 5 6 7 8 91011121314151617181920平均初始污染菌各样品平均菌落——————数总和÷样品数校正后初始污染菌————(平均初始污染菌*校正因子)注:1、在对照的平板中,“+”表示长菌,“-”表示不长菌,“±”表示可疑长菌2、阳性对照管应生长良好,阴性对照管不得有菌生长。
否则,试验无效。
初始污染检测记录文件编号:样品名称:生产批号:型号规格:样品数量:培养皿个数样品号空白对照阳性对照培养皿编号平均菌落数(cfu/SIP)初始污染菌(cfu/件)1 2 3 4 512345678910平均初始污染菌(cfu/件)校正后初始污染菌注:1、在对照的平板中,“+”表示长菌,“-”表示不长菌,“±”表示可疑长菌2、阳性对照管应生长良好,阴性对照管不得有菌生长。
否则,试验无效。
初始污染菌检验记录
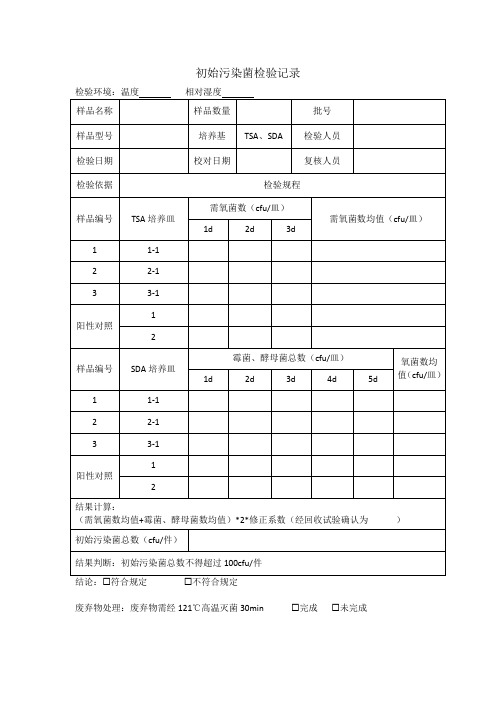
初始污染菌检验记录
相对湿度
样品数量
批号
样品型号
培养基 TSA、SDA 检验人员
检验日期
校对日期
复核人员
检验依据
检验规程
样品编号 TSA 培养皿
1
1-1
2
2-1
需氧菌数(cfu/皿)
1d
2d
3d
需氧菌数均值(cfu/皿)
3
3-1
1 阳性对照
2
样品编号 SDA 培养皿
1
1-1
霉菌、酵母菌总数(cfu/皿)
氧菌数均
1d
2d
3d
4d
5d 值(cfu/皿)
2
2-1
3
3-1
1 阳性对照
2
结果计算:
(需氧菌数均值+霉菌、酵母菌数均值)*2*修正系数(经回收试验确认为
)
初始污染菌总数(cfu/件)
结果判断:初始污染菌总数不得超过 100cfu/件
结论:符合规定
不符合规定
废弃物处理:废弃物需经 121℃高温灭菌 30min
完成 未完成
3 产品初包装初始污染菌的验证报告

产品初包装初始污染菌的验证报告编号:YFB100301编制:评审:评审组成员批准:日期:有限公司一、验证目的确定公司产品初包装高密度聚乙烯袋在贮存过程中不破损、无污染,具有防护能力,并确定高密度聚乙烯袋的贮存期限。
二、验证范围适用于本公司产品(XXXXXX)的初包装-xxxxx的贮存时限的验证。
三、验证依据GB15979-2002一次性使用卫生用品卫生标准聚乙烯袋四、验证小组成员五、验证项目产品初包装高密度聚乙烯袋初始污染菌在产品初包装贮存过程中的变化情况,并确定高密度聚乙烯袋的贮存期限。
六、验证过程及结果1.对采购进厂的初包装在进厂时和贮存3个月、6个月、9个月及12个月后的初始污染菌分别进行检测。
2.检测结果:1.运输包装医用XXXXX 的应该以 个为单元装入双层聚乙烯塑料袋内,再装入纸箱。
纸箱应能充分保护小包装在运输贮存过程不受损坏、污染。
2.小包装的贮存时间储存3个月、6个月、9个月的的初始污染菌符合要求。
储存12个月的高密度聚乙烯袋的初始污染菌虽然合格,但已接近不合格范围了,所以小包装自进厂之日起最长贮存时间不得超过9个月。
八. 验证的周期产品初包装高密度聚乙烯袋初始污染菌的验证周期为2年贮存期 细菌数(cfu/ 100cm 2)真菌数(cfu/ 100cm 2)大肠埃希菌(cfu/ 100cm 2)进厂时 3个月 6个月 9个月 12个月九.附表:产品初包装高密度聚乙烯袋初始污染菌微生物检查记录内包装袋微生物限度检查记录检验人:日期:年月日复核人:日期:年月日内包装材料初始污染菌微生物检查记录检验人:日期:年月日复核人:日期:年月日。
初始污染菌校正因子的测定报告(模板)

初始污染菌校正因子确认报告1.概述公司制定的《初始污染菌检验规程》是用于描述产品中的活微生物群体。
但准确地确定初始污染菌是不可能的,因此,在实践中,采用校正因子将活菌计数转换成产品中初始污染菌评估,此因子用于补偿洗脱效率。
2.检验依据ISO 11737.1-2006医疗器械的灭菌微生物方法第1部分:产品上微生物总数的测定方法进行测定。
中国药典2015版第四部 1105 非无菌产品微生物限度3.实验过程3.1 洗脱液的制备:分别选取三支新制备的样品,在净化工作台上,用无菌医用钳将每支样品剪碎,称重10g,放入事先灭菌的具塞三角瓶中,加入约(样品重量×10)ml的pH7.0 氯化钠-蛋白胨灭菌洗脱液,加塞,充分震荡,使样品得到充分的洗脱,然后将洗脱液转移到另一个无菌的具塞三角瓶中,立即盖好备用。
3.2 营养琼脂培养基的制备:将营养琼脂培养基按说明书要求进行配制,在121℃高压蒸气灭菌锅内灭菌15min,放入50℃左右的水浴中备用。
3.3 接种:在净化工作台上,用移液管吸取1ml上述制备的洗脱液注入经过灭菌的平皿内,将约15-20ml已融化的45℃左右的营养琼脂培养基倾注到平皿中,并立即旋摇平皿,使水样与培养基充分混匀。
同样方法每组洗脱液做10个平行试验,同时另用一个平皿只倾注1ml灭菌洗脱液于营养琼脂培养基内作为空白对照。
3.4 培养:待上述培养基冷却凝固后,翻转平皿,使低面朝上,置于36±1℃恒温箱中培养48±2h。
3.5 菌落计数:记录各平皿中的菌落数,取平均值,然后再乘以洗脱液总体积数(ml),即得到洗脱液中的全部菌落数。
重复3.1-3.5步,分别进行第二次、第三次、第四次、第五次洗脱,其中第五次洗脱为直接将四次洗脱后的产品接种于培养基内,将五次洗脱后所得的菌落数分别填入数据表1、表2。
4.校正因子的计算用第一次洗脱液得到的菌落数除以五次洗脱得到的总菌落数,得到第一次冲洗去除率,取三个样品的第一次冲洗去除率的平均值,平均值的倒数即为校正因子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
产品初始污染菌检测记录
规格型号
ISM-QR-0075-A/0
生产批 号
抽样数 量
检验依 据
检验日 期
供试液制备:取
待测试产品,根据产品物性的大小,分别采用直接浸入法或
棉拭子擦洗法或冲洗法收集洗脱液,制取 1:10 供试液。保温于 45℃水浴中 5~10min,
不时振摇。
试验操作:1.取营养琼脂培养基 个,分别接各种供试品各 ml。
培养皿 1#
号
洁净台 菌落数
48h 菌落 数
平均菌 落数
检验结果
培养基名称
营养琼脂培养基
培养温度
37℃ 48h
细
平
1:10
菌
皿
平
行
数 样
号 1#
ห้องสมุดไป่ตู้
2#
Ⅰ
Ⅱ
Ⅲ
Ⅳ
Ⅴ
菌落均值
菌落总数(cfu/件)
2#
1:100
1#
2#
3# 空白对照
检验结论
检定标准:菌落计数的报告,菌落数在 100 以内时,按实有数值 报告。在报告菌落数为“不可记”时,应表明样品的稀释度。参 考标准:菌落总数≤10cfu/件
检定结果:
备注
如果样品菌落总数超过标准的规定,按(复检方法)进行复检和 撰写结果报告
照)。
2.取营养琼脂培养基
个加
%无菌氯化钠溶液做空白对照(阴性对
3.转动平皿,使供试液与培养基充分混匀。将已经凝固的平板倒置于 37℃ 培养箱中,一般培养 48±2h。
计算平板上的菌落数。
培养基预培养:营养琼脂培养基: 月 日 时 至 月 日 时 (16-18h)
紫外线消毒时间:实验前: 时 分 至 时 分()实验后: 时 分 至 时 分()
