肺粘液表皮样癌的CT诊断
肺部结节的CT鉴别诊断-肺部磨玻璃样病变

中分化腺癌与BAC混合亚型
23
46/F 右肺癌术后发现左上肺结节
腺癌与BAC混合亚型
2022/2/7
24
44/F 发现肺内多发结节
2022/2/7
右中肺粘液型BAC、右下肺AAH
25
66/F 发现肺内多发结节
2022/2/7
两上肺多发BAC、左下肺AAH
26
57/F 因发热10天CT检查发现左上肺结节
BAC(炎症型)
2022/2/7
38
65/F 痰血1周
BAC (炎症
型)
2022/2/7
39
52/M
BAC
2022/2/7
40
47/F,乳癌术后
抗炎治疗后消失
2022/2/7
另一例FGGO抗炎 治疗后消失
41
57/F
腺癌与BAC 混合亚型
2022/2/7
42
53/M 食管癌术后发现左上肺结节
AAH
18
54/M 体检发现右上肺结节
中分化腺癌与BAC混合亚型
2022/2/7
19
50/M 发现左上肺结节
2022/2/7
腺癌与BAC混合亚型
20
50/M 咳嗽一周。
2022/2/7
炎性GGO
抗炎治疗后
21
45/F 体检发现左下肺结节
腺癌与BAC混合亚型
2022/2/7
22
20d
2022/2/7
左上肺球形 肺炎
2022/2/7
抗炎治疗后
27
41/F 发现右肺占位一周
2022/2/7
细支气管肺泡癌
28
41/F 发现右肺占位一周
31例原发性肺黏液腺癌的CT表现与病理特点分析

31例原发性肺黏液腺癌的CT表现与病理特点分析英天舒;张晓晔【摘要】Objective To analyze the CT manifestations and pathological features of primary lung mucinous adenocarci -noma.Methods 31 cases of primary lung mucinous adenocarcinoma were selected ,all patients were diagnosed to be lung mucin-ous adenocarcinoma by pathology , preoperative imaging data and relevant pathological data werecomplete .Results Peripheral type was 26 cases (83.9%),central type was 5 cases (16.1%),irregular nodules,ground glass sign was 14 cases (45.2%), spicule sign was 11 cases (35.5%),lobulated sign was 14 cases(45.2%).Conclusion Primary pulmonary mucinous adeno-carcinoma mainly is peripheral type .The clinical manifestations lack of specificity .The CT image has a certain specificity ,it can present irregular mass shadow with soft tissue density or ground glass nodules ,with lobulated and spiculesign .%目的分析原发性肺黏液腺癌的CT表现及病理特点.方法选取31例原发性肺黏液腺癌患者的临床资料,全部病例均经病理检查确诊为肺黏液腺癌,且术前影像资料和相关病理资料均完整.结果 31例病例中,周围型26例(83.9%),中央型5例(16.1%),不规则、磨玻璃结节14例(45.2%)、伴毛刺征11例(35.5%)、分叶征14例(45.2%).结论原发性肺黏液性腺癌,以周围型居多,临床表现缺乏特异性.其CT影像表现具有一定特异性,可呈现为软组织密度不规则团块影或磨玻璃结节,伴分叶征、毛刺征.【期刊名称】《实用癌症杂志》【年(卷),期】2016(031)004【总页数】3页(P567-568,571)【关键词】原发性肺黏液腺癌;CT;病理【作者】英天舒;张晓晔【作者单位】110022 中国医科大学附属盛京医院;110022 中国医科大学附属盛京医院【正文语种】中文【中图分类】R734.2原发性肺黏液腺癌(primary pulmonary mucinous adenocarcinoma,PPMA),又称胶样腺癌,是1种特殊类型的腺癌,仅占其0.25%,属肺腺癌的1种较少见的病理亚型[1-3]。
2例胸腺黏液表皮样癌
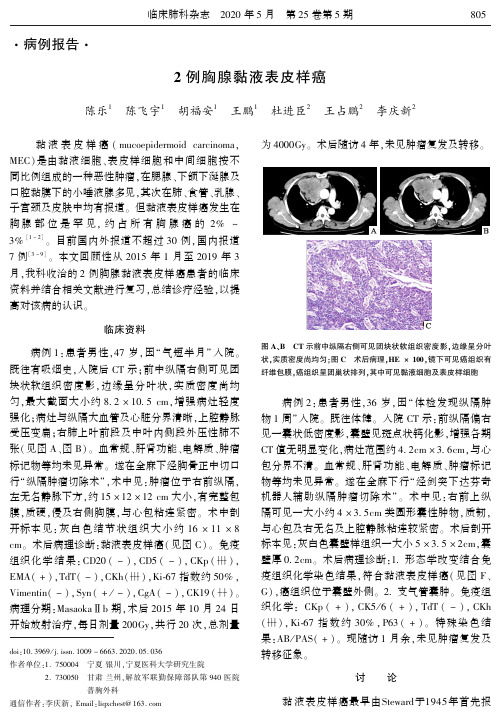
病例报告2例胸腺黏液表皮样癌陈乐1㊀陈飞宇1㊀胡福安1㊀王鹏1㊀杜进臣2㊀王占鹏2㊀李庆新2doi:10.3969/j.issn.1009-6663.2020.05.036作者单位:1.750004㊀宁夏银川ꎬ宁夏医科大学研究生院2.730050㊀甘肃兰州ꎬ解放军联勤保障部队第940医院普胸外科通信作者:李庆新ꎬEmail:liqxchest@163.com㊀㊀黏液表皮样癌(mucoepidermoidcarcinomaꎬMEC)是由黏液细胞㊁表皮样细胞和中间细胞按不同比例组成的一种恶性肿瘤ꎬ在腮腺㊁下颌下涎腺及口腔黏膜下的小唾液腺多见ꎬ其次在肺㊁食管㊁乳腺㊁子宫颈及皮肤中均有报道ꎮ但黏液表皮样癌发生在胸腺部位是罕见ꎬ约占所有胸腺癌的2%~3%[1-2]ꎮ目前国内外报道不超过30例ꎬ国内报道7例[3-9]ꎮ本文回顾性从2015年1月至2019年3月ꎬ我科收治的2例胸腺黏液表皮样癌患者的临床资料并结合相关文献进行复习ꎬ总结诊疗经验ꎬ以提高对该病的认识ꎮ临床资料病例1:患者男性ꎬ47岁ꎬ因 气短半月 入院ꎮ既往有吸烟史ꎬ入院后CT示ꎻ前中纵隔右侧可见团块状软组织密度影ꎬ边缘呈分叶状ꎬ实质密度尚均匀ꎬ最大截面大小约8 2ˑ10 5cmꎬ增强病灶轻度强化ꎻ病灶与纵隔大血管及心脏分界清晰ꎬ上腔静脉受压变扁ꎻ右肺上叶前段及中叶内侧段外压性肺不张(见图A㊁图B)ꎮ血常规㊁肝肾功能㊁电解质㊁肿瘤标记物等均未见异常ꎮ遂在全麻下经胸骨正中切口行 纵隔肿瘤切除术 ꎬ术中见:肿瘤位于右前纵隔ꎬ左无名静脉下方ꎬ约15ˑ12ˑ12cm大小ꎬ有完整包膜ꎬ质硬ꎬ侵及右侧胸膜ꎬ与心包粘连紧密ꎮ术中剖开标本见:灰白色结节状组织大小约16ˑ11ˑ8cmꎮ术后病理诊断:黏液表皮样癌(见图C)ꎮ免疫组织化学结果:CD20(-)ꎬCD5(-)ꎬCKp( )ꎬEMA(+)ꎬTdT(-)ꎬCKh( )ꎬKi ̄67指数约50%ꎬVimentin(-)ꎬSyn(+/-)ꎬCgA(-)ꎬCK19( )ꎮ病理分期:MasaokaⅡb期ꎬ术后2015年10月24日开始放射治疗ꎬ每日剂量200Gyꎬ共行20次ꎬ总剂量为4000Gyꎮ术后随访4年ꎬ未见肿瘤复发及转移ꎮ图A㊁B㊀CT示前中纵隔右侧可见团块状软组织密度影ꎬ边缘呈分叶状ꎬ实质密度尚均匀ꎻ图C㊀术后病理ꎬHEˑ100ꎬ镜下可见癌组织有纤维包膜ꎬ癌组织呈团巢状排列ꎬ其中可见黏液细胞及表皮样细胞㊀㊀病例2:患者男性ꎬ36岁ꎬ因 体检发现纵隔肿物1周 入院ꎮ既往体健ꎮ入院CT示:前纵隔偏右见一囊状低密度影ꎬ囊壁见斑点状钙化影ꎬ增强各期CT值无明显变化ꎬ病灶范围约4 2cmˑ3 6cmꎬ与心包分界不清ꎮ血常规㊁肝肾功能㊁电解质㊁肿瘤标记物等均未见异常ꎮ遂在全麻下行 经剑突下达芬奇机器人辅助纵隔肿瘤切除术 ꎮ术中见:右前上纵隔可见一大小约4ˑ3 5cm类圆形囊性肿物ꎬ质韧ꎬ与心包及右无名及上腔静脉粘连较紧密ꎮ术后剖开标本见:灰白色囊壁样组织一大小5ˑ3 5ˑ2cmꎬ囊壁厚0 2cmꎮ术后病理诊断:1 形态学改变结合免疫组织化学染色结果ꎬ符合黏液表皮样癌(见图F㊁G)ꎬ癌组织位于囊壁外侧ꎮ2 支气管囊肿ꎮ免疫组织化学:CKp(+)ꎬCK5/6(+)ꎬTdT(-)ꎬCKh( )ꎬKi ̄67指数约30%ꎬP63(+)ꎮ特殊染色结果:AB/PAS(+)ꎮ现随访1月余ꎬ未见肿瘤复发及转移征象ꎮ讨㊀㊀论黏液表皮样癌最早由Steward于1945年首先报508临床肺科杂志㊀2020年5月㊀第25卷第5期图D㊁E㊀CT示前纵隔偏右见一囊状低密度影ꎬ囊壁见斑点状钙化影㊀㊀图F㊁G㊀术后病理ꎬHEˑ100ꎬ镜下癌组织中见表皮样细胞及黏液细胞ꎬ并可见大量黏液道并命名[10]ꎬ于腮腺㊁下颌下涎腺及口腔黏膜下的小唾液腺多见ꎬ其次在肺㊁食管㊁乳腺及皮肤中均有报道ꎮ但胸腺黏液表皮样癌于1980年以后才被报道[11-12]ꎬ目前国外报道不超过30例ꎬ国内报道7例[3-9]ꎮ有文献报道黏液表皮样癌的发生与t(11ꎻ19)染色体易位和MECT1 ̄MAML2(mucoepidermoidcarcinomatranslocated1 ̄mastermind ̄like2ꎬMECT1 ̄MAML2)基因重排ꎬ最常见的染色体易位是t(11ꎻ19)(q21ꎻp13)ꎮt(11ꎻ19)(q21ꎻp13)染色体涉及的两个基因MECT1㊁MAML2分别位于19p13和11q21ꎮ这种易位产生一个新的融合产物ꎬ即MECT1 ̄MAML2ꎮ它融合了MECT1的外显子1和MAML2的外显子2~5ꎮMECT1 ̄MAML2融合蛋白产物ꎬ对Notch信号通路阻断ꎬ激活cAMP/CREB(cAMPresponseelement ̄bindingproteinꎬCREB)转录ꎬ从而阻断Notch和CREB信号转导通路ꎬ诱导肿瘤的发生[13]ꎮRoden等[14]报道了2例胸腺黏液表皮样癌也存在MAML2基因重排ꎬMAML2基因重排可作为黏液表皮样癌与鳞癌和腺鳞癌的鉴别诊断中一项依据ꎬ可能存在其他通路诱导胸腺黏液表皮样癌的发生ꎮ胸腺黏液表皮样癌(TMEC)是一种罕见的胸腺癌ꎬ占胸腺恶性肿瘤的2%~3%[1-2]ꎮ研究显示它的发病年龄在8~84岁ꎬ年龄在40~60岁之间的患者中多见ꎮ胸腺黏液表皮样癌的临床症状与肿瘤的大小及位置ꎬ主要是肿瘤对周围组织压迫ꎬ早期因肿瘤体积较小对周围组织无明显侵犯ꎬ无明显临床症状ꎬ待肿瘤逐渐增大后对周围组织压迫时多表现为胸闷㊁气短㊁胸骨后疼痛ꎬ若肿瘤继续增大时可出现颈部㊁颜面部肿胀ꎬ声音嘶哑和膈肌膨升等表现ꎬ全身可有乏力及体重减轻等表现[15]ꎮWoo等[16]报道1例重症肌无力的胸腺黏液表皮样癌ꎬ手术切除后重症肌无力症状仍然存在ꎮ本文中2组病例均为男性ꎬ1例临床表现为气短ꎬ1例为体检发现ꎬ与文献报道基本吻合ꎮ胸腺黏液表皮样癌与其他胸腺病变相比并无临床特异性ꎬ影像学表现亦无特异性ꎮ胸腺黏液表皮样癌影像学表现可分为囊性肿块和实性肿块ꎬ边界清楚ꎬ病变组织密度不均匀ꎬ部分增强后有明显不均匀强化ꎬ强化明显部分与血管相仿ꎮ本文中病例1患者行胸部增强CT后可见轻度强化ꎬ病例2患者行胸部增强CT后无明显强化ꎬ与文献[3]报道相符合ꎮ考虑胸腺黏液表皮样癌目前多为个案报道ꎬ根据胸腺黏液表皮样癌的临床症状ꎬ影像学表现并无明显特异性ꎮ对于TMEC的术前诊断比较困难ꎬ诊断主要依靠组织病理学形态特点及免疫组织化学染色ꎮTMEC的组织学特征与唾液腺等部位相似ꎮ显微镜下可见表皮样细胞㊁黏液细胞及中间细胞ꎬ也可见嗜酸性细胞ꎮ邻近肿瘤的非肿瘤性胸腺组织可见囊性变或黏液性化生[17]ꎮ贾雯等[4]报道肿瘤主要由片状分布的表皮样细胞㊁黏液细胞及中间细胞构成ꎮ黏液细胞呈灶状或散在分布ꎬ中间细胞常呈实性条索或片状ꎻ表皮样细胞呈巢状或片状排列ꎬ部分区域形成囊腔ꎬ细胞界限清楚ꎮ周围组织汇总可见萎缩胸腺组织ꎮ胸腺黏液表皮样癌根据肿瘤内囊实性成分所占比例不同㊁细胞异型性㊁核分裂像及是否伴有神经侵犯和坏死的情况分为:低度恶性㊁中度恶性㊁高度恶性[18-19]ꎮ也可根据肿瘤细胞多表现大小㊁核分裂像多少以及相关细胞分化特点的显现等可将肿瘤分为高㊁中㊁低分化三种类型ꎮ胸腺瘤与胸腺癌采用Masaoka分期系统[20]ꎮ分期如期:Ⅰ期:包膜完整ꎬ镜下无包膜浸润ꎻⅡa期:镜下包膜浸润ꎬⅡb期:肿瘤浸润包膜外纵隔脂肪或肿瘤与临近胸膜ꎬ心包粘连ꎻⅢ期:侵犯邻近组织器官ꎻⅣa期:胸膜与心包种植播散ꎬⅣb期:远处淋巴结及血行转移ꎮ因此根据Masaoka分期并结合组织学分型判断预后是有效的ꎬ高级别的患者5年生存率较低ꎮTMEC的治疗首选手术完整切除病灶㊁局部淋巴结清扫及尽可能切除周围受侵犯的组织器官ꎮ手608临床肺科杂志㊀2020年5月㊀第25卷第5期术方式多采用胸骨正中切口㊁前外侧㊁后外侧切口或腋下切口开胸手术ꎬ胸腔镜手术或达芬奇手术ꎮ胸腔镜手术具有创伤小㊁疼痛轻㊁并发症少及恢复快等优势ꎬ随着技术不断的发展ꎬ达芬奇机器人手术具有病灶定位更精确㊁创伤更小㊁操作更灵活ꎬ切除更彻底等优势ꎮ但手术切除是治疗低级别肿瘤的首选治疗方案ꎬ考虑高级别(低分化)局部侵袭强和易远处转移ꎬ因此对高级别(低分化)或有复发的TMECꎬ外科手术将病灶切除后还需积极行放疗和化疗ꎬ延长患者生存期ꎮLiu等[21]报道胸腺癌对放疗敏感度较高ꎬ并报告术后放疗可使局部复发率降低至17%ꎬ对TMEC可以选择用放疗ꎬ延长患者生存期ꎮFuse等[22]报道称伊立替康+顺铂联合的化疗方案ꎬ患者出现3个月的完全缓解ꎮ因此对不能手术的患者ꎬ采用放疗及化疗结合的治疗方案ꎬ延长患者生存期ꎮTMEC预后普遍较差ꎬ高中分化生存时间较低分化型长ꎮ本文中病例1患者病灶侵犯胸膜ꎬ术后行放疗ꎬ随访4年ꎬ未见肿瘤复发及转移ꎮ综上所述ꎬ胸腺黏液表皮样癌发病率低且临床症状㊁体征和影像学检查均无明显特异性ꎮ诊断主要依靠术后病理及免疫组织化学结果ꎮ目前对于胸腺黏液表皮样癌的治疗首选手术完整切除ꎮTMEC预后普遍较差ꎬ高中分化生存时间较低分化型长ꎬ因此对TMEC采用手术治疗及放疗㊁化疗ꎬ改善患者生存质量ꎬ延长患者生存时间ꎮ本文中病例1因病灶较大ꎬ与周围组织及器官粘连ꎬ因此选择胸骨正中切口ꎬ病例2因病灶较小ꎬ与周围组织界限较为清晰ꎬ故选择达芬奇手术ꎬ患者术后恢复好ꎮ但手术具体选择哪种手术方式ꎬ需要临床医师慎重考虑ꎮ参考文献[1]㊀SNOVERDCꎬLEVINEGDꎬROSAIJ.Thymiccarcinoma.Fivedistinctivehistologicalvariants[J].AmJSurgPatholꎬ1982ꎬ6(5):451-470.[2]㊀TANAKAMꎬSHIMOKAWARꎬMATSUBARAOꎬetal.Mucoepi ̄dermoidcarcinomaofthethymicregion[J].ActaPatholJpnꎬ1982ꎬ32(4):703-712.[3]㊀尤小芳ꎬ肖湘生ꎬ孙希文.胸腺黏液表皮样癌1例[J].中国医学影像技术ꎬ2012ꎬ28(2):210.[4]㊀贾雯ꎬ马小兵.胸腺黏液表皮样癌1例[J].临床与实验病理学杂志ꎬ2015ꎬ31(8):959-960.[5]㊀盛峰喜ꎬ黄壮士ꎬ李丰科ꎬ等.胸腺黏液表皮样癌一例并文献复习[J].郑州大学学报(医学版)ꎬ2018ꎬ53(2):264-267. [6]㊀张薇珊ꎬ曾浩ꎬ刘禄ꎬ等.胸腺黏液表皮样癌的临床病理特征[J].临床与病理杂志ꎬ2019ꎬ39(1):218-221. [7]㊀李飞ꎬ李芳ꎬ李勇ꎬ等.胸腺黏液表皮样癌一例报道并文献复习[J].中华肿瘤防治杂志ꎬ2018ꎬ25(20):1466-1469. [8]㊀郑家奎ꎬ白宝音ꎬ刘立明.电视胸腔镜治疗胸腺癌1例报告[J].中国微创外科杂志ꎬ2016ꎬ16(10):956-957. [9]㊀沈莎莎ꎬ常雯ꎬ韩丹ꎬ等.胸腺黏液表皮样癌1例[J].实用放射学杂志ꎬ2019ꎬ35(1):167-168.[10]STEWARTFWꎬFOOTEFWꎬBECKERWF.Muco ̄epidermoidtumorsofsalivaryglands[J].AnnSurgꎬ1945ꎬ122(5):820-844.[11]SUSTERSꎬROSAIJ.Thymiccarcinoma:aclinicopathologyicstudyof60cases[J].Cancerꎬ1991ꎬ67(4):1025-1032.[12]RODENACꎬYIESꎬCASSIVISDꎬetal.Clinicopathologyicfea ̄turesofthymiccarcinomaandtheimpactofhistopathologicala ̄greementonprognosticalstudies[J].EurJCardiothoracSurgꎬ2013ꎬ43(6):1131-1139.[13]NODAHꎬOKUMURAYꎬNAKAYAMATꎬetal.Clinicopathologi ̄calsignificanceofMAML2genesplitinmucoepidermoidcarcino ̄ma[J].CancerSciꎬ2013ꎬ104(1):85-92.[14]RODENACꎬERICKSON ̄JOHNSONMRꎬYIESꎬetal.AnalysisofMAML2rearrangementinmucoepidermoidcarcinomaofthethy ̄mus[J].HumPatholꎬ2013ꎬ44(12):2799-2805.[15]MORANCAꎬSUSTERS.Primarymucoepidermoidcarcinomaofthepleura.Aclinicopathologicstudyoftwocases[J].AmJClinPatholꎬ2003ꎬ120(3):381-385.[16]WOOWLꎬPANAGIOTOPOULOSNꎬGVINIANIDZELꎬetal.Pri ̄marymucoepidermoidcarcinomaofthethymuspresentingwithmy ̄astheniagravis[J].JThoracDisꎬ2014ꎬ6(10):E223-E225. [17]YASUDAMꎬYASUKAWATꎬOZAKIDꎬetal.Mucoepidermoidcarcinomaofthethymus[J].JpnJThoracCardiovascSurgꎬ2006ꎬ54(1):23-26.[18]李佩章ꎬ王英ꎬ黄玲莎ꎬ等.恶性肿瘤患者血浆纤维蛋白原检测的意义[J].中华实用诊断与治疗杂志ꎬ2009ꎬ23(6):566-567.[19]AMSALEMHꎬNADJARIMꎬPRUSDꎬetal.Growingteratomasyn ̄dromevschemotherapeuticretroconversion:casereportandreviewoftheliterature[J].GynecolOncolꎬ2004ꎬ92(1):357-360. [20]MASAOKAAꎬMONDENYꎬNAKAHARAKꎬetal.Follow ̄upstudyofthymomaswithspecialreferencetotheirclinicalstages[J].Cancerꎬ1981ꎬ48(11):2485-2492.[21]LIUQWꎬGUZTꎬYANGFꎬetal.Theroleofpostoperativeradio ̄therapyforstageⅠ/Ⅱ/Ⅲthymictumor ̄resultsoftheChARTret ̄rospectivedatabase[J].JThoracDisꎬ2016ꎬ8(4):687-695. [22]FUSEETꎬKAMIMURAMꎬTAKEDAYꎬetal.Responseofathy ̄micmucoepidermoidcarcinomatocombinationchemotherapywithcisplatinandirinotecan:acasereport[J].LungCancerꎬ2008ꎬ59(3):403-406.[收稿日期:2019-11-27]708临床肺科杂志㊀2020年5月㊀第25卷第5期。
粘液表皮样癌的影像诊断与鉴别诊断

淋巴瘤
谢谢
粘液表皮样癌的影像诊断 与鉴别诊断
概述
➢ 最常见的腮腺恶性肿瘤,中青年多见。 ➢ 无痛性肿块,膨隆浸润性生长,体积较大。 ➢ 不规则、分叶状、边界不清,可见坏死。 ➢ 大部分位于腮腺浅叶。 ➢ 侵犯神经时可引起面瘫;可伴有淋巴结转移。
影像表现
• 分化不同,恶性程度不同,影像表现差异大。 • 高分化型呈良性特征,可见囊变、出血,含有粘液成分
鉴别诊断
淋巴瘤: 原 发 少 见 , 继 发 较 多 , 多 为 N H L 。 可 双 侧 发 病 。 多 数 表 现 多 发 结 节 , T 1 W I 等 信 号 , T 2 W I 稍 高 信 号 , 信 号 较
均匀,坏死囊变少,DWI高信号,ADC低信号。 中度均匀强化。 常 伴 周 围 淋 巴 结 肿 大 。
围侵袭。 • 很少发生淋巴结转移。
❖囊实性多见,体积较大时内部呈筛状 改变。
❖T1WI等或低信号,T2WI等或高信号, 可见分隔状改变。
❖增强扫描可见中或明显强化,病灶常 有线状强化的完整或不完整的包膜。
腺样囊性癌
鉴别诊断
腺泡细胞癌: 中 年 以 上 发 病 率 高 。 是 腮 腺 恶 性 肿 瘤 中 预 后 最 好 的 , 属 于 低 度 恶 性 , 但 常 侵 犯 包 膜 。 可 双 侧 发 病 。 多 数 表 现 为 良 性 特 点 , 与 多 形 性 腺 瘤 难 鉴 别 。 晚 期 发 生 淋 巴 结 转 移 或 血 行 转 移 。 转 移 部 位 常 见 于 肺 和 骨 , 骨 转 移 多 发 生 在 椎 骨 。 长 T 1 长 T 2 , 明 显 强 化 。
较多时,T2WI稍高信号,T1WI低信号。 • 低分化型浸润性生长,实性成分多,粘液少,T2WI信号
多层螺旋CT鉴别孤立型肺黏液腺癌与非黏液浸润性腺癌的应用价值

74·中国CT和MRI杂志 2023年10月 第21卷 第10期 总第168期【通讯作者】钱伟军,男,主任医师,主要研究方向:胸部影像诊断技术。
E-mail:*****************Application Value of Multislice Spiral CT·75CHINESE JOURNAL OF CT AND MRI, OCT. 2023, Vol.21, No.10 Total No.168有异议,由副主任医师经讨论后确定。
1.4 统计学分析 采用SPSS 20.0统计学软件对两组数据进行统计学分析。
对患者年龄、病变大小、Δ病灶直径差值、净强化CT值采用两个独立样本t检验; 对患者的性别、各CT征象构成比采用χ2检验,以P <0.05时,差异有统计学意义。
2 结 果2.1 一般资料 两组患者年龄及性别比较差异无统计学意义(P >0.05)(表1)2.2 两组CT征象比较密度、空泡征、平扫肺窗最大直径差异无统计学意义(P >0.05)。
SPMA组发生在双肺下叶、边缘模糊、混合磨玻璃密度、钙化、空气支气管征、瘤周卫星灶、血管造影征、无强化坏死区、∆病灶直径差值(mm)均高于NMIPA组,差异有统计学意义(P <0.05)。
SPMA发生在双肺上中叶、边缘清晰、实性密度、胸膜牵拉征、转移、平扫纵隔窗最大直径(mm)、∆动、静脉期低于NMIPA 组,差异有统计学意义(P <0.05),见表2。
2.3 两组病灶的参数比较(见表3)2.4 典型病例(见图1-2)图1 男性,65岁,图1A-图1B 右肺下叶胸膜下结节影,肺窗最大直径12mm,纵隔窗最大直径8mm,差值为4mm,边缘模糊,其内小泡征,图1C-图1D 增强CT病灶呈轻度强化。
病理证实肺黏液性腺癌。
1A 1C1B图2 男,62岁,图2A-图2B 右肺上叶结节影,肺窗最大直径18mm,纵隔窗最大直径17mm,差值为1mm,边缘清晰,密度均匀,图2C-图2D 增强CT病灶呈中度强化。
原发性肺涎腺肿瘤的临床及CT表现

原发性肺涎腺肿瘤的临床及CT表现原发性肺涎腺肿瘤属肺低度恶性肿瘤,肿瘤发生于支气管混合性腺体,其肿瘤组织学表现与涎腺肿瘤基本相仿。
2004年版肺及胸膜肿瘤病理分类中将其称为涎腺肿瘤,主要包括黏液表皮样癌(mucoepidermoid carcinoma, MEC)、腺样囊性癌(adenoid cystic carcinoma, ACC)、上皮-肌上皮癌三类。
该类肿瘤临床罕见,发病率在肺原发恶性肿瘤中约为0.1%~0.5%,术前诊断困难。
补充内容-链接:【WHO分类】肺部肿瘤(2015版)原发性肺涎腺肿瘤以ACC及MEC多见,发病年龄均低于常见类型肺癌,文献报道ACC好发年龄为 40-50岁,MEC患者中30岁以下者占50%,男女发病率没有明显差异。
ACC常发生于中央气道( 气管、主支气管或叶支气管) ,在气管原发性恶性肿瘤中占第2位,仅次于鳞状细胞癌;其生长速度缓慢,低度恶性,转移少,局部复发常见;临床病程相对较长,主要症状为刺激性咳嗽、偶伴痰血,肿瘤较大致管腔阻塞,出现进行性呼吸困难、喘鸣、咳嗽、咯血等。
大多数MEC发生在叶或段支气管,最常见症状包括长期咳嗽、咳痰、呼吸困难、反复发作的肺炎,偶尔出现咯血。
该类肿瘤的临床症状无特异性,与肿瘤发生的部位及阻塞气道的程度相关。
因为混合腺和透明软骨存在于3级以上支气管黏膜下层,在更小的气道几乎看不到,因此原发性肺涎腺肿瘤多为中心型,出现在肺的外周部罕见。
ACC来源于支气管黏膜的腺管或腺体的黏液分泌细胞,在气管侧壁及后壁等腺体丰富的区域发病率相对较高,其特异性组织学特征是沿黏膜下和周围浸润性生长,肿瘤范围远远超出肉眼所见。
MEC起源于气管支气管的小涎腺,肿瘤上皮由黏蛋白分泌细胞、鳞状细胞和没有特异性分化的中间型细胞组成。
根据肿瘤细胞异型度、有丝分裂活性、局部侵袭范围及肿瘤坏死情况,分为高分化型和低分化型,以高分化型多见。
肺涎腺肿瘤与发生于口腔大小涎腺的同源肿瘤组织学类似,肌上皮细胞是其特有的细胞成分,是诊断该类肿瘤的关键,肌上皮( 基底) 细胞的抗体如CK17、S-100、P63等阳性表达有助于诊断。
肺粘液表皮样癌的CT影像表现

肺原发性黏液表皮样癌(pulmo...

肺原发性黏液表皮样癌(pulmo...粘液表皮样癌(mucoepidermoid carcinoma, MEC)是由不同比例的表皮样细胞、粘液细胞和中间细胞组成的恶性肿瘤,黏液表皮样癌主要发生在涎腺,其中约一半(53%)发生在大涎腺,其中腮腺占45%,颌下腺为7%,舌下腺为1%。
口腔内最常见的发生部位是腭和颊黏膜。
在肺内也可以发生与涎腺肿瘤相似的上皮性肿瘤,原发于肺部的较为少见,肺原发性黏液表皮样癌(pulmonary mucoepidermoid carcinoma,PMEC)是一种罕见的肿瘤(如图1)。
由smetana等人1952年首次报道,一般认为起源于气管及支气管浆液腺和黏液腺的Kulchitsky细胞。
PMEC占支气管肿瘤的1%-5%,全部肺肿瘤0.1%-0.2%。
融合蛋白MECT1-MAML2被认为是唾液腺和 PMEC中的致病性遗传事件。
有研究发现88%的PMEC与MECT1-MAML2融合转录相关,并且MAML2基因重排的存在可以支持PMEC的诊断。
t(11;19) (12;P13)融合蛋白MECT1-MAML2被认为是涎腺和支气管肺黏液表皮样癌的驱动基因事件。
也可发生在皮肤、乳腺和宫颈等部位。
大约6%的病例存在CRTC3-MAML2基因融合,而非MECT1-MAML2基因融合。
有研究表明,存在基因融合的黏液表皮样癌预后更好。
图1:肿瘤位于支气管粘膜下,肿瘤细胞巢状分布,部分细胞内有粘液,可见片状肿瘤性坏死。
临床特征:PMEC可发生于任何年龄段,但患者总体发病年龄较轻,国内文献报道平均年龄在40岁左右,青少年患者也屡见不鲜。
通常认为发病无性别差异,有研究显示大于40岁男性以低级别多见,而高级别多见于年轻女性。
PEMC大体可分为四型: 腔内息肉型、腔内外肿块型、管壁全层浸润型、外周型,而腔内息肉型最多见。
CT检查是一种无创且有效的方法。
Kim等人总结以下征象:①肿瘤长径与所属肺叶或肺段气道平行;②常伴远端肺叶的阻塞性肺炎或肺不张;③“空气新月征”,即病灶部分阻塞气道所形成周围含气的空腔。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
肺粘液表皮样癌的CT诊断【摘要】目的讨论肺粘液表皮样癌的CT特点,提高诊断水平。
方法搜集我院5例病理证实为肺粘液表皮样癌的病例,并结合回顾国内外相关文献,讨论其CT表现。
结果 5例病例中有4例位于右肺,多为椭圆形,肿块密度较均匀,未见液化坏死,增强后呈轻中度强化,1例见点状钙化;1例伴有阻塞性肺炎、肺不张;2例伴有纵隔淋巴结转移。
结论肺粘液表皮样癌多为气管、支气管内或孤立的肺内结节,呈卵圆形或分叶状,可伴有阻塞性病变,部份可见点片状钙化,注射对比剂后呈轻中度强化。
结合临床资料,CT能为该病的诊断提供帮助。
【关键词】肺粘液表皮样癌;CT[Abstract] Objective To discuss the computed tomography (CT) findings of mucoepidermoid carcinoma of the lung and improve the diagnosis. Methods CT images of five cases proved by pathology were studied with review of the literatures. Results On CT images, 4 cases located in the right lung, multiple with elliptical shape and mass density, no liquefaction necrosis, and showed mild to moderate enhancement. One case showed punctate calcification, two cases showed obstructive pneumonia and atelectasis, two cases with mediastinal lymph node metastases. Conclusion Mucoepidermoid carcinoma of the lung was seen as an endotracheal or endobronchial nodule, which was either smoothly oval or lobulated and punctate calcification be seen in some patients. Some were illustrated with post obstructive pneumonia or atelectasis. Mild to moderate enhancement was shown after the administration of the contrast medium. Combined with clinical data, CT could be helpful to diagnose the disease.[Key words] mucoepidermoid carcinoma of the lung;computed tomography肺粘液表皮样癌(Mucoepidermoid carcinoma of the lung)的发病率极低,仅占支气管腺瘤的3%[1],它的起源是气管、支气管粘膜下腺体的Kulchitsky 细胞。
国内外文献偶见报道,且内容多为该病的临床及病理表现,至于影像学表现探讨很少。
现收集5例经我院手术病理确诊的肺粘液表皮样癌,总结其CT表现,并通过文献回顾,提高对该病的认识。
资料与方法1.一般资料收集2001~2009年在我院接受手术治疗并经病理证实的肺粘液表皮样癌5例。
其中男性3例,女性2例,年龄23~69岁,平均56.3岁。
临床表现为咳嗽、咳痰3例,其中2例伴有咯血,血量每次达300ml~500ml不等。
表现为单侧胸痛伴有发热1例,体温38.5℃~39.3℃;无明显临床症状,偶然发现的1例。
病程1天~2月,平均35天。
2.检查方法 5例患者均接受CT平扫+增强扫描,检查采用美国GE公司Hispeed NXI双排螺旋CT扫描机,扫描电压120KV,管电流为120mAs。
扫描范围包括胸廓入口至肋膈角,先以5~10mm层厚和间距扫描,后对病变局部进行薄层扫描,增强扫描采用静脉团注方法,经内侧肘前浅静脉注入非离子造影剂80ml,注射速率3ml/s,于注射完毕后开始扫描。
3.图像分析由两名有经验的放射科医师对病变的CT表现进行分析,并达成一致意见。
分析内容包括:肿块发生的部位、形态、大小,增强后的变化,间接征象(阻塞性改变、淋巴结转移、肺内及其他部位转移),淋巴结肿大的标准为淋巴结最大横径≥1cm。
结果病变位于右肺4例,左肺1例;位于主支气管1例,位于叶、段支气管2例,位于周边2例;病变多成椭圆形,最大径2~4cm,平均3.5cm。
肿块密度较均匀,未见液化坏死,CT值32~53Hu,平均45Hu,增强扫描后强化幅度13~32Hu,平均22Hu;1例内部可见点状钙化;1例伴有阻塞性肺炎、肺不张;2例伴有纵隔淋巴结转移。
5例分别行全肺及肺叶切除术,并清扫肺门纵隔淋巴结。
术后病理学检查证实为肺粘液表皮样癌,其中高分化3例,低分化2例。
讨论1.组织学来源根据世界卫生组织的分类,肺粘液表皮样癌是一种起源于气管、支气管粘膜下腺体Kulchitsky细胞的罕见恶性肿瘤,其在原发性肺恶性肿瘤中所占的比例约0.1~0.2%,发病年龄4~78岁不等,成年人多见,平均为28.5岁[2]。
但研究学者在对其生物学特征评价中观点不一:部份学者认为其是原发性支气管低度恶性肿瘤;还有学者认为不能简单将其归为低度恶性肿瘤,因为有文献报道部份病例表现为高度恶性,进展迅速,早期就可出现转移,生存时间短[3]。
图1a~1e 左主支气管近端管腔内软组织密度肿块,左肺体积缩小,伴有不全节段性肺不张,纵隔向左偏移,肿块见中等程度强化图2a~2c 右上肺叶软组织肿块,边缘呈分叶状并有短小毛刺,纵隔内见多发淋巴结转移图3a~3b 右下肺叶周边软组织肿块,边缘清晰,可见分叶,肿块内见点状钙化灶2.病理学表现肺粘液表皮样癌的瘤体主要由粘液细胞、表皮样细胞和少量中间型细胞构成。
这三种细胞以不同的比例构成巢团或不规则的腺样结构。
粘液细胞呈多边形或高柱状,胞浆淡染,弱嗜碱性,核居于一侧,细胞内可见粘液颗粒,细胞外可见大量粘液;表皮样细胞呈多边形似鳞状细胞,细胞间可见细胞间桥,但角化不完全;中间型细胞似表皮基底层细胞。
瘤体可被间质纤维组织分隔成大小不同的小叶结构。
按照分化程度的不同,病理上一般将其分为高分化(低度恶性)粘液表皮样癌和低分化(高度恶性)粘液表皮样癌两类[5],在高分化肿瘤中,囊性变占主要成分,典型的实性区的组成为分泌粘液的柱状上皮形成小腺体、小管和囊肿,坏死不显著,这些囊肿内通常含有浓缩的粘液,使肿瘤呈胶样外观而且常常钙化。
高级别粘液表皮样癌罕见,具有与腺鳞癌一致的组织学特点,癌细胞染色质深染、有不典型性的细胞核,活跃的核分裂活性和高的核浆比例。
3.临床表现以往研究表明,肺粘液表皮样癌10%发生于主支气管,75%发生于段、叶支气管,15%发生于周围,右侧略多于左侧[4]。
本组病例中,位于右肺4例,左肺1例;以右肺居多,与文献一致。
5例病例中,1例位于主支气管,2例位于叶、段支气管,2例位于周边,分布比例与文献不完全一致;临床症状和体征与肿瘤发生的部位有着密切相关性,发生于气管、支气管管腔内的肿块,临床上多伴随气道阻塞表现,包括咳嗽、咯痰、咳血及反复感染等,但也有部分病例无明显临床症状,如Tae SK等[5]研究的12 例中有3人没有症状,占25%,本组病例中有1例是无明显临床症状,约20%,与上述文献结果大致相似。
粘液表皮样癌临床病程较长,平均可达数年,一般术后预后长,平均可达数年,一般术后预后良好,仅有2%的低度恶性和15%的高度恶性肿瘤伴有纵隔淋巴结转移,本组病例中2例出现淋巴结转移,略高于文献报道。
4.影像学表现粘液表皮样癌在胸部X平片上常常表现为肺内弧立性结节或肿块,部分患者可合并或仅表现为肺部炎症和(或)肺不张,亦有部分患者没有阳性发现[5]。
CT比X线有更高的空间分辨率和密度分辨率,能够提供更多的有意义的发现。
通过复习文献并结合本组5个病例,笔者认为肺粘液表皮样癌具有以下的CT征象[6 -9]:①大多数肺粘液表皮样癌属于中央型,发生于气管树的各级分支内;CT扫描表现为气管、支气管内的肿瘤,多呈边缘光滑、境界清楚的椭圆形或分叶状的结节或肿块影,并且主要向腔内生长,肿瘤长轴大多沿着支气管分支方向走行。
少部份表现为肺周边肿块,为周围型,边缘光滑或分叶,一般无液化、空洞。
②肿瘤密度相对比较均匀,增强扫描后肿瘤多呈轻中度的强化。
本研究中5例均行平扫加增强扫描,平均增强强化的幅度约22Hu。
③以往研究表明,约超过一半的肺粘液表皮样癌的病例在肿块瘤体内可以发现点片状的钙化影,与其他的常见肺恶性肿瘤相比,此比例明显较高,由此可见笔者认为肿瘤瘤体内的散在点状钙化是其诊断特点之一。
④间接征象包括:支气管粘液栓塞形成、阻塞性的肺炎、肺不张、肺气肿以及在肿块周围可以看见新月状的气体影,以上征象均由肿块在气管、支气管管腔内生长,完全或不完全阻塞气管所致;⑤研究表明有2%的低度恶性和15%的高度恶性粘液表皮样癌会发生局部淋巴结转移,本组病例中有2例伴发纵隔淋巴结转移,病理分类上均属于高度恶性。
5.鉴别诊断肺粘液表皮样癌应与支气管类癌和囊腺癌相鉴别[10]:类癌富含血管,增强扫描可见显著强化,而支气管粘液表皮样癌仅有轻度强化;囊腺癌易向气管外蔓延,常发生于下段支气管、主支气管、叶支气管,而支气管粘液表皮样癌最好发于段支气管,大多表现为管腔内的光滑的卵圆形或分叶状肿块,向气道外蔓延少见。
肺粘液表皮样癌也可与肺癌相鉴别,后者表现为边缘不光滑,可见分叶与短毛刺征、胸膜凹陷、阻塞性肺炎肺不张、胸腔积液及淋巴结转移多见,且多有偏心空洞。
6.治疗及预后目前认为肿瘤对放化疗不敏感,手术是唯一有效的治疗方法,多数在肿瘤完整切除后不再复发,即便是姑息性切除,术后也能带瘤生存多年。
参考文献1. Nagahiro I, Ando A, Ichiba S, et al. Three cases of pulmonary mucoepidermoid carcinoma [J]. Kyobu Geka. 2000, 53:702 - 7052. 张舰,冉鹏. 支气管粘液表皮样癌一例并文献复习[J]. 贵州医药2006;30:(11),1035.3. Shimizu J, Watanabe Y, Oda M, et al. Clinic pathologic Studyof mucoepidermoid carcinoma of the Lung [J]. Int Surg.1998, 83(1):1 - 3.4. 林敏芳,杨之怡,张宏英. 支气管粘液表皮样癌96例临床分析[J]. 实用肿瘤学杂志2006;20(2):129-130.5. Tae SK, Kyung SL, Joungho H, ET al.Mucoepidermoid Carcinoma of the Teacheobronchial Tree: Radiographic and CT Findings in 12 Patients. Radiology 1999; 212:643-648.6. Ishizumi T, Tateishi U, Watanabe S, et al. Mucoepidermoid carcinoma of the lung: high-resolution CT and histopathologic findingsin five cases. Lung Cancer. 2008 Apr; 60(1):125-31.7. Jiang T, Shi M,Lü N. Correlation study of high-resolution CT with pathologic finding of solitary small lung nodules. Zhonghua ZhongLiu Za Zhi. 1998 May; 20(3):216-8.8. Zubair W, Baloch, Alyson C, et al. Primary Mucoepidermoid Carcinoma and Sclerosing Mucoepidermoid Carcinoma with Eosinophilia ofthe Thyroid Gland: A Report of Nine Cases. Mod Pathol 2000;13(7):802�C807.9. KM Wolf, D Mehta, WD Claypool. Mucoepidermoid carcinoma of the lung with intracranial metastases. Chest 1988; 94(1); 435-438.10. 赵一平,刘白鹭,边杰,等.CT动态增强扫描诊断肺癌的初探[J]. 实用放射学杂志,2007,23(1):39-4211. 藏建,肖勇,齐天伟.周围型肺腺癌CT征象在评估其病理学分级中价值的初探. 中国CT和MRI杂志,2009,6(3):33-35.12. 金志发,罗良平,陈金城,等.孤立性肺结节CT动态增强扫描的实用研究. 中国CT和MRI杂志,2009,8(4):8-11.。
