北大中级无机化学有机金属化学共48页文档
2024版年度《北京大学有机化学》ppt课件

2024/2/2
31
THANKS
感谢观看
2024/2/2
32
14
酚
酚的分类与命名
根据羟基所连苯环的不同,酚可 分为一元酚和多元酚等。
2024/2/2
酚的物理性质
多数酚为无色或淡黄色晶体,具有 特殊气味,微溶于水,易溶于有机 溶剂。
酚的化学性质
酚分子中的羟基和苯环相互影响, 使得酚具有一些特殊的化学性质, 如酸性、氧化反应等。
15
醚
醚的分类与命名
根据醚键两端所连基团的不同,醚可分为单醚、混醚等。
实例与应用
乙炔是常见的炔烃之一,广泛应用于 焊接、切割、照明等领域。
10
芳香烃
定义与通式
结构特点
芳香烃是由苯环或稠环结构组成的烃类化合 物。
芳香烃分子中含有苯环或稠环结构,具有特 殊的稳定性和芳香性。
性质与反应
实例与应用
芳香烃的化学性质较为特殊,可以发生取代、 加成、氧化等多种反应,但反应条件较为苛 刻。
机溶剂。
卤代烃的化学性质
03
卤代烃中的卤素原子较为活泼,可发生取代反应、消除反应等。
13
醇
醇的分类与命名
根据羟基所连碳原子的不 同,醇可分为伯醇、仲醇、 叔醇等。
2024/2/2
醇的物理性质
多数醇为无色液体,具有 特殊气味,可溶于水,也 可溶于有机溶剂。
醇的化学性质
醇分子中的羟基具有亲核 性,可发生氧化反应、酯 化反应等。
遵守实验室规章制度,尊重实验数据,不抄袭、不造假,保持诚信 和实事求是的科学精神。
29
实验操作规范与安全注意事项
1
实验前准备
熟悉实验步骤和操作规程,检查实验仪器和试剂 是否齐全、完好,做好个人防护措施。
中级无机化学

CCl4难水解,是因C的价轨道已用于成键且又没有孤电子对之故。 NF3的分子结构与NCl3同,其中N原子也是采用sp3杂化轨道成键,其上有一对孤 对电子。然而, 1 由于F原子的电负性较大,使得NF3的碱性(给电子性)比NCl3小,因而亲电水解 很难发生; 2 由于N是第二周期元素,只有4条价轨道(没有d轨道),不可能有空轨道接受水 的亲核进攻; 3 N-F键的键能比N-Cl键的键能大,不容易断裂。 这些原因决定了NF3不会发生水解作用。
第一章 原子、分子及元素周期性
第一节 原子结构理论概述 第二节 原子参数及元素周期性 第三节 共价键理论概述 第四节 键参数与分子构型 第五节 分子对称性与点群 第六节 单质的性质及其周期性递变规律 第七节 主族元素化合物的周期性性质 以上七节主要自学,要求掌握: 1 用徐光宪的改进的Slater规则计算电子的屏蔽常数 2 了解电负性的几种标度,理解环境对电负性的影响和基 团电负性的概念 3 键参数 价层电子对互斥理论 分子对称性知识 4 单质及其化合物的一些性质的周期性变化规律 同时,还要特别注意 5 掌握周期反常现象的几种表现形式及合理解释
习题:1,2,3,4,6,7,8,10,11,12,13,15,17
原子所带电荷
电负性与电荷的关系可用式 χ = a + b 表示。 式中为分子中原子所带的部分电荷。a、b为两个 参数。其意义是: a表示中性原子的电负性(中性原 子=0), b为电荷参数,表示电负性随电荷而改变 的变化率。大的、易极化的原子有较小的b值; 小 的、难以极化的原子b值较大。
分子
是
是 D∞h i i? 否 C∞v
直线型 ?
是
否 两个或多个 Cn(n≥3) ?
否 Cn ? 否 ζ?
T,Th,Td,O,Oh 是
2024版北京大学有机化学ppt课件[1]
![2024版北京大学有机化学ppt课件[1]](https://img.taocdn.com/s3/m/ea51b34b0640be1e650e52ea551810a6f524c8cb.png)
含氧官能团的保护与脱保护
阐述在有机合成中如何对含氧官能团 进行保护和脱保护,以实现复杂有机 分子的合成。
14
04
含氮有机化合物
2024/1/2915源自胺类化合物结构和性质胺类化合物的结构特点
包括伯胺、仲胺和叔胺的结构特征, 以及它们与氨分子的结构差异。
胺类化合物的物理性质
胺类化合物的化学性质
阐述胺类化合物的碱性、亲核性、氧 化还原性以及它们的特征反应,如酰 化反应、烷基化反应等。
炔烃 含有碳碳三键的链状烃类化合物。具有不饱和性,可发生 加成、聚合等反应。性质较为活泼,可与多种物质发生反 应。
8
芳香烃及其衍生物
芳香烃
含有苯环的烃类化合物,如苯、甲苯、二甲苯等。具有特殊的芳香气味和稳定 的化学性质。
芳香烃衍生物
以芳香烃为母体,通过取代反应引入其他官能团的化合物,如硝基苯、苯酚、 苯胺等。具有多样化的化学性质和广泛的应用领域。
2024/1/29
13
含氧官能团转化反应及合成策略
醇与醛、酮的转化 讲解醇氧化成醛或酮的反应条件及机 理,以及醛或酮还原成醇的方法。
酚与醚的转化
阐述酚羟基化合成醚的反应条件及机 理,以及醚裂解生成酚的方法。
2024/1/29
羧酸及其衍生物的转化
介绍羧酸及其衍生物之间的转化反应, 如酯化反应、酰胺化反应等,并讲解 其合成策略。
6
02
烃类化合物
2024/1/29
7
烷烃、烯烃、炔烃等结构和性质
2024/1/29
烷烃 由碳和氢元素组成,分子中只含有单键的链状烃类化合物。 根据碳原子数不同,可分为甲烷、乙烷、丙烷等。具有饱 和性、稳定性,不易发生化学反应。
烯烃 含有碳碳双键的链状烃类化合物。根据双键位置不同,可 分为α-烯烃、β-烯烃等。具有不饱和性,可发生加成、氧 化等反应。
北京大学无机化学PPT课件

第12页/共32页
二 金属原子簇
1. HNCC(High Nuclear Carbonyl Cluster )
Wade 规 则 : M(CO)3 与 BH ( 或 CH ) 的 等 瓣 关 系 , (2n+2)、 (2n+4)、(2n+6)骨架电子数规则,
CO2和SiO2; “ PO33 – ”和SO32 – 是否为等电子体?
H
H
H
H
CH4
H
H H NH3
H H
OH2
H FH
第1页/共32页
2. 等瓣(等叶片)相似
R. Hoffmann, (Nobel Lecture, 1982) “Building Bridges between Inorganic and Organic Chemistry”
一.等瓣(isolobal) 相似
1. 等电子(isoelectronic)原理: 电子数相等 N2, CO, CN –, NO+ (10e) CH4, NH3, OH2, FH (8e) NO3 –, CO32 –, BO33 – (24e) ClO3 –, SO32 – (26e) SiO44– , PO43–, SO42–, ClO4– (32e)
(n为金属原子数)
14n+2 14n+4 14n+6 14n+8
第16页/共32页
高价过渡金属卤化物(硫化物)原子簇
M6X8
或 [ M6(3-X)8 ]
Mo6Cl84+ Mo6S84–
Mo(II) 簇电子数: 4×6 = 24e
Mo—Mo间的电子数: 24/12(棱)=2 Mo—Mo 单键(2e) ~ 2.60Å
北京大学中级无机化学答案

无机化学习题参考答案(II) 1.4.解:(1)H2O22C(2)S2O32-3vC(3)N2O (N-N-O方式)vC∞(4)Hg2Cl2hD∞(5)H2C=C=CH22dD(6)UOF4C5v(7)BF4-dT(8)SClF54vC(9)反-Pt(NH3)2Cl22hD(10)PtCl3(C2H4)-2vC1.B(CH3)3和BCl3相比,哪一个的Lewis 酸性强,为什么?一般来说,CH3为推电子基团,Cl 为吸电子基团,因此的Lewis 酸性强。
(BCl3易水解;B(CH3)3不溶于水,在空气中易燃)2.BH3和BF3都可和(CH3)2NPF2生成加合物,在一种加合物中,B原子和N相连,另一种则和P相连,绘出两种结构式,并说明形成两种结构的原因。
(该题可参考史启桢等翻译的"无机化学",作者Shriver等,由高教社出版, 其中关于热力学酸度参数的部分,p.190-191; 或者该书的英文原版第5章的相关内容)3. 无水AlCl3可作为傅-克烷基化反应的催化剂, 而吸水后则失效, 原因何在?配位饱和(6配位),失去Lewis酸性4. 吸水后失效的AlCl3有什么方法可以脱水?因为Al3+是典型的硬酸,与氧的亲合力很强,因此实验室不能在HCl,NH4Cl,SOCl2等气氛下加热脱水。
(只能加强热生成 Al2O3后,用高温下用加C和Cl2用还原氯化法制备,这就不是脱水方法了)。
第二章2.1 解:Ni2+ d8组态Pt2+ d8组态第四周期(分裂能小)第六周期(分裂能大)trans cis 四面体构型平面四方形构型(两种构型)只有一种结构(P代表PPh3)2.2 解(1)MA2B4(2)MA3B3trans cis fac(面式) mer(经式)D 4h C 2v C 3v C 2vμ=0 μ≠0 μ≠0 μ≠0μfac >μmer2.3 Co(en)2Cl 2+D 2hC 2 光活异构体 C 2Co(en)2(NH 3)Cl 2+trans cis Co(en)(NH 3)2Cl 2+trans(1) trans(2) cis 2.4 Co(en)33+Ru(bipy)32+手性分子D 3D 3PtCl(dien)+dien HNCH 2CH 2CH 2NH 2NH 2CH 2基本上为平面分子,无手性2.5 (1) 分别用BaCl 2溶液滴入,有白色沉液出现的为[Co(NH 3)5Br]SO 4,或分别加入AgNO 3溶液,产生浅黄色沉淀的为[Co(NH 3)5SO 4]Br 。
北京大学无机化学课件

第一章 酸碱化学
1. 元素在周期表中的酸碱性 2. 酸碱质子理论和酸碱概念的相对性 3. Lewis酸碱 4. 软硬酸碱
1.元素在周期表中的酸碱性
元素周期表中酸性和碱性元素的分布区域
第一过渡系金属的氧化态和酸性的关系
2. 酸碱概念的相对性
醋酸为碱: CH3COOH +H2SO4 CH3COOH2+ HSO4 醋酸为酸: CH3COOH + H2O H3O + CH3COO
EDTA
配位数(coordination number,CN )和配位点
Ag(NH3)2+ CN=2, Cu(CN)2- CN=?
Zn(EDTA)2- CN=6,
配位数 化学计量比 配位数 配体数
二.常见的配体
1. 单齿配体(monodentate ligands)
F、Cl、Br、I、
NH3 、NR3 、PR3、PPh3、P(OR)3,
多齿配体
-OOC -OOC
NCH2CH2N
COOCOO-
六齿配体 EDTA
L
N
N
Co
O
O
四齿配体
二水杨醛缩乙二 胺合钴Co(Salen)
EDTA配合物的结构
三.配合物的几何构形
❖配位数2 (D∞h ) ❖配位数3 (D3h)
❖配位数4 (D4h和Td 点群) ❖ 配位数5 (D3h和T4v 点群) ❖ 配位数6 (Oh, D4h , D3h , D3d , D2h点群) ❖ 配位数8 (D4d四方反棱柱 , D2d 12面体 )
K2Pt(CN)4.0.3Br.3H2O 配合物(分子导线)
2. 基础研究: 量子化学为基础, 波谱学方法 新型无机化合物的合成, 反应机理, 结构表征
北大中级无机化学有机金属化学(2)
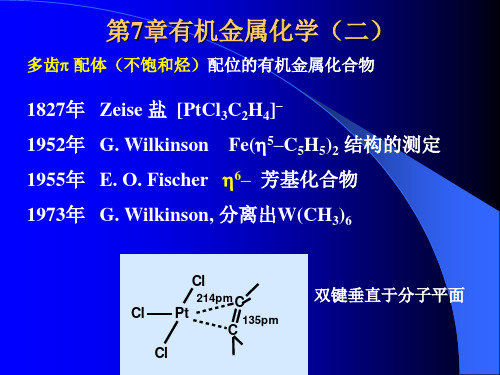
H H H CH 4
H H H N H3 OH2 H H FH H
H
2. 等瓣相似
R. Hoffmann, (Nobel Lecture, 1982) ―Building Bridges between Inorganic and Organic Chemistry‖
练习
写出下列化合物 的结构、总价电子计数和金属原子 的氧化态 1. (5–C5H5)Mn(CO)3 2. (5–C5H5)Mo(CO)2 (3–C3H5) 3. (5–C5H5)2Ta (CH2)(CH3)
Fe(5–C5H5)2
Fluxional ferrocene 转动势垒低,~ 3.8kJ.mol–1
固态:交错型 D5d
气相:重叠型 D5h 室温时不规则,低温为D5
合成方法: C5H6 C5H5–
1) C5H6(二聚体) + Na (THF) C5H5– + Na+ + H2
FeCl2+ NaC5H5(THF, 苯) Fe(5–C5H5)2
Alkylidyne ( CR )次烷基配合物 Carbyne配合物
3电子给体
OM e (O C ) 5 M o= C Ph OC
+
Br CO Mo OC C O C Ph
+
B B r3
CO
+
B B r2 (O M e )
卡宾化合物
卡拜化合物
Carbene 和 Carbyne的配合物
讨论:
1. 烯丙基配合物[PdC3H5Cl]2的结构和总价电子计数,
R2 C M CR
东北大学中级无机化学复习资料

第一章酸碱理论与非水溶液化学>>学习单元1 酸碱概念1、NH4+的共轭碱是(B)。
(A) OH-(B) NH3(C)NH2-(D) NH2-提示:由质子理论定义: NH4+(酸) H++NH3(碱),故选B。
2、在反应BF3 + NH3 F3BNH3中,BF3为(D)。
(A) Arrhenius碱(B) Br nsted酸(C) Lewis碱(D) Lewis酸提示:B具有缺电子性,可以接受孤对电子,故为Lewis酸。
3、根据酸碱的溶剂理论,在液态 SO2体系中的碱是( B )。
(A) SOCl2(B) Na2SO3(C) Na2SO4(D) PCl3 提示:2SO2 SO2+ SO32-,能生成溶剂阴离子的是Na2SO3,故选B。
为什么Fe3+与F-形成的配合物的稳定性大于Fe3+与Cl-形成的配合物的稳定性?酸碱定义:电负性较小的路易斯碱称为软碱;与软碱形成稳定配合物的路易斯酸为软酸。
电负性较大的路易斯碱称为硬碱硬”对应的是小的、高氧化态的粒子,这些粒子都很难被极化。
相反,“软”是指大的,低氧化态的粒子,很容易被极化。
软-软和硬-硬之间的酸碱反应最为稳定。
这个理论在有机化学和无;与硬碱形成稳定配合物的路易斯酸为硬酸。
硬”对应的是小的、高氧化态的粒子,这些粒子硬”对应的是小的、高氧化态的粒子,这些粒子都很难被极化。
相反,“软”是指大的,低氧化态的粒子,很容易被极化。
软-软和硬-硬之间的酸碱反应最为稳定。
这个理论在有机化学和无都很难被极化。
相反,“软”是指大的,低氧化态的粒子,很容易被极化。
软-软和硬-硬之间的酸碱反应最为稳定。
这个理论在有机化学和无机化学均有应用。
酸碱反应实质:硬酸倾向于与硬碱反应(硬亲硬),软酸倾向于软碱反应(软亲软)。
Fe3++6F–=[FeF6]3-(硬-硬)Hg2++4I-=[HgI4]2-(软-软)Fe4++4:Cl–=[FeCl4]–(硬-软),故[FeCl4]–不稳定第一章酸碱理论与非水溶液化学>>学习单元2 酸碱强度一、填空题1、判断相对Lewis碱性(1)(H3Si)2O和(H3C)2O;(2)(H3Si)3N和(H3C)3N ;其中较强的是(1)__(H3C)2O __,(2)__(H3C)3N___。
