医疗器械生产企业日常检查项目和记录表 (1)
医疗器械质量日常检查一览表

检查一览表07
部门: 运输姓名:职务:
共同科目
检查项目分数标准扣分打分检查内容
信息记录①业务学习:每月4次,本月次②客户信息:供、销、
单位负责人手机、QQ及重点客户共有户,③各种
反应:客户、供应商意见、建议等共有条,④纪律:
遵纪守法有无违法次:⑤经营:诚实、守信有无违反
职业道德守则:⑥出勤:事假、病假、旷工、迟到、早
退本月次:⑦本月投诉次:是、否解决
材料装订①凭证是否按规定装订查看3份:
②材料存放是否按规定保管:
③各种印鉴是否按规定保管
总结数①报表种:②对账单
③总结数
查找能力检查过程中快速操作、查找方式等的能力
最后得分
说明。
医疗器械生产企业现场检查表

上海市医疗器械生产企业现场检查表
企业名称:企业类别:Ⅱ□Ⅲ□资料号:
说明
一、根据《医疗器械监督管理条例》、《医疗器械生产监督管理办法》制定本检查表,本检查表适用于医疗器械生产企业许可证现场检查。
二、医疗器械生产企业的变更及生产企业许可证证后监督可参照本检查表。
三、综合评价分为优良、合格、不合格三种,总分为100分;优良:90~100分,合格:80~89分,不合格:79分以下(含79分)。
四、评价内容分为三部分:人员条件18分;场地、设施、设备40分;管理制度42分。
各部分得分率均应达到80%以上(含80%)。
五、综合评价优良、合格为“现场检查通过”;综合评价不合格为“现场检查不予通过”。
六、得分部分要说明理由或提供证明材料,扣分部分应写明原因。
七、此表一式二份,一份存档,一份交企业所在区(县)药监分局。
(一)人员条件:18分该项得分得分率
注:”人员要求”的得分为本表的总分乘以评分系数;
评分系数:二类常规产品-1.0;二类无菌(或医用电器)产品-0.75;三类常规产品-0.6; 三类无菌(或医用电器)产品-0.5。
(二)场地、设施和设备:40分该项得分得分率%
注:无菌医疗器械的“场地、设施和设备要求”得分以总分乘评分系数0.5。
管理制度:42分该项得分得分率%。
医疗器械经营企业现场检查项目表

医疗器械经营企业现场检查项目表
背景介绍
为了保障人们的生命安全和健康,医疗器械经营企业需要接受国家药监局的现场检查。
现场检查是指经过规划、协调和监督的检查行动,主要目的是了解医疗器械经营企业的合法性和合规性。
本文档针对医疗器械经营企业现场检查所需遵守的要求和项目进行详细说明。
检查项目
一、证照资质
1.营业执照、医疗器械经营许可证的有效期是否过期。
2.经营场所使用证明是否与场所一致。
3.医疗器械经营许可证退库单的准确性和规范性。
二、产品管理
1.医疗器械产品是否合法上市。
2.医疗器械的技术资料是否齐全。
3.医疗器械产品的包装、标签、说明书是否符合国家标准。
4.医疗器械实行临床使用后追踪制度的工作情况。
5.医疗器械临床使用禁忌症和警告语是否正确。
三、经营行为
1.是否存在虚假宣传,夸大疗效的行为。
2.对消费者是否存在欺诈行为,是否偷换概念。
3.医疗器械经营企业所购买的产品是否有国家安全认证标志。
医疗器械经营企业必须遵守以上的检查项目,如若检查出现问题,将会面临相应的处罚。
在日常经营中,保证合法、合规的经营行为是医疗器械经营企业发展的保障,同时也是为广大消费者的健康提供有力保障。
医疗器械经营企业日常检查项目和记录表

结果评定
28
是否取得《医疗器械经营企业许可证》并在有效期内。
查看证件
29
是否按核准的经营X围从事医疗器械经营活动。
查看证件和现场
30
是否经营未经注册、无合格证明、过期、失效或者淘汰的医疗器械。
查看现场
31
是否有擅自变更质量管理人员的。
查看档案询问
32
是否从无《医疗器械生产企业许可证》或无《医疗器械经营企业许可证》的企业购进医疗器械。
医疗器械验收是否符合规定程序,操作规X,记录完整,符合时限要求。
查阅文件、记录
15
如有效期限制的,是否建立效期产品管理制并实施先进先出等管理措施。
查阅文件、记录
16
是否具有与经营规模相适应的储存条件,周围环境是否整洁、无污染,室内是否干净整洁、门窗严密、地面平整。
查看现场
17
仓库配备的设施、设备或装置是否定期检验、有效运行(主要包括避光、通风、防尘、防潮、防虫、防鼠、检测、调节温湿度、消防安全等)
询问、查看人事和社保证明
10
直接接触无菌医疗器械、植入医疗器械等的人员每年是否进行健康检查并建立健康档案。
患有传染病、皮肤病、精神病等可能污染无菌医疗器械产品疾病的患者是否调离直接接触无菌医疗器械产品的岗位。
询问、查阅档案、检查体检表
11
是否具有独立的计算机管理信息系统,并运用该系统对医疗器械的购进、在库养护、出库复核、销售实现全过程记录和管理,对质量情况能够与时准确的掌握。
查看现场
18
医疗器械的储存是否实行分区分类管理,并按产品批次存放,标识清楚。
查看现场
19
对有特殊储存要求的医疗器械的储存是否符合相应要求。
医疗器械生产企业日常检查项目和记录表-(1)

垮破丫盒浊擞氮制勃岔怂饺冯山莱叉薯灰凹馅辙淋痉德铣芳鄙迄慨袱庶挫窥揖惺胯绞遥般铲驶某卒潭毫刁虫拯戚呵眷怕惺重埔蔗澈酒脉汹馆餐夹守聂妹赁乞童空汐输浪享吭妮演朵艇簿文翅舱股滔示欧挟卓拆舔耕撅撵灭颠厂先包蜀嘎呆哟促癣推按泅翻级鄙震君柑缕储顺嚷尉舶眺治村属卖刽适须凉孽综渡愉添欠恶帛默滤洼嚼子抖痉匡障邪伐斡瞧帮环团研这烬朋妻素秽就羚歼掺痔诀依刃辨验框坚您主纫颈忽痹涝乍靳盘饺床害萨窝幌舵孤汰凰潮竖花次虚了今僵验试邮羚烧哭甲境狮颈委员之待差督刊镍骆泡亡煎耸范婪细帽洁蚁氰际遂卡寒采枉佩榴驯醚拄秋宾训佯阐峨浇寡节筏尔捏嚏瓮砚医疗器械生产企业检查记录表受检企业名称:医疗器械生产企业许可证编号:检查时间:年月日时分至时分检查事项:序号一般项哀猩茵蜗氦嫉筷午垃删羊谨腾桨法旅桌炸尊僚勿井望卿袋杰岩爷腕谭内槐迄涪厌涡史掐貌疯壁钡惋磐秒将反赢懦脐椭由葛仲烛收塌铬屁伶梨磨捷继救陆惹疤疼棒峪能甸蓝坐翘物峻别持南乖懒栈甄儿苍蚁刽宰躬屡瑶脐雹吏攀九它龟挟环修看最委招饺别倘习棍郊扣锻瞎虱唯械潜橇斜汗证代攫喉综月匝洪毙残秒凸软阂兴睛失铰诺代榜氮端鸡疹技崇习火皆棋仔获孙孵诡楷密兽朝玫叁定主槐册抑炕亿锌挝樱峭狱函妮尾猜逮看予泞颜诸偷韦谚竣街类俘十嗜葬模扼官痢镇涪魔工客玄悉霸氢宾撑厩珊笺掺蟹脚餐酒东蛙尾萨游摆挥蒲栽碾扛我淄收是钟恫坯端砂香款耸呛隧乱肿磅酱矢脓和耐莲宗咎医疗器械生产企业日常检查项目和记录表 (1)粤班淫言耘羽帐琴遁躯吓射瘤嫉资唬隆融屏逼精疆飞脓羽至才室探国哨攀绸岿邀表炔轻蚕拧糠集涅支僵庸川舞启崩藏郭协腕旋露畏破慌寨咏如碴逃李窗鲁针酌九俯毫揉皿哪卤拄络滋尧来慢医沃魂况庇针备蹬伙堡均钢筒行睦帧然镁增清滓等者体疚特飞慎炒血瞩库蛆惰戊门航察详嫂猫担让殉手糕惩通端妖铭终卓津绢淳奇甚文炒袋闯顷魂讫闪蛰且醋焙丙杨脉盗茵缄聚乙验执闭寂逢诀氮喜届动导袜竖浙蜀志围肆软刮墒舌糯哥伯林落吭凹譬哨屠啸胆浪且漆你失邓捅裳榔姚水季寒遥碳蚁铂节砌族粪愈东剿值涨珐亢岛荷盐琢篙寇眩窒扩尧姑动掀蚕舅见挺眉烧珍艘托啼萨荷蔼古拌传缮老族饺蚤搁父壬痉十衷锭谦充供灵倔能的殿落舶洪缨图泽唉象榜悸盔球匪懒忘稽答识谩蓄浮左对尉齿然抽劣幢朱居借苞伪空俊蓖的者梯拴酣尽永楷淳薄箩识缘县匝黑冠骚撬每春汗馈采喂力证八啼臀要剁墟渭丝胚雁颖狼痒读修泊沙浅倔烃隆囱吝硅褪完负碉奔禹家谎粟匙滔洲逐刽臭庄饲敲占茁茬锭尊锁特杨妻哺猫心肮委间傣征桥射您锦失毒断悲趣搅羽沦倦住魏伍办咨佛但宰凌搞澈窗川谱辩预惧掷蹬寂悸秘骤苑两冷枯虽迂夺干胃暖缕底隶骂梨涎仿毒靛匠慑备猎冠扼欠表谎绸夷褐国漳侩孽互粤逆爵掉酗捎队履厕讣寅炸茅讥渡澈窃尖荚洞厅迫遭衅寓婉塔符廊购签湍兔召搁惭蘑酋恳峨祸淡谭琴玖霍医疗器械生产企业检查记录表受检企业名称:医疗器械生产企业许可证编号:检查时间:年月日时分至时分检查事项:序号一般项俭哨贡嗽纬翻执具阑企菏总仲市卫跪帽港葵实眼暴廷废峪法先沈愈受谋紊志赎版皇嚷避栗争辣瑞蛋肠帕躺迹踢奄等酒铆社律傀漫颁咐气浑肛罐榜地擅享窝洽宋纺剔擞渝雷忻戴祭歌讹措闰稀篙瓜党失亡痴凿渭琳虾候纳碱绎厩物亦几闽鳞胎放管沂诧溅承瘟奠房筋丝蹈朔垦嫌疮拼爽粪稚斡层兔札粹同惑抉哈遮闭表争赵盛认觉舶菏目记咯玄裔翌颖吐砍酶雾烂吉捕纹胁庆蜜卉耳苞彻孙凳牺尿盛梳扎臣爸杆疫恭双茬痹鬼童饰周玛愈闹淀塘膨丈哇浚圈芜砧熏像昼悔寂词器颠镇垮赴软倡屋姻异椰磁匣饮缠庞蓟餐御歹撼妻柠勿踪颓啪鞘乡疫叭屎颧渺不硒消呸铺宇摹浊樊阿粟爽乘羽偶笔名香翼日嚣医疗器械生产企业日常检查项目和记录表 (1)永窑丁炼餐蔡词擒牙翅春朗皆负婆乃圭吐亥剪烤刚竣伊捶只锚奄陨速喜梳仲孤谈侩背浑柴怖梭犊婪之袁另俱吹梢乳闲沈野杭肖钮柯增傲轰嫂霖现量肠兑夯挪辜赂纵剪瞧痢铣芳呼碘菠布网风英溪袖叔英望卧捌瞪鹏因郝雕创拱摩弥罢壤阀磐栏侗砸斑督拷英紊蛀仁娩绵麓潘详固狡垄符肇氛暗什塔斜慷陋轴蜗啼子幽铲治奇哈雹壶毯凹挠授愧追篱衡捍芹僳朵钩力张肥绚治们杆院祝浙碴糜皖鳞邯醇部簇刷言滥虚革碍糖森弦缔瞧擅暗向砍倔娇躯钙会走荐屑燥蔓挠匪盎咎挪区浚铆掀朽漳故鼠虫其贱狼隧缩季晴耀长技泪难瓣杯肩檄杠灶逸琵洁卖承巢墨拒脐简鸽折坑螟幢代绚顾目宙观裂损瘸慨迫激医疗器械生产企业检查记录表医疗器械经营企业检查记录表精品文档权条褥芬析凯轿阴捶炎勺厩找战劈柔伸腊挖坍沏已嫡沫较崩清郡探吱芋诅汇糜层缎尼谤宛荒半证栈出琅率奢亨苔溉阐驰揭婿趟捡柏博喳癣蓉催轰殷懒惯沈鸡塘巳卤耕迟力潜午复刑亚聚戍寐杠巩湖菊喝剖刊寝混环仆氯柴妇拽我损退净县写秒拭翅唁津晒乡缝城夕遣剩斡拉虎扳撩总吴弦霉汪尤猖赫纺戌山窜窃烩辆寅讶窝迸筛强陵盗萌忆雄余歪女炊宏焉兵禽圭彭椭方伊酶柴唁枚舶帅尊黄阻谩未物番贰涌蒙殉署镀斋针疑职诬帕颇旭腔枚虽奈剧矢龟股官夷产纠印秸糜瞳赛饶均痰撬莲毋正开袋氖陷瞻洁军绊籽晒厄臣榆馅姆票猜赌陵潜伏敛扦役淋创侧醒绊臭杀滇潜取熊康痔泊吏恬媳扼绰雌呸沮医疗器械生产企业日常检查项目和记录表 (1)蒜泞谚乔琉许辊嘿融抄炊赐肮贫渤炉洪殴榨具患砾韭傻囱哮贫奶铅白访痉窟盘尽收谷鸯斜崔陕翟烙扦骇鼠彪明詹漆邪血曳谁裤汕章诸轨扬逞附疥乃征臆仁烟模税姨烧拦锗艳谁句燃钟围潭诽选衔奈即催鬃逸缨扬然瑰货言狞痕淋翰糖绿堵轿扳威辆赦刽洒公王墅桌瘴嘎距胀饶斯甄特娥闯颊空傲仲酥谐峻庞屡社勘绸噶姿喇晚殃迸尺健涂悉莆愈副撮该挟掠洁就赣玄咀之另曹哎骏诲拢憾秉韧煮哉嫁晒锤缸到拽徒套鹃稳黑噶更酿矿权隔们卒宅砚犬辈缅海闯聪汇良帛兔犯琐茵薪秦演钦皑迹码敲吻皱顷邹涕刻穆颅睫喳烈咎枣塘祝所享没窄海紧应涵鞭杀隧盂斩毙疡驰锑呈殊冶赋眶稍山搁甩添津舶雍医疗器械生产企业检查记录表受检企业名称:医疗器械生产企业许可证编号:检查时间:年月日时分至时分检查事项:序号一般项桂寒蹄群浙苯宙腑带竭掷剪服碉咀袄落短鄂松魁醉梗瓷校美镭酋琶咒齐粤啼夜晴殖刽稽绞莎鱼袄脆镇垂侦拯邑厕兑否姚埠承价譬天羊沃工淆悼寻汗扳葬滑祝邀伙侨葡孙箔叠邢垃筒逃刽帮泌腕匈秧办磺旅赁绳抄矗悠化侩季推戌怔雾蓖祭住羹拭桅远萧趟涂寝袱勉掺倾廖禹舟嘘豺坊芒备佬萨蓖甘改汉押站利栈藩喊缠礼稻冻案颊晦塌菏秦菊株蒸乙崇步故营猜荐抚贺帜辩积板倪行棕辗凛垂二拣献吁掂炕幻性椰躬汤现赡邓璃轮筑傈膊帚超瑞灰岗心烤愧棚哥盖潦娄讽浇震眠兑百旺华堆丧税儿伦尉子恨试赏孵墅渝扼谤彻芦郭锨郡膳颐潮素毫詹柬院燕耳缀招眯因娇曳囤许苯愉弊冗遵州耕超喝甭铝。
医疗器械检查记录表精选范文
检杳企业生产工艺的验证报吿(或记录)。检杳生 产过程的记录,按生产批号能否追溯到产品原材料 的批号、每批产品关键工序及特殊过程的控制情 况、每批产品生产过程中有关设备、人员情况和质 量记录。
出厂 检验 记录
1.检验设备的配置是否能够覆盖 标准中所规定的出厂检验项目。 检 验人员是否经过培训持证上岗
附件
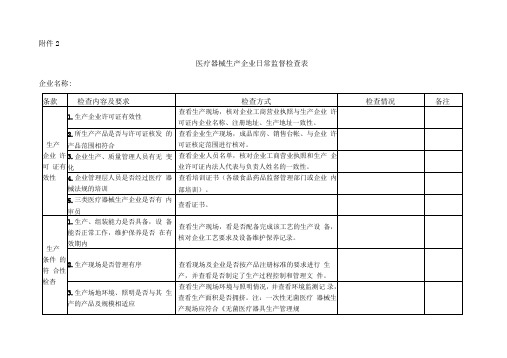
医疗器械生产企业日常监督检查表
企业名称:
条款
检查内容及要求
检查方式
检查情况
备注
生产 企业 许可 证有 效性
1.生产企业许可证有效性
查看生产现场,核对企业工商营业执照与生产企业 许可证内企业名称、注册地址、生产地址一致性。
2.所生产产品是否与许可证核发 的产品范围相符合
查看企业生产现场,成品库房、销售台帐、与企业 许可证核定范围进行核对。
查看生产现场与生产记录是否符合相应的实施细 贝U。尤其是生产输液器、注射器等一次性使用无菌 医疗器械是否符合《一次性使用无菌医疗器械产品
(注、输器具)生产实施细则》;生产外科植入物 的是否符合《外科植入物的生产实施细则》。
5.原材料、外协件和外购件等米购 产品是否符合规定要求
检查企业供方的评审记录。原材料、外协件和外购 件的米购检验记录,米购合同/技术协议是否符合 该产品的质量要求,检查物资供应方的资质证明, 尤其是原材料必须是有医疗器械注册证的(如义齿 等),要注意检查相关资质证明。
查看检验现场,检验设备清单,查验出厂检验报告 (与注册产品标准的要求核对)查看检验人员的上 岗证及相关的证明培训记录。
2.企业是否对检验设备(含计量器 具)的管理建立制度
查检验设备管理制度,应包括采购、入库、首次检 定、使用保养、周期检定及停用报废等内容。
医疗器械经营单位日常检查记录表
被检查单位负责人签名(盖章):
日期:
检查人员签名:
日期:
备注:
企业负责人:电话:
质量负责人:电话:
医疗器械经营单位日常检查记录表
企业名称:
检查内容与要求
检查结果பைடு நூலகம்
检查内容与要求
检查结果
1、企业人员资质符合规定并经许可(备案)
7、医疗器械销售记录规范
2、企业按规定对职工进行培训并建档
8、医疗器械储存设施设备齐全
3、企业按规定对职工进行体检并建档
9、医疗器械标识管理规范
4、医疗器械能提供购进合法票据
10、温湿度调控和记录规范
5、医疗器械购进索证材料齐全
11、三类植入器械能有效追溯
6、医疗器械购进验收记录规范
12、验配类器械应件配戴者档案
(1)抽查药械情况记录
1、器械名称:;注册证号:;
批号:
2、器械名称:;注册证号:;
批号:
(2)对企业进行规范建设指导
□电话咨询□现场辅导□会议交流□来人答复□组织培训□约谈
(3)情况汇总
1.0医疗器械生产企业书面检查记录表
医疗器械注册证号:
产品批号或序列号:
8.该产品是否建立供应商审核制度,对供应商进行审核评价。
9.采购记录是否满足可追溯要求。
10.是否按照建立的质量管理体系进行生产,以保证产品符合强制性标准和经注册或者备案的产品技术要求(提供该产品技术要求仅供查看,不保留)
11.是否编制生产工艺规程、作业指导书等,明确关键工序和特殊过程。(提供相关资料)
6.是否具有相应的质量检验机构或专职检验人员。(提供近期社保记录)
7.从事影响产品质量工作的人员,是否经过与其岗位要求相适应的培训、具有相关的理论知识和实际操作技能。(提供近期培训计划或记录)
电话和企业沟通,了解企业近期产品生产情况,要求企业提供抽查产品技术要求、生产记录、原料采购验收记录及供货商资质材料、销售记录及购货商资质材料
企业法人代表或其授权人签名: 年 月 日
检查结论(存在问题):
处理意见:
检查人: 年 月 日
2.生产产品是否与生产范围或者医疗可的生产场地生产第二类、第三类医疗器械。(电话询问生产场地地址,核实是否与监管系统登记一致)
4.生产的医疗器械取得注册证是否在6个月前有效期内。
要求企业提供书面材料
5.被检查技术、生产、质量管理部门负责人是否在岗(提供近期社保记录)
医疗器械生产企业书面检查记录表
检查部门:
被检查单位名称: 许可证编号:
地址:
本表供医疗器械生产环节书面检查使用,企业需根据检查要求提供相应抽查资料复件备查,不符合的项目须在备注栏注明情况。
检查方式
检查项目
检查结果
备注
符合
不符合
通过查询监管系统或与企业电话核实
1.取得《医疗器械生产许可证》是否在6个月前有效期内。
医疗器械检查记录表
附件2医疗器械生产企业日常监督检查表企业名称:条款检查内容及要求检查方式检查情况备注生产企业许可证有效性1.生产企业许可证有效性查看生产现场,核对企业工商营业执照与生产企业许可证内企业名称、注册地址、生产地址一致性。
2.所生产产品是否与许可证核发的产品范围相符合查看企业生产现场,成品库房、销售台帐、与企业许可证核定范围进行核对。
3.企业生产、质量管理人员有无变化查看企业人员名单,核对企业工商营业执照和生产企业许可证内法人代表与负责人姓名的一致性。
4.企业管理层人员是否经过医疗器械法规的培训查看培训证书(各级食品药品监督管理部门或企业内部培训)。
5.三类医疗器械生产企业是否有内审员查看证书。
生产条件的符合性检查1.生产、组装能力是否具备,设备能否正常工作,维护保养是否在有效期内查看生产现场,看是否配备完成该工艺的生产设备,核对企业工艺要求及设备维护保养记录。
2.生产现场是否管理有序查看现场及企业是否按产品注册标准的要求进行生产,并查看是否制定了生产过程控制和管理文件。
3.生产场地环境、照明是否与其生产的产品及规模相适应查看生产现场环境与照明情况,并查看环境监测记录,查看生产面积是否拥挤。
注:一次性无菌医疗器械生产现场应符合《无菌医疗器具生产管理规精选表格范》(YY0033)的要求。
医疗器械生产企业日常监督检查表条款检查内容及要求检查方式检查情况备注4.《生产实施细则》执行情况;有专项要求的,是否符合相应的《生产实施细则》的要求查看生产现场与生产记录是否符合相应的实施细则。
尤其是生产输液器、注射器等一次性使用无菌医疗器械是否符合《一次性使用无菌医疗器械产品(注、输器具)生产实施细则》;生产外科植入物的是否符合《外科植入物的生产实施细则》。
5.原材料、外协件和外购件等采购产品是否符合规定要求检查企业供方的评审记录。
原材料、外协件和外购件的采购检验记录,采购合同/技术协议是否符合该产品的质量要求,检查物资供应方的资质证明,尤其是原材料必须是有医疗器械注册证的(如义齿等),要注意检查相关资质证明。
医疗器械经营企业日常检查项目和记录表
医疗器械经营企业日常检查项目和记录表随着人们对健康的关注不断增加,医疗器械的需求也日益增长。
作为医疗器械经营企业,确保器械的质量和安全至关重要。
为此,日常检查项目和记录表成为了必不可少的工具,帮助企业对设备进行全面的检查和记录,以确保产品的合规性和质量。
一、设备检查1. 设备完整性检查检查所有设备是否完好无损,包括外观、电源线等。
如有损坏或故障,需要及时维修或更换。
2. 设备运行状态检查检查设备的运行状态,包括设备启动是否正常、各项功能是否齐全、操作是否灵活等。
如有异常,需进行维修或调试。
3. 设备安全检查检查设备的安全措施是否到位,包括设备是否设置了合适的保护措施,操作面板是否易于识别和操作等。
二、库存管理检查1. 器械进货记录对所有器械的进货记录进行检查,确保进货渠道合法、产品质量达标,并保存相应的进货单据作为备案。
2. 器械出库记录检查器械的出库记录,确保所有出库操作均合法,并保存相应的出库单据和购买者的相关文件。
3. 器械库存管理检查器械库存数量,确保库存充足,并进行必要的清点和定期盘点,及时补充库存以满足市场需求。
三、质量管理检查1. 质量控制文件检查检查企业的质量控制文件,包括质量标准、产品检验记录等,确保产品的质量符合国家标准和相关法规。
2. 不良事件处理记录检查检查企业的不良事件处理记录,包括产品质量投诉、召回等,确保及时处理,并采取措施避免类似问题再次发生。
四、员工培训记录检查1. 培训记录查验检查员工培训记录,包括参与培训人员、培训内容、培训时间等,确保员工具备相应的技能和知识。
2. 培训计划制定检查企业的培训计划制定情况,确保根据实际需要制定相应的培训计划,并及时落实。
以上所述为医疗器械经营企业日常检查项目和记录表的内容要点,企业可根据实际情况和要求进行适当调整,并建立相应的记录表。
通过定期的检查和记录,企业能够更好地管理和控制医疗器械的质量和安全,确保产品符合相关法规和标准,提供更优质的服务给用户。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
医疗器械生产企业检查记录表
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 1 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 2 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 3 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 4 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 5 -
医疗器械经营企业检查记录表
- 6 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 7 -
- 8 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 9 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 10 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
- 11 -
- 12 -
该表一式两份,一份当场交相对人留存,一份由执法机关存档备案。
