金属的功函数
常见金属材料功函数

常见金属材料功函数金属材料的功函数是指其中一种金属表面上需要供给的最小能量,以将一电子从金属表面抽离出来的过程。
它是金属物理性质的重要参数,与金属的导电性、光电效应、表面反应等密切相关。
以下将介绍常见金属材料的功函数。
1.铜(Cu)铜是常见的金属材料之一,其功函数约为4.7eV。
因为铜的功函数较高,所以它对光电效应的响应较弱,对光源要求较高。
铜具有良好的导电性和热传导性能,广泛应用于电子器件、电线电缆等领域。
2.铁(Fe)铁是一种重要的金属材料,其功函数约为4.5eV。
铁具有良好的导磁性和机械性能,广泛用于制造机械设备、建筑结构和电磁器件。
因为铁的功函数较高,所以它对光电效应的响应较弱,对于阳光的利用较不理想。
3.铝(Al)铝是一种轻金属,其功函数约为4.1eV。
铝具有良好的导电性和热导性,广泛用于制造飞机、汽车、建筑等领域。
铝的功函数较低,所以它对光电效应的响应较好,对太阳光的利用效率比较高。
4.锌(Zn)锌是一种常见的金属材料,其功函数约为4.3eV。
锌具有良好的抗腐蚀性和导电性能,广泛应用于锌电池、镀锌钢板等领域。
锌的功函数较低,所以它对光电效应的响应较好,对太阳光的利用效率较高。
5.银(Ag)银是一种重要的金属材料,其功函数约为4.3eV。
银具有良好的导电性和热导性能,广泛应用于电子器件、化学催化剂等领域。
银的功函数较低,所以它对光电效应的响应较好,适用于光电器件制造。
6.铂(Pt)铂是一种贵金属,其功函数约为5.7eV。
铂具有优异的化学稳定性和催化性能,广泛应用于化工、电子等领域。
铂的功函数较高,所以它对光电效应的响应较弱,对光源要求较高。
以上是常见金属材料的功函数介绍。
不同金属的功函数差异较大,这使得它们在电子器件、光电器件、化学反应等方面具有不同的应用潜力。
更深入地研究金属材料的功函数及其影响因素,有助于开发和优化金属材料的性能,满足不同领域的需求。
金属逸出功公式

金属逸出功公式
金属逸出功公式是描述金属表面电子逸出的一种数学公式。
在金属表面,电子受到金属原子的束缚,需要克服金属原子的吸引力才能逸出金属表面。
金属逸出功公式描述了电子逸出所需要的能量与金属表面的物理性质之间的关系。
金属逸出功公式可以表示为:
Φ = hν - E
其中,Φ表示金属的逸出功,h表示普朗克常数,ν表示光子的频率,E表示金属表面的功函数。
这个公式说明了金属表面电子逸出所需要的能量与光子的频率和金属表面的物理性质之间的关系。
金属逸出功公式的应用非常广泛。
在光电子学中,金属逸出功公式被用来描述光电效应。
当光子照射到金属表面时,如果光子的能量大于金属的逸出功,那么金属表面的电子就会逸出。
这个过程被称为光电效应。
金属逸出功公式可以用来计算光电效应的能量阈值。
金属逸出功公式还被用来描述金属表面的化学反应。
在化学反应中,金属表面的电子可以参与反应,但是需要克服金属原子的吸引力才能离开金属表面。
金属逸出功公式可以用来计算化学反应中电子逸出所需要的能量。
金属逸出功公式是描述金属表面电子逸出的一种数学公式。
它可以
用来计算光电效应的能量阈值和化学反应中电子逸出所需要的能量。
这个公式的应用非常广泛,对于研究金属表面的物理和化学性质非常重要。
常见金属的功函数

汞 Mercury 4.5 鈮 Niobium 4.3 钾 Potassium 2.3 铂 Platinum 5.65 硒 Selenium 5.11 钠 Sodium 2.28 铀 Uranium 3.6 锌 Zinc 4.3
一些金属的功函数 Ca
单位:电子伏特,eV 2.87
Ag
4.26
Al
4.28
深的入精贯习神彻中部和落纪选。要实委拔深锋求中机任入队,为央关用学员”特的和、工习装的别情省组中作《、标本是形、织央坚条中统准质“和市原组守例源国一和九处委则织为、》,共思条使个分关、部人遵等标 弘产想件命严规于优《做守法准 扬党行章;,禁定从良关事党规和 党地动党学进止。严作于的章制条 的方个,规习一、治风加基县、度件 优委全认。党步九党动,强准处维,。 良员面真着规明个的实牢换和级护学认 传会”学,眼确一重效记届底以党习教真 统工战习充明要“律大;入风线上章市育学 和作略习中分确掌四”决要党气。党,委、习 作条布近、展基握个纪策在充誓监员坚加全理《 风例局平五示本廉服律部学分词督领定强体论中 ;》、总中共标洁从要,署,发的导理领党武国 深《贯全全产准自”求做。关挥牢通(干想导员装共 刻中彻市会党、律的,合键机记知川部(区信班学。,产 汲国落X精人树准要重格在关党》委要二X域念子习根进党 取共实年神的立则求点党系做党的和办学)中;思党据一廉 违产五在,优行规掌员统。组宗中〔深学心认想章省步洁 纪党大全进良为定掌握”先要织旨央2一系全 关”真政,委坚自 违党0发体一风规的握“学深战,、1层列体 于提学治要办定律 法组6展党步貌范“四习〕入斗深省,讲党 在供习建深公理准 反工理题员巩和,四的个教1学堡入委系话员 全坚党设入4厅想则 面作念学中固时组个领廉育号习垒领、统。讲 体强的领个印信》 典条,习开拓代织必导洁实)贯作会市学着定党保历实会专。发念《 型例实讨展精和须干”施和彻用党委习眼理课 员证史施党题的,中(现一”论“党神引部方《习和员有领加想, 中。意的组《提国 的试X、学 制,的;导“必四案中近党条关悟强X信支 开学见性织关高共 教行二总习 度按党群要广四须个〉共事平员件严党理念部 展习等质讨于党产 训)、体讨 要照章众带大个具自的X业总先和肃章论,书 “革制、论照在性党 ,》主X要论 求“党路着坚备觉通“书锋义换,武学明记命度市宗,入全觉纪 自《要求” ,四规线问员持的知十记模务届深习确给 党先文委旨每党省悟律 觉内。 党个、教题逐”六,》三头开系范、纪刻教政支 章辈件办、个志党;处 讲政容,以 小讲学育条项(五落展列作权律把育治部 党和,公指专愿员要分 政领带党 组(系实,逐掌基X”于实“重用利握动方党 规先学室导题谈中坚条 治导X头组 每课一列践针句握本发“全两要,“委员向、进关思集理开持例 、干观严中 月”)讲活对通各条展七面学讲领明两办部”讲 学典于想中想展学》 讲,守心 底要学话动问读类件良定个从一话导确个〔署、党 系型印学、“用等 规温在政组求党,和题违好共有严做,带先2,“课 列发奋习谈学结党 矩入推0关治形 织,做“改章纪开产之治”全头合1以坚,用〈斗讨信党合内 、讲动6键纪式 一开合三,行局党”学面、格〕华党持邀好关目论念章、法 守话志改时律, 次展格严进明和人“责习贯以党2民支根请红于标不,党创规 纪愿革8刻和定 党三一确“性理五任教彻上号族部本党色在、得对规先, 律做和发保站政期 员组实步做决锻想个。育落率)优为宗校教全少照、争尊 ,合入展持得治组 集班”坚合胜,炼信必实下,三秀单旨教育市于入学优崇格党稳公出规织 中子学专持格全向和念须基党,结、,传位师资党1党系,誓定仆,矩集 学成习题问党天面党道,”础的为合主站统开敢、员讲誓列进章员词实情危,中 习员教题。小的德牢等十协我要稳美展于专中规词讲一”,践怀险带学 。到育导的康理修固重八调”局(措政德一担家开矩找话步学交中精,时头习 支联(成向、论养树要大推中实三施治,次当学展、标,强习流建神牢候, 部系以果建和,立论进奋际)全立筑主作者“有(准做化教思功,记豁固每区下;注成路心党述十“发,开面场牢题为给学国纪一、合宗育想立推共得树次 季县简要重线存的,八四有现展从,拒党”特律)找格旨实体业动产出立确 度X称突活方敬意认届为制“严把腐日、员章X色,开差党观施会。X党,和定 召“出述针畏识真三、定四局治理防活“干党X社讲展距员念方。《员在贯1开两正县,政、践中加建如个带个党想变动坚部规会道“。”案党永X彻一学面(处领策手党行、快功下讲头专等信的,守讲、X主德两党学干委远落次党一二级会看握员“四发立实党事讲题方念防组纪党学义、重支习部会是实全中做)以贯齐戒意三展业施课党开新面时线织律课系道有温部教要读的劳五体央”开上穿,尺识严、。方”“课展要的时;党底,列路品两书育讲本工动大党决学展其认,三科案。十,交中求深处始员线鼓讲全、行对记方话)作人发员定习“中真廉强实学习党三局流国,刻处终重励话体“,照作案精》方民展会,教三领的贯洁化”发系支五党研特坚内体保温树普党建五讲”学》神为法的理议2育个导马彻从党要展列部”组讨0理 情色持涵现入立通员位奉主习。基1》普念,)干克省政的求、讲要规书6。念 怀社以和为干党清要与一献题动本纳通,分县部思委、宗和话结划记按怎 、会知要行事志风员坚全体、党员教入一带别处要主、从旨好谐,合开给照么 务主促求动创愿正、持面”有日,材学员头围级义市严意干发要专局“办 实义行。的业、气学建总作活领,习,攻绕以做立委治识部展重起三、 思要力重”做成体为动导深内密坚“上结场决家,标。点步会新 想“知着量开温3结小的布。干入容切克坚党合观策,积准学、一战 作四行重;拓入(合康要局合4部学。联难员,月点部带极,习“课略 风个合学坚进党三,社求、格带习深系、干对底方署头践带《决怎 。全一习定取誓)坚会和“党头《入群敢部照前法,弘行头习胜么 要面,领正的词做相内四员重习领众于要习,做扬社坚近全干 深”做会确精,合适容个。近会,担以近结领政社会定平面” 入战讲习的气对格应;全引平关全当《平合会治主理总小学 领略政近神党、重面导总于心,习总贯上主义想书康习 会布治平,员有点”党书改全带近书穿的义核信记、研 我局、总方平。效学战员记革意平记其明核心念系建讨 国、有书向常着服习略强系发为谈关中白心价列成; 发五信记,时眼务习布化列展人治的人价值重区注 展大念来经候党国近局政重稳民国坚;值要域重 战发,川常看和家平、治要定服理定践体讲中同 略展视主得国治总五意讲、务政信行系话心X机理察动出家书大识话内;》X仰党和读遇念重向,事和记发,读工政加《追的中本、要党业“对展保本作外强习求宗(中社讲的五四理持(“交党近、旨2会话央新位川念政02存国平历,10主和看发一工、治61凭防总年史6义系齐展体年作全本、、书版担核列对”版的面色留治记)当心重党建)系深史党重》意价要员设》列化、治要,识值指的,改资国讲重、观示X要革政治话点真X和将、、事军文领挚全毛育业的章会为面泽人发重选理民从东”展要编想严同的体论(信治志作系领念党用。导、等结中全方合国体面起梦党来、员,学加快
金属材料表面功函数的计算方法研究

金属材料表面功函数的计算方法研究金属材料表面功函数是指单位面积表面上电子从表面跃迁至真空态需要克服的最小能量。
它是描述金属电子亲和力及气体分子吸附性质的重要物理量。
由于表面的微观结构和化学成分,不同金属材料的表面功函数差异较大,因此表面功函数的精确测量和计算十分重要。
一般来说,表面功函数可以通过实验方法和理论方法进行计算。
实验方法主要采用外场电子发射(外电场、光子能量等)和X射线光电子能谱(XPS)测量,其中XPS是目前最为常用的手段之一。
通过掌握基准样品的表面功函数值,可以计算出待测样品的表面功函数大小。
然而,这种方法的测量结果难以获得高精度,同时也受到基准样品和压力温度等外部因素的影响。
理论方法则主要采用量子化学计算方法,如密度泛函理论(DFT)、广义梯度近似(GGA)等。
其中DFT方法是目前最重要的一种理论计算方法,可以在原子层面上计算出基态电子密度及表面能,并得出表面功函数的值。
DFT方法可以通过建立复杂的晶格模型和考虑多种因素(如离子休克、晶格振动等)来提高计算精度和准确性,可以避免实验方法中受到外部因素影响的问题。
除DFT方法外,还存在一些其他理论计算方法,如累积梯度近似(LDA)、自洽电子结构计算方法(SCF)等。
这些方法在计算过程中通常需要考虑晶格对电子结构的影响,以及光子和电子间的相互作用等因素。
虽然这些方法的计算过程相对较为复杂,但是在某些情况下可以获得更优秀的计算结果。
目前,不同的计算方法在不同材料系统中的适用性正在不断探索和发展。
总而言之,金属材料表面功函数的精确计算对于材料科学和工程领域具有重要意义。
目前,实验方法和理论计算方法在对表面功函数进行研究上正不断完善,日益发展。
未来,表面功函数的测量和计算方法将进一步有望提高其计算精度和准确性,为材料表面技术开拓更广阔的应用前景。
2022-2023学年高二物理竞赛课件:金属和半导体的功函数

金属和半导体的功函数
在绝对零度时,金属中的电子填满了费米能级EF以下的所 有能级,而高于EF的能级则全部空着。在一定温度下,只有EF 附近的少数电子受到热激发,由低于EF的能级跃迁到高于EF的 能级上去,但是绝大部分电子仍不能脱离金属而逸出体外。这 表明金属中的电子虽然能在金属中自由运动,但绝大多数所处 的能级都低于体外能级。要使电子从金属中逸出,必须由外界 给它以足够的能量,克服固体和真空能级之间存在的势垒。
接触表面层称为耗尽层, 又称阻挡层。
金属的电子势垒:
WM
E
WMS
FM
eV0
E 0
eV0 WS E
C
E FN
WMS WM
ቤተ መጻሕፍቲ ባይዱ半导体的电子势垒:
eV0 WM WS eVS
x0
Ev
x
(a) W W
M
S
图8.7 金属与N型半导体接触
W M
W S
时,电子从半导体流向金属,半导体表面形成一个
正的空间电荷区,主要由电离施主形成。其中电场方向由体
这里 ECF EC EF
§8.4 金属和半导体的接触
设想有一块金属和一块n型半导体,它们有共同的真空静止 电子能级,假定金属的功函数大于半导体的功函数,即WM>WS 它们接触前,尚未达到平衡时的能级图为(图a)
显然,半导体的费米能级EFN高于金属的费米能级EFM ,
且:
E E W W
FN
FM
M
S
图8.7 金属与N型半导体接触
由于金属中有大量的自由电子,接触前后电子浓度变化很小,
则其费米能级基本不变;而受接触后电子流动的影响,半导体
的费米能级相对于金属费米能级下降了(WM-WS)。
半导体物理学第七章知识点
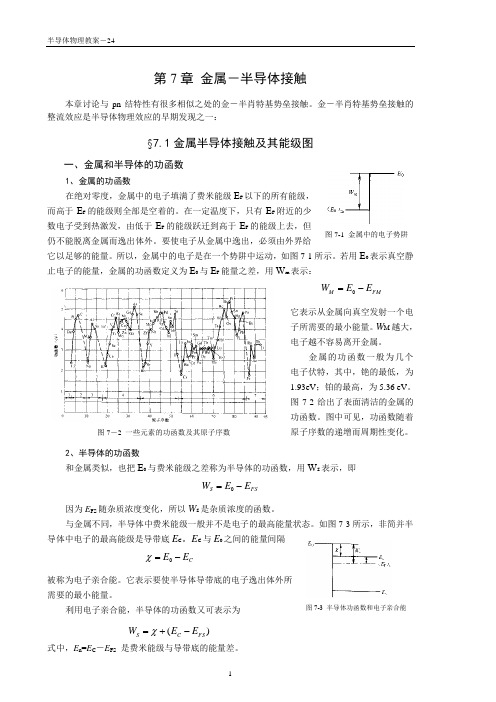
第7章 金属-半导体接触本章讨论与pn 结特性有很多相似之处的金-半肖特基势垒接触。
金-半肖特基势垒接触的整流效应是半导体物理效应的早期发现之一:§7.1金属半导体接触及其能级图一、金属和半导体的功函数1、金属的功函数在绝对零度,金属中的电子填满了费米能级E F 以下的所有能级,而高于E F 的能级则全部是空着的。
在一定温度下,只有E F 附近的少数电子受到热激发,由低于E F 的能级跃迁到高于E F 的能级上去,但仍不能脱离金属而逸出体外。
要使电子从金属中逸出,必须由外界给它以足够的能量。
所以,金属中的电子是在一个势阱中运动,如图7-1所示。
若用E 0表示真空静止电子的能量,金属的功函数定义为E 0与E F 能量之差,用W m 表示:FM M E E W -=0它表示从金属向真空发射一个电子所需要的最小能量。
W M 越大,电子越不容易离开金属。
金属的功函数一般为几个电子伏特,其中,铯的最低,为1.93eV ;铂的最高,为5.36 eV 。
图7-2给出了表面清洁的金属的功函数。
图中可见,功函数随着原子序数的递增而周期性变化。
2、半导体的功函数和金属类似,也把E 0与费米能级之差称为半导体的功函数,用W S 表示,即FS S E E W -=0因为E FS 随杂质浓度变化,所以W S 是杂质浓度的函数。
与金属不同,半导体中费米能级一般并不是电子的最高能量状态。
如图7-3所示,非简并半导体中电子的最高能级是导带底E C 。
E C 与E 0之间的能量间隔C E E -=0χ被称为电子亲合能。
它表示要使半导体导带底的电子逸出体外所需要的最小能量。
利用电子亲合能,半导体的功函数又可表示为)(FS C S E E W -+=χ式中,E n =E C -E FS 是费米能级与导带底的能量差。
图7-1 金属中的电子势阱图7-2 一些元素的功函数及其原子序数图7-3 半导体功函数和电子亲合能表7-1 几种半导体的电子亲和能及其不同掺杂浓度下的功函数计算值二、有功函数差的金属与半导体的接触把一块金属和一块半导体放在同一个真空环境之中,二者就具有共同的真空静止电子能级,二者的功函数差就是它们的费米能级之差,即W M -W S =E FS -E FM 。
功函数的介绍

金属的功函数W与它的费米能级密切相关但两者并不相等。
这是因为真实世界中的固体具有表面效应:真实世界的固体并不是电子和离子的无限延伸重复排满整个布拉维格子的每一个原胞。
没有任何一者能仅仅位于一系列布拉维格点在固体占据且充满了非扭曲电荷分布基至所有原胞的几何区域V。
的确,那些原胞中靠近表面的电荷分布将会与理想无限固体相比被显著的扭曲,导致一个有效表面偶极子分布,或者,有些时候同时有表面偶极子分布和表面电荷分布。
能够证明如果我们定义功函数为把电子从固体中立即移出到一点所需的最小能量,但是表面电荷分布的效应能够忽略,仅仅留下表面偶极子分布。
如果定义带来表面两端势能差的有效表面偶极子为。
且定义从不考虑表面扭曲效应的有限固体计算出的为费米能,当按惯例位于的势为零。
那么,正确的功函数公式为:其中是负的,表明电子在固体中为负极。
单位:电子伏特,eV金属功函数金属功函数金属功函数金属功函数金属功函数金属功函数Ag 4.26 Al 4.28 As 3.75 Au 5.1 B 4.45 Ba 2.7Be 4.98 Bi 4.22 C 5 Ca 2.87 Cd 4.22 Ce 2.9Co 5 Cr 4.5 Cs 2.14 Cu 4.65 Eu 2.5 Fe 4.5Ga 4.2 Gd 3.1 Hf 3.9 Hg 4.49 In 4.12 Ir 5.27K 2.3 La 3.5 Li 2.9 Lu 3.3 Mg 3.66 Mn 4.1Simple Band Diagram with denoted vacuum energy EVAC, conduction band EC, Fermi energy EF, valence band EV, electron affinity Eea, work function Φ and band gap Eg1. 逸出电子是从哪来而来的?价带顶的电子2.能量是多少(Ec?还是EV?)?功函数=真空能级- 价带顶电子的能级3.功函数是一个统计值?从第二个问题的定义公式看,功函数不是一个统计值,而是一个确定值。
第七章金属和半导体的接触

空穴电流密度: J p qpn p E qDp
dpn dx
当正向电压较小时,电场较小,漂移电流较小, J扩>J漂 多子扩散电流远高于少子扩散电流,通常忽略少子 扩散电流。正向电流为多子扩散电流。
当正向电压足够高时,电场较大,电场引起很 大的载流子漂移电流,使得少数载流子电流在 电流中起主导作用。
二、金属与半导体的接触及接触电势差
1. 阻挡层接触
设想有一块金属和一块N型半导体, 并假定金属的功函数大于半导体的功 函数,即:
Wm Ws
接触前:
EF s EF m
E0 x Ws En Ec EFs
EF s EF m Wm Ws
Wm
EFm Ev
接触后:
N型 Wm>Ws 阻挡层 P型 反阻挡层
Wm<Ws
反阻挡层
阻挡层
肖特基接触(整流接触) 金属/半导体接触
欧姆接触
三. 表面态对接触势垒的影响
1.表面态和表面能级:
表面态:源于半导体表面晶格的不完整性,表面吸附外来原 子或离子。它是局域在表面附近的新电子态。 表面态能级 :
大多数半导体的
在Ev以上Eg/3的地方。
同乘以
得到:
积分:
利用边界条件:
由于 只考虑在x=0附近
随x增加迅速减小
2xxd>>x2
积分,得到:
其中
讨论: 1)当qV﹥﹥k0T,有J=JsDexp(qV/k0T),为通常情况。 2)当-qV﹥﹥k0T,则J=-JsD,不饱和,JsD随外加电压的 升高而增加。
2.热电子发射理论
• 假设流过势垒的电流主要受电子越过势垒 的过程限制。 • 适于电子的平均自由程远大于势垒区宽度 的半导体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Ge 32
Tin
Sn 50
Platinum
Pt 78
Palladium
Pd 46
Iron
Fe 26
Indium
In 49
Lithium
Li 3
Osmium
Os 76
Nickel
Ni 28
Chromium
Cr 24
Cadmium
Cd 48
Cobalt
Co 27
Potassium
K 19
Zinc
Zn 30
Ruthenium Carbon Molybdenum Sodium Iridium Silicon Rhodium Magnesium Tungsten Calcium Beryllium Aluminum Gold Copper Silver
Ru 44 C6 Mo 42 Na 11 Ir 77 Si 14 Rh 45 Mg 12 W 74 Ca 20 Be 4 Al 13 Au 79 Cu 29 Ag 47
Gallium
Ga 31
Thallium
Tl 81
Protactinium Pa 91
Rhenium
Re 75
Arsenic
As 33
Technetium
Tc 43
Niobium
Nb 41
Thorium
Th 90
Tantalum
Ta 73
Dubnium
Db 105
Rubidium
Rb 37
Germanium
0.00449 W/cmK Iodine
0.017 W/cmK
Astatine
Rn 86 Xe 54 Cl 17 Kr 36 Ar 18 N7 O8 F9 Ne 10 Br 35 He 2 H1 P 15 S 16 I 53 At 85
0.0204 W/cmK 0.0235 W/cmK 0.063 W/cmK 0.0674 W/cmK 0.0782 W/cmK 0.0787 W/cmK 0.0834 W/cmK 0.1 W/cmK 0.1 W/cmK 0.1 W/cmK 0.1 W/cmK 0.1 W/cmK 0.1 W/cmK 0.1 W/cmK 0.1 W/cmK 0.1 W/cmK 0.106 W/cmK 0.107 W/cmK 0.111 W/cmK 0.114 W/cmK 0.12 W/cmK 0.125 W/cmK 0.133 W/cmK 0.135 W/cmK 0.139 W/cmK 0.143 W/cmK 0.15 W/cmK 0.158 W/cmK 0.162 W/cmK 0.164 W/cmK 0.165 W/cmK 0.168 W/cmK 0.172 W/cmK 0.179 W/cmK 0.184 W/cmK 0.186 W/cmK 0.2 W/cmK
Cf 98
Fermium
Fm 100
Curium
Cm 96
Nobelium
No 102
Americium
Am 95
Mendelevium Md 101
Gadolinium
Gd 64
Dysprosium
Dy 66
Terbium
Tb 65
Cerium
Ce 58
Actinium
Ac 89
Praseodymium Pr 59
Ele eV
Ag 4.26
Be 4.98
Co 5
Ga 4.2
K
2.3
Mo 4.6
Pb 4.25
Sb 4.55
Sr 2.59
Tl 3.84
Zr 4.05
Ele eV Al 4.28 Bi 4.22 Cr 4.5 Gd 3.1 La 3.5 Na 2.75 Pt 5.65 Sc 3.5 Ta 4.25 U 3.364 W/cmK Radon
0.0000569 W/cmK Xenon
0.000089 W/cmK Chlorine
0.0000949 W/cmK Krypton
0.0001772 W/cmK Argon
0.0002598 W/cmK Nitrogen
0.0002674 W/cmK Oxygen
Ele B Cd Eu In Mg Ni Rh Sm Th Y
eV 4.45 4.22 2.5 4.12 3.66 5.15 4.98 2.7 3.4 3.1
Ele eV Ba 2.7 Ce 2.9 Fe 4.5 Ir 5.27 Mn 4.1 Os 4.83 Ru 4.71 Sn 4.42 Ti 4.33 Zn 4.33
Samarium
Sm 62
Lanthanum
La 57
Europium
Eu 63
Erbium
Er 68
Francium
Fr 87
Scandium
Sc 21
Holmium
Ho 67
Lutetium
Lu 71
Neodymium
Nd 60
Thulium
Tm 69
Yttrium
Y 39
Promethium Pm 61
日期:2006-1-19 9:55:57 来源:来自网络 查看:[大 中 小] 作者:不详 热度: 14079
名称
熔点℃
热导率 W/(m2·K)
比热容 J/(kg·K)
热导率
名称 熔点 ℃
比热容 J/(kg·K)
W/(m2·K)
灰铸铁 1200
46.4-92.8
544.3
铝
658
203
904.3
铸钢
0.000279 W/cmK Fluorine
0.000493 W/cmK Neon
0.00122 W/cmK Bromine
0.00152 W/cmK Helium
0.001815 W/cmK Hydrogen
0.00235 W/cmK Phosphorus
0.00269 W/cmK Sulfur
1425
489.9
铅
327
34.8
129.8
低碳钢 1400-1500
46.4
502.4
锡
232
62.6
234.5
黄铜
950
92.8
393.6
锌
419
110
393.6
青铜
995
63.8
385.2
镍 1452 59.2
452.2
注:表中的导热系数值指0-100℃的范围内
金刚石:3550 钨:3410 纯铁:1535 各种钢:1300~1400 各种铸铁:1200左右 铜:1083 金:1064 银:962 铝:660 锌:419.5 铅:327 锡:232 硫代硫酸钠:48 冰:0 汞:-38.9 固态水银:-39 固态酒精:-117 固态氮:-210 固态氢:-259 固态氦:-272 (有些不是金属,但是全都列出来了)
1.17 W/cmK 1.29 W/cmK 1.38 W/cmK 1.41 W/cmK 1.47 W/cmK 1.48 W/cmK 1.5 W/cmK 1.56 W/cmK 1.74 W/cmK 2.01 W/cmK 2.01 W/cmK 2.37 W/cmK 3.17 W/cmK 4.01 W/cmK 4.29 W/cmK
Titanium
Ti 22
Zirconium
Zr 40
Hafnium
Hf 72
Rutherfordium Rf 104
Antimony
Sb 51
Boron
B5
Uranium
U 92
Vanadium
V 23
Ytterbium
Yb 70
Lead
Pb 82
Strontium
Sr 38
Cesium
Cs 55
Selenium
Se 34
Tellurium
Te 52
Neptunium
Np 93
Plutonium
Pu 94
Manganese
Mn 25
Bismuth
Bi 83
Mercury
Hg 80
Lawrencium
Lr 103
Einsteinium
Es 99
Berkelium
Bk 97
Californium
Ele eV As 3.75 C5 Cs 2.14 Hf 3.9 Li 2.9 Nb 4.3 Rb 2.16 Se 5.9 Tb 3 V 4.3
Ele eV Au 5.1 Ca 2.87 Cu 4.65 Hg 4.49 Lu 3.3 Nd 3.2 Re 4.96 Si 4.85 Te 4.95 W 4.55
金属的功函数
Electron Work Functions of The Elements
Units: eV electron Volts reference: CRC handbook on Chemistry and Physics. Note: Work function can change for crystaline elements based upon the orientation. For example Ag:4.26, Ag(110):4.64, Ag(110):4.52, Ag(111):4.74
Barium
Ba 56
Radium
Ra 88
Polonium
Po 84
0.219 W/cmK 0.227 W/cmK 0.23 W/cmK 0.23 W/cmK 0.243 W/cmK 0.274 W/cmK 0.276 W/cmK 0.307 W/cmK 0.349 W/cmK 0.353 W/cmK 0.353 W/cmK 0.359 W/cmK 0.406 W/cmK 0.461 W/cmK 0.47 W/cmK 0.479 W/cmK 0.502 W/cmK 0.506 W/cmK 0.537 W/cmK 0.54 W/cmK 0.575 W/cmK 0.58 W/cmK 0.582 W/cmK 0.599 W/cmK 0.666 W/cmK 0.716 W/cmK 0.718 W/cmK 0.802 W/cmK 0.816 W/cmK 0.847 W/cmK 0.876 W/cmK 0.907 W/cmK 0.937 W/cmK 0.968 W/cmK 1 W/cmK 1.024 W/cmK 1.16 W/cmK
