有机化学-二烯烃 共轭体系-2018年
合集下载
二烯烃和共轭体系

4、共轭体系的分类 (1)π-π共轭 结构特征:双(叁)键、单键、双(叁)键交替 连接。 − + − + δ δ δ δ 4 CH2 CH CH CH 2 π4
C H 2= C H
(2)p-π共轭
δ
+
δ
−
CH =O
δ
+
δ
−
π4 4
与双键碳原子直接相连的原子上有 p 轨道 (或未共用电子),这个p 轨道与π 键的 p 轨 道平行,从侧面重叠构成 p ,π - 共轭体系。
+
1,3-丁二烯
CH 2 CH 2
200 C
。
环己烯
高压
双烯体 亲双烯体
双烯体:共轭双烯。 亲双烯体:烯烃或炔烃( 重键碳上连吸电子基)。
CHO COOR O O O
+Байду номын сангаас
1,3-丁二烯 (s-顺式)
CH2 CH2
=
环状过渡态 环己烯
亲双烯体上带有吸电子基如:-CHO、-COR、 -CN、-NO2时,Diels-Alder反应更容易进行。
1,3-丁二烯的结构示意图
1,3-丁二烯的π键
① 分子在同一平面 内; ② 四个碳原子各余 下一个垂直于此分 子平面的p轨道,且 互相平行,因而形 成一个离域的大π 4 π 键( 4 ),四个p 电子在四个原子间 运动。这样的共轭 也叫做π-π共轭。
δ δ δ CH2 CH CH
极性分子
−
+
−
δ CH2
CH2 CH2 CH =CH2 。 1 碳正离子
+
δ
CH =CH2
+
反应活性中间体的稳定性是: 烯丙型碳正离子 >
二烯烃的相关性质.
1,4-¼ ¼¼-2-¼ ¼¼ ¨¼ ¼ à ¼ 3,4-¼ ¼¼-1-¼ ¼¼ ¨¼¼ ¼ 1,4-¼ ¼¼¼ ú ¼ 1,2-¼ ¼¼¼ ú ¼
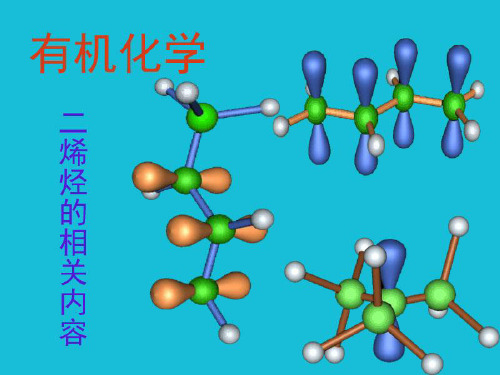
CH2=CH-CH=CH2
HBr
H Br Br H CH2-CH=CH-CH2 + CH2=CH-CH-CH2
1-¼ ¼-2-¼ ¼¼ ¼ ¨¼ à ¼ 1,4-¼ ¼¼¼ ú ¼ ¨¼¼ 2-¼ ¼-1-¼ ¼¼ ¼ 1,2-¼ ¼¼¼ ú ¼
14
彭永杰
小 结 共轭体系的表示方法及其特点:
①用弯箭头表示由共轭效应引起的电子流动方向;
②共轭碳链产生极性交替现象,并伴随着键长平均化; ③共轭效应不随碳链增长而减弱。
CH2
CH
CH
Leabharlann CH
CH
CH
CH
CH 2
2018/10/4
彭永杰
15
超共轭作用
H H C H
+
H H
一般情况下,以1,4-加成为主,但其他反应条件也对产物的组成有影响: ◇ 高温有利于1,4-加成,低温有利于1,2-加成; ◇ 极性溶剂有利于1,4-加成,非极性溶剂有利于1,2-加成。
2018/10/4
彭永杰
6
(3) 双烯合成
+
1,3-丁二烯
CH2 CH2
200 C
。
环己烯
高压
双烯体 亲双烯体
该反应旧键的断裂和新键的生成同时进行,途经一个 环状过渡态:
C
在乙基碳正离子中,带正电的碳原子上空的P轨道与甲基上C-H键 的电子云部分重叠,使部分正电荷向甲基分散,碳正离子的稳定性也相应 提高。这与Pπ共轭体系使烯丙基碳正离子稳定性提高有相似地方,称超共 轭作用(hyperconjugation)。甲基越多,碳正离子越稳定。故:
CH2=CH-CH=CH2
HBr
H Br Br H CH2-CH=CH-CH2 + CH2=CH-CH-CH2
1-¼ ¼-2-¼ ¼¼ ¼ ¨¼ à ¼ 1,4-¼ ¼¼¼ ú ¼ ¨¼¼ 2-¼ ¼-1-¼ ¼¼ ¼ 1,2-¼ ¼¼¼ ú ¼
14
彭永杰
小 结 共轭体系的表示方法及其特点:
①用弯箭头表示由共轭效应引起的电子流动方向;
②共轭碳链产生极性交替现象,并伴随着键长平均化; ③共轭效应不随碳链增长而减弱。
CH2
CH
CH
Leabharlann CH
CH
CH
CH
CH 2
2018/10/4
彭永杰
15
超共轭作用
H H C H
+
H H
一般情况下,以1,4-加成为主,但其他反应条件也对产物的组成有影响: ◇ 高温有利于1,4-加成,低温有利于1,2-加成; ◇ 极性溶剂有利于1,4-加成,非极性溶剂有利于1,2-加成。
2018/10/4
彭永杰
6
(3) 双烯合成
+
1,3-丁二烯
CH2 CH2
200 C
。
环己烯
高压
双烯体 亲双烯体
该反应旧键的断裂和新键的生成同时进行,途经一个 环状过渡态:
C
在乙基碳正离子中,带正电的碳原子上空的P轨道与甲基上C-H键 的电子云部分重叠,使部分正电荷向甲基分散,碳正离子的稳定性也相应 提高。这与Pπ共轭体系使烯丙基碳正离子稳定性提高有相似地方,称超共 轭作用(hyperconjugation)。甲基越多,碳正离子越稳定。故:
第四章 二烯烃与共轭体系

反-5,6-二甲基环己二烯
光照 顺旋
CH3 H CH3 H
(Z,Z,E)-2,4,6-辛三烯
对旋
光照 顺旋
H H CH3 CH3
顺-5,6-二甲基环己二烯
CH3 H H CH3
加热 对旋 (E,Z,E)-2,4,6-辛三烯
4.5.4 双烯合成:Diels-Alder 反应
•含环己烯环的化合物的制备方法
CH2
+
BrCH2CH
CHCH2Br
Br
(37%) (63%)
结论
1,4加成产物更稳定; 1,2加成产物和1,4加成产物是可逆的; 1,2加成产物的活化能低,反应速度快。
练习题: 由丁二烯合成重要的药物前体及 材料合成中间体3-羟甲基戊二酸
HO2C
OH CO2H
HO2C
OH CO2H
第四章 二烯烃与共轭体系
分子中含有两个碳–碳双键的不饱和烃称为二烯 烃, 包括链状二烯烃和环状二烯烃.
链状二烯烃
环状二烯烃
4.1 二烯烃的分类和命名
•隔离二烯烃 •共轭二烯烃
C
•累积二烯烃
4.2 二烯烃的结构
(1) 丙二烯的结构 (2) 1,3–丁二烯的结构
4.2 二烯烃的结构
4.2.1 丙二烯的结构
C +
+
+ C -
C + C +
p *3
C -
C
p2
成 键 轨 道
+ C + C -
+ C + C -
C + + C -
C + + C -
+ C + C C C C C
光照 顺旋
CH3 H CH3 H
(Z,Z,E)-2,4,6-辛三烯
对旋
光照 顺旋
H H CH3 CH3
顺-5,6-二甲基环己二烯
CH3 H H CH3
加热 对旋 (E,Z,E)-2,4,6-辛三烯
4.5.4 双烯合成:Diels-Alder 反应
•含环己烯环的化合物的制备方法
CH2
+
BrCH2CH
CHCH2Br
Br
(37%) (63%)
结论
1,4加成产物更稳定; 1,2加成产物和1,4加成产物是可逆的; 1,2加成产物的活化能低,反应速度快。
练习题: 由丁二烯合成重要的药物前体及 材料合成中间体3-羟甲基戊二酸
HO2C
OH CO2H
HO2C
OH CO2H
第四章 二烯烃与共轭体系
分子中含有两个碳–碳双键的不饱和烃称为二烯 烃, 包括链状二烯烃和环状二烯烃.
链状二烯烃
环状二烯烃
4.1 二烯烃的分类和命名
•隔离二烯烃 •共轭二烯烃
C
•累积二烯烃
4.2 二烯烃的结构
(1) 丙二烯的结构 (2) 1,3–丁二烯的结构
4.2 二烯烃的结构
4.2.1 丙二烯的结构
C +
+
+ C -
C + C +
p *3
C -
C
p2
成 键 轨 道
+ C + C -
+ C + C -
C + + C -
C + + C -
+ C + C C C C C
二烯烃和共轭体系

H
.. .
C
.
C H
Cl
多电子共轭π键 共轭) 多电子共轭 键(p-π共轭 共轭 电子数大于原子数,双键或三键碳原子上连接的原子带有孤对电子。 电子数大于原子数,双键或三键碳原子上连接的原子带有孤对电子。 由孤电子的p轨道和双键 轨道参与的共轭, 轨道和双键π轨道参与的共轭 由孤电子的 轨道和双键 轨道参与的共轭,叫p-π共轭 共轭
π- π共轭体系中的电子效应 共轭体系中的电子效应
δ
+ =CH2 =
π- π共轭体系中 不管共轭链有多长 分子一端电子云受到的影 共轭体系中, 共轭体系中 不管共轭链有多长, 响能通过共轭链传递到另一端. 响能通过共轭链传递到另一端 共轭体系中的这种特殊的电子效应叫做共轭效应 共轭效应. 共轭体系中的这种特殊的电子效应叫做共轭效应
+ H H H
.
C
.
C
C H
H
烯丙基自由基(p-π共轭 : 共轭) 烯丙基自由基 共轭 其未成对电子的p轨道与双键 轨道在侧面相互交盖 其未成对电子的 轨道与双键π轨道在侧面相互交盖,构成的共 轨道与双键 轨道在侧面相互交盖, 轭体系也叫p-π共轭 共轭。 轭体系也叫 共轭。
4.5.3.超共轭: 超共轭: 超共轭
CH2
CH2 C C H
H CH2
H
s-顺式
s-反式
“s”表示单键(single bond),s-顺式表示两个双键在单键的 表示单键( 表示单键 , 顺式表示两个双键在单键的 同侧; 反式表示两个双键在单键的两侧 反式表示两个双键在单键的两侧。 同侧;s-反式表示两个双键在单键的两侧。
无法改变的 S-顺构象
H H C1 H H H H C C H C C H H C
.. .
C
.
C H
Cl
多电子共轭π键 共轭) 多电子共轭 键(p-π共轭 共轭 电子数大于原子数,双键或三键碳原子上连接的原子带有孤对电子。 电子数大于原子数,双键或三键碳原子上连接的原子带有孤对电子。 由孤电子的p轨道和双键 轨道参与的共轭, 轨道和双键π轨道参与的共轭 由孤电子的 轨道和双键 轨道参与的共轭,叫p-π共轭 共轭
π- π共轭体系中的电子效应 共轭体系中的电子效应
δ
+ =CH2 =
π- π共轭体系中 不管共轭链有多长 分子一端电子云受到的影 共轭体系中, 共轭体系中 不管共轭链有多长, 响能通过共轭链传递到另一端. 响能通过共轭链传递到另一端 共轭体系中的这种特殊的电子效应叫做共轭效应 共轭效应. 共轭体系中的这种特殊的电子效应叫做共轭效应
+ H H H
.
C
.
C
C H
H
烯丙基自由基(p-π共轭 : 共轭) 烯丙基自由基 共轭 其未成对电子的p轨道与双键 轨道在侧面相互交盖 其未成对电子的 轨道与双键π轨道在侧面相互交盖,构成的共 轨道与双键 轨道在侧面相互交盖, 轭体系也叫p-π共轭 共轭。 轭体系也叫 共轭。
4.5.3.超共轭: 超共轭: 超共轭
CH2
CH2 C C H
H CH2
H
s-顺式
s-反式
“s”表示单键(single bond),s-顺式表示两个双键在单键的 表示单键( 表示单键 , 顺式表示两个双键在单键的 同侧; 反式表示两个双键在单键的两侧 反式表示两个双键在单键的两侧。 同侧;s-反式表示两个双键在单键的两侧。
无法改变的 S-顺构象
H H C1 H H H H C C H C C H H C
有机化学 第4章 二烯烃

CH2 CH CH=CH2 (5)
CH2 CH CH=CH2 (6)
CH2=CH CH CH2 (7)
共振式书写的基本原则 ➢ 参与共振的原子应有平行的 p 轨道 ➢ 所有共振式的原子排列相同 ➢ 所有共振式均符合Lewis结构式 ➢ 所有共振式具有相等的未成对电子数
CH2=CHCHCH3
CH2CH=CHCH3
诱导效应 由原子或基团电负性不同引起的;通过静电引 力沿σ键传递。其作用是近程的。
共轭效应 由p电子在整个分子轨道中的离域作用引起的, 沿π键传递。其作用是远程的 。
二者都属电子效应。当二者共存时,哪种效应的作用 占主导,要具体问题具体分析。通常共轭的作用大于诱导 的作用。
3. 超共轭效应
CH 键可以和相邻的 键上的 p 轨道有部分重叠, 电子离域,使体系能量降低,这种作用称为超共轭效 应。
-28.0kJ/mol 离域能
-254.4kJ/mol -226.4kJ/mol
共轭二烯烃比 孤立二烯烃稳定
✓ 共轭二烯的两种平面构象 共轭二烯主要以平面构象存在(为什么?)
例:1,3-丁二烯的两个平面构象
s - trans
s —— single bond 由单键产生的顺反异构
s - cis
s - trans为优势构象,二者仅相差9.6kJ·mol-1
✓ 共轭二烯稳定性
➢ 氢化热比较
氢化热(kJ/mol) 平均每个双键
H2C CH CH CH2 H2C CH CH CH CH3
238.9 226.4
119.5 较稳定
113.2
CH3 CH CH2 H3C CH2 CH CH2 H2C CH CH2 CH CH2
254.4
第4章--二烯烃 共轭体系
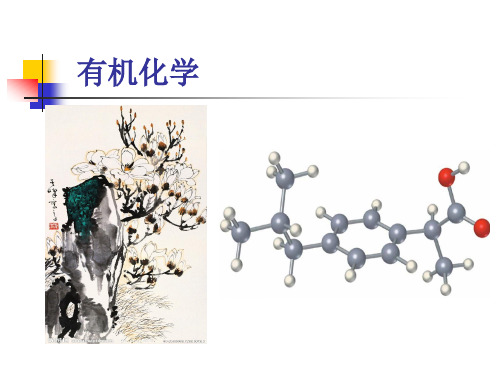
CH2Cl 高温高压
+
高温
CH2Cl HC Na
HgSO4/H2SO4
O
4.5.4 周环反应理论解释
福井谦一
伍德沃德
Robert Burns Woodward
霍夫曼 Roald Hoffmann
1981年诺贝尔化学奖
4.5.5 聚合反应
丁钠橡胶
Na n CH2 CH CH CH2 60 oC
*
CH2
4.5.2 1,4-加成的理论解释 第一步:亲电试剂H+的进攻
1
2
3
4
CH2 CH CH CH2 + H
空p轨道
H
CH3
CC
HC
H
H
CH2 CH CH CH3
稳定
CH2 CH CH2 CH2
4.5.2 1,4-加成的理论解释 第二步:溴离子( Br- )加成
共轭二烯烃的亲电加成产物1,2-加成和1,4-加成产物之比 与分子结构、所用试剂和反应条件(溶剂、温度、反应时 间)有关。
4.1.2 二烯烃的命名 主链必须包括两个双键在内,同时应标明两个双键的位置
顺反异构现象
H
H
H3C
CC
CC
CH3 S-反-(2Z, 4Z)-2,4-己二烯
H
H
s = single bond
4.2 二烯烃的结构
4.2.1 丙二烯的结构 sp sp2
H C C CH2
H 0.108nm 0.131nm
共振理论--是鲍林在20世纪30年代提出的。应用量子
力学的变分法近似地计算和处理象苯那样难于用价键 结构式代表结构的分子能量,从而认为:苯的真实结 构可以由多种假设的结构,共振(或叠加)而形成的共 振杂化体来代表。
09-二烯烃 共轭体系和共轭加成
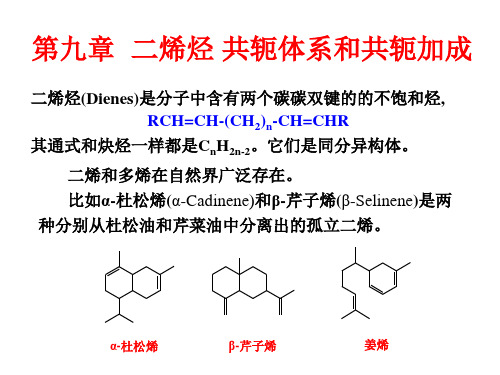
CH2=CHCH2- + H+ CH3CH2- + H+
pKa = 40 pKa = 50
丙烯分子中甲基 C-H 的酸性比烷烃强(pKa分别约为 40和50),说明其共轭碱(CH2=CH—CH2-)烯丙基 碳负离子比烷基碳负离子更稳定。
+
+
+
α - 1.414β
-
π3*
π3*
π3*
E
+
-
.
+
+
α
π2
α-杜松烯
β-芹子烯
姜烯
许多具有重要的生理活性天然分子含有共轭双键。
CH2OH
视黄醇
CHO
视黄醛
胡萝卜素
9.1 二烯烃的分类
C C C n
(共轭二烯烃) (累积二烯烃)
CH2=CH-CH=CH2 CH2=C=CH2
(孤立二烯烃)
CH2=CHCH2CH2CH=CH2
1,3-丁二烯
丙二烯
1,5-己二烯
9.4.2 共振结构和共轭效应
+
H2C CH CH2 H2C CH CH2 H2C CH CH2
烯丙基正离子
烯丙基自由基
烯丙基负离子
电子离域结构式——烯丙基碳正离子中的正电荷、烯丙基 自由基中的单电子和烯丙基碳负离子中的负电荷都不是局 限在一个p轨道中,而是分散在了三个碳原子上。
H 2C + CH-CH2 _ CH-CH2 H2C-HC _ H2C-HC
成键电子不再局限于两个原子之间而是分布在所有成 键原子上的现象称作电子的离域作用,该分子轨道称为离
域轨道。
α - 1.618β π4*
4、有机化学:二烯烃和共轭体系(4H).

分子轨道对称守恒原理主要有三种理论解释,即前线 轨道理论、能量相关理论和芳香过渡态理论。其中前线轨 道理论最为简明、易懂。
前线轨道理论是由[日]福井谦一提出的。该理论将分 子轨道中最高占有分子轨道(简称HOMO)和最低空分子 轨道(简称LUMO)统称为称为前线分子轨道(FMO), 将分布在前线分子轨道中的电子称为前线电子。认为化学 键的形成主要是由FMO的相互作用所决定的。
键迁移反应等几种类型。
1、电环化反应
1.1 含“4n”个π电子共轭多烯烃体系
CH3
H
H
顺旋
CH3
(2E,4E)-2,4-己二烯
CH3 H
H CH3
反-3,4-二甲基环丁烯
CH3 H H
CH3
hv 对旋
CH3 H3C
H H
顺-3,4-二甲基环丁烯
1.2 含“4n+2”个π电子共轭多烯烃体系
CH3 H CH3 H
CO2CH3
2、
CCO2Et +
CCO2Et
CH3 CO2CH3
CH3
?
+
CO2CH3
(61%)
(39%)
CO2Et
?
CO2Et
3、 2
?
or
4、完成反应(表明产物的立体构型)
H H
4.1
CH3
CH3
CH3 H CH3
H
(苏大06年)
O
4.2
+
O
O
O O
O
(湘大06年)
3、周环反应的理论解释
1965年,[美]伍德沃德和霍夫曼提出了“分子轨道对 称守恒原理”,从而揭开了周环反应的奥秘。
1、顺丁橡胶
前线轨道理论是由[日]福井谦一提出的。该理论将分 子轨道中最高占有分子轨道(简称HOMO)和最低空分子 轨道(简称LUMO)统称为称为前线分子轨道(FMO), 将分布在前线分子轨道中的电子称为前线电子。认为化学 键的形成主要是由FMO的相互作用所决定的。
键迁移反应等几种类型。
1、电环化反应
1.1 含“4n”个π电子共轭多烯烃体系
CH3
H
H
顺旋
CH3
(2E,4E)-2,4-己二烯
CH3 H
H CH3
反-3,4-二甲基环丁烯
CH3 H H
CH3
hv 对旋
CH3 H3C
H H
顺-3,4-二甲基环丁烯
1.2 含“4n+2”个π电子共轭多烯烃体系
CH3 H CH3 H
CO2CH3
2、
CCO2Et +
CCO2Et
CH3 CO2CH3
CH3
?
+
CO2CH3
(61%)
(39%)
CO2Et
?
CO2Et
3、 2
?
or
4、完成反应(表明产物的立体构型)
H H
4.1
CH3
CH3
CH3 H CH3
H
(苏大06年)
O
4.2
+
O
O
O O
O
(湘大06年)
3、周环反应的理论解释
1965年,[美]伍德沃德和霍夫曼提出了“分子轨道对 称守恒原理”,从而揭开了周环反应的奥秘。
1、顺丁橡胶
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1,4-¹ ¹¹ ú¹ ¹ ¹ 1,4-¹ ¹ ú ¹ ¹ 1,2-¹ ¹¹ ú¹ ¹ ¹ 1,2-¹ ¹ ú ¹ ¹
1,4-¹ ¹¹ -2-¹ ¹ ¨¹ ๠¹ 1,4-¹ ¹ ¹¹ -2-¹ ¹ ¨ à ¹ ¹ 3,4-¹ ¹¹ -1-¹ ¹ ¨¹ ¹ ¹ ¹ 3,4-¹ ¹ ¹¹ -1-¹ ¹ ¨ ¹ ¹¹
2019/1/30 12/64
4.2 二烯烃的结构
4. 二烯烃 共轭体系
4.2.2 1.3-丁二烯(共轭双烯)的结构
(3)1,3-丁二烯结构的分子轨道理论解释 分子轨道理论主要用来处理π电子 丁二烯分子中四个碳原子上的未参加sp2杂化的p轨 道,通过线性组合形成四个分子轨道
2019/1/30
13/64
4.2 二烯烃的结构
4. 二烯烃 共轭体系
4.2.2 1.3-丁二烯(共轭双烯)的结构
(3)1,3-丁二烯结构的分子轨道理论解释
2019/1/30
14/64
《有机化学》
第4章 二烯烃 共轭体系
4.1 4.2 4.3 4.4 4.5 4.6 4.7
2019/1/30
二烯烃的分类和命名 二烯烃的结构 电子离域与共轭体系 离域体系的共振论表述法(自学) 共轭二烯烃的化学性质 共轭二烯烃的工业制法(自学) 环戊二烯(自学)
一般情况下,以1,4-加成为主 高温利于1,4-加成,低温利于1,2-加成;
2019/1/30 23/64
4.5 共轭二烯烃的化学性质 4.5.2 1,4-加成的理论解释
(1)1,3-丁二烯与HBr加成
4. 二烯烃 共轭体系
p空
HBr
+
+
CH2=CH-CH=CH2
[CH2=CH-CH-CH3]
共轭效应: 由于电子的离域使体系的能量降低、分子趋于稳定、键长 趋于平均化的现象叫做共轭效应(Conjugative effect,用C 表示——C效应)
离域能: 由于共轭体系中键的离域而导致分子更稳定的能量 离域能越大,体系越稳定
2019/1/30 17/64
4.3 电子离域与共轭体系
2019/1/30
19/64
4.3 电子离域与共轭体系 4.3.1 π-π共轭
4. 二烯烃 共轭体系
π电子离域所体现的共轭效应称为π-π共轭效应
参与共轭的重键不限于两个,亦可以是多个
共轭体系表示方法 思考:与诱导效应有什么不同? ①共轭碳链产生电荷正负交替现象 ②共轭效应不随碳链增长而减弱 (不管多大,共轭效应贯穿于整个共轭体系中)
C
CH3 H p空
+
sp 3
d CH 2
+
H2C + CH 2 ] CH =CH-CH-CH 2 3
CH2
CH 2 CH
Br-
CH
2
d
+
1
Br CH2-CH=CH-CH3
1,4-加成产物 2
CH 3
1
Br H CH2=CH-CH-CH2
1,2-加成产物
25/64
2019/1/30
4.5 共轭二烯烃的化学性质 4.5.2 1,4-加成的理论解释
s-反-1,3-丁二烯 s-(E)- 1,3-丁二烯
7/64
《有机化学》
第4章 二烯烃 共轭体系
4.1 4.2 4.3 4.4 4.5 4.6 4.7
2019/1/30
二烯烃的分类和命名 二烯烃的结构 电子离域与共轭体系 离域体系的共振论表述法(自学) 共轭二烯烃的化学性质 共轭二烯烃的工业制法(自学) 环戊二烯(自学)
15/64
4.3 电子离域与共轭体系
什么是共轭体系?
4. 二烯烃 共轭体系
成键电子不局限于成键原子之间的分子体系 举例: 1,3-丁二烯分子
2019/1/30
16/64
4.3 电子离域与共轭体系
4. 二烯烃 共轭体系
什么是共轭体系? 成键电子不局限于成键原子之间的分子体系 电子离域: 共轭体系中成键原子的电子云运动范围扩大的现象;又 称为键的离域,使共轭体系能量降低
离域能:
4. 二烯烃 共轭体系
由于共轭体系中键的离域而导致分子更稳定的能量 离域能越大,体系越稳定 1,4-戊二烯 1,3-戊二烯
2H2 2H2 氢化热/kJmol-1 254 226
共轭体系由什么结构特征呢? 构成共轭体系的原子必须共平面 p轨道垂直于该平面
2019/1/30 1烯烃的化学性质 4.5.2 1,4-加成的理论解释
(2)1,3-丁二烯与Br2加成
4. 二烯烃 共轭体系
C C C C + Br2
温度(℃) -80
1,2加成 80%
1,4加成 20%
-15 25 40
60
2019/1/30
46% 30% 20%
/
54% 70% 80%
有机化学
第4章 二烯烃 共轭体系
2019/1/30
1/64
《有机化学》
第4章 二烯烃 共轭体系
4.1 4.2 4.3 4.4 4.5 4.6 4.7
2019/1/30
二烯烃的分类和命名 二烯烃的结构 电子离域与共轭体系 离域体系的共振论表述法(自学) 共轭二烯烃的化学性质 共轭二烯烃的工业制法(自学) 环戊二烯(自学)
(1)1,3-丁二烯与HBr加成 温度的影响(P134)
4. 二烯烃 共轭体系
2019/1/30
26/64
4.5 共轭二烯烃的化学性质 4.5.2 1,4-加成的理论解释
(2)1,3-丁二烯与Br2加成
4. 二烯烃 共轭体系
p
+
空
H2C
CH
C
CH2Br H
CH2 CH CH CH 2 + + + d d d d
29/64
4.5 共轭二烯烃的化学性质 4.5.3 周环反应
4. 二烯烃 共轭体系
反应过程中形成环状过渡态而不生成任何活性中间体的 反应,称为周环反应。 主要特点: 旧键断裂和新键生成同时、一步完成,经过环状过渡态而 无活性中间体
受加热或光照影响明显
具有高度的立体化学专一性 电环化反应 环加成反应 σ键迁移反应
CH2=C=CH2
少见
(2)共轭双键二烯烃(共轭二烯烃)
CH2=CH-CH=CH2
(3)隔离双键二烯烃
特殊结构和性质
CH2=CH-CH2-CH=CH2
与单烯烃类似
2019/1/30 4/64
4.1 二烯烃的分类和命名 4.1.2 二烯烃的命名
4. 二烯烃 共轭体系
主链、 编号、 >10加“碳”,称“二烯” 用阿拉伯数字标明两个双键的位次 用“Z/E”或“顺/反”表明双键的构型 3-甲基-2,4-己二烯
>90%
28/64
4.5 共轭二烯烃的化学性质 4.5.3 周环反应
4. 二烯烃 共轭体系
反应过程中形成环状过渡态而不生成任何活性中间体的 反应,称为周环反应。 主要特点: 旧键断裂和新键生成同时、一步完成,经过环状过渡态而 无活性中间体
受加热或光照影响明显
具有高度的立体化学专一性
2019/1/30
2019/1/30
5/64
4.1 二烯烃的分类和命名 4.1.2 二烯烃的命名
4. 二烯烃 共轭体系
用“Z/E”或“顺/反”表明双键的构型
顺,顺-3-甲基-2,4-己二烯 (2Z,4Z)-3-甲基-2,4-己二烯 反,顺-3-甲基-2,4-己二烯 (2E,4Z)-3-甲基-2,4-己二烯 顺,反-3-甲基-2,4-己二烯 (2Z,4E)-3-甲基-2,4-己二烯
2019/1/30
二烯烃的分类和命名 二烯烃的结构 电子离域与共轭体系 离域体系的共振论表述法(自学) 共轭二烯烃的化学性质 共轭二烯烃的工业制法(自学) 环戊二烯(自学)
22/64
4.5 共轭二烯烃的化学性质 4.5.1 1,4-加成反应
Br2 Br2
4. 二烯烃 共轭体系
Br Br Br Br Br Br Br Br CH2CH -CH=CH-CH =CH-CH-CH + 2CH 2 + 2 2 2-CH=CH-CH 2 CH 2=CH-CH-CH
2019/1/30 10/64
4.2 二烯烃的结构
(2)1,3-丁二烯结构的价键理论解释 1,3-丁二烯中的碳原子是 sp2杂化态 (sp2杂化—平 面构型,轨道夹角约 120°)
4. 二烯烃 共轭体系
4.2.2 1.3-丁二烯(共轭双烯)的结构
C
四个sp2杂化碳搭起平面构 型的1,3-丁二烯的σ骨架
4.3 电子离域与共轭体系 4.3.1 π-π共轭
4. 二烯烃 共轭体系
π电子离域所体现的共轭效应称为π-π共轭效应
π-π共轭体系结构特征 单双键交替
d
CH2
+
CH
d
-
CH
d
+
d
CH 2
-
( p-p ¹é ¹)
不限于双键,叁键亦可;不限于碳,氧、氮原子均可
CH2=CH C CH 乙烯基乙炔 CH2=CH CH=O 丙烯醛 CH2=CH C N 丙烯腈
2019/1/30 9/64
4.2 二烯烃的结构
(1)结构特征 1,3-丁二烯中C的轨道结构
4. 二烯烃 共轭体系
4.2.2 1.3-丁二烯(共轭双烯)的结构
1,3-丁二烯中C的轨道特点 1,3-丁二烯分子中的10个原子共平面(优势构象) 1,3-丁二烯分子中存在着明显的键长平均化趋势
2019/1/30
1,4-¹ ¹¹ -2-¹ ¹ ¨¹ ๠¹ 1,4-¹ ¹ ¹¹ -2-¹ ¹ ¨ à ¹ ¹ 3,4-¹ ¹¹ -1-¹ ¹ ¨¹ ¹ ¹ ¹ 3,4-¹ ¹ ¹¹ -1-¹ ¹ ¨ ¹ ¹¹
2019/1/30 12/64
4.2 二烯烃的结构
4. 二烯烃 共轭体系
4.2.2 1.3-丁二烯(共轭双烯)的结构
(3)1,3-丁二烯结构的分子轨道理论解释 分子轨道理论主要用来处理π电子 丁二烯分子中四个碳原子上的未参加sp2杂化的p轨 道,通过线性组合形成四个分子轨道
2019/1/30
13/64
4.2 二烯烃的结构
4. 二烯烃 共轭体系
4.2.2 1.3-丁二烯(共轭双烯)的结构
(3)1,3-丁二烯结构的分子轨道理论解释
2019/1/30
14/64
《有机化学》
第4章 二烯烃 共轭体系
4.1 4.2 4.3 4.4 4.5 4.6 4.7
2019/1/30
二烯烃的分类和命名 二烯烃的结构 电子离域与共轭体系 离域体系的共振论表述法(自学) 共轭二烯烃的化学性质 共轭二烯烃的工业制法(自学) 环戊二烯(自学)
一般情况下,以1,4-加成为主 高温利于1,4-加成,低温利于1,2-加成;
2019/1/30 23/64
4.5 共轭二烯烃的化学性质 4.5.2 1,4-加成的理论解释
(1)1,3-丁二烯与HBr加成
4. 二烯烃 共轭体系
p空
HBr
+
+
CH2=CH-CH=CH2
[CH2=CH-CH-CH3]
共轭效应: 由于电子的离域使体系的能量降低、分子趋于稳定、键长 趋于平均化的现象叫做共轭效应(Conjugative effect,用C 表示——C效应)
离域能: 由于共轭体系中键的离域而导致分子更稳定的能量 离域能越大,体系越稳定
2019/1/30 17/64
4.3 电子离域与共轭体系
2019/1/30
19/64
4.3 电子离域与共轭体系 4.3.1 π-π共轭
4. 二烯烃 共轭体系
π电子离域所体现的共轭效应称为π-π共轭效应
参与共轭的重键不限于两个,亦可以是多个
共轭体系表示方法 思考:与诱导效应有什么不同? ①共轭碳链产生电荷正负交替现象 ②共轭效应不随碳链增长而减弱 (不管多大,共轭效应贯穿于整个共轭体系中)
C
CH3 H p空
+
sp 3
d CH 2
+
H2C + CH 2 ] CH =CH-CH-CH 2 3
CH2
CH 2 CH
Br-
CH
2
d
+
1
Br CH2-CH=CH-CH3
1,4-加成产物 2
CH 3
1
Br H CH2=CH-CH-CH2
1,2-加成产物
25/64
2019/1/30
4.5 共轭二烯烃的化学性质 4.5.2 1,4-加成的理论解释
s-反-1,3-丁二烯 s-(E)- 1,3-丁二烯
7/64
《有机化学》
第4章 二烯烃 共轭体系
4.1 4.2 4.3 4.4 4.5 4.6 4.7
2019/1/30
二烯烃的分类和命名 二烯烃的结构 电子离域与共轭体系 离域体系的共振论表述法(自学) 共轭二烯烃的化学性质 共轭二烯烃的工业制法(自学) 环戊二烯(自学)
15/64
4.3 电子离域与共轭体系
什么是共轭体系?
4. 二烯烃 共轭体系
成键电子不局限于成键原子之间的分子体系 举例: 1,3-丁二烯分子
2019/1/30
16/64
4.3 电子离域与共轭体系
4. 二烯烃 共轭体系
什么是共轭体系? 成键电子不局限于成键原子之间的分子体系 电子离域: 共轭体系中成键原子的电子云运动范围扩大的现象;又 称为键的离域,使共轭体系能量降低
离域能:
4. 二烯烃 共轭体系
由于共轭体系中键的离域而导致分子更稳定的能量 离域能越大,体系越稳定 1,4-戊二烯 1,3-戊二烯
2H2 2H2 氢化热/kJmol-1 254 226
共轭体系由什么结构特征呢? 构成共轭体系的原子必须共平面 p轨道垂直于该平面
2019/1/30 1烯烃的化学性质 4.5.2 1,4-加成的理论解释
(2)1,3-丁二烯与Br2加成
4. 二烯烃 共轭体系
C C C C + Br2
温度(℃) -80
1,2加成 80%
1,4加成 20%
-15 25 40
60
2019/1/30
46% 30% 20%
/
54% 70% 80%
有机化学
第4章 二烯烃 共轭体系
2019/1/30
1/64
《有机化学》
第4章 二烯烃 共轭体系
4.1 4.2 4.3 4.4 4.5 4.6 4.7
2019/1/30
二烯烃的分类和命名 二烯烃的结构 电子离域与共轭体系 离域体系的共振论表述法(自学) 共轭二烯烃的化学性质 共轭二烯烃的工业制法(自学) 环戊二烯(自学)
(1)1,3-丁二烯与HBr加成 温度的影响(P134)
4. 二烯烃 共轭体系
2019/1/30
26/64
4.5 共轭二烯烃的化学性质 4.5.2 1,4-加成的理论解释
(2)1,3-丁二烯与Br2加成
4. 二烯烃 共轭体系
p
+
空
H2C
CH
C
CH2Br H
CH2 CH CH CH 2 + + + d d d d
29/64
4.5 共轭二烯烃的化学性质 4.5.3 周环反应
4. 二烯烃 共轭体系
反应过程中形成环状过渡态而不生成任何活性中间体的 反应,称为周环反应。 主要特点: 旧键断裂和新键生成同时、一步完成,经过环状过渡态而 无活性中间体
受加热或光照影响明显
具有高度的立体化学专一性 电环化反应 环加成反应 σ键迁移反应
CH2=C=CH2
少见
(2)共轭双键二烯烃(共轭二烯烃)
CH2=CH-CH=CH2
(3)隔离双键二烯烃
特殊结构和性质
CH2=CH-CH2-CH=CH2
与单烯烃类似
2019/1/30 4/64
4.1 二烯烃的分类和命名 4.1.2 二烯烃的命名
4. 二烯烃 共轭体系
主链、 编号、 >10加“碳”,称“二烯” 用阿拉伯数字标明两个双键的位次 用“Z/E”或“顺/反”表明双键的构型 3-甲基-2,4-己二烯
>90%
28/64
4.5 共轭二烯烃的化学性质 4.5.3 周环反应
4. 二烯烃 共轭体系
反应过程中形成环状过渡态而不生成任何活性中间体的 反应,称为周环反应。 主要特点: 旧键断裂和新键生成同时、一步完成,经过环状过渡态而 无活性中间体
受加热或光照影响明显
具有高度的立体化学专一性
2019/1/30
2019/1/30
5/64
4.1 二烯烃的分类和命名 4.1.2 二烯烃的命名
4. 二烯烃 共轭体系
用“Z/E”或“顺/反”表明双键的构型
顺,顺-3-甲基-2,4-己二烯 (2Z,4Z)-3-甲基-2,4-己二烯 反,顺-3-甲基-2,4-己二烯 (2E,4Z)-3-甲基-2,4-己二烯 顺,反-3-甲基-2,4-己二烯 (2Z,4E)-3-甲基-2,4-己二烯
2019/1/30
二烯烃的分类和命名 二烯烃的结构 电子离域与共轭体系 离域体系的共振论表述法(自学) 共轭二烯烃的化学性质 共轭二烯烃的工业制法(自学) 环戊二烯(自学)
22/64
4.5 共轭二烯烃的化学性质 4.5.1 1,4-加成反应
Br2 Br2
4. 二烯烃 共轭体系
Br Br Br Br Br Br Br Br CH2CH -CH=CH-CH =CH-CH-CH + 2CH 2 + 2 2 2-CH=CH-CH 2 CH 2=CH-CH-CH
2019/1/30 10/64
4.2 二烯烃的结构
(2)1,3-丁二烯结构的价键理论解释 1,3-丁二烯中的碳原子是 sp2杂化态 (sp2杂化—平 面构型,轨道夹角约 120°)
4. 二烯烃 共轭体系
4.2.2 1.3-丁二烯(共轭双烯)的结构
C
四个sp2杂化碳搭起平面构 型的1,3-丁二烯的σ骨架
4.3 电子离域与共轭体系 4.3.1 π-π共轭
4. 二烯烃 共轭体系
π电子离域所体现的共轭效应称为π-π共轭效应
π-π共轭体系结构特征 单双键交替
d
CH2
+
CH
d
-
CH
d
+
d
CH 2
-
( p-p ¹é ¹)
不限于双键,叁键亦可;不限于碳,氧、氮原子均可
CH2=CH C CH 乙烯基乙炔 CH2=CH CH=O 丙烯醛 CH2=CH C N 丙烯腈
2019/1/30 9/64
4.2 二烯烃的结构
(1)结构特征 1,3-丁二烯中C的轨道结构
4. 二烯烃 共轭体系
4.2.2 1.3-丁二烯(共轭双烯)的结构
1,3-丁二烯中C的轨道特点 1,3-丁二烯分子中的10个原子共平面(优势构象) 1,3-丁二烯分子中存在着明显的键长平均化趋势
2019/1/30
