黄酒生产分析检验
黄酒的质量检测方法

随着黄酒消费市场的迅速增长,黄酒的质量安全问题越来越受到消费者的关注。
GB/T 13662-2018《黄酒》于 2018年9月出台,对黄酒品质分析及质量安全控制起着重要作用。
现行国标中用于黄酒质量检测的方法大多是常规的分析化学方法,存在着操作繁琐、重现性差、效率较低等问题。
1黄酒品质分析研究我国黄酒品质分析的研究主要集中在感官指标、理化指标和酒龄等方面。
感官评定主要通过口、鼻等感觉器官对酒样的外观、香气、口味和风格特征等感官指标进行分析评价,其具有快速、简便的特点,但易受地区、个人爱好和心理等因素的影响,存在一定的模糊性和不确定性。
理化指标检测主要包含总糖、酒精度、非糖固形物、氨基酸态氮、灸苯乙醇和氧化钙等项目,黄酒国标中采用的常规分析化学方法虽较简便、快速,但精密度和准确度较差。
目前更为高效、稳定、精准的改良国标法和电子鼻、电子舌及近红外等技术的研究已取得一系列成果。
1.1电子舌电子舌又称嗅辨仪,是一种模拟人类味觉感受机制,以传感器阵列检测样品信息,结合模式识别对被测样品整体品质进行分析检测的现代化仪器。
研究表明,电子舌对甜度、酸度和醇度的品评结果与人类似。
电子舌PCA和LDA 可以分辨不同区域和同一区域不同品种的黄酒,电子舌在黄酒检测与辨识方面有很大的应用潜力。
与传统检测技术相比,电子舌技术性能稳定、重现性好,无需进行样品前处理,大大提高了检测效率。
1.2电子鼻电子鼻也称人工嗅觉或仿生嗅觉系统,主要根据气味来识别物质的类别和成分,具有检测速度快、范围广、检测数据客观和重复性好等特点。
开展电子鼻技术替代人类嗅觉系统评价黄酒中香气的研究。
结果表明,利用电子鼻建立的醇香、陈香、焦香3个因素的定量模型预测可替代品酒员,有效减少人为误差。
结果表明采用电子鼻建立的定量模型预测的结果重复性好、准确度高,可替代人工品酒员,为黄酒鉴别进一步研究打下基础。
电子舌和电子鼻技术使气味的客观化表达得以实现, 使气味成为可量化的指标,更适用于实际生产中大批量生产的需要。
黄酒检测报告

黄酒检测报告
检测对象:黄酒
检测项目:含酒精度、异味成分、重金属含量、色泽、透明度
检测结果:
1. 含酒精度:本次检测的黄酒样品酒精度为15度。
2. 异味成分:经过气相色谱-质谱联用仪检测,本次黄酒样品中未检出任何致异味成分。
3. 重金属含量:本次黄酒样品的铅含量为0.009mg/kg,远低于国家卫生标准的限量标准,属于安全范围内。
4. 色泽:本次黄酒样品的色泽为琥珀色,呈现清澈透亮状态。
颜色正常,符合黄酒的要求。
5. 透明度:本次黄酒样品的透明度完好,无浑浊、沉淀及杂质存在。
综上所述,本次黄酒样品检测结果全部符合国家卫生标准,合格率100%。
同时,为了保证黄酒的品质和食品安全,建议餐厅管理人员应该定期对进货的黄酒进行检测,确保食品安全和消费者身体健康。
成品黄酒检验作业指导

成品黄酒检验作业指导书1感官指标检验1.1仪器及用具品酒杯、水浴锅1.2操作方法1.2.1酒样的准备将酒样密码编号,置于水浴中,调温至20℃-25℃。
将洁净干燥的品酒杯对应酒样编号,对号注入酒样约25mL。
1.2.2外观评价将注入酒样的品酒杯置于明亮处,举杯齐眉,用眼观察其杯中酒的透明度、清澈度以及有无沉淀和聚集物等,做好详细记录。
1.2.3香气与口味评价手握杯柱,慢慢将酒杯置于鼻孔下方,嗅闻其挥发香气,慢慢摇动酒杯,嗅闻香气。
用手握酒杯腹部摇动后2min,再嗅闻香气。
依据上述程序,判断是原料香或有其他异香,写出评语。
饮入少量酒样(约2mL)于口中,尽量均匀分布于味觉区,仔细品评口感,有了明确感觉后咽下,再回味口感及后味,记录口感特征。
1.2.4风格评价依据外观、香气、口味的特征,综合评价酒样的风格及典型性程度,写出评价结论。
1.2.5结果与判定观察结果与规定相符者,判为符合规定;否则,判为不符合规定。
2理化指标检验2.1非糖固形物2.1.1原理试样经100℃~105℃加热,其中的水分,乙醇等可挥发性物质被蒸发,剩余的残留物即总固形物。
总固形物减去总糖为非糖固形物。
2.1.2.主要仪器及用具分析天平(感量0.0001g)、干燥箱(控温±1)、蒸发皿、移液管、容量瓶、干燥器(内装盛有效干燥剂)。
2.1.3操作方法准确吸取下述量各酒样,注入已知干燥至恒重的蒸发皿中,放入100~105℃电热干燥箱中烘干4h,取出称量。
干、半干黄酒:5ml;半甜黄酒:取25ml定容至50ml,取5ml;甜黄酒、浓甜黄酒:取25ml定容至100ml,取5ml;2.1.4结果与判定试样中总固形物含量按下式计算(m1-m0)nX1 = ×1000V式中:X1—试样中总固形物的含量,单位为克每升(g/L);m1—蒸发皿和试样烘干后至恒重的质量,单位为克(g);m0—蒸发皿烘干后至恒重的质量,单位为克(g);V—试样的体积,单位为毫升(mL);n—试样的稀释倍数。
黄酒发酵过程的质量安全监测分析

黄酒前发酵过程质量控制技术 研究
黄酒发酵过程研究 黄酒生产中的每个流程都可能有
质量安全问题,各流程分工不同,采 取的质控措施不同。黄酒的生产离不 开关键的前发酵程序,发酵中温度等 参数的不确定性因素会影响黄酒成品 的口感等。
黄 酒 的 发 酵 工 艺 有 多 种, 黄 酒 发 酵中温度与酒精度是黄酒发酵成功的 关键因素。开粑基本由经验丰富的师 傅现场操作,前后发酵有 4 个温度阶段, 发酵时间为 96 h,后发酵过程容易控 制,温度变化会使发酵中的酒精度参 数产生变化。黄酒发酵的控制难点是 温度与酒精度的控制。
基于 HACCP 的黄酒质量安全 控制分析
黄酒生产过程中有一定的质量安 全隐患,如操作不当易感染细菌,出 现质量缺陷。HACCP 对生产流程中的 微生物、化学等污染有良好的控制方 法。采用 HACCP 质量控制体系对降低 黄酒的发酵次品率有显著效果。
黄酒酿造对质量安全有特殊要求。 应严格控制每个生产环节,全面考虑 食品安全问题。本文依据黄酒实际生 产发酵特性,对质量安全控制进行分 析,构建控制体系。结合黄酒生产流 程实际情况,将黄酒质量安全作为关 注点,强化企业内部培训学习。构建 黄酒生产安全体系,包括质量安全控 制策略,对黄酒生产流程流程中的安 全隐患进行识别,策划体系文件。
黄酒的酿造分为传统工艺与新工 艺两种生产方式,机械化发酵减少了 人力浪费,随着社会的发展,黄酒发 酵新工艺不断改进。新工艺酿造出的 黄酒的品质基本接近传统工艺,其发 酵工艺包括浸米、蒸饭、前后发酵、 压榨、勾兑、过滤及煎酒。
黄酒质量标准及检验操作规程
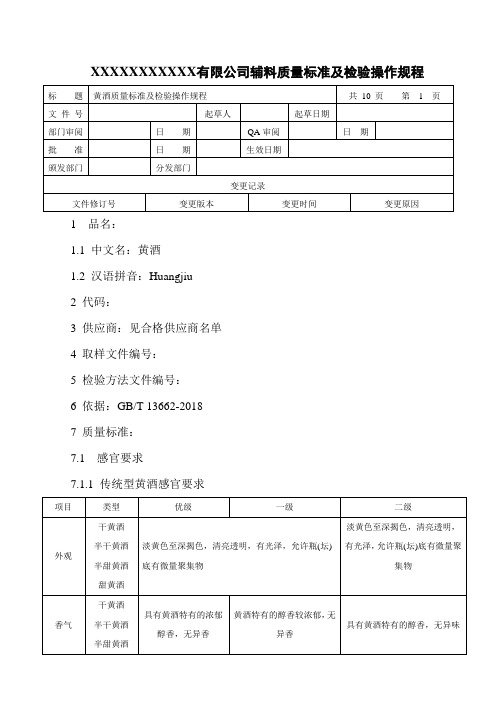
XXXXXXXXXXX有限公司辅料质量标准及检验操作规程1 品名:1.1 中文名:黄酒1.2 汉语拼音:Huangjiu2 代码:3 供应商:见合格供应商名单4 取样文件编号:5 检验方法文件编号:6 依据:GB/T 13662-20187 质量标准:7.1 感官要求7.1.1 传统型黄酒感官要求7.1.2 清爽型黄酒感官要求7.1.3特性黄酒感官的基本要求应符合上述的要求。
7.2 理化指标7.2.1 传统型干黄酒理化要求7.2.2 传统型半干黄酒理化要求7.2.3 传统型半甜黄酒理化要求7.2.4 传统型甜黄酒理化要求7.2.5 清爽型干黄酒理化要求7.2.5 清爽型半干黄酒理化要求7.2.6 清爽型半甜黄酒理化要求8 检验操作规程:8.1 感官检查:8.1.1外观:将酒样置于明亮处,举杯齐眉,用眼观察杯中酒的透明度、澄清度以及有无沉淀和聚集物等。
8.1.2香气:手握杯柱,慢慢将酒杯置于鼻孔下方,嗅闻其挥发香气,慢慢摇动酒杯,嗅闻香气。
用手握酒杯腹部2min,摇动后,再嗅闻香气。
依据上述程序,判断是原料香或有其他异香。
8.1.3口味:饮入少量酒样(约2mL)于口中,尽量均匀分布于味觉区,仔细品评口感,有了明确感觉后咽下,再回味口感及后味,记录口感特征。
8.1.4风格:依据外观、香气、口味的特征,综合评价酒样的风格及典型性程度,写出评价结论。
8.2总糖8.2.1廉爱农法:适用甜酒和半甜酒。
费林溶液与还原糖共沸,生成氧化亚铜沉淀。
以次甲基蓝为指示液,用试样水解液滴定沸腾状态的费林溶液。
达到终点时,稍微过量的还原糖将次甲基蓝还原成无色为终点,依据试样水解液的消耗体积,计算总糖含量。
8.2.1.1试剂准备费林甲液:称取硫酸铜69. 8 g,加水溶解并定容至1000ml。
费林乙液:称取酒石酸钾钠346g及氢氧化钠100g,加水溶解并定容至1000 ml,摇匀,过滤,备用。
葡萄糖标准溶液(2.5 g/L):称取经103℃~105℃烘干至恒重的无水葡萄2.5 g(精确至0. 0001 g),加水溶解,并加浓盐酸5 ml,再用水定容至1000ml。
黄酒检验标准操作规程

*********公司GMP管理文件目的:制定黄酒检验操作规程,规范黄酒的质量检查。
范围:适用于黄酒的质量检测。
责任:QC检验员引用标准:CCGF 103.3-2008,2010年版中国药典;STP-QMP-508。
内容:一、品名:黄酒1、以稻米、黍米、玉米、小米、小麦等为主要原料,经蒸馏、加油、糖化、发酵、压榨、过滤、煎酒、贮存、勾兑而成的酿造酒。
2、本质量标准主要是指干黄酒。
二、质量指标三、操作1、外观:将供试品注入小烧杯置明亮处,观察透明度、澄清度以及有无沉淀和聚集物等应符合规定。
2、PH值2.1仪器:酸度计2.2操作:按PH值测定法标准操作规程(SOP-QMP-214)操作,PH值应为3.5-4.5。
*********GMP管理文件3、总糖-铁氰化钾滴定法3.1试剂3.1.1斐林溶液甲液:称取CuSO4·5H20 15.0g及次甲基蓝0.05g,加水溶解成1000ml,摇匀备用。
3.1.2 斐林溶液乙液:分别称取酒石酸钾钠50g、NaOH 54g、亚铁氰化钾4g,加水溶解使成1000ml,摇匀备用。
3.1.3 1g/L葡萄糖标准溶液:精密称取葡萄糖(AR级)1.0g[葡萄糖经103℃-105℃干燥至恒重,取出置干燥器冷却30分钟至恒重],加适量纯化水溶解后,加入5ml浓HCl,并稀释至1000ml,摇匀备用。
3.1.4(6mol/L)盐酸溶液:取浓盐酸50ml,加水适量使成100ml,摇匀。
3.1.5(200g/L)氢氧化钠溶液:称取氢氧化钠20g,用水溶解成100ml,摇匀。
3.1.6甲基红指示剂:称取甲基红0.10g,加乙醇溶解并稀释至100ml。
3.2操作:3.2.1精密吸取黄酒2.00-10.00ml(控制水解液含糖量在1--2g/L)于100ml容量瓶中,加水30ml和盐酸溶液5ml,在60-70℃水浴中加热水解15分钟。
冷却后,加入甲基红指示剂2滴,用氢氧化钠溶液中和至红色消失,加水稀释至100ml,摇匀,用滤纸过滤后作为供试品溶液备用。
浅析黄酒理化检验效果的优化举措

分析与检测■浅析黄酒理化检验效果的优化举措□陈琳江苏张家港酿酒有限公司摘要:黄酒是我国的传统名酒,和葡萄酒、啤酒合称为世界三大古酒,在酒产品中占据了至关重要的地位。
由于黄 酒的酿造工艺复杂,在生产和销售过程中又会出现“以次充好”的现象,因此对黄酒进行理化检验有着重要的意义,它能 够帮助分析黄酒的内部成分,判断黄酒的品质好坏。
本文分析了黄酒理化检验技术,探讨了应当如何对黄酒进行理化检验 才能达到最佳的检验效果,以期促进黄酒市场朝着更好的方向发展。
关键词:黄酒;理化检验;效果黄酒是我国传统的名酒,它的制 造工艺起源于我国古代,不仅营养丰 富,而且浓度较低,在老百姓中享有 很高声誉。
黄酒是酒类中的奇葩,也 是中华文明数千年来诞生的瑰宝,在 我国占据了重要地位[1]。
现如今黄酒 行业发展迅速,在我国的销量非常高,人们都热衷于喝黄酒,黄酒逐渐挤进 了酒类销售中的前三位。
就是在这种 情况下,黄酒中以次充好的现象大量 出现,生产厂家和销售商家为了牟取 更多的利益,原本销售的应当是陈酒,却用低龄酒替代,给黄酒行业造成了 不可磨灭的负面影响[2]。
为了维护消 费者的权益,有必要对黄酒进行理化 检验,从而保证黄酒高品质_直持续稳定下去,保障黄酒的地位。
1近红外透射光谱分析技术近红外透射光谱分析技术在酒类品质检测中应用非常广泛,黄酒也不 例外,在这项检测技术的运用下取得 了良好的效果,不仅检测过程非常便 捷,检测结果非常精确,对酒类原样 也没有损坏[3]。
近红外透射光谱分析 技术可以用来检测黄酒中的总糖含量, 氨基酸、酒精度、总酸、pH值、非糖 固形物等成分,将每种成分的含量测 定出来,用以判断黄酒的品质优劣,还可以在短时间内有效地将不超过5 年的黄酒的年份辨别出来,帮助辨别 市场上黄酒年份掺假的现象,让低龄 酒在检测的保障下无法再替代陈酒,杜绝以次充好。
近红外透射光谱分析 技术还可以在不同光程的选用下,将 黄酒中的金属元素钾、镁、锌等成分 进行定量测定,判断金属元素在黄酒 中的比重。
黄酒的酿制实验报告

黄酒的酿制实验报告1. 实验目的本实验的主要目的是通过黄酒的酿制过程,了解并掌握黄酒的酿造原理和方法,探究不同参数对黄酒品质的影响,为黄酒的酿造提供科学依据。
2. 实验原理黄酒是一种传统发酵酒,以糯米、麦曲为主要原料,经过蒸煮、糖化、发酵、储存等过程,最终形成具有独特风味和香气的酒品。
其中,糯米为主要碳水化合物来源,通过糖化过程将淀粉转化成糖,再由酵母菌发酵生成酒精和二氧化碳,最后经过陈化存放来进一步提升酒质。
3. 实验步骤3.1 准备工作(1)准备所需原料和器材:糯米、麦曲、水、发酵桶等。
(2)对器材进行消毒处理,以保证实验过程的卫生。
3.2 糯米的处理(1)将糯米浸泡在清水中,提前2-3小时让其吸足水分。
(2)将浸泡好的糯米进行蒸煮,直至煮熟,并保持适当的湿度。
3.3 糖化过程(1)将蒸煮好的糯米放置在容器中,加入适量的温水,与麦曲混合搅拌均匀。
(2)将混合物放置在恒温箱内,保持温度在50-60摄氏度范围内进行静置。
(3)在糖化过程中,定期搅拌混合物,促进淀粉的转化和发酵的进行。
3.4 发酵过程(1)将糖化好的混合物倒入发酵桶中,加入适量的酵母菌。
(2)将发酵桶封闭,保持恒定的温度和适当的通风条件。
(3)发酵过程中,定期观察发酵情况,确保发酵进行顺利。
3.5 陈化和储存(1)发酵完成后,将黄酒放置静置,进行陈化和储存。
(2)选择适当的储存温度和时间,让黄酒进一步陈化,提升口感和香气。
4. 实验结果与讨论通过上述的实验步骤,我们成功酿造出了黄酒。
在糖化和发酵过程中,我们注意到不同的参数会对黄酒的品质产生显著影响。
例如,糯米的煮熟程度、糖化温度的控制、麦曲的使用量等都会直接影响到黄酒的口感、香气和酒精含量。
此外,发酵过程中酵母菌的选择也对黄酒的品质有重要影响。
不同的酵母菌菌种会产生不同的酵母代谢产物,从而影响黄酒的风味。
因此,选择合适的酵母菌进行发酵是酿造优质黄酒的关键。
在陈化和储存过程中,黄酒的品质也会进一步得到提升。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
黄酒总糖的测定
(一)廉—爱农法
适用于甜酒和半甜酒。
1.原理
斐林溶液与还原糖共沸,生成氧化亚铜沉淀。
以亚甲基蓝为指示剂,用试样水解液滴定沸腾状态的斐林溶液。
达到终点时,稍微过量的还原糖将亚甲基蓝还原成无色为终点,依据试样水解液的消耗体积,计算总糖含量。
2试剂
①斐林甲液:称取69.28g 硫酸铜(O H CuSO 245∙),加水溶解并稀释至1000mL 。
②斐林乙液:称取346g 酒石酸钾钠及100g NaOH ,加水溶解并稀释至1000mL 。
③2.5L g /葡萄糖标准溶液:称取2.5000g 经103~105℃烘干至恒重的无水葡萄糖(准确至0.0002g ),加水溶解,并加5mL 浓盐酸,再用水定容至1000mL 。
④10L g /亚甲基蓝指示剂:称取1.0g 亚甲基蓝,加水溶解并稀释至100mL 。
⑤(1+1)HCl 溶液:量取50mL 浓盐酸,加水稀释至100mL 。
⑥1L g /甲基红指示剂:称取0.10g 甲基红,溶于乙醇并稀释至100mL 。
⑦200L g /NaOH 溶液:称取20g NaOH ,溶于水并稀释至 100mL 。
3. 测定步骤
①标定斐林溶液的预滴定:吸取5mL 斐林甲液、5mL 乙液于250mL 三角瓶中,加30mL 水,混合后置于电炉上加热至沸腾。
滴入葡萄糖标准溶液,保持沸腾,待试液蓝色即将消失时,加人2滴亚甲基蓝指示剂,继续用葡萄糖标准溶液滴定至蓝色消失为终点。
记录消耗葡萄糖标准溶液的体积。
②斐林溶液的标定:吸取5mL 斐林甲液、5mL 乙液于250mL 锥形瓶中,加30mL 水。
混匀后,加入比预滴定体积少lmL 的葡萄糖标准溶液,置于电炉上加热至沸,保持沸腾2min ,加入2滴亚甲基蓝指示剂,继续用葡萄糖标准溶液滴定至蓝色刚好消失为终点,井记录消耗葡萄糖标准溶液的总体积。
全部滴定操作需在3min 内完成。
斐林溶液的浓度计算:
11000
V m F ⨯=
式中
F ——斐林甲液、乙液各5mL 相当于葡萄糖的质量,g ; m ——称取葡萄糖的质量,g ;
1V ——正式标定时,消耗葡萄糖标准溶液的总体积,mL 。
③试样的测定:吸取2~10mL 试样(控制水解液总糖量为1~2L g /)于500mL 容量瓶中,加 50mL 水和 5mL (1+1)HCl 溶液,在68~70℃水浴中加热 15min 。
冷却后,加入 2滴甲基红指示剂,用200L g /NaOH 溶液中和至红色消失(近似于中性)。
加水定容至刻度,摇匀,用滤纸过滤后备用。
测定时,以试样水解液代替葡萄糖标准溶液,同上操作。
同一试样的两次滴定结果之差,不得超过0.1mL.
4.计算
100011500/3
2⨯⨯⨯
=V V F L g )总含糖量( 式中
F ——斐林甲液、乙液各5mL 相当于葡萄糖的质量,g ; 2V ——滴定时消耗试样稀释液的体积,mL ;
3V ——吸取试样的体积,mL 。
(二)亚铁氰化钾滴定法
适用于干黄酒和半干黄酒。
1.原理
斐林溶液与还原糖共沸,在碱性溶液中将铜离子还原成亚铜离子,并与溶液中的亚铁氰化钾络合而呈黄色。
以亚甲基蓝为指示剂,达到终点时,稍微过量的还原糖将亚甲基蓝还原成无色为终点。
依据试样水解液的消耗体积,计算总糖含量。
2.试剂
①斐林甲液:称取15.0g 硫酸铜(O H CuSO 245∙)及0.05g 亚甲基蓝,加水溶解并稀释至1000mL 。
②斐林乙液:称取50g 酒石酸钾钠、54g 氢氧化钠、4g 亚铁氰化钾。
加水溶解并稀释至1000mL 。
③1L g /葡萄糖标准溶液:称取1.0000g 经103~ 105℃烘干至恒重的无水葡萄糖加水溶解,并加5mL 浓盐酸,用水定容至1000mL 。
3.测定步骤
①空白试验:吸取5mL 斐林甲液、5mL 斐林乙液溶液于100mL 三角瓶中,加入9mL 葡萄糖标准溶液,混匀后置于电炉上加热,在2min 内沸腾,然后以4~5s l 滴的速度继续滴入
葡萄糖标准溶液,直至蓝色消失立即呈现黄色为终点,记录消耗葡萄糖标准溶液的总量。
②试样的测定
a. 试样水解:吸取2~10mL 试样(控制水解液含糖量在1~2g/L )于100mL 容量瓶中,加30mL 水和5mL (1+1)HCl 溶液,在68~70℃水浴中加热水解15min 。
冷却后,加入2滴1L g /甲基红酒精液,用200L g /NaOH 溶液中和至红色消失(近似于中性),加水定容至100mL ,摇匀,用滤纸过滤后,作为试样水解液备用。
b. 预滴定:吸取5mL 斐林甲液、5mL 斐林乙液及5mL 试样水解液于100mL 三角瓶中,摇匀后置于电炉上加热至沸腾,用葡萄糖标准溶液滴定至终点,记录消耗葡萄糖标准溶液的体积。
c .滴定:准确吸取5mL 斐林甲液、5mL 斐林乙液及5ml 试样水解液于100mL 三角瓶中,加入比预滴定少lmL 的葡萄糖标准溶液,摇匀后置于电炉上加热至沸腾,继续用葡萄糖标准溶液滴定至终点。
记录消耗葡萄糖标准溶液的体积。
同一试样的两次滴定结果之差,不得超过0.1mL 。
4.计算
10005
1/0⨯⨯⨯⨯-=n c V V L g )()总糖含量( 式中
0V ——空白试验时,消耗葡萄糖标准溶液的体积,mL ;
V ——试样侧定时,消耗葡萄糖标准溶液的体积,mL ;
c ——葡萄糖标准溶液的浓度,g /mL ;
5——吸取试样水解液的体积,mL ;
n ——试样的稀释倍数。
