无机化学元素化学部分练习
无机化学练习题(含答案)

1-4周期系中哪一个元素的电负性最大?哪一个元素的电负性最小?周期系从左到右和从上到下元素的电负性变化呈现什么规律?为什么?
1-5 什么叫惰性电子对效应?它对元素的性质有何影响?
1-6当氢原子的一个电子从第二能级层跃迁至第一能级层时发射出光子的波长是121.6nm;当电子从第三能级层跃迁至第二能级层时,发射出光子的波长是656.3nm。问哪一个光子的能量大?
(1)[FeCl2(C2O4)en]-;(2)[Co(C2O4)3]3-;(3)[Co(en)2Cl2]+。
第5章化学热力学基础
5-1在10000C和97kPa下测得硫蒸气的密度为0.5977g/dm3,求硫蒸气的摩尔质量和化学式。
5-2分辨如下概念的物理意义:
(1)封闭系统和孤立系统。
(2)功、热和能。
已知
N2H4(l)N2O4(g)H2O(l)
50.69.16-285.8
第6章化学平衡常数
6-1下列反应的Kp和Kc之间存在什么关系?
(1)4H2(g)+Fe3O4(s)=3Fe(s)+4H2O(g)
(2)N2(g)+3H2(g)=2NH3(g)
(3)N2O4(g)=2NO2(g)
6-2下面的反应在一个1升的容器里,在298K下达成平衡;
CO(g)CO2(g)H2O(g)
-110.5 -393.5 -241.8
5-6.在一密闭的量热计中将2.456 g正癸烷(C10H12,l)完全燃烧,使量热计中的水温由296.32 K升至303.51K。已知量热计的热容为16.24 kJ·K-1,求正癸烷的燃烧热。
无机化学题库15-d区元素.

十五、d 区元素(319题)一、选择题 ( 共69题 )1. 2 分 (1607)将K 2MnO 4溶液调节到酸性时,可以观察到的现象是………………………………( )(A)紫红色褪去 (B)绿色加深(C)有棕色沉淀生成 (D)溶液变成紫红色且有棕色沉淀生成2. 2 分 (1622)用Cr 2O 3为原料制备铬酸盐应选用的试剂是…………………………………………( )(A) 浓硝酸 (B) KOH(s)+KClO 3(s) (C) Cl 2 (D) H 2O 23. 2 分 (1627)用作治疗癌症的含铂药物是……………………………………………………………( )(A) H 3NPt Cl H 3N Cl (B) H 3N Pt ClCl NH 3(橙黄) (鲜黄)(C) H 2PtCl 6 (D) PtCl 44. 1 分 (1637)在Fe 3+溶液中加入NH 3·H 2O 生成的物质是…………………………………………( ) (A) Fe (OH)3 (B) Fe (OH)6]3- (C) [Fe (NH 3)6]3+ (D) [Fe (NH 3)3(H 2O)3]3+5. 2 分 (1638)[Ni(CN)4]2-和[Ni(CO)4]中未成对电子数分别是………………………………………( )(A) 0和2 (B) 2和2 (C) 2和0 (D) 0和06. 1 分 (1644)在Cr 2(SO 4)3溶液中,加入Na 2S 溶液,其主要产物是…………………………………( )(A) Cr + S (B) Cr 2S 3 + Na 2SO 4(C) Cr(OH)3 + H 2S (D)+ S−2CrO 2−7. 1 分 (1654)在下列氢氧化物中,既能溶于过量NaOH ,又能溶于氨水的是………………………( )(A) Ni(OH)2 (B) Zn(OH)2 (C) Fe(OH)3 (D) Al(OH)38. 2 分 (1655)某金属离子在八面体弱场中的磁矩是4.90 B.M.,而在八面体强场中的磁矩为0,该中心金属离子可能是……………………………………………………………………………( )(A) Cr(III) (B) Mn(II) (C) Mn(III) (D) Fe(II)9. 2 分 (1657)含有下列离子的溶液,与Na 2S 溶液反应不生成黑色沉淀的一组是…………………( ) (A) Fe 2+,Bi 3+ (B) Cd 2+,Zn 2+ (C)Fe 3+,Cu 2+ (D) Mn 2+,Pb 2+10. 2 分 (1659)下列各组元素中,性质最相似的两种元素是……………………………………………( )(A) Mg 和Al (B) Zr 和Hf (C) Ag 和Au (D) Fe 和Co11. 2 分 (1660)下列氧化物与浓H 2SO 4共热,没有O 2生成的是………………………………………( )(A) CrO 3(B) MnO 2 (C) PbO 2 (D) V 2O 5 12. 2 分 (1661)下列各组自由离子的顺磁磁矩从小到大变化顺序,正确的是………………………( ) (A) Cu 2+ < Ni 2+ < Co 2+ (B) Cr 2+ < Fe 2+ <Fe 3+ (C) Cr 2+ < Mn 2+ < V 2+ (D) Ti 2+ < V 3+ < Cr 2+13. 2 分 (1664)在酸性介质中加入过氧化氢(H 2O 2)时不生成过氧化物的化合物是…………………( )(A) 钛酸盐 (B) 重铬酸盐 (C) 钒酸盐 (D) 高锰酸盐14. 2 分 (1674)在碱性溶液中氧化能力最强的是………………………………………………………( )(A) (B) NaBiO −4MnO 3 (C) Co 2O 3 (D)-272O Cr 15. 1 分 (1694)下列元素中,可形成多酸的是…………………………………………………………( )(A) Na (B) W (C) Fe (D) Ag16. 2 分 (1695)在强碱性介质中,钒(Ⅴ)存在的形式是……………………………………………… ( )(A) VO 2+(B) VO 3+ (C) V 2O 5·n H 2O (D) -34VO 17. 2 分 (1699)CrO 5中Cr 的氧化数为 ………………………………………………………………( )(A) 4 (B) 6 (C) 8 (D) 1018. 1 分 (4601)在硝酸介质中,欲使 Mn 2+ 氧化为可加的氧化剂是…………………………( ) −4MnO (A) KClO 3 (B) (NH 4)2S 2O 8(Ag +催化) (C) K 2Cr 2O 7 (D) 王水19. 2 分 (4603)下列物质不能大量在溶液中共存的是…………………………………………………( )(A)和OH -36Fe(CN)−(B)和I -36Fe(CN)− (C)和I -46Fe(CN)2 (D) Fe 3+ 和Br −20. 2 分 (4604)根据价层电子的排布,下列化合物中为无色的是……………………………………( )(A) CuCl (B) CuCl 2(C) FeCl 3 (D) FeCl 221. 2 分 (4605)根据价层电子的排布,预料下列化合物中为无色的是………………………………( )(A) TiCl 3(B) ScF 3 (C) MnF 3 (D) CrF 322. 2 分 (4606)下列离子中磁性最大的是………………………………………………………………( ) (A) V 2+ (B) Cr 3+ (C) Mn 2+ (D) Fe2+23. 2 分 (4607)最适于对 Fe(H 2O) 描述的是………………………………………………………( ) (A) sp 3d 2杂化,顺磁性(B) sp 3d 2杂化,反磁性 (C) d 2sp 3杂化,顺磁性 (D) d 2sp 3杂化,反磁性24. 2 分 (4608)过渡金属和许多非金属的共同点是……………………………………………………( )(A) 有高的电负性 (B) 许多化合物有颜色(C) 多种氧化态 (D) 许多顺磁性化合物25. 2 分 (4609)对第四周期的过渡元素,不具备的性质是……………………………………………( )(A) 形成多种氧化态(B) 形成配位化合物(C) 配位数为4或6(D) 形成的离子必具有4s 23d n 的电子排布26. 2 分 (4610)下列化合物中显反磁性的是……………………………………………………………( )(A) NiCl 2 (B) CoSO 4 (C) VOCl 3 (D) TiF 327. 2 分 (4616)在某种酸化的黄色溶液中,加入锌粒,溶液颜色从黄经过蓝、绿直到变为紫色,该溶液中含有…………………………………………………………………………………………( )(A) Fe 3+ (B) (C) (D) Fe (CN) +2VO -24CrO −4628. 2 分 (4617)下列离子中氧化性最强的是……………………………………………………………( )(A) CoF (B) Co(NH −363) (C) Co(CN) (D) Co +33−363+29. 2 分 (4636)根据晶体场理论,FeF 高自旋配合物的理论判据是………………………………( ) −36 (A) 分裂能 > 成对能 (B) 电离能 > 成对能(C) 分裂能 > 成键能 (D) 分裂能 < 成对能30. 2 分 (4643)下列气体中能用氯化钯(PdCl 2)稀溶液检验的是………………………………………() (A) O 3 (B) CO 2 (C) CO (D) Cl 231. 2 分 (4645)下列物质的氧化性与惰性电子对效应无关的是………………………………………() (A) Pb(IV) (B) Bi(V) (C) Cr(VI) (D) Tl(III)32. 2 分 (4646)欲将K 2MnO 4转变为KMnO 4,下列方法中可得到产率高、质量好的是………………() (A) CO 2通入碱性K 2MnO 4溶液 (B) 用Cl 2氧化K 2MnO 4溶液(C) 电解氧化K 2MnO 4溶液 (D) 用HAc 酸化K 2MnO 433. 1 分 (4648)Al(Ⅲ)和Cr(Ⅲ)化学性质的不同点表现在…………………………………………… () (A) 形成配合物的能力 (B) 形成复盐的能力(C) 盐类的水解性 (D) 氢氧化物的两性34. 1 分 (4653)下列四种绿色溶液,加酸后,溶液变为紫红色并有棕色沉淀产生的是( )(A) NiSO 4 (B) CuCl 2(浓) (C) NaCrO 2 (D) K 2MnO 435. 1 分 (4654)在下列化合物中,属杂多酸盐的是……………………………………………………() (A) Na 3[P(W 12O 40)] (B) KCr(SO 4)2·12H 2O(C) Na 4Mo 7O 23 (D) Fe 2(CO)936. 2 分 (4659)下列提炼金属的方法,不可行的是……………………………………………………() (A) Mg 还原TiCl 4制备Ti (B) 热分解Cr 2O 3制备Cr(C) H 2还原WO 3制备W (D) 羰化法提纯Ni37. 1 分 (4663)欲使软锰矿(MnO 2)转变为 MnO 4应选择的试剂是…………………………………() (A) KClO 3(s) + KOH(s) (B) 浓HNO 3(C) Cl 2 (D) O 238. 1 分 (4670)下列新制备出的氢氧化物沉淀在空气中放置,颜色不发生变化的是………………() (A) Fe(OH)2 (B) Mn(OH)2 (C) Co(OH)2 (D) Ni(OH)239. 1 分 (4671)下列锰的氧化物中酸性最强的是………………………………………………………() (A) MnO (B) Mn 2O 3 (C) MnO 2 (D) Mn 20740. 2 分 (4672)在FeCl 3与KSCN 的混合液中加入过量NaF ,其现象是………………………………() (A) 产生沉淀 (B) 变为无色 (C) 颜色加深 (D) 无变化41. 1 分 (4673)同一族过渡元素,从上到下,氧化态的变化是………………………………………() (A) 趋向形成稳定的高氧化态 (B) 先升高后降低(C) 趋向形成稳定的低氧化态 (D) 没有一定规律42. 2 分 (4677)在水溶液中不能存在的离子是………………………………………………………… ( ) (A) [Ti(H 2O)6]3+ (B) [Ti(H 2O)6]4+ (C) [Ti(OH)2(H 2O)4]2+ (D) [Ti(O 2)OH(H 2O)4] 43. 1 分 (4678)当和I −4MnO −在浓强碱性溶液中反应,产物最可能是………………………………( )(A) Mn(s)和I 2 (B)和-24MnO −3IO (C) MnO 2、O 2和IO − (D) Mn 2+ 和I 244. 1 分 (4679)性质最相似的两种元素是………………………………………………………………( )(A) Zr 和Hf (B) Ru 和Rh (C) Mn 和Mg (D) Cu 和Cr45. 1 分 (4680)由于La 系收缩,导致下列元素中性质相似的一组是…………………………………( )(A) Ti 和V (B) Hg 和Pb (C) Nb 和Ta (D) Mn 和Re46. 2 分 (4681)用Cr 2O 3为原料制备铬酸盐应选用的试剂是…………………………………………( )(A) 浓硝酸 (B) KOH(s) + KClO 3(s)(C) KMnO 4 (D) H 2O 247. 2 分 (4682)弱场中,八面体和四面体配合物的 CFSE 相等的是…………………………………( ) (A) Fe 2+(B) Ni 2+ (C) Mn 2+ (D) Cu 2+48. 2 分 (7612)PR 3在配合物M(PR 3)6中可能形成键,这种π 键属于…………………………………( )(A) M(d π ) → L(p π )(B) M(d π ) → L(d π ) (C) L(p π ) → M(d π ) (D) L(p π ) → M(p π )49. 2 分 (7618)在向紫色V 2+ 溶液中滴加KMnO 4溶液时,观察到溶液中钒离子价态和颜色的变化的过程为_________________→_________________→_________________→ ________________。
高中化学竞赛辅导无机元素练习题

(1)确定A的结构简式。写出生成A的化学反应方程式。
(2)在室温或高于室温的条件下,A能定量地分解,产生B和C。已知B的阳离子的价电子总数比C的价电子总数少4。试确定B的结构简式,写出B中阴、阳离子各中心原子的杂化形态。
3为什么NF3常温不水解,而NCl3常温可以水解?写出水解产物。
九、回答下列关于磷的问题:
高中化学竞赛练习(无机化学主族元素)
第一章卤素
一、于酸性溶液中混合等物质的量的KBrO3和KI,生成哪些氧化还原产物,它们的物质量的比是多少?
(2)用漂白粉漂白物料时,常采用以下步骤:将物料浸入漂白粉溶液,然后暴露在空气中;将物料浸在稀盐酸中;将物料浸在大苏打溶液中,最后取出放在空气中干燥;试说明每一步处理的作用,并写出有关的反应方程式。
(2)石硫合剂在空气中与H2O及CO2作用又生成具有杀虫作用的S,写出分步的反应方程式。
四.氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂。
1.氯化亚砜分子的几何构型是;中心原子采取杂方式,
是(等性、不等性)杂化。
2.写出亚硫酸钙和五氯化磷共热,制备氯化亚砜反应的化学方程式
3.氯化亚砜在有机化学中用作氯化剂,写出乙醇和氯化亚砜反应的化学方程式
1.写出N2O4在登月飞船的液体推进系统中所发生主要反应的方程式;
2.说明N2O4分子中N原子的杂化方式和成键情况;
3.画出偏二甲肼的构型。
4.写出我国长征系列火箭二元推进剂反应的化学方程式。
5.偏二甲肼可用二甲胺被亚硝酸氧化、再用锌还原来制备,写出各步反应方程式。
无机化学第五章习题参考答案
第五章原子结构与元素周期律1、下列说法是否正确,为什么?(1)主量子数为1时,有两个方向相反的轨道;(2)主量子数为2时,有2s,2p两个轨道;(3)主量子数为2时,有4个轨道,即2s,2p,2d,2f;(4)因为H原子中只有一个电子,故它只有一个轨道;(5)当主量子数为2时,其角量子数只能取一个数,即l =1;(6)任何原子中,电子的能量只与主量子数有关。
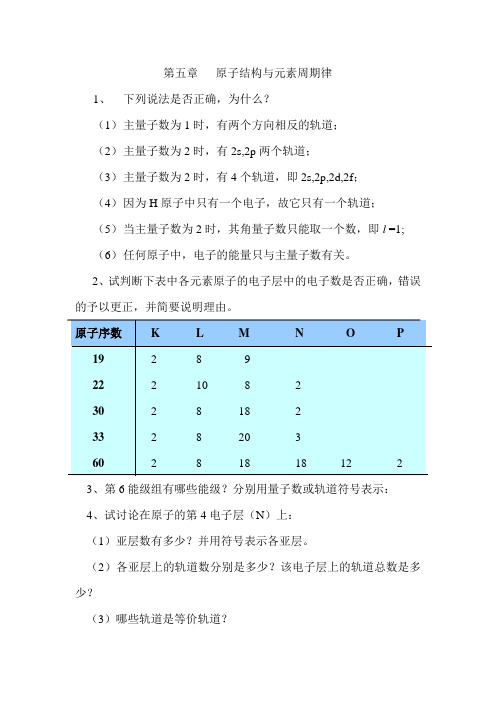
2、试判断下表中各元素原子的电子层中的电子数是否正确,错误的予以更正,并简要说明理由。
3、第6能级组有哪些能级?分别用量子数或轨道符号表示:4、试讨论在原子的第4电子层(N)上:(1)亚层数有多少?并用符号表示各亚层。
(2)各亚层上的轨道数分别是多少?该电子层上的轨道总数是多少?(3)哪些轨道是等价轨道?5、写出与下列量子数相应的各类轨道符号,并写出其在近似能级图中的前后能级所对应的符号:(1)n=2, l=1(2) n=3, l =2(3) n=4, l =0(4) n=4, l =36、在下列各项中,填入合适的量子数:(1)n=?, l=2, m=0, m s=±1/2(2)n=2, l=?, m=-1, m s=±1/2(3)n=4, l=?, m=+2, m s=±1/2(4)n=3, l=0, m=?, m s=±1/27、指出下列假设的电子运动状态(依次为n,l,m, m s),哪几种不可能存在?为什么?(1)3,2,+2,+1/2 (2)2, 2, -2, +1/2(3)2, 0, +1, -1/2 (4) 2, -1, 0, +1/2(5) 4, 3, -1, 18、原子吸收能量由基态变成激发态时,通常是最外层电子向更高的能级跃迁。
试指出下列原子的电子排布中,哪些属于基态或激发态,哪些是错误的。
(1)1s2 2s2 2p1(2)1s2 2s2 2p62d1(3) 1s22s22p43s1(4) 1s2 2s4 2p29、写出原子序数为45,52,79各元素的原子核外电子排布式及其价层电子构型。
无机化学s区元素测试题及答案

无机化学s区元素测试题及答案一、选择题(每题2分,共10分)1. 以下哪种元素属于s区元素?A. 锂(Li)B. 钠(Na)C. 氧(O)D. 氯(Cl)答案:B2. s区元素的价电子排布是什么?A. ns^2B. ns^2np^xC. nd^xns^2D. (n-1)d^xns^2答案:A3. s区元素中,哪个元素的原子半径最大?A. 锂(Li)B. 钠(Na)C. 钾(K)D. 铯(Cs)答案:D4. s区元素中,哪个元素的电负性最高?A. 锂(Li)B. 钠(Na)C. 钾(K)D. 铯(Cs)答案:A5. 下列化合物中,哪一个是s区元素形成的?A. NaClB. MgOC. SO2D. CO2答案:A二、填空题(每题2分,共10分)1. s区元素包括碱金属元素和______元素。
答案:碱土金属2. 碱金属元素的原子序数从______到______。
答案:3 到 113. 碱土金属元素的原子序数从______到______。
答案:12 到 184. s区元素的电子亲和能通常______。
答案:较低5. s区元素的电负性通常______。
答案:较低三、简答题(每题5分,共20分)1. 描述s区元素的一般化学性质。
答案:s区元素通常具有较低的电负性,容易失去最外层的电子形成阳离子,表现出强碱性,与水反应生成氢气和相应的碱。
2. 解释为什么碱金属元素的原子半径随着原子序数的增加而增大。
答案:碱金属元素的原子半径随着原子序数的增加而增大,是因为随着核电荷的增加,电子云的屏蔽效应增强,使得外层电子受到的吸引力减弱,从而导致原子半径增加。
3. 碱土金属元素与碱金属元素相比,其化学性质有何不同?答案:碱土金属元素的电负性比碱金属元素高,因此它们更容易形成化合物,并且它们的金属性比碱金属元素弱。
4. 举例说明s区元素在日常生活和工业中的应用。
答案:s区元素在日常生活和工业中有广泛的应用,例如钠(Na)用于制造食盐,钾(K)用于农业肥料,钙(Ca)用于建筑材料和骨骼强化,铯(Cs)用于原子钟等。
无机化学练习氧族元素的性质与反应

无机化学练习氧族元素的性质与反应氧族元素是周期表中的第16族元素,包括氧、硫、硒、碲和钋。
它们在自然界中广泛存在,具有一系列独特的性质和反应。
本文将重点介绍氧族元素的性质和反应,包括物理性质、化学性质以及常见的反应类型。
一、物理性质1. 氧族元素的原子结构氧族元素的原子结构包括原子核、质子、中子和电子。
它们的原子数分别为8、16、32、34和84。
它们的原子量依次增加,呈现出一定的趋势。
2. 外层电子结构氧族元素拥有6个外层电子,包含了2个s电子和4个p电子。
这使得它们能够参与不同种类的化学反应。
二、化学性质1. 氧族元素的氧化性氧族元素都具有较强的氧化性,能够与其他元素形成化合物。
其中,氧是最常见的元素之一,能够与大多数元素反应,形成氧化物。
2. 氧族元素的还原性虽然氧族元素具有一定的氧化性,但它们在某些条件下也可以发生还原反应。
例如,对于氧化物,可以通过加热或与一些还原剂反应来进行还原。
3. 氧族元素的电负性氧族元素的电负性逐渐减弱,由氧最高,钋最低。
这意味着氧族元素与其他元素形成化合物时,元素间的电子密度存在差异,从而影响了化合物的性质。
三、氧族元素的反应1. 与氢气的反应氧族元素与氢气可以反应,形成相应的氢化物。
其中,氧化氢是最常见的氢化物。
氧化氢在化学和生物体系中起着重要的作用,具有酸性。
2. 与金属的反应氧族元素可以与许多金属发生反应,形成金属氧化物。
这些金属氧化物在日常生活中广泛应用,如氧化铁、氧化铜等。
3. 与非金属的反应氧族元素与非金属元素也可以发生反应,形成相应的化合物。
例如,氧和硫可以反应生成二氧化硫,硒和氧可以反应生成二氧化硒。
4. 与水的反应氧族元素与水可以发生反应。
其中,氧与水反应生成氢氧化物,硫与水反应生成亚硫酸,硒和水反应生成亚硒酸。
5. 其他反应类型氧族元素还可以与氮、碳、氯等元素形成多种化合物。
例如,五氧化二磷、四硫化三碳、四氯化硒等。
结论氧族元素具有独特的物理性质和化学性质,可以通过与其他元素的反应形成各种化合物。
高三化学无机化学练习题及答案

高三化学无机化学练习题及答案1. 题目:元素周期表和原子结构答案:在元素周期表中,元素按照原子序数的大小排列,原子序数表示了一个原子核中的质子数。
原子由质子、中子和电子组成。
原子核中质子和中子质量远大于电子的质量,电子在原子的外层环绕核运动。
2. 题目:元素周期表的分类答案:元素周期表根据元素的性质和化学特性进行了分类。
通常分为金属、非金属和半金属三大类。
金属具有良好的导电性和导热性,大多数元素属于金属。
非金属大多数为气体或者是脆性固体,导热和导电性较差。
半金属则介于金属和非金属之间,具有一部分金属和非金属的性质。
3. 题目:键合与离子半径答案:原子通过化学键进行结合形成分子或晶格。
共价键是由两个非金属原子之间通过电子共享而形成的。
离子键是由一个金属和非金属原子之间通过电子转移而形成的。
键长与原子半径有关,原子半径较小的元素常常形成较短的键。
4. 题目:化合价与元素周期表答案:化合价是一个元素在化合物中与其他元素结合的电荷数目。
化合价与元素在元素周期表中的位置有关。
在周期表中,化合价一般等于主族元素的主量子数。
5. 题目:氧化还原反应答案:氧化还原反应是指元素的氧化态和还原态发生变化的化学反应。
在氧化还原反应中,氧化剂接受电子,还原剂损失电子。
电子的转移导致物质的氧化和还原。
6. 题目:氧化物和酸碱性答案:氧化物是由氧元素和其他元素形成的化合物。
氧化物的碱性和酸性取决于其中金属元素和氧化物之间的化学键。
金属氧化物通常具有碱性性质,而非金属氧化物通常具有酸性性质。
7. 题目:化学计量与物质的组成答案:化学计量是指在化学反应中物质的质量关系。
化学计量可以用化学方程式表示。
化学方程式中的系数表示了物质的摩尔比例关系,从而确定了物质的组成。
8. 题目:尿素的合成和应用答案:尿素是一种有机化合物,通常用于肥料和农业上,也被应用于许多其他领域,如塑料、医药和化妆品工业。
尿素的合成可以通过氨和二氧化碳的反应产生。
无机化学练习题(含答案)第一章 原子结构与元素周期系

第一章原子结构与元素周期系1-1:区分下列概念(1) 质量数和相对原子质量(2) 连续光谱和线状光谱(3) 定态、基态和激发态(4) 顺磁性和逆磁性(5) 波长、波数和频率(6) 经典力学轨道和波动力学轨道(7) 电子的粒性与波性(8) 核电荷和有效核电荷答:(1) 质量数:指同位数原子核中质子数和中子数之和, 是接近同位素量的整数。
相对原子质量:符号为Ar,被定义为元素的平均原子质量与核素12C 原子质量的1/12 之比,代替“原子量”概念(后者已被废弃);量纲为1(注意相对概念)。
(2) 连续光谱: 波长连续分布的光谱。
炽热的固体、液体或高压气体往往发射连续光谱。
电子和离子复合时,以及高速带电离子在加速场中运动时亦能发射这种光谱。
线状光谱:彼此分立、波长恒定的谱线。
原子受激发(高温、电孤等)时,电子由低能级轨道跃迁到高能级轨道,回到低能级时产生发射光谱(不同原子具有各自特征波长的谱线)。
(3) 定态是由固定轨道延伸出来的一个概念。
电子只能沿若干条固定轨道运动,意味着原子只能处于与那些轨道对应的能态,所有这些允许能态统称为定态。
主量子数为1 的定态叫基态,其余的定态都是激发态。
波动力学中也用基态和激发态的概念。
(4) 物质在外磁场中表现出来的性质。
受吸引的性质叫顺磁性,这类物质中含有未成对电子;受排斥的性质叫抗磁性,这类物质中不含未成对电子。
(5) 波长:符号λ,单位m(或m 的倍数单位);波数:符号σ,单位m-1(常用cm-1);频率:符号ν,单位Hz,相互关系:σ=1/λ,ν= c/λ。
(6) 汉语中都叫原子轨道,但英语中的区分却是明确的。
“orbital”是波动力学的原子轨道,是特定能量的某一电子在核外空间出现机会最多的那个区域,亦叫“原子轨函”。
“orbit”是玻尔从旧量子学提出的圆型原子轨道。
(7) 粒性:电子运动具有微粒运动的性质,可用表征微粒运动的物理量(如距离和动量)描述;波性:电子运动也具有波的性质(如衍射),可用表征波的物理量(如波长和频率)描述。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氢、稀有气体1.氙的氟化物是很好的氧化剂,其原因是(D )(A) 氧化性强 (B) 还原到氙 (C) 不污染反应体系 (D) A 、B 、C 都是 2.下列分子或离子中,几何构型不是正四面体的一组是( D )(A) SO 42-,ClO 4-,PO 43- (B) SiCl 4,SnCl 4,CCl 4 (C) BF 4-,B(OH)4-,BH 4-(D) SF 4,XeF 4,SeF 43.用化学方程式表示H 2 的三种主要工业制法和两种较为方便的实验室制法。
工业上高温:CH 4 + H 2O −→−CO + 3H 2 CO + H 2O −→−CO 2 + H 2 C + 2H 2O −→−CO 2 + 2H 2 实验室常温: 2HCl + Zn −→−ZnCl 2 + H 2 NaH + CH 3OH −→−NaOCH 3 +H 2 4.举出第2/IIA 、第11/IB 和第16/VIA 族元素氢化合物的实例并进行归类,他们当中有无能参与形成氢键的物种?第2族:MgH 2,盐型;第11族:CuH ,过渡型;第16族:H 2O ,分子型。
三例当中只有H 2O 形成氢键硼族元素1.铝在空气中燃烧时,生成(D )(A) 单一化合物Al 2O 3 (B) Al 2O 3和Al 2N 3 (C) 单一化合物Al 2N 3 (D) Al 2O 3和AlN 2. BF 3通入过量的Na 2CO 3溶液,得到的产物是( C )(A) HF 和H 3BO 3 (B) HBF 4和B(OH)3 (C) NaBF 4和NaB(OH)4 (D) HF 和B 4O 3 3.从分子轨道理论出发,可以认为在B 2分子中存在的化学键是(C )(A) 三中心二电子键 (B) 一个σ 键 (C) 二个单电子π 键 (D) 一个σ 键和一个π 键 4. BX 3分子若再接受一对电子,分子重排需要能量最大的是( A )(A) BF 3 (B) BCl 3 (C) BBr 3 (D) 不能比较5. H 3BO 3是极弱的一元酸,在定量分析中不能直接用强碱滴定,如果加一定量的甘油或甘露醇(己六醇),生成配合物 HOCHCH 2OCH 2BOCH 2OCH 2CHOHH 后,因酸性大为增强,则就可滴定了。
6. BF 3的几何构型为平面三角形,而BF 4-的几何构型为正四面体。
BF 3中的B —F 键长比BF 4-中的键要短。
7. BF 3与BCl 3的水解方程式分别为 4BF 3 +3H 2O = H 3BO 3 + 3H[BF 4]和BCl 3 + 3H 2O =H 3BO 3 + 3HCl 。
8. 为什么BH 3不存在,而BF 3却能稳定存在,其原因是什么? BH 3系缺电子分子,不稳定,极易形成B 2H 6。
BF 3也属缺电子分子,但BF 3中的F 原子有未成键的p 孤电子对,它可以提供出来,与B 的空轨道形成大π 键,补偿了缺电子的性质,因此BF 3就很稳定,能单独存在。
9. 为什么BCl 3能强烈地水解?写出水解反应式。
因为BCl 3的配位数为3,还有一空轨道可给H 2O 分子的未配电子对进攻:HH +B Cl ClCl=O H HB Cl Cl Cl=HO B Cl+ H + + Cl -第一步的水解产物二氯氢氧化硼继续与水反应,重复配位和取代作用,最后得H 3BO 3和 HCl 。
BCl 3 + 3H 2O =H 3BO 3 + 3HCl10. 苯和无机苯(B 3N 3H 6)为等电子体,都具有环状结构,但无机苯与HCl 能发生加成反应,而苯却不能,试简要说明原因。
苯和无机苯都为共轭体系,但由于B 和N 的电负性差异使得离域π 键的电荷分布不均匀,即电荷分布主要是定域在N 原子,导致离域π 键不稳定,与极性分子易发生加成反应,加成时,N 为Lewis 碱中心,B 为Lewis 酸中心。
11. 写出下列各物种的结构式,并指出中心原子B 的杂化轨道类型:(1) BF3·NH3BFFFN HH,B以sp3杂化(2) (BO)233-BBBO--O O-3-,B以sp2杂化(3) [B4O5(OH)4]]2-OOBB OB OHOOOO B OHHH2-,B有sp2和sp3两种杂化方式碳族元素1. IV A族元素从Ge到Pb;下列性质随原子序数的增大而增加的是(A )(A) +2氧化态的稳定性(B) 二氧化物的酸性(C) 单质的熔点(D) 氢化物的稳定性2. 试判断Ge、Sn、Pb 分别与浓HNO3作用时,正确的说法是(C )(A) 三元素都被氧化成+2价(B) 三元素都被氧化成+4价(C) Ge和Sn被氧化成+4价,但Pb却被氧化成+2价(D) Ge被氧化成+4价,但Sn和Pb只却被氧化成+2价3. 下列硫化物,能溶于Na2S溶液生成硫代酸盐的是(B )(A) SnS (B) SnS2(C) PbS (D) Bi2S34. 下列说法不正确的是(D )(A)HCO3-可通过氢键形成双聚离子(B) NaHCO3的热稳定性不如NaCO3高(C) BeCO3在热水中就可发生分解(D) 所有碱金属碳酸盐都是易溶于水的5. 将过量SiF4通入NaOH溶液中,主要产物是(C )(A) H4SiO4,NaF (B) Na2SiO3,NaF (C) Na2SiO3,Na2SiF6(D) SiO2,HF6. 下列分子中,C与O之间键长最短的是(A)(A) CO (B) Ni(CO)4(C) CO2(D) CH3COOH7. 鉴别Sn4+和Sn2+离子,应加的试剂为(D )(A) 盐酸(B) 硝酸(C) 硫酸钠(D) 硫化钠(过量)8. 分离SnS和PbS,应加的试剂为(D)(A) 氨水(B) 硫化钠(C) 硫酸钠(D) 多硫化铵9 在气态C2中,最高能量的电子所处的分子轨道是(C )(A) σ2p(B) σ *2p(C) π2p(D) π *2p10.由于SnCl2极易__水解__和__被氧化__,所以在配制SnCl2水溶液时,必须先将SnCl2溶于较浓的盐酸溶液中,而后还要加入少量_锡粒。
11.由碳或硅形成的化合物中,碳原子间能以单键、双键、叁键结合,而硅原子间很难以双键结合,其原因是C原子半径较小而电负性较大易形成稳定的σ单键及π键;Si原子半径较大而电负性较小难形成π键进而构成复键。
12.用> 或< 号表示下列各对碳酸盐热稳定性的大小。
(A) Na 2CO 3 > BeCO 3 (B) NaHCO 3 < Na 2CO 3 (C) PbCO 3 < CaCO 313. C 和O 的电负性相差较大,但CO 分子的偶极矩却很小。
其原因是由于CO 的结构可表示为C O 在CO 分子内有一个由O 单方面提供一对电子而形成的配位键。
从而使分子中电子云重心不再明显偏向电负性较大的O的一方,而移向C 的一端,使C 端反而略带负电即配位键的形成削弱了由于C 与O 电负性差别,使偶极矩变小。
14. 两种区别开NaHCO 3和Na 2CO 3的方法是:(1) NaHCO 3固体加热有CO 2气体产生,而Na 2CO 3加热到熔融也不分解; (2) NaHCO 3溶液的pH 值(~8)小于Na 2CO 3液的pH 值(~ 11)。
15.将Cl 2通入Pb(II)的碱性溶液中,这时发生的反应是 Pb(OH)4-+ Cl 2 =PbO 2 + 2Cl - + 2H 2O 。
16. K 2CO 3与HCl(aq),Na 2SiO 3与酸反应的化学方程式分别是K 2CO 3 + 2HCl −→−2KCl + H 2O +CO 2 和Na 2SiO 3 + 2H +−→−2Na + + SiO 2·H 2O(硅胶) 17.在Sn(II)的强碱溶液中加入硝酸铋溶液,发生变化的化学方程式为:3Sn(OH)3-+ 2Bi 3+ + 9OH - =3Sn(OH)62-+ 2Bi ↓(黑)18.HF 腐蚀SiO 2玻璃的反应方程式为SiO 2 + 4HF −→−2H 2O +SiF 4 SiF 4 + 2HF −→−H 2SiF 6 19. 一般教科书中把CO 32-离子的结构写为:C O OO2-(1) 试说明上述结构中的键合情况;(2) 但实验数据表明,其中C —O 键是等价的,而不是上述的非等价形式,仿照苯中的大π键(非定域键)更确切的表示CO 32-的结构。
(1) C 原子通过sp 2杂化,形成三个σ 键,键角120°。
C 的第四个价电子和三个氧原子上的价电子及二个负电荷的电子组成离域π 键∏46键。
(2) COOO2-20. 绘出分离和鉴定Pb 2+、Bi 3+ 和Sn 4+ 三种离子的示意图。
21. 回答关于CO 分子的下列问题:(1) 用分子轨道理论说明CO 分子中的键级;分子轨道表示(σ 1s )2 (σ 1s *)2 (σ 2s )2 (σ 2s *)2 (σ 2px )2 (π 2py )2 (π 2pz )2 键级=(10 - 4) / 2=3 (2) CO 分子为什么能作配合物的配位体?举二例此类配合物;CO 作为配位体是因为它的孤电子对和金属原子的空轨道形成σ 键;此外CO 分子中的反键轨道(π 2p *)和金属原子的d 电子形成反馈键如羰基化合物Fe(CO)5、Ni(CO)4等 (3) 举例说CO 的还原性。
如在反应 CuO + CO== Cu + CO 2 FeO + CO ==Fe + CO 2 中CO 起还原剂作用 22.有一种白色固体,可能是SnCl 2、SnO 2、PbCl 2、PbSO 4中的一种,由下列实验判断,该白色固体是什么化合物?写出有关方程式。
(1) 加水生成悬浊液;(2) 将该白色固体加入盐酸中溶解后,滴加碘淀粉溶液可以褪色;(3) 通H 2S 于白色固体的盐酸溶液中,得到棕色沉淀,沉淀与H 2O 2反应又析出白色沉淀。
根据实验现象可判断此化合物为SnCl 2,发生的各步反应如下:(1) SnCl 2 + H 2O = Sn(OH)Cl ↓ + HCl (2) SnCl 2 + I 2 + 4HCl =H 2SnCl 6 + 2HI(3) SnCl 2 + H 2S =SnS ↓(棕色) + 2HCl (4) SnS + 2H 2O 2 =Sn(OH)4↓(白色) + S ↓23.碳与硅为同族元素,SiCl 4和CCl 4结构相似,且根据:CCl 4(l) + 2H 2O(l) =CO 2(g) + 4HCl(g)m r G ∆= -377 kJ ·mol -1SiCl 4(l) + 2H 2O(l) =SiO 2(s) + 4HCl(g)m r G ∆= -282 kJ ·mol -1CCl 4(l)的水解比SiCl 4(l) 的水解在热力学上趋势更大。
