初中化学计算题汇总
九年级化学化学计算题题20套(带答案)及解析
九年级化学化学计算题题20套(带答案)及解析一、中考化学计算题1.小王同学为了测定某Na2CO3溶液中溶质的质量分数,取10g该溶液于烧杯中,然后将400g澄清石灰水分四次加入,烧杯中沉淀的质量与每次加入澄清石灰水的质量关系如表。
请计算:第一次第二次第三次第四次加入澄清石灰水100100100100的质量/g生成沉淀的质量0.4m 1.0 1.0/g(1)表中m的值为_____。
(2)Na2CO3溶液中溶质的质量分数_____(写出计算过程)。
【答案】0.8 10.6%【解析】【分析】第一次生成沉淀0.4g,而第三次不到0.4g的3倍,则第二次应该为0.4g的二倍,所以m=0.4g×2=0.8g,根据碳酸钙的质量和对应的化学方程式求算碳酸钠溶液中溶质的质量分数。
【详解】由分析可知,m=0.4g×2=0.8g设原Na2CO3溶液中溶质的质量分数为x。
106100=10g?x 1.0gx=10.6%答:(1)表中的m的值为 0.8。
(2)原Na2CO3溶液中溶质的质量分数是10.6%。
2.将含有杂质(不溶于水)的氯化钡样品12.5g放入39.6g水中充分搅拌,完全溶解后过滤。
取20g滤液与足量的稀硫酸完全反应,得到4.66g沉淀。
请计算:①配制的氯化钡溶液中溶质的质量分数。
②样品中氯化钡的质量分数。
【答案】20.8%;83.2%【解析】【详解】①设参加反应的氯化钡的质量为x 。
2244BaCl +H SO =BaSO +2H 208233x4Cl.66g208233=x 4.66gx= 4.16g则配制的氯化钡溶液中溶质的质量分数为 :4.16g20g×100%=20.8% ②由于20g 溶液中含有4.16g 氯化钡,则可设样品中氯化钡的质量为y 。
则4.16g y=20g-4.16g 39.6gy=10.4g样品中氯化钡的质量分数为:10.4g12.5g×100%=83.2%答:①氯化钡溶液中溶质的质量分数为20.8% ②样品中氯化钡的质量分数为83.2%。
化学计算题试题含答案
化学计算题试题含答案一、初中化学计算题1.把250g稀盐酸加入盛有60g石灰石的烧杯中,恰好完全反应,反应后称量,烧杯中剩余物质的质量为288g。
试计算:(1)生成二氧化碳的质量;(2)60g石灰石中碳酸钙的质量。
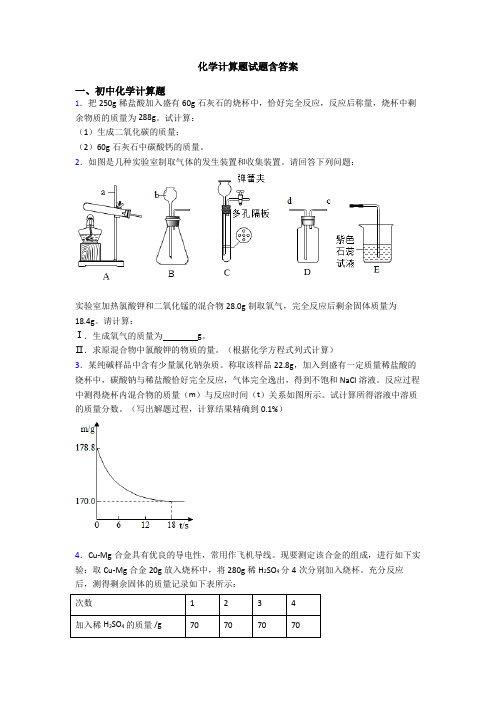
2.如图是几种实验室制取气体的发生装置和收集装置。
请回答下列问题:实验室加热氯酸钾和二氧化锰的混合物28.0g制取氧气,完全反应后剩余固体质量为18.4g。
请计算:Ⅰ.生成氧气的质量为g。
Ⅱ.求原混合物中氯酸钾的物质的量。
(根据化学方程式列式计算)3.某纯碱样品中含有少量氯化钠杂质。
称取该样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。
反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。
试计算所得溶液中溶质的质量分数。
(写出解题过程,计算结果精确到0.1%)4.Cu-Mg合金具有优良的导电性,常用作飞机导线。
现要测定该合金的组成,进行如下实验:取Cu-Mg合金20g放入烧杯中,将280g稀H2SO4分4次分别加入烧杯。
充分反应后,测得剩余固体的质量记录如下表所示:次数1234加入稀H2SO4的质量 /g7*******(2)所用稀H2SO4 中溶质的质量分数。
(3)第1次反应后所得溶液中溶质的质量分数。
(计算结果精确到0.1%)5.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10g样品放入烧杯中,再取60g稀硫酸分六次加入烧杯中,充分反应,实验数据如下:的值为.(2)黄铜样品中锌的质量分数为.(写出计算步骤,下同)(3)所用稀硫酸的溶质质量分数为多少?6.某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品10.0g于烧杯中,将50.0g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量记录如下:(1)X的值为_____。
(2)计算该实验中产生二氧化碳的质量。
50套初中化学化学计算题含解析

(2)废液中含有的溶质是___(写化学式)
(3)通过计算说明,图象横坐标中b点表示的溶液的质量是____?
【答案】(1)1.1;(2)HCl、CaCl2;
(3)图象横坐标中b点表示的溶液的质量是30g.
【解析】
试题分析:石灰石和稀盐酸制取二氧化碳产生的废液中一定含有生成的氯化钙,可能含有盐酸;取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,说明废液中含有盐酸;滴加至10克开始出现白色沉淀,说明废液中含有氯化钙;故废液是盐酸和氯化钙溶液的混合物.
原样品中碳酸钠的质量分数为:10.6克/12克×100%=88.3%
考点:质量守恒定律根据化学方程式的计算溶质的质量分数
10.纸包皮蛋是一项新技术,制作过程中需要配制料液。某配方料液中含NaOH、
NaCl、红茶末、五香粉等,技术员先配得NaOH、NaCl的昆合液2400g,其中含80gNaOH,81gNaCl。计算:
(1)混合液中NaOH的质量分数。
(2)如果取24g混合液,加入一定质量3.65%的稀盐酸恰好完全反应,计算所加稀盐酸的质量。
106 44
10g×26.5% x
x=1.1g.
(2)取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,说明废液中含有盐酸;滴加至10克开始出现白色沉淀,说明废液中含有氯化钙;故废液是盐酸和氯化钙溶液的混合物,废液中含有的溶质是HCl、CaCl2.
(3)设与氯化钙反应的碳酸钠溶液中溶质质量为y,
200
200
200
200
剩余固体质量(g)
37.6
15.2
4
4
(说明:生铁中杂质不溶于水,也不与硫酸反应.)
初中化学元素计算题专题训练含答案

初中化学元素计算题专题训练含答案姓名:__________ 班级:__________考号:__________一、计算题(共19题)1、 目前,我国绝大多数干洗店都是使用四氯乙烯(C 2Cl 4)作干洗剂.四氯乙烯干洗剂并不是理想的干洗剂,它已经被国际研究机构列为2A 致癌物.残留在衣服上的四氯乙烯可以部分进入人体,对人造成伤害.请根据四氯乙烯化学式计算: (1)四氯乙烯的相对分子质量为多少?(2)四氯乙烯中碳元素与氯元素的质量比为多少?(3)多少质量的四氯乙烯与96克甲烷(CH 4)所含的碳元素质量相等?2、 据报道,常州、广州等地一些液化气充气站在液化气中填充二甲醚(化学式C 2H 6O ),有的含量竟高达61.3%.二甲醚是一种化工原料,对液化气罐的配件有较强腐蚀作用,易造成气罐泄气,严重会引起爆炸.请阅读信息后回答(1)二甲醚能腐蚀液化气罐的配件,此性质属于二甲醚的 (填“物理”或“化学”)性质.(2)二甲醚中碳、氢、氧三种元素的质量比为 (3)计算二甲醚中碳元素的质量分数.(4)常温常压下,10L 二甲醚(密度为2.05g/L )中含碳元素多少克. 3、 计算下列各题:(1)计算Cu (OH )2的相对分子质量;(2)8千克硝酸铵(NH 4NO 3)中含有多少千克氮元素?4、 当氯化铵(NH 4Cl )的质量是硝酸铵(NH 4NO 3)的多少倍时,前者的含氮量是后者的两倍?5、 某化肥产品的广告如右图:请通过计算判断此广告是真实广告,还是虚假广告.(提示:先算出纯硝酸铵中氮元素的质量分数,再进行比较后得出结论,必须写出详细的计算过程,结果精确到0.1%.)6、缺钙能导致儿童发育不良或佝偻病.小明同学从食物中摄入钙元素的量不足,每天需要服用2片某种钙片.该钙片标签的部分内容如图所示(假设钙片中只有碳酸钙含有钙元素),请计算:(1)碳酸钙中钙元素的质量分数;(2)小明同学每天从钙片中摄入钙元素的质量.7、世界卫生组织早已把铝列为食品污染源之一,成人每日铝的摄入量应控制在0.004g以下.炸油条时需在面粉中加水、明矾[KAl(SO4)312H2O]及辅料(纯碱和盐等).炸熟的1000g油条中含面粉660克、水330克、明矾2.65克,其余是辅料.若某成人每天早餐食用油条100g,请通过计算回答该人每天摄入的铝元素的质量是否已超过安全摄入量(精确到0.0001g).8、已知某铁的氧化物相对分子质量为160,化学式为Fe2O3,求此氧化物中铁元素和氧元素的质量比.9、在160g SO2和O2的混合物中,其中硫元素的质量分数为40%,求混合物中O2的质量分数?10、合格奶粉每100 g中含蛋白质约18g,蛋白质中氮元素的平均质量分数为16%。
(完整版)初中化学计算题大全

初中化学计算专题(一)有关化学式计算题类型: 第一种类型:标签型化学式计算题:1、在现代生活中,人们越来越注重微量元素的摄取。
碘元素对人体健康有至关重要的作用。
下表是某地市场销售的一种“加碘食盐”包装袋上的部分说明。
请回答下列问题:(1)由食用方法和贮藏指南可推测碘酸钾(KIO 3)的化学性质之一是 ; (2)计算碘酸钾(KIO 3)中,钾元素、碘元素、氧元素的质量比 ; (3)计算碘酸钾(KIO 3)中,碘元素的质量分数是多少? ;(计算结果精确到0.01,下同)(4)计算1kg 这样的食盐中,应加入 g 碘酸钾(用最高含碘量计算) 第二种类型:叙述型化学式计算题:1、蛋白质是由多种氨基酸[丙氨酸:CH 3CH(NH 2)COOH 等]构成的极为复杂的化合物,人体通过食物获得蛋白质,在胃肠道里与水发生反应,生成氨基酸,试计算:(1)丙氨酸分子中氮原子与氧原子的个数比 。
(2)丙氨酸的相对分子质量 。
(3)丙氨酸中碳、氢、氧、氮元素的质量比 。
2、抗震救灾,众志成城。
用于汶川震后防疫的众多消毒剂中,有一种高效消毒剂的主要成分为三氯异氰尿酸(C 3O 3N 3Cl 3),又称高氯精。
下列有关高氯精的说法不正确的是( ) A .高氯精由4种元素组成 B .高氰精中C 、O 、N 、Cl 的原子个数比为1∶1∶1∶1 C .高氯精中C 、N 两种元索的质量比为12∶14 D .高氯精中氯元素的质量分数为25% 第三种类型:综合型化学式计算题:1、青少年正处于生长发育时期,每天需要摄取足量的蛋白质,蛋白质的代谢产物主要是尿素[CO(NH 2)2]。
若从食物中摄取的蛋白质经体内新陈代谢后完全转化为尿素排出体外,每人每天相当于排出尿素30g 。
(1)30g 尿素中含氮元素多少克?(2)已知蛋白质中氮元素的平均质量分数为16%,则每人每天至少应从食物里摄取的蛋白质为多少克?(3)请你根据下表中几种常见食物的蛋白质含量,计算出每天至少应摄人多少克下列食物才能满足你对蛋白质的需求(可以只摄取一种食物,也可同时摄取几种食物)。
初中化学计算题大全(含答案及解析)

2024年中考化学《必考经典》计算题大全(含答案及解析)1.实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。
分析并计算:(1)a点溶液中含有的离子是_____。
(2)当pH=7时,消耗氢氧化钠溶液中NaOH质量为_____g。
(3)计算稀H2SO4中溶质的质量分数。
_____(4)计算恰好完全反应时所得溶液的溶质质量分数。
_____【答案】Na+、H+、SO42- 0.8 稀H2SO4的溶质质量分数是9.8%;恰好完全反应时所得溶液的溶质质量分数是5.5%。
【解析】【详解】(1)由图示可知,在a点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以,溶液中含有的离子为:Na+、H+、SO42-;(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;(3)10g稀硫酸样品含有H2SO4的质量为x,生成的硫酸钠的质量为y2NaOH+H SO=Na SO+2H O2424280981420.8g x y解得:x=0.98g y=1.42g稀H2SO4的溶质质量分数为:×100%=9.8%;(4)恰好完全反应时所得溶液的溶质质量分数:×100%≈5.5%。
2.某小组同学将530 g碳酸钠溶液加入到280 g石灰乳(水和氢氧化钙的混合物)中,使之恰好完全反应,所得溶液中溶质的质量分数为1%,计算加入的碳酸钠溶液中溶质的质量分数。
【答案】2%【解析】【详解】设原碳酸钠溶液中溶质的质量为xNa2CO3+ Ca(OH)2=CaCO3↓+ 2NaOH106 100 80X则解得x =10.6g所以加入的碳酸钠溶液中溶质的质量分数为答:加入的碳酸钠溶液中溶质的质量分数为2%。
3.取一定量的氯化钠与氢氧化钠的混合物,加一定量的水配成溶液,然后向其中滴加溶质质量分数为7.3%稀盐酸,直至恰好反应,共消耗稀盐酸50g。
初中化学计算题100题含答案

初中化学计算题100题含答案
1、一块铝热量发生变化时所放出的热量为?
答案:Q=m·C·ΔT
2、一次反应所需的能量是多少?
答案:ΔH=Hf-Hi
3、一克硝酸钠可与多少毫升水反应?
答案:1克硝酸钠可与25毫升水反应。
4、一克重氢氧化钠在室温时最多可溶解多少克水?
答案:一克重氢氧化钠在室温时最多可溶解5.6克水。
5、1 mol酸能把多少ml水搞碱?
答案:1 mol酸能把1000ml水搞碱。
6、醋酸的PH值是多少?
答案:醋酸的PH值为2.4
7、H2SO4形成的水溶液中,氢离子的浓度是多少?
答案:H2SO4形成的水溶液中,氢离子的浓度为1 mol/L。
8、浓硫酸中含有多少原子硫?
答案:浓硫酸中含有2个原子硫。
9、一克CuSO4能溶解多少克水?
答案:一克CuSO4能溶解37.2克水。
10、氢化钠可与100g水反应吗?
答案:可以,氢化钠可与100g水反应。
化学计算题试题含答案
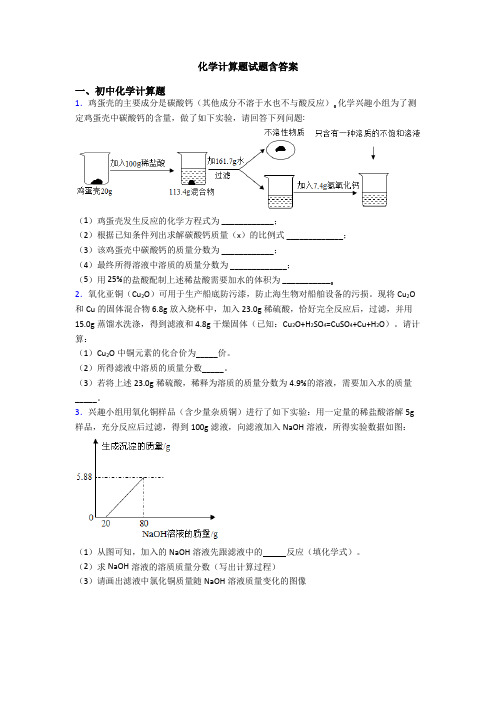
化学计算题试题含答案一、初中化学计算题1.鸡蛋壳的主要成分是碳酸钙(其他成分不溶于水也不与酸反应)。化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做了如下实验,请回答下列问题:(1)鸡蛋壳发生反应的化学方程式为 ____________;(2)根据已知条件列出求解碳酸钙质量(x)的比例式 _____________;(3)该鸡蛋壳中碳酸钙的质量分数为 ____________;(4)最终所得溶液中溶质的质量分数为 _____________;(5)用 25%的盐酸配制上述稀盐酸需要加水的体积为 ___________。2.氧化亚铜(Cu2O)可用于生产船底防污漆,防止海生物对船舶设备的污损。
现将Cu2O 和Cu的固体混合物6.8g放入烧杯中,加入23.0g稀硫酸,恰好完全反应后,过滤,并用15.0g蒸馏水洗涤,得到滤液和4.8g干燥固体(已知:Cu2O+H2SO4=CuSO4+Cu+H2O)。
请计算:(1)Cu2O中铜元素的化合价为_____价。
(2)所得滤液中溶质的质量分数_____。
(3)若将上述23.0g稀硫酸,稀释为溶质的质量分数为4.9%的溶液,需要加入水的质量_____。
3.兴趣小组用氧化铜样品(含少量杂质铜)进行了如下实验:用一定量的稀盐酸溶解5g 样品,充分反应后过滤,得到100g滤液,向滤液加入NaOH溶液,所得实验数据如图:(1)从图可知,加入的NaOH溶液先跟滤液中的反应(填化学式)。
(2)求NaOH溶液的溶质质量分数(写出计算过程)(3)请画出滤液中氯化铜质量随NaOH溶液质量变化的图像(4)另取5g该样品,用足量的CO还原成纯铜,理论上可得到纯铜 g。
4.某课外活动小组为测定一包碳酸钠样品的质量分数,取来了一些样品,准确称取样品10g放于烧杯中(杂质既不溶于水,也不与稀盐酸反应),向其中加入足量的稀盐酸,根据实验测得的数据绘制出所加稀盐酸的质量和放出的CO2的质量关系图。
(1)10g样品可以产生多少克二氧化碳?(2)该样品中碳酸钠的质量分数是多少?(3)加入稀盐酸到恰好完全反应时,所得的溶液中溶质的质量分数是多少?(写出计算过程)5.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10g样品放入烧杯中,再取60g稀硫酸分六次加入烧杯中,充分反应,实验数据如下:第1次第2次第3次第4次第5次第6次加入稀硫酸的质量(g)101010101010剩余固体的质量(g)9.35m8.057.4 6.75 6.75的值为.(2)黄铜样品中锌的质量分数为.(写出计算步骤,下同)(3)所用稀硫酸的溶质质量分数为多少?6.“学化学,爱化学,用好化学”学习小组为测出鸡蛋壳(主要成分是碳酸钙)中碳酸钙的质量分数,某同学称取已洗净、晾干、研成粉末的鸡蛋壳10g置于烧杯中,将烧杯放在电子天平上,往烧杯中平均分5次加入50g的稀盐酸,测得实验数据如表:实验次数12345加入稀盐酸质量/g10.020.030.040.050.0剩余物质质量/g19.028.037.046.756.7(1)第_____ 次实验时鸡蛋壳已经完全反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学计算题分类初中化学计算题的类型有多种,其中包括化学式计算、化合价计算、化学方程式计算、溶液计算、化学方程式和溶液简单综合计算、应用质量守恒定律计算等,下面针对2007、2008两年各地中考试题中的计算题进行一下归类:(一)有关化学式计算题类型:第一种类型:标签型化学式计算题:1、(2008 甘肃兰州)锌是人体健康必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫功能低下。
市售的葡萄糖酸锌口服液对治疗锌缺乏病具有较好的疗效。
下图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答:1文档来源为:从网络收集整理.word版本可编辑.1文档来源为:从网络收集整理.word版本可编辑.1、(2007徐州市)青少年正处于生长发育时期,每天需要摄取足量的蛋白质,蛋白质的代谢产物主要是尿素[CO(NH2)2]。
若从食物中摄取的蛋白质经体内新陈代谢后完全转化为尿素排出体外,每人每天相当于排出尿素30g。
(1)30g尿素中含氮元素多少克?(2)已知蛋白质中氮元素的平均质量分数为16%,则每人每天至少应从食物里摄取的蛋白质为多少克?(3)请你根据下表中几种常见食物的蛋白质含量,计算出每天至少应摄人多少克下列食物才能满足你对蛋白质的需求(可以只摄取一种食物,也可同时摄取几种食物)。
1文档来源为:从网络收集整理.word版本可编辑.1、(2007北京市)工业上使用一种“渗铬(Cr)技术”可以大大提高钢铁制品的抗腐蚀能力。
其中一个主要反应的化学方程式为。
已知参加反应铁的质量为28g,则生成铬的质量为多少克?2、(2007泉州市)发射通讯卫星的火箭用联氨(N2H4)做燃料,用四氧化二氮(N2O4)助燃,反应的化学方程式如下:2N2H4+ N2O4=== 3N2+4H2O,生成物不会对大气造成污染。
请计算:3.2Kg N2H4发生燃烧,需要助燃物N2O4的质量。
(2)含有杂质的反应物和生成物的计算1、某炼铁厂用含氧化铁80%的赤铁矿冶炼生铁。
若要炼出1120t含铁95%的生铁,需要含氧化铁80%的赤铁矿多少吨?2、(2008太原市)将100g含CaCO3质量分数为80%的石灰石样品(杂质不发生化学反应也不含钙),高温灼烧一段时间后,冷却,测得剩余固体中含钙元素的质量分数为41%,则生成CaO的质量约为(3)和实验相结合的计算题(2007永州市)石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验。
实验步骤①称取烧杯的质量②将适量盐酸加入烧杯中并称重③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应④待反应完全后,称重实验图示实验数据烧杯的质量为50.0g烧杯和盐酸的质量为100.0g石灰石样品样品的质量为12.0g烧杯和其中混合物的质量为107.6g试通过分析计算:该实验中生成的二氧化碳的质量是多少克?1文档来源为:从网络收集整理.word版本可编辑.该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水)(4)标签型化学方程式的计算1、(2007鄂州市)消化药片所含的物质能中和胃里过多的胃酸。
某种消化药品的标签如图4所示。
医生给某胃酸过多的患者开出服用此药的处方为:每日3次,每次2片。
试计算,患者按此处方服用该药一天,理论上可中和HCl多少毫克?(计算结果取整数)2、(2007太原市)过氧化氢溶液在存放过程中会缓慢分解。
右图为实验室保存的一瓶过氧化氢溶液的标签。
某小组同学为了解过氧化氢的分解情况,取5g该溶液共制得0.64g氧气。
试分析计算这瓶过氧化氢溶液在保存过程中已经分解的过氧化氢的质量。
(5)有关混合原料参加反应的化学方程式的计算1、不纯的铁片5.6g与足量的HCl反应,放出0.21g氢气,则铁片中可能含有的一种金属杂质为[]A.Zn B.Pb C.Cu D.Mg2、(2007德阳市)将26g某金属混合物投入到足量的稀硫酸中,共收集到2g氢气,该金属混合物的组成可能是()A、Mg和ZnB、Fe和ZnC、Zn和CuD、Cu和Fe(6)有关字母型化学反应方程式计算题1、(2008南通市)A、B、C三种物质各15 g,它们化合时只能生成30 g新物质D。
若增加10 g A,则反应停止后,原反应物中只余C。
根据上述条件推断下列说法中正确的是A.第一次反应停止后,B剩余9 g B.第二次反应后,D的质量为50 gC.反应中A和B的质量比是3∶2 D.反应中A和C的质量比是5∶22、(2008南京市)在反应2A+5B=2C+4D中,C、D的相对分子质量之比为9∶22.若2.6 gA与B完全反应后.生成8.8gD。
则在此反应中B与D的质量比为( )A.4∶9 B.8∶1 C.10 ∶11 D.31∶44(7)有关表格型化学方程式计算题1文档来源为:从网络收集整理.word版本可编辑.(2008青岛市)在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下表:1文档来源为:从网络收集整理.word版本可编辑.(1)稀释后硫酸溶液溶质的质量为 _____ g,(2)稀释时所需水的质量为 _________ g。
②溶液增浓问题:(蒸发溶剂法增加溶质法增加浓溶液法)1、(总复习)现有8%的铝化钠溶液50g,若是其溶质质量分数增达到16%,可采用的方法是:①需要蒸发多少克水?②需要加入多少g 氯化钠?③需要加入多少克40%的铝化钠溶液?2、(2007重庆市)电解水时,常常要加入少量氢氧化钠使反应容易进行。
现将加有氢氧化钠的水通电一段时间后,产生lg氢气,其中氢氧化钠的质量分数也由4.8%变为5%。
计算:(1)生成氧气的质量。
(2)电解后剩余水的质量。
(3)配制溶液问题:①计算类:1、( 2007柳州市)欲配制溶质质量分数为5%的葡萄糖溶液100g。
下列说法正确的是()A、只需要托盘天平和量筒两种仪器B、配制时要用葡萄糖作溶质C、用托盘天平称取5g葡萄糖D、用量筒量取100ml水2、(2007威海市)实验室要配制50 g溶质质量分数为20%的硝酸钾溶液,现有25 g溶质质量分数为40%的硝酸钾溶液、20 g溶质质量分数为15%的硝酸钾溶液及足够多的硝酸钾晶体和蒸馏水,请选用上述的药品,设计三种配制方案填入下表1文档来源为:从网络收集整理.word版本可编辑.②实验类:1、(2007太原市)下图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图。
配制过程中使用的四种玻璃仪器,分别是广口瓶、________、_________、量筒。
请你指出图中一处错误操作,并分析该操作可能造成的后果。
____________________________________________________。
图②、图③表示的操作步骤分别是________________。
配制时需称量氯化钠_______g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会__________(填“偏大”或“偏小”);量取水最好选择____________的量筒(填序号①10mL②50mL③100mL)。
(水的密度为1g/cm3)2、(2007宿迁市)在实验室配制溶液时,常涉及以下过程:①溶解②称量③计算④装瓶存放。
请按要求回答问题:⑴现欲配制50g 5%氯化钠溶液,配制过程的先后顺序是________(填序号)。
⑵用已调节平衡的天平称取氯化钠固体时,发现指针偏右,接下来的操作是。
⑶在量取蒸馏水体积时,若仰视读数,则会导致氯化钠溶液的溶质质量分数______(填“<”或“>”)5%。
⑷在溶解步骤中需要的仪器有 _____、________ 。
(四)有关溶液和化学方程式的简单综合计算:(1)叙述型计算题:①涉及沉淀的叙述型计算题:1、(2007重庆市)家里蒸馒头用的纯碱中含有少量的氯化钠,课外探究小组的同学欲测定纯碱中碳酸钠的含量。
他们取该纯碱样品11.0g,全部溶解在100.0g水中,再加入氯化钙溶液141.0g,恰好完全反应。
过滤干燥后,称得沉淀质量为10.0g。
请计算:(1)纯碱样品中碳酸钠的质量;(2)反应后所得滤液中溶质的质量分数。
1文档来源为:从网络收集整理.word版本可编辑.2、(2008宜昌市)50g Ca(NO3)2溶液与50g K2CO3溶液混合后,恰好完全反应。
经过滤、干燥、称量,得到5g沉淀。
反应的化学方程式是:K2CO3+Ca(NO3)2==CaCO3↓+2KNO3。
请计算:(1) 参加反应的K2CO3的质量。
(2) 过滤后所得溶液的溶质质量分数。
②涉及气体的叙述型计算题:1、(2006天津市)将10g不纯的锌粒(杂质不容与水也不与酸反应)投入到100g稀硫酸中,恰好完全反应,得到0.2气体,试计算:(1)锌粒中纯锌的质量;(2)稀硫酸中溶质的质量分数。
2、(2006 天津市)我国化工专家侯得榜的“侯是制碱法”为世界制碱工业做出了杰出贡献。
工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。
现称取只含氯化钠的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液质量为121g,试求:该纯碱样品的纯度(计算结果精确到0.1%)所的溶液中溶质的质量分数。
③由溶液质量和质量分数进行计算:1、(2007天津市)现有Na2CO3和Na2SO4的固体混合物共12g,将它放入98g20%的H2SO4溶液中,充分反应后溶液呈酸性;在此酸性溶液中再加入80g10%的NaOH溶液,恰好完全中和。
计算:(1)恰好完全中和后,所得溶液中溶质的质量分数。
(计算结果精确到0.1%)(2)样品中碳酸钙的质量分数是 _____ 。
(3)求盐酸中溶质的质量分数。
2、(2007南充市)南充市名优特产阆中保宁醋,是中国四大名醋之一,其主要成分是醋酸,化学式为:CH3COOH。
测定保宁醋醋酸含量的原理是:CH3COOH + NaOH = CH3COONa + H2O。
化学课外活动小组中和30g保宁醋,用去质1文档来源为:从网络收集整理.word版本可编辑.量分数为5%的NaOH溶液20g。
请你计算:(1)30g保宁醋中含醋酸的质量;(2)该保宁醋中醋酸的质量分数。
(2)标签型计算题:(2007德阳市)某校化学实验室有一瓶标签残缺的过氧化氢溶液(如图所示)。
该校化学课外兴趣小组的同学为了测定其中溶质的质量分数,他们取出该溶液34g,加入适量催化剂,待完全反应后,共收集到0.32g氧气。
试计算该溶液中溶质的质量分数。
(3)图像型计算题:1、(2007无锡市)小红同学在某化工厂进行社会实践,技术员与小红一起分析由氯化钡和氯化钠组成的产品中氯化钠的质量分数。
取16.25g 固体样品,全部溶于143.6mL水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系。
