实验一 硫酸苯酚法测多糖含量
实验一、硫酸苯酚法测多糖含量

实验一硫酸-苯酚法测多糖含量1.目的要求测量蒽酮硫酸法不能测量的血清型的过程样品中的多糖含量2.方法原理糖在浓硫酸作用下,水解生成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚缩合成橙黄色化合物,且颜色稳定,在波长490 nm处和一定的浓度范围内,其吸光度与多糖含量呈线性关系正比,从而可以利用分光度计测定其吸光度,并利用标准曲线定量测定样品的多糖含量,本方法可用于多糖、单糖含量的测定。
3.主要实验仪器及材料浓硫酸,苯酚,蒸馏装置,分光光度计,电子天平,坐标纸或电脑等。
4.掌握要点硫酸显色的安全、准确操作,单糖到多糖的转换系数。
5.试剂配制1)葡萄糖标准液的配制准确称取干燥恒重的葡萄糖100 mg,蒸馏水准确定容至100 mL的1 mg/L的葡萄糖液,摇匀后准确吸取10 mL该溶液,蒸馏水稀释定容至100 mL,即得100 ug/mL的葡萄糖标准液。
2)90%苯酚液的配制准确移取苯酚90mL,蒸馏水定容至100 mL,即得90%苯酚液,棕色瓶中避光保存3)6%苯酚液的配制将90%苯酚液稀释至6%,即一体积储存液对应十四体积纯水,临用现配。
6.实验步骤表1 标准曲线的制作步骤管号0 1 2 3 4 5 6 7葡萄糖 0.0 0.1 0.2 0.3 0.4 0.6 0.8 1.0苯酚液 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5浓硫酸 3.0 3.0 3.0 3.0 3.0 3.0 3.0 3.0取8支干净的具塞试管按表2方法在操作,先在冰水浴中加入0.5ml的苯酚溶液,震荡摇匀后缓慢逐滴加入纯硫酸,以不放热或微量放热为宜,摇匀后恒温加塞沸水放置20min,取出凉水冷却10min,以0号作为空白调零,在最大吸收波长处(490nm)测定吸光度。
以葡萄糖浓度X为横坐标(ug/mL),吸光度Y为纵坐标,从而来绘制标准曲线。
用exceL软件求得回归方程2)待测样品多糖的测定与计算将提取得到的待测多糖用蒸馏水溶解,定容至100 mL,取溶解后的溶液,按标准曲线中的测定方法,以样液为参比液,测定溶液的吸光值,按回归方程计算待测溶液的多糖浓度,注意乘换算系数。
苯酚硫酸法测多糖含量
一【2 】.硫酸苯酚法测多糖含量
1.试剂配制
1.浓硫酸:剖析纯,95.5%
2. 5%苯酚:取苯酚5 g,置100 ml容量瓶中,加蒸馏水至刻度,摇匀后,置棕色试
剂瓶中,冰箱中冷藏储存备用.
3.标准葡聚糖(Dextran,瑞典Pharmacia)或剖析纯葡萄糖.精确称取20m g经105℃湿润至恒重的葡萄糖标准品于500ml容量瓶中,蒸馏水消融定容.
2.制造标准曲线
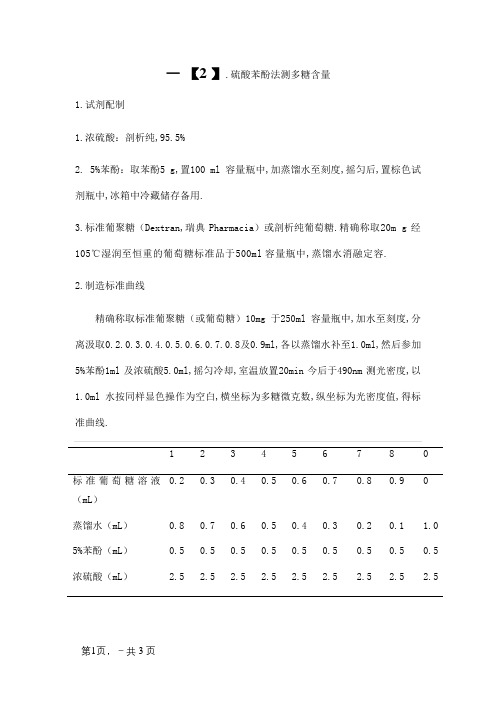
精确称取标准葡聚糖(或葡萄糖)10mg于250ml容量瓶中,加水至刻度,分
离汲取0.2.0.3.0.4.0.5.0.6.0.7.0.8及0.9ml,各以蒸馏水补至1.0ml,然后参加
5%苯酚1ml及浓硫酸5.0ml,摇匀冷却,室温放置20min今后于490nm测光密度,以
1.0ml水按同样显色操作为空白,横坐标为多糖微克数,纵坐标为光密度值,得标
准曲线.
1 2 3 4 5 6 7 8 0
0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0 标准葡萄糖溶液
(mL)
蒸馏水(mL)0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 1.0 5%苯酚(mL)0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 浓硫酸(mL) 2.5 2.5 2.5 2.5 2.5 2.5 2.5 2.5 2.5
操作的时刻有几条你须要留意的,这些对你的检测成果影响极大1.苯酚须要重蒸,配制的苯酚溶液须要妥当保存.2.样品检测的时刻,向样品中加了苯酚溶液须要敏捷摇匀,参加硫酸根本操作:硫酸沿壁加,最好能扭转比色管,让硫酸能平均的沿壁流下.3.加完硫酸须要立刻摇匀,前提是塞子要配套,不怕烫热.冷水浴,要精确.。
测蛋白、多糖的方法

一、硫酸苯酚法测多糖含量1、试剂配制①浓硫酸:分析纯,95.5%②80%苯酚:80克苯酚(分析纯重蒸馏试剂)加20克水使之溶解,可置冰箱中避光长期储存。
6%苯酚:临用前以80%苯酚配制。
(每次测定均需现配)③5%苯酚:取苯酚100 g,加铝片0. 1 g和碳酸钠0. 05 g,常压蒸馏,收集182℃馏分。
称取该馏分(100%苯酚)5 g,置100 ml容量瓶中,加蒸馏水至刻度,摇匀后,置棕色试剂瓶中,冰箱中冷藏储存备用。
④标准葡聚糖(Dextran,瑞典Pharmacia)或分析纯葡萄糖。
准确称取20m g经105℃干燥至恒重的葡萄糖标准品于500ml容量瓶中,蒸馏水溶解定容。
2、制作标准曲线准确称取标准葡聚糖(或葡萄糖)20mg于500ml容量瓶中,加水至刻度,分别吸取0.2、0.3、0.4、0.5、0.6、0.7、0.8及0.9ml,各以蒸馏水补至1.0ml,然后加入6%(5%,9%)苯酚0.5ml及浓硫酸5.0ml,摇匀冷却,室温放置20min以后于490nm测光密度,以2.0ml水按同样显色操作为空白,横坐标为多糖微克数,纵坐标为光密度值,得标准曲线。
1 2 3 4 5 6 7 8 0 标准葡萄糖溶液(mL)0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0 蒸馏水(mL)0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 1.0 6%苯酚(mL)0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 浓硫酸(mL) 2.5 2.5 2.5 2.5 2.5 2.5 2.5 2.5 2.53 注意事项(1)此法简单、快速、灵敏、重复性好,对每种糖仅制作一条标准曲线,颜色持久。
(2)制作标准线宜用相应的标准多糖,如用葡萄糖,应以校正系数0.9校正μg数。
(3)对杂多糖,分析结果可根据各单糖的组成比及主要组分单糖的标准曲线的校正系数加以校正计算(4)测定时根据光密度值确定取样的量。
苯酚硫酸法测多糖含量

一、硫酸苯酚法测多糖含量之相礼和热创作1、试剂配制1.浓硫酸:分析纯,95.5%2. 5%苯酚:取苯酚5 g,置100 ml容量瓶中,加蒸馏水至刻度,摇匀后,置棕色试剂瓶中,冰箱中冷藏储存备用.3.尺度葡聚糖(Dextran,瑞典Pharmacia)或分析纯葡萄糖.精确称取20m g经105℃干燥至恒重的葡萄糖尺度品于500ml容量瓶中,蒸馏水溶解定容.2、制造尺度曲线精确称取尺度葡聚糖(或葡萄糖)10mg于250ml容量瓶中,加水至刻度,分别汲取0.2、0.3、0.4、、、、及ml,各以蒸馏水补至1.0ml,然后加入5%苯酚1ml及浓硫酸5.0ml,摇匀冷却,室温放置20min当前于490nm测光密度,以1.0ml水按异样显色操纵为空白,横坐标为多糖微克数,纵坐标为光密度值,得尺度曲线.1 2 3 4 5 6 7 8 0 尺度葡萄糖溶液0 (mL)蒸馏水(mL)5%苯酚(mL)浓硫酸(mL)3 留意事项(1)此法简单、快速、灵敏、反复性好,对每种糖仅制造一条尺度曲线,颜色持久.(2)制造尺度线宜用相应的尺度多糖,如用葡萄糖,应以校正系数0.9校正μg数.(3)对杂多糖,分析结果可根据各单糖的组成等到次要组分单糖的尺度曲线的校正系数加以校正计算(4)测定时根据光密度值确定取样的量.光密度值最好在0.1——0.3之间.比方:小于0.1之下可以考虑取样品时取2克,仍取0.2ml样品液,如大于0.3可以减半取0.1ml的样品液测定.(5)正常的反应溶液是深棕色.糖越多颜色越深.留意硫酸的纯度.空白的颜色很深,阐明你的空白中的苯酚被氧化了深红是醌(苯酚氧化生成)的颜色颜色过深的话阐明你的酚的难度过大,一样平常是5%但是没遇到你说的那么严重,不是深红色的做的好的时分颜色很浅,颜色深点也有肯能.操纵的时分有几条你必要留意的,这些对你的检测结果影响极大1、苯酚必要重蒸,配制的苯酚溶液必要妥善保管.2、样品检测的时分,向样品中加了苯酚溶液必要迅速摇匀,加入硫酸基本操纵:硫酸沿壁加,最好能旋转比色管,让硫酸能均匀的沿壁流下.3、加完硫酸必要马上摇匀,前提是塞子要配套,不怕烫热、冷水浴,要精确.。
苯酚硫酸法测多糖含量

一、硫酸苯酚法测多糖含量之五兆芳芳创作1、试剂配制1.浓硫酸:阐发纯,95.5%2. 5%苯酚:取苯酚5 g,置100 ml容量瓶中,加蒸馏水至刻度,摇匀后,置棕色试剂瓶中,冰箱中冷藏储存备用.3.尺度葡聚糖(Dextran,瑞典Pharmacia)或阐发纯葡萄糖.准确称取20m g经105℃枯燥至恒重的葡萄糖尺度品于500ml容量瓶中,蒸馏水溶解定容.2、制作尺度曲线准确称取尺度葡聚糖(或葡萄糖)10mg于250ml容量瓶中,加水至刻度,辨别吸取0.2、0.3、0.4、、、、及ml,各以蒸馏水补至1.0ml,然后参加5%苯酚1ml及浓硫酸5.0ml,摇匀冷却,室温放置20min以后于490nm测光密度,以1.0ml水按同样显色操纵为空白,横坐标为多糖微克数,纵坐标为光密度值,得尺度曲线.1 2 3 4 5 6 7 8 0 尺度葡萄糖溶液0 (mL)蒸馏水(mL)5%苯酚(mL)浓硫酸(mL)3 注意事项(1)此法复杂、快速、灵敏、重复性好,对每种糖仅制作一条尺度曲线,颜色持久.(2)制作尺度线宜用相应的尺度多糖,如用葡萄糖,应以校正系数0.9校正μg数.(3)对杂多糖,阐发结果可按照各单糖的组成等到主要组分单糖的尺度曲线的校正系数加以校正计较(4)测定时按照光密度值确定取样的量.光密度值最好在0.1——0.3之间.比方:小于0.1之下可以考虑取样品时取2克,仍取0.2ml样品液,如大于0.3可以减半取0.1ml的样品液测定.(5)正常的反响溶液是深棕色.糖越多颜色越深.注意硫酸的纯度.空白的颜色很深,说明你的空白中的苯酚被氧化了深红是醌(苯酚氧化生成)的颜色颜色过深的话说明你的酚的难度过大,一般是5%但是没遇到你说的那么严重,不是深白色的做的好的时候颜色很浅,颜色深点也有肯能.操纵的时候有几条你需要注意的,这些对你的检测结果影响极大1、苯酚需要重蒸,配制的苯酚溶液需要妥善保管.2、样品检测的时候,向样品中加了苯酚溶液需要迅速摇匀,参加硫酸根本操纵:硫酸沿壁加,最好能旋转比色管,让硫酸能均匀的沿壁流下.3、加完硫酸需要立即摇匀,前提是塞子要配套,不怕烫热、冷水浴,要准确.。
硫酸苯酚法测多糖

一、总糖含量标准曲线的绘制
准确称取无水葡萄糖10 mg,溶解后转入100 mL容量瓶定容。
按表4所示操作。
表4 总糖含量标准曲线绘制方法
管号0 1 2 3 4 5
标准葡萄
糖溶液
(mL)
0 0.2 0.6 1.0 1.4 1.8
蒸馏水
(mL)
2.0 1.8 1.4 1.0 0.6 0.2 6%苯酚各1.0 mL
浓硫酸各5.0 mL
检测
摇匀后沸水加热10 min,冷却至室温后于490 nm处以0号管为空白对照,测光密度值,以葡萄糖含量为横坐标,吸光值为纵坐标作标准曲线:Y=aX+b(Y为吸光值,X为葡萄糖质量/ug)。
二、试液总糖含量的测定
用移液枪从总体积V中吸取一定体积V1ml的待测液,用蒸馏水补至体积为2 mL,加入6%苯酚1.0 mL,浓硫酸5.0 mL,空白对照以蒸馏水代替待测液,摇匀后沸水加热10 min,冷却后,在490 nm处测定吸光值为A。
查标准曲线,算出总糖含量。
m(g)=V(A−b)/a
1000000V1。
实验一硫酸苯酚法测多糖含量

实验一硫酸苯酚法测多糖含量The pony was revised in January 2021实验一硫酸-苯酚法测多糖含量1.目的要求? 测量蒽酮硫酸法不能测量的血清型的过程样品中的多糖含量2.2.方法原理3.糖在浓硫酸作用下,水解生成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚缩合成橙黄色化合物,且颜色稳定,在波长490 nm处和一定的浓度范围内,其吸光度与多糖含量呈线性关系正比,从而可以利用分光度计测定其吸光度,并利用标准曲线定量测定样品的多糖含量,本方法可用于多糖、单糖含量的测定。
4.3.主要实验仪器及材料5.浓硫酸,苯酚,蒸馏装置,分光光度计,电子天平,坐标纸或电脑等。
6.4.掌握要点7.硫酸显色的安全、准确操作,单糖到多糖的转换系数。
8.5.试剂配制9.1)葡萄糖标准液的配制10.准确称取干燥恒重的葡萄糖100 mg,蒸馏水准确定容至100 mL的1 mg/L的葡萄糖液,摇匀后准确吸取10 mL该溶液,蒸馏水稀释定容至100 mL,即得100 ug/mL的葡萄糖标准液。
11.2)90%苯酚液的配制12.?准确移取苯酚90mL,蒸馏水定容至100 mL,即得90%苯酚液,棕色瓶中避光保存3)6%苯酚液的配制将90%苯酚液稀释至6%,即一体积储存液对应十四体积纯水,临用现配。
6.实验步骤表1 标准曲线的制作步骤7.管号 0? 1 2 3 4 5 6 78.葡萄糖9.10.苯酚液11.浓硫酸?12.取8支干净的具塞试管按表2方法在操作,先在冰水浴中加入的苯酚溶液,震荡摇匀后缓慢逐滴加入纯硫酸,以不放热或微量放热为宜,摇匀后恒温加塞沸水放置20min,取出凉水冷却10min,以0号作为空白调零,在最大吸收波长处(490nm)测定吸光度。
以葡萄糖浓度X为横坐标(ug/mL),吸光度Y为纵坐标,从而来绘制标准曲线。
用exceL 软件求得回归方程13.2)待测样品多糖的测定与计算14.将提取得到的待测多糖用蒸馏水溶解,定容至100 mL,取溶解后的溶液,按标准曲线中的测定方法,以样液为参比液,测定溶液的吸光值,按回归方程计算待测溶液的多糖浓度,注意乘换算系数。
苯酚-硫酸法测多糖含量

苯酚-硫酸法测多糖含量原理多糖在硫酸的作用下先水解成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚生成橙黄色化合物。
再以比色法测定。
试剂1.浓硫酸:分析纯,95.5%2. 80%苯酚:80克苯酚(分析纯重蒸馏试剂)加20克水使之溶解,可置冰箱中避光长期储存。
3. 6%苯酚:临用前以80%苯酚配制。
(每次测定均需现配)4.标准葡聚糖(Dextran,瑞典Pharmacia),或分析纯葡萄糖。
5. 15%三氯乙酸(15%TCA):15克TCA加85克水使之溶解,可置冰箱中长期储存。
6. 5%三氯乙酸(5%TCA):25克TCA加475克水使之溶解,可置冰箱中长期储存。
7. 6mol/L 氢氧化钠:120克分析纯氢氧化钠溶于500ml水。
8. 6mol/L 盐酸操作1.制作标准曲线:准确称取标准葡聚糖(或葡萄糖)20mg于500ml容量瓶中,加水至刻度,分别吸取0.4、0.6、0.8、1.0、1.2、1.4、1.6及1.8ml,各以蒸馏水补至2.0ml,然后加入6%苯酚1.0ml及浓硫酸5.0ml,摇匀冷却,室温放置20分钟以后于490nm测光密度,以2.0ml水按同样显色操作为空白,横坐标为多糖微克数,纵坐标为光密度值,得标准曲线。
2.样品含量测定:①取样品1克(湿样)加1ml 15%TCA溶液研磨,再加少许5%TCA溶液研磨,倒上清液于10毫升离心管中,再加少许5%TCA溶液研磨,倒上清液,重复3次。
最后一次将残渣一起到入离心管。
注意:总的溶液不要超出10毫升。
(既不要超出离心管的容量)。
②离心,转速3000转/分钟,共三次。
第一次15分钟,取上清液。
后两次各5分钟取上清液到25毫升锥形比色管中。
最后滤液保持18毫升左右。
(测肝胰腺样品时,每次取上清液时应过滤。
因为其脂肪含量大容易夹带残渣。
)③水浴,在向比色管中加入2毫升6mol/L 盐酸之后摇匀,在96℃水浴锅中水浴2小时。
④定容取样。
水浴后,用流水冷却后加入2毫升6mol/L 氢氧化钠摇匀。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验一硫酸-苯酚法测多糖含量
1.目的要求
2.测量蒽酮硫酸法不能测量的血清型的过程样品中的多糖含量3.2.方法原理
4.糖在浓硫酸作用下,水解生成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚缩合成橙黄色化合物,且颜色稳定,在波长490 nm处和一定的浓度范围内,其吸光度与多糖含量呈线性关系正比,从而可以利用分光度计测定其吸光度,并利用标准曲线定量测定样品的多糖含量,本方法可用于多糖、单糖含量的测定。
5.3.主要实验仪器及材料
6.浓硫酸,苯酚,蒸馏装置,分光光度计,电子天平,坐标纸或电脑等。
7.4.掌握要点
8.硫酸显色的安全、准确操作,单糖到多糖的转换系数。
9.5.试剂配制
10.1)葡萄糖标准液的配制
11.准确称取干燥恒重的葡萄糖100 mg,蒸馏水准确定容至100 mL的1 mg/L的葡萄糖液,摇匀后准确吸取10 mL该溶液,蒸馏水稀释定容至100 mL,即得100 ug/mL的葡萄糖标准液。
12.2)90%苯酚液的配制
13.准确移取苯酚90mL,蒸馏水定容至100 mL,即得90%苯酚液,棕色瓶中避光保存
3)6%苯酚液的配制
将90%苯酚液稀释至6%,即一体积储存液对应十四体积纯水,临用现配。
6.实验步骤表1 标准曲线的制作步骤
7.管号0 1 2 3 4 5 6 7
8.葡萄糖 0.0 0.1 0.2 0.3 0.4 0.6 0.8 1.0
9.苯酚液 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5
10.浓硫酸 3.0 3.0 3.0 3.0 3.0 3.0 3.0 3.0
11.取8支干净的具塞试管按表2方法在操作,先在冰水浴中加入0.5ml 的苯酚溶液,震荡摇匀后缓慢逐滴加入纯硫酸,以不放热或微量放热为宜,摇匀后恒温加塞沸水放置20min,取出凉水冷却10min,以0号作为空白调零,在最大吸收波长处(490nm)测定吸光度。
以葡萄糖浓度X为横坐标(ug/mL),吸光度Y为纵坐标,从而来绘制标准曲线。
用exceL软件求得回归方程12.2)待测样品多糖的测定与计算
13.将提取得到的待测多糖用蒸馏水溶解,定容至100 mL,取溶解后的溶液,按标准曲线中的测定方法,以样液为参比液,测定溶液的吸光值,按回归方程计算待测溶液的多糖浓度,注意乘换算系数。
二、实验原理
游离的己糖或多糖中的己糖基、戊糠醛及己糖醛酸在浓硫酸的作用下脱水生成糠醛衍生物,糠醛衍生物与蒽酮缩合成蓝色的化合物,在620nm处有最大吸收,在一定糖浓度范围内(200ug/ml),溶液吸光度值与糖溶液的浓度成线性关系。
用酸将植物组织中没有还原性的多糖和寡糖彻底水解成具有还原性的单糖,或直接提取植物组织中的还原糖,即可对植物组织中的总糖和还原糖进行定量测定。
三、实验材料
1.可见分光光度计、电子天平(1/100)、粉碎机、水浴锅、电炉。
研钵、量筒、三角烧瓶、烧杯、容量瓶、玻璃漏斗、试管1.5cm×15cm、刻度吸管、胶头滴管、pH试纸、坐标纸。
四、实验试剂
1.蒽酮试剂:取2g蒽酮溶于l000ml体积分数为80%的硫酸中,当日配制使用。
2.标准葡萄糖溶液(0.1mg-m1):称取100mg葡萄糖,溶于蒸馏水并稀释至1 000ml(可滴加几滴甲苯作防腐剂)。
3.6mol-L HCl溶液:50ml盐酸,加水至100ml。
4.10%NaOH溶液:称取10g NaOH固体,溶于蒸馏水并稀释至100ml。
五、操作步骤
1.葡萄糖标准曲线的绘制
取干净试管6支,按下表进行操作。
以吸光度为纵坐标各标准液浓度(mg-m1)为横坐标做图。
2.样品中还原糖的提取和测定
称取植物原料干粉0.1~0.5g,加水约3ml,在研钵中磨成匀浆,转入三角烧瓶中,并用约30ml的蒸馏水冲洗研钵2~3次,洗出液也转入三角烧瓶中。
于50℃水浴中保温半小时(使还原糖浸出),取出,冷却后定容至100ml。
过滤,取lml滤液进行还原糖的测定:吸取lml总糖类溶液置试管中,浸于冰浴中冷却,再加入4ml蒽酮试剂,沸水浴中准确加热10min,取出用自来水冷却后比色,其他条件与做标准曲线相同,测得的吸光度值由标准曲线查算出样品液的糖含量。
(样品液显色后若颜色很深,其吸光度超过标准曲线浓度范围,则应将样品提取液适当稀释后再加蒽酮显色测定)。
标准曲线的制作及样品测定参考表
1# 2# 3# 4# 5# 6# 7#(样品)8#(样品)
标准葡萄糖溶液(ml) 0 0.2 0.4 0.6 0.8 1.0 还原糖总糖
蒸馏水(ml) 1.0 0.8 0.6 0.4 0.2 0
样品液(ml) - - - - - - 1.0 1.0
糖溶液浓度(mg/ml) 0 0.02 0.04 0.06 0.08 0.10 待测待测
置冰水浴中冷却
蒽酮试剂(ml) 4.0 4.0 4.0 4.0 4.0 4.0 4.0 4.0
沸水浴中准确加热10min,取出,用自来水冷却,室温放置10min
A620nm
3.样品中总糖的提取、水解和测定
称取植物原料干粉0.1~0.5g,加水约3ml,在研钵中磨成匀浆,转入三角烧瓶中,并用约12ml的蒸馏水冲洗研钵2~3次,洗出液也转入三角烧瓶中。
再向三角烧瓶中加入6mol/L盐酸10ml,搅拌均匀后在沸水浴中水解半小时,冷却后用10%NaOH溶液中和pH呈中性。
然后用蒸馏水定容至100ml,过滤,取滤液10ml,用蒸馏水定容100ml,成稀释1000倍的总糖水解液。
取lml总糖水解液,测定其还原糖的含量:吸取lml总糖类溶液置试管中,浸于冰浴中冷却,再加入4ml蒽酮试剂,沸水浴中准确加热10min,取出用自来水冷却后比色,其他条件与做标准曲线相同,测得的吸光度值由标准曲线查算出样品液的糖含量。
六、实验结果
按照下列公式分别计算植物原料干粉中还原糖和总糖的质量分数(ω)。
ω(还原糖)= (C1V1/m)×100%
ω(总糖)= (C2V2/m)×0.9①×100%
式中ω(还原糖):还原糖的质量分数(%);ω(总糖):总糖的质量分数(%);
C1:还原糖的质量浓度(mg/ml);
C2:水解后还原糖的质量浓度(mg/ml);
V1:样品中还原糖提取液的体积(m1);
V2:样品中总糖提取液的体积(m1);
m :样品质量(mg)。
注①:计算总糖含量的公式,在测定干扰杂质很少、还原糖含量相对总糖含量很少时适用,乘0.9是为了从测定出的总糖水解成的单糖量中,扣除水解时所消耗的水量。
七、注意事项
1.总糖:食品中的总糖通常是指具有还原性的糖(葡萄糖,果糖,乳糖,麦芽糖等)和在测定条件下能水解为还原性单糖的糖的总量。
2.本法适用于可溶性还原糖测定。
测定结果是还原性糖和能水解为还原性糖的总和。
3.如要求结果中不含淀粉,则样品处理不应用高浓度酸,而应改用80%乙醇。
4.如提取液中有较多的可溶性蛋白,必须先除去蛋白。
5.若样液较深,可用活性碳脱色。
