病例报告表样式
临床研究病例分析报告表格模板

XXXXXXXXXXXXXXXXXXXXXXXXXXXXXXX受试者姓名缩写□□□□药物编号:□□□试验中心编号:□试验开始日期年月日填表说明1.请用签字笔填写,字迹应清晰,易于辨认。
2.受试者姓名按汉语拼音首字母缩写靠左对齐填写。
345试验观察流程图入组筛选表1.受试者应为:♦年龄:18 -70岁癌症患者(一般情况尚好,可适当放宽)♦性别不限♦预计生存期2个月以上的住院患者♦疼痛强度为中到重度,评分≥4♦并符合一下条件之一(请在符合的项目上画圈)1)入选前1周内曾使用XX,日剂量为40-60mg,疼痛强度可缓解到≤2;♦血压高于正常值♦血液系统疾病♦肝、肾功能明显异常(即指标高于正常值一倍以上)♦脑部疾病,判定能力异常♦XX药耐受、过敏,或曾在使用时因不良反应停药♦药物及∕或酒精滥用♦孕妇或哺乳期妇女如以上任何一个答案为“是”,此受试者不能参加是□□□□□□□□□□否□□□□□□□□□□结论:该患者是否符合上述要求,同意入组医生签名:______日期____年___月___日病历简况1.1检查日期:年月日.2受试者病历号:2.1出生日期:年月.2性别:□1.男□2.女.3临床诊断:分期1. T□ 2. N□ 3. M□.4现接受的抗癌治疗:□1.放疗间歇期□2.化疗间歇期□3.中医药□4.手术□5.无□6.其他(请注明)如有,请回答:.61药品名称用药剂量: .62用药方式:□1.口服□2.静注□3.肌注□4.其他 .63用药时间:□1.近四周内□2.近三天□3.其他.64其它与镇痛有关合并用药,如有,请详述:3.0既往史.1药物过敏史□1.无□2.有 .2脑部疾患□1.无□2.有.3心脏疾患□1.无□2.有 .4哮喘□1.无□2.有.5胆道疾患□1.无□2.有 .6习惯性便秘□1.无□2.有.7肾脏疾患□1.无□2.有 .8糖尿病□1.无□2.有如有,请描述:1.2.4.0体格检查.1 1.T ._℃ 2.P 次/分 3.R 次/分4.SBP mmHg5.DBP mmHg6.身高 cm7.体重 Kg.2皮肤粘膜□ 1.无□2.苍白□3.黄染□4.紫绀□5.皮疹□1.存在□2.部分存在□3.不存在.81病理反射□1.未引出□2.有引出5.入组前可能与镇痛药物有关的基础症状(如果患者出现没有标识的症状,请自行填写文字)填表医生签名:______日期____年___月___日给药前生活质量记录表入组时实验室检查血常规检查心电图检查医生签名:______日期____年___月___日试验结束时生活质量记录表很可能有肯定有关可能有关可能无关肯定无关关与药物有合理时间顺++++—序为已知的药物反应类+++——型停药后反应减轻或消++±±—失再次给药后反应复出+???—现无法用受试者疾病来++—±—解释不良事件记录表同期治疗用药表用药后辅助检查结果心电图检查医生签名:______日期____年___月___日研究完成情况总结CRF审核声明我已审阅过此病例报告表中的全部内容和数据,确认信息记录真实、准确,项目填写完整,符合试验方案的要求,特此声明。
疼痛病例报告表模板

疼痛病例报告表模板病例信息
患者基本信息
•姓名:
•年龄:
•性别:
•职业:
•地址:
主要症状
•疼痛类型:
•疼痛部位:
•疼痛程度:
•疼痛频率:
疼痛史
•疼痛开始时间:
•疼痛持续时间:
•疼痛是否有加重或缓解:
•疼痛是否伴随其他症状:
详细病史
健康状况
•既往病史:
•家族史:
•近期生活变化:
治疗方案
•治疗方法:
•用药方案:
•其他疗法:
评估记录
•病人自我评估:
•医师评估:
治疗效果
•疼痛程度:
•疼痛持续时间:
总结
本次疼痛病例报告表记录了患者的症状、病史、治疗方案以及其治疗效果。
通过对病人进行详细的评估和相应的治疗,患者的疼痛症状得到了缓解,生活质量得到了提高。
我们将继续关注病人的病情变化,为其健康献力。
死亡病例报告表模板

死亡病例报告表模板
背景介绍
死亡病例报告表是医疗机构或者疾病防控部门进行疾病统计和统计分析的重要表单,也是医疗事故案例分析和病理诊断评估的重要依据。
死亡病例报告表的主要作用是对死亡患者的基本情况、病史、死因等信息进行统计和分析,帮助医疗机构或者疾病防控部门掌握死亡原因和死亡趋势,及时发现疾病的变化和发展趋势,进而制定有效的防控措施,提高公共卫生水平,保障人民生命健康。
死亡病例报告表模板
填表单位
•填表日期:
•填报单位名称:
•填表人:
死亡患者基本信息
•姓名:
•性别:
•年龄:
•身份证号:
•死亡日期:
•死亡时间:
•直系亲属姓名:
•联系方式:
死亡患者病史
•既往史:
•主要病史:
•入院日期:
•入院诊断:
•出院日期:
•出院诊断:
死因分析
•自然死亡:
–病因:
–相关检查结果:
•意外死亡:
–事故类型:
–相关检查结果:
•突发性死亡:
–症状:
–相关检查结果:
其他信息
•填表人联系方式:
•填表人签字及日期:
结语
以上是死亡病例报告表模板的具体内容,填写时应根据实际情况进行填写,确保准确性和完整性。
同时,建议医疗机构或者疾病防控部门进行经常性的死亡病例分析和统计,及时发现疾病变化和趋势,提高公共卫生水平,保障人民生命健康。
病例报告表

病例报告表病例报告表病例报告编号:_________一、基本信息:患者姓名:年龄:性别:出生日期:职业:联系电话:家庭住址:二、主诉:患者主诉症状或不适感,如:发热、咳嗽、胸痛等。
三、现病史:患者起病时间:起病方式及特点:持续时间:有无进展;主要症状表现:具体体征和症状;治疗情况:用药,疗效;四、既往史:既往病史(慢性疾病、传染病等);手术史/外伤史;药物过敏史;家族史(对本次问题可能有影响的家族病史);五、个人史:吸烟史:日均()支×年;饮酒史:频率,种类,饮酒量;饮食习惯:如恶心呕吐、食欲减退等;睡眠情况:如失眠、多梦、嗜睡等;排尿情况:如尿频、尿急、尿痛等;大便情况:如便秘、腹泻、血便等;月经状况(女性):周期、量,有无异常症状;性生活史:性伴、保护措施、性疾病史;六、体格检查:一般状况:精神、面色、体型;生命体征:体温、呼吸、脉搏;面容:黄染、水肿、皮疹、溃疡等;皮肤和黏膜:皮疹、瘀斑、水肿、黄染等;淋巴结:颈部、腋窝、腹股沟、锁骨上窝等;头部:眼结膜、巩膜、口唇黏膜、咽、鼻腔、牙齿、舌等;颈部:甲状腺、淋巴结、颈动脉、颈静脉、颈软组织等;心肺:心脏听诊区、心律、心音、杂音、呼吸音、啰音、胸廓形状等;腹部:触诊、压痛、肿块、移动性、包块、肠鸣音、肠型等;四肢:肌力、肌张力、活动度、肢体水肿/畸形等;神经系统:病理征、骨反射、病理反射、感觉、运动、余震等;七、辅助检查:实验室检查:血常规、尿常规、生化指标、肝肾功能、电解质、凝血功能、血型、感染性指标、肿瘤标记物、风湿免疫学指标等;影像学检查:X线、CT、MRI、超声、心电图等;病理学检查:病理活检、穿刺活检、细胞学等;其他特殊检查:如内窥镜、皮肤测试等;八、初步诊断:九、治疗方案:给予药物治疗、手术治疗、放射治疗等;用药方案及剂量;手术操作方法及时间;治疗进展及疗效评估;十、随访计划:随访时间、内容及方法;十一、注意事项:备注:其他需要补充的内容。
病例报告表(肿瘤案例)

病例报告表姓名:性别:□男□女年龄:岁基础疾病:恶性实体肿瘤病史:月,类型为:□Ⅰ期□Ⅱ期□Ⅲ期□Ⅳ期肿瘤并发症:疼痛:□无□有出血:□无□有发热:□无□有窒息:□无□有感染:□无□有积液:□无□有弥散性血管内凝血:□无□有用法用量:负离子氧气机30分钟/次,3次/天;开始时间:年月日,共治疗天;合并用药方案:药物名称①:,剂量:;药物名称②:,剂量:;药物名称③:,剂量:;药物名称④:,剂量:;1. 瘤体大小治前和治疗后1个月、2个月CT 、B 超复查,目标病灶的评价如下。
CR :所有目标病灶消失。
PR :基线病灶长径总和缩小 ≥ 30%。
PD :基线病灶长径总和增加 ≥ 20%或出现新病灶。
SD :基线病灶长径总和有缩小但未达PR 或有增加但未达PD 。
2.体重变化**:每周检测记录1次。
除外体腔积液、浮肿等因素引起的体重变化。
好转:体重增加>2kg ,并维持4周以上。
稳定:体重增加或减少≤2kg 。
进展:体重减少>2kg ,持续4周以上。
3. 综合症状***:每周记录1次。
以体力状况、疼痛和食欲状况评分为评价内容,根据患者主诉,由患者本人综合评定为好转(3项指标中有2项好转,1项稳定,或3项好转,并维持4周以上)、稳定(3项指标中有1项好转,2项稳定;或2项好转,一项恶化,并维持4 周以上)、恶化(3项指标中有2项恶化,一项稳定,或3项恶化,并维持4周以上)。
综合症状评分指标:(1)体力状况:依据主诉程度,未发病时患者自身体力情况为正常,为0 级;轻度乏力,体力情况为正常情况的1/2 到3/4,为Ⅰ级;中度乏力,体力情况为正常情况的1/4 到1/2,为Ⅱ级;重度乏力,体力情况为正常情况的1/ 4 以下,为Ⅲ级。
好转:体力变化减轻≥ 1 个等级并维持四周以上。
稳定:体力变化基本不变并持续4 周以上;进展:体力变化增加≥ 1 个等级并持续4 周以上。
(2)食欲变化:依据主诉程度,未发病时患者一日食量为正常,为0 级;食量轻度下降,为正常食量的1/ 2到3/4,为Ⅰ级;食量中度下降,为正常食量的1/4 到1/2,为Ⅱ级;食量严重下降,为正常食量的1/4 以下,为Ⅲ级。
完整版病例报告表(CRF表)

完整版病例报告表(CRF表)XXXX临床研究病例报告表方案编号:版本号: 1.0版本日期:受试者姓名拼音缩写:|__|__|__|__|受试者编号:|__|__|__|__|__|研究者签名:________________主要研究者:XX 教授申办单位:XX医院正式填表前,请认真阅读以下说明填表说明1.参加本研究的人员均需经过GCP培训,并充分阅读了解本试验方案及相关资料,严格按方案执行,并如实填写。
2.已入选的受试者,不论是否剔除或淘汰,都需要填写病例报告表。
3.填写务必认真.准确.清晰.如实,不能随意涂改,如填写确有错误,修改时不能涂黑或使用涂改液,应将填写错误的数据用横线居中划出,在旁边写上正确的数据,并由临床试验负责医师在修改处签名.注明日期。
例如:10 20 刘明2018.01.014.请在各选择项□内划“×”,在|_|填写相应的数字,所有栏目内应填写,在____填写文字。
选用钢笔或签字笔用力填写表格,以便第三份亦能看清。
为防止复写至一下页,请在填写时用垫板衬在下一页前。
5.患者姓名拼音缩写需填满四格,两字姓名分填两字前两个字母,三字姓名填前两字首字母与第三字前两个字母,四字姓名填每字首字母。
举例:李明L I M I 王晓亮W X L I 欧阳青山O Y Q S。
6.所有检查项目因故未查或漏查请填写ND,具体用药剂量和时间不明请填写NK。
7.严格观察和如实填写不良事件记录表。
记录不良事件的发生时间.严重程度.持续时间.采取的措施和转归。
临床研究过程中发生的任何严重不良事件,必须立即报告协办单位.临床研究负责单位主要研究者和伦理委员会。
严重不良事件报告单位报告单位联系人联系电话XX医院伦理委员会XXXX国家食品药品监督管理局注册司- 010-********/32/42/20筛选期签署知情同意书?知情同意书签署日期:20|__|__|年|__|__|月|__|__|日访视日期:20|__|__|年|__|__|月|__|__|日人口学资料出生日期:|__|__|__|__|年|__|__|月|__|__|日性别:□男□女民族:□汉族□其他,其他说明:_____________________体重|__|__|__|.|__| kg 身高|__|.|__|__| m肿瘤诊断首次病理学确诊日期:|__|__|__|__|年|__|__|月|__|__|日□外科手术□活检□其他病理诊断:原发灶大小及部位:_______________________是否有转移灶:□是□否转移灶累及器官数:≤2□;3-5□;>5□转移灶部位:病理分期:T|__|N|__|M|__|临床分期:□I期□II期□III期□IV期肿瘤手术史是否有肿瘤手术史?□是□否手术名称手术日期|__|__|__|__|年|__|__|月|__|__|日|__|__|__|__|年|__|__|月|__|__|日|__|__|__|__|年|__|__|月|__|__|日|__|__|__|__|年|__|__|月|__|__|日|__|__|__|__|年|__|__|月|__|__|日化疗史是否有化疗史(包括新辅助治疗和辅助治疗)?□是□否属于何种治疗#化疗方案①开始日期/ 结束日期最佳疗效进展日期|__| |__||__|__|__|__|年|__|__|月|__|__|日/|__|__|__|__|年|__|__|月|__|__|日□CR □PR □SD□PD* □不耐受*□不详 |__|__|__|__|年|__|__|月|__|__|日|__| |__||__|__|__|__|年|__|__|月|__|__|日/|__|__|__|__|年|__|__|月|__|__|日□CR □PR □SD□PD □不耐受□不详 |__|__|__|__|年|__|__|月|__|__|日|__| |__||__|__|__|__|年|__|__|月|__|__|日/|__|__|__|__|年|__|__|月|__|__|日□CR □PR □SD□PD □不耐受□不详|__|__|__|__|年|__|__|月|__|__|日#:1=辅助治疗,2=新辅助治疗,3=系统治疗史① :1=阿霉素;2=表阿霉素;3=异环磷酰胺;4=达卡巴嗪5=美司钠;6=恩度;9=其它*:若因疾病进展而换药,需记录进展影像学依据;若不耐受,需记录发生的不良反应和严重程度。
完整版病例报告表(CRF表)

XXXX临床研究病例报告表受试者姓名拼音缩写:|__|__|__|__|受试者编号:|__|__|__|__|__|研究者签名:________________主要研究者:XX 教授申办单位:XX医院正式填表前,请认真阅读以下说明填表说明1.参加本研究的人员均需经过GCP培训,并充分阅读了解本试验方案及相关资料,严格按方案执行,并如实填写。
2.已入选的受试者,不论是否剔除或淘汰,都需要填写病例报告表。
3.填写务必认真.准确.清晰.如实,不能随意涂改,如填写确有错误,修改时不能涂黑或使用涂改液,应将填写错误的数据用横线居中划出,在旁边写上正确的数据,并由临床试验负责医师在修改处签名.注明日期。
例如:10 20 刘明请在各选择项□内划“×”,在|_|填写相应的数字,所有栏目内应填写,在____填写文字。
选用钢笔或签字笔用力填写表格,以便第三份亦能看清。
为防止复写至一下页,请在填写时用垫板衬在下一页前。
5.患者姓名拼音缩写需填满四格,ND,具体用药剂量和时间不明请填写NK。
7.严格观察和如实填写不良事件记录表。
记录不良事件的发生时间.严重程度.持续时间.采取的措施和转归。
临床研究过程中发生的任何严重不良事件,必须立即报告协办单位.临床研究负责单位主要研究者和伦理委员会。
严重不良事件报告单位报告单位联系人联系电话XX医院伦理委员会XXXX国家食品药品监督管理局注册司-0/32/42/20筛选期签署知情同意书知情同意书签署日期:20|__|__|年|__|__|月|__|__|日访视日期:20|__|__|年|__|__|月|__|__|日人口学资料肿瘤诊断肿瘤手术史是否有肿瘤手术史□是□否化疗史是否有化疗史(包括新辅助治疗和辅助治疗)□是□否#:1=辅助治疗,2=新辅助治疗,3=系统治疗史:1=阿霉素;2=表阿霉素;3=异环磷酰胺;4=达卡巴嗪5=美司钠;6=恩度;9=其它*:若因疾病进展而换药,需记录进展影像学依据;若不耐受,需记录发生的不良反应和严重程度。
11.院感病例报告表(新版)
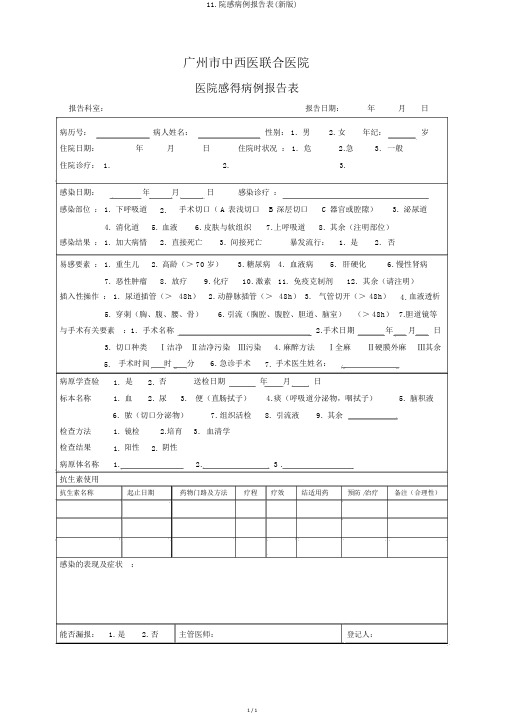
11.院感病例报告表(新版)广州市中西医联合医院医院感得病例报告表报告科室:报告日期:年月日病历号:病人姓名:性别: 1. 男 2. 女年纪:岁住院日期:年月日住院时状况: 1. 危 2. 急 3. 一般住院诊疗: 1. 2. 3.感染日期:年月日感染诊疗:感染部位: 1. 下呼吸道 2. 手术切口( A 表浅切口 B 深层切口 C 器官或腔隙) 3. 泌尿道4. 消化道5. 血液6. 皮肤与软组织7. 上呼吸道8. 其余(注明部位)感染结果: 1. 加大病情 2. 直接死亡 3. 间接死亡暴发流行: 1. 是 2. 否易感要素: 1. 重生儿 2. 高龄(> 70 岁) 3. 糖尿病 4. 血液病 5. 肝硬化 6. 慢性肾病7. 恶性肿瘤8. 放疗9. 化疗10. 激素11. 免疫克制剂12. 其余(请注明)插入性操作: 1. 尿道插管(>48h) 2. 动静脉插管(>48h) 3. 气管切开(>48h) 4. 血液透析5. 穿刺(胸、腹、腰、骨)6. 引流(胸腔、腹腔、胆道、脑室)(> 48h)7.胆道镜等与手术有关要素:1. 手术名称 2. 手术日期年月日3. 切口种类Ⅰ洁净Ⅱ洁净污染Ⅲ污染4. 麻醉方法Ⅰ全麻Ⅱ硬膜外麻Ⅲ其余5. 手术时间时分6. 急诊手术7. 手术医生姓名:病原学查验 1. 是 2. 否送检日期年月日标本名称 1. 血 2. 尿 3. 便(直肠拭子) 4. 痰(呼吸道分泌物,咽拭子) 5. 脑积液6. 脓(切口分泌物)7. 组织活检8. 引流液9. 其余检查方法 1. 镜检 2. 培育 3. 血清学检查结果 1. 阳性 2. 阴性病原体名称 1. 2. 3 .抗生素使用抗生素名称起止日期药物门路及方法疗程疗效结适用药预防 /治疗备注(合理性)感染的表现及症状:能否漏报: 1. 是 2. 否主管医师:登记人:1 / 1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
医疗器械临床试验病例报告表样表
试验项目名称
受试者病例号:□□□□□
试验用医疗器械编号:□□□
临床试验机构(或编号):□□
临床试验方案编号和日期(修改编号和日期若有)
试验开始日期年月日
跟踪结束日期年月日
记录人签名:
填表说明
1.请用钢笔或签字笔填写,字迹应清晰,易于辨认。
2.每项填写内容务必准确,不得随便涂改,如发现填写内容有误,应在原记录上划单横线,在旁边写明正确内容及修改原因,由研究者签名并注明日期。
不得用任何方式(橡皮、涂改液等)涂抹原记录。
一、受试者病历简况
1、入组日期年月日
2、受试者姓名
3、出生日期年月
4、性别□1.男□2.女
5、临床诊断
6、接受的诊断/治疗方式(既往用药和/或手术)
7、入组前基础症状
8、入组时实验室检查
二、符合纳入/排除标准
三、诊断/治疗情况记录
五、一般情况观察记录
六、不良事件记录表
七、试验结论
八、声明
此病例报告表中的信息记录真实、准确,符合试验方案的要求,特此声明。
研究者签名:
年月日
监查与检查记录粘贴处。
