冻融土壤中碳、氮矿化测定实验方案
土壤全碳测定实验报告

土壤全碳测定实验报告实验目的:本实验旨在通过测定土壤全碳含量,了解土壤中有机质的含量以及土壤的肥力状况,并对土壤质量进行评估。
实验原理:土壤全碳测定是通过定量测定土壤中有机碳的含量来评估土壤质量和肥力状况的常用方法之一。
有机碳是土壤中有机质的主要组成部分,其含量高低直接影响土壤的物理、化学和生物学性质。
本实验采用酸化铜氧化法测定土壤全碳含量。
酸化铜氧化法是一种常用的有机碳测定方法,原理上是将有机碳氧化为CO2,风化铜被还原为铜。
其中,土壤样品经过预处理后,添加硫酸铜溶液和液体硝酸,然后加热反应,使有机碳氧化生成CO2,并被稀硝酸捕集,通过测定捕集的CO2的体积可计算出土壤中有机碳的含量。
实验材料和仪器设备:- 土壤样品- 化学草酸- 硫酸铜溶液- 液体硝酸- 高压消解管- 电磁加热板- 试管- 酸碱滴定装置实验步骤:1. 准备土壤样品,将土壤样品收集并去除杂质,取所需重量的土壤样品放入高压消解管中;2. 加入适量的化学草酸,使土壤样品与草酸的比例为10:1,用搅拌棒充分混合;3. 加入适量的硫酸铜溶液和液体硝酸,使样品完全酸化;4. 将高压消解管放入电磁加热板上,加热至样品完全分解,产生CO2气体;5. 用试管将产生的CO2气体捕集起来,并用酸碱滴定装置测定CO2气体体积;6. 根据CO2气体的体积,计算出土壤中有机碳的含量。
实验结果和数据处理:根据测定所得的CO2气体体积,通过计算公式可以得到土壤中有机碳的含量。
将得到的数据整理并进行统计分析,比较不同样品之间的有机碳含量差异。
根据有机碳含量的高低,可以评估土壤质量和肥力状况。
实验结论:通过本实验测定土壤全碳含量,可以评估土壤质量和肥力状况。
有机碳含量高的土壤通常具有较好的肥力和较高的土壤质量;而有机碳含量低的土壤则相对瘠薄。
因此,合理调控土壤有机质含量,对于提高土壤肥力和改善土壤质量具有重要意义。
冻融对湿地土壤可溶性碳、氮和氮矿化的影响

c t st a h f c ffe zn n h w n tr ai n wi i h r i e o ssg i c n n DOC a d DON i h ae h tte e f to re i ga d t a i g a e n t t n a s o t me p r d wa inf a t e l o h t i i o n n t e s i.I wa lo q i b i u h t nto e n r iain i h e ln ol w s a e t y f e i g tmp r t r n ol t sa s u t o v o s t a i g n mi ea z t n t e w t d s i a f ce b r zn e e au e a d e r l o a f d e
d f r n n fe zn n h w n y l r n e t ae h o g n i d o n u ai n e p rme t i ee t e i g a d t a i g c c ewee iv s g td t r u h a n o r i c b t x ei n .Re u t s o h tw t f i r i o s l h w t a i s h
T pcl eln ol F o S nin li, i n a g C ia Z O a gm n , A i d LU Jn — y i t d S i rm aja gPan He o 翻in , hn . H U W n — i 。 W NG J a ,I i aW a s l g n g
A src:C net o otns f i l dog i a na ioe D CadD N)adnt gnm nr i t now t n os dsv a b n r n ioe ieaz i e adsi r l ao f l l
土壤中碳氮磷实验报告单

一、实验目的1. 了解土壤中碳、氮、磷的组成及含量。
2. 掌握土壤中碳、氮、磷的测定方法。
3. 分析土壤中碳、氮、磷的相互作用及影响因素。
二、实验原理土壤中碳、氮、磷是土壤肥力的重要组成部分,对植物生长具有重要意义。
本实验采用重铬酸钾氧化法测定土壤有机碳,采用凯氏定氮法测定土壤全氮,采用钼锑抗比色法测定土壤有效磷。
三、实验材料与仪器1. 实验材料:土壤样品(采集自某地区),重铬酸钾、硫酸、硫酸银、钼酸铵、抗坏血酸、盐酸、氢氧化钠等试剂。
2. 实验仪器:电子天平、高温炉、电热板、酸度计、分光光度计、凯氏瓶、消化器、蒸馏器、移液管、容量瓶等。
四、实验方法1. 土壤有机碳测定(1)称取土壤样品1.0g,置于消化器中。
(2)加入10mL浓硫酸,混匀后置于高温炉中消化,待消化液呈无色透明时取出。
(3)将消化液转移至100mL容量瓶中,用去离子水定容至刻度。
(4)取1mL消化液,加入10mL重铬酸钾溶液,混匀后置于电热板上煮沸5min。
(5)取出冷却后,用去离子水定容至50mL,用分光光度计在570nm波长下测定吸光度。
2. 土壤全氮测定(1)称取土壤样品1.0g,置于凯氏瓶中。
(2)加入10mL浓硫酸,混匀后置于电热板上消化,待消化液呈无色透明时取出。
(3)将消化液转移至100mL容量瓶中,用去离子水定容至刻度。
(4)取2mL消化液,加入1mL硫酸银溶液,混匀后置于电热板上煮沸,直至溶液呈红色。
(5)取出冷却后,用去离子水定容至50mL,用分光光度计在620nm波长下测定吸光度。
3. 土壤有效磷测定(1)称取土壤样品1.0g,置于100mL容量瓶中。
(2)加入10mL钼酸铵溶液,混匀后置于电热板上煮沸5min。
(3)取出冷却后,加入1mL抗坏血酸溶液,混匀后置于电热板上煮沸,直至溶液呈无色。
(4)取出冷却后,用去离子水定容至50mL,用分光光度计在690nm波长下测定吸光度。
五、实验结果与分析1. 土壤有机碳含量实验结果显示,土壤有机碳含量为12.34g/kg。
土壤碳的测定

土壤碳的测定实验目的:掌握测定土壤碳的方法,学会用图解表示的方法对试验结果进行分析。
实验原理:有机质在一定条件下会分解成简单无机物,根据此特性可采用凯氏定氮法测定土壤中碳的含量。
1实验准备实验材料和用具实验所需要的材料有:烧杯、酒精灯、称量瓶、量筒、蒸馏水,托盘天平、玻璃棒、镊子、酒精灯等;测定土壤中碳的工具有:容量瓶、酒精灯、滴管、 pH试纸、燃烧匙、铁架台、量筒、秒表等。
实验仪器见课本P82。
2实验步骤一、营养液的配制取草木灰适量(约500g),加水至1000ml,溶解后加入0.1mol/L 的硫酸亚铁溶液,即成营养液。
二、测定pH1.加入试剂将待测定的土样与营养液充分混合,在搅拌下徐徐注入容量瓶中,至刻度线处,此时土样与溶液之间应有大气泡。
然后,小心地用玻璃棒沿刻度线向上滴入一滴0.1mol/L的酸性高锰酸钾溶液,边滴边用玻璃棒搅拌,使药品全部被吸收,最后加入蒸馏水至刻度线。
加入试剂前先摇匀,且一定要将PH计水平,读出0.1,这个值即为pH。
实验过程一、配制营养液将草木灰放入烧杯中加水配成0.1mol/L 的营养液备用。
二、调pH二、调pH实验室配制试剂如下: K2HPO4+H2SO4== KCl+Ca(NO3)2,Na2HPO4+Ca(NO3)2== CaCl2+MgCl2, MgSO4+Ca(NO3)2==Ca(NO3)2+MgSO4, CaCl2+H2O==CaCl2+H2O, NaCl+2HCl==KCl+NaCl。
根据已知的缓冲溶液的配制: ClO3+H2O==Cl2+OH-,可以求得其pH值为6。
三、测定土壤中碳的含量1.测定土壤中碳的含量取容量瓶中的溶液,移入到一个带温度计的水槽中,直至温度稳定不再变化,便可测定了。
如果温度升高或降低,都会导致土壤溶液浓度发生改变,从而引起结果误差。
在测定时,不仅需要控制温度的变化,还必须控制相对湿度。
在进行比色法测定时,一定要先对溶液进行稀释,稀释的比例由所测土样的多少而定。
冻融对长白山森林土壤碳氮矿化的影响
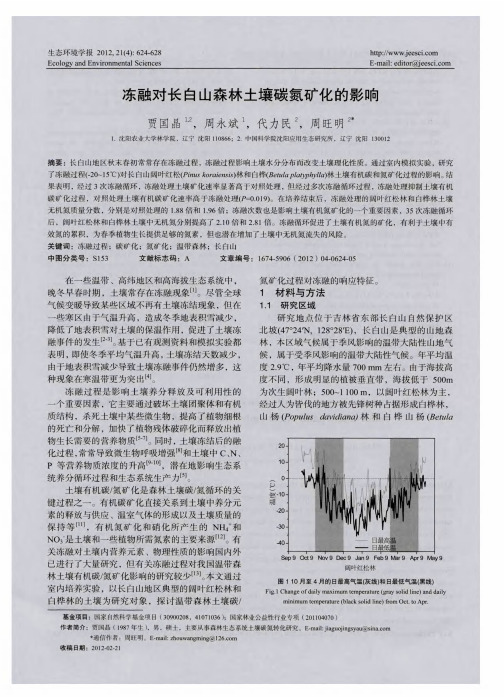
不同处理土壤 C 2 O 排放速率不同 , 在整个培养 期间 , 土壤有机碳矿化速率表现为随时间而降低( 图 2。对 照处 理 白桦 土壤 C 排 放速 率 在 8 O l.3 ) O2 . ~ 73 O m ・ -d 之间 ,冻融处理 白桦土壤 C 2 g 1 . O 排放速率 在 49- 46 ・g ・ . 1.0mgk ~d 间 ;对 照处理 阔 叶红松 7 之 土壤 C 2 O 排放 速率 在 42~ .7mgk~d 间 , .3 98 ・g ・ 之 冻 融处理 阔叶红松土壤 C O2排 放 速 率 在 3 9 8 0 . ~. 0 4 mgk ~d ・g ・ 之 间 ;两 种土 壤有 机碳 矿 化速 率差 异性 显著 (< . 1。整个 培养 期 间 ,对 照处理 土壤 有机 尸 0O ) O 碳矿化速率高于冻融处理 ,差异性显著( 0 ) . 。 09 1 但第 3 次冻融过程 , 冻融处理白桦有机碳矿化速率 比对 照处 理 高 6 .1 P 00 1, 59 %(< . )冻融 处理 阔 叶红松 0 土 壤 有 机 碳 矿 化 速 率 比 对 照 处 理 高 2 . %(= . 7, 融处 理显 著 提高 了土 壤有 机碳 72 P 00 ) 冻 7 4 矿化 速 率 。 22 冻 融对 土壤 碳矿 化量 的影 响 _ 在培养前期 ,由于土壤有机碳矿化速率较大 , 各处理 C 2 累积量变化较大 ,随着培养 时间延 O一 C 长, 除阔叶红松土壤外 , 其他土壤 C 2 O一 C累积量变 化较小( 3。经过 3 培养 ,阔叶红松林 土壤对 图 ) 5d 照处 理 C 2C累积量 为(9 .8 1. ) ・g ,冻 O. 2 7  ̄ 41 mgk ~ 5 2 融处理 C . O2 C累积量 为 (3 .5土 .8 2 51 45 )mgk - ・g ,对 照处理累积量显著高于冻融处理 < .1;白桦林 PO ) O 土 壤 对 照 处 理 C 2 累 积 量 为 (7.0 57) O一 C 5 80士 . 7 mgk ~,冻 融 处 理 C 一 累积 量 为 (2 . 2 . ) ‘g O2 C 4 53 87 3 2 mg g ・ ~,对 照 处 理 累 积 量 显 著 高 于 冻 融 处 理 k (l .0) 尸 00 1;方差 分析 表 明 ,白桦林 土 壤有 机碳 矿化 < 累 积 量 显 著 高 于 阔 叶红 松 林 土 壤 有 机 碳 矿 化 累 积 量 < . 1。 00 ) 0 23 冻 融对 土壤 氮矿 化 的影 响 . 图 4 不 同处 理培养 后 土壤 中无 机氮 的 累积量 是 变化 。经过 3 5d培养 后 ,阔叶红 松林 土壤 冻 融处理 和 对 照 处 理 的无 机 氮 质 量 分 数 分 别 为 (00+ . ) 5 . 20 5 5 mgk 和 (6 1 1 7 mgk ~ g 2 .  ̄ . ) ’g ,冻融 处理 土壤 无 机 6 3 氮质 量 分数是 对 照处 理 1 8倍 ; . 8 白桦 林土 壤 冻融处 理 和对 照处 理 的无 机氮 质量 分数 分别 为 (67+ .5 5 .2 6 ) 2 mgk 和 (8 9 06) g ,冻融 处理 土壤 无 机 ‘g 2 . + .6 mgk ~ 9 氮质 量分 数是 对 照处 理 1 6 ; 差分 析表 明 , . 倍 方 9 冻 融过程显著影n  ̄壤有机氮矿化过程(l . 1 在 C j 尸 0 0) <0 。 冻融 处理 条 件下 ,土壤 中无 机氮 累积 量 随着 冻融 次 数 的增 加 呈增 加 趋势 ,经 过 3 次冻 融 ,阔 叶红松 5
土壤中全氮的测定

土壤中全氮的测定4.1.2.2 土壤全氮测定—半微量开氏法4.1.2.2.1 方法原理样品在加速剂的参与下,用浓硫酸消煮时,各种含氮有机化合物,经过复杂的高温分解反应,转化为氧化为硝态氮后,再用还原铁粉使全部硝态氮还原,转化成铵态氮氨与硫酸结合成硫酸铵。
碱化后蒸馏出来的氨用硼酸吸收,以标准酸溶液滴定,求出土壤全氮含量(不包括全部硝态氮)包括硝态和亚硝态氮的全氮测定,在样品消煮前,需先用高锰酸钾将样品中的亚硝态氮。
在高温下硫酸是一种强氧化剂,能氧化有机化合物中的碳,生成CO2,从而分解有机质。
2H2SO4+C→H2O+2SO2↑+CO2↑高温样品中的含氮有机化合物,如蛋白质在浓H2SO4的作用下,水解成为氨基酸,氨基酸又在H2SO4的脱氨作用下,还原成氨,氨与硫酸结合成为硫酸铵留在溶液中。
Se的催化过程如下:2H2SO4+Se→H2SeO3+2SO2↑+H2O(亚硒酸)2SeO3→SeO2+H2OSeO2+C→Se+CO2由于Se的催化效能高,一般常量法Se粉用量不超过0.1-0.2g,如用量过多则将引起氮的损失。
(NH4) 2SO4 + H2SeO3→(NH4) 2SeO3 + H2SO43(NH4) 2SeO3→2NH3 + 3Se + 9H2O + 2N2↑以Se作催化剂的消煮液,也不能用于氮磷联合测定。
硒是一种有毒元素,在消化过程中,放出H2Se,H2Se的毒性较H2S更大,易引起人中毒,所以实验室要有良好的通风设备,方可使用这种催化剂。
当土壤中有机质分解完毕,碳质被氧化后,消煮液则呈现清澈的蓝绿色即“清亮”,因此硫酸铜不仅起催化作用,也起指示作用。
同时应该注意开氏法刚刚清亮并不表示所有的氮均已转化为铵,有机杂环态氮还未完全转化为铵态氮,因此消煮液清亮后仍需消煮一段时间,这个过程叫“后煮”。
消化液中硫酸铵加碱蒸馏,使氨逸出,以硼酸吸收之,然后用标准酸液滴定之。
蒸馏过程的反应:(NH4) 2SO4+ 2NaOH→Na2SO4 + 2NH3 +2H2ONH3 +H2O→NH4OHNH4OH+H3BO3→NH4·H2BO3+H2O滴定过程的反应:2NH4·H2BO3+H2SO4→(NH4) 2SO4+2H3BO34.1.2.2.2 主要仪器消煮炉;半微量定氮蒸馏装置(图4-2);半微量滴定 1.蒸馏瓶 2.冷凝器 3.承受瓶 4.分水筒5.蒸汽发生器6.加碱小漏斗7、8、9.螺旋夹子10.开关4.1.2.2.3 试剂(1)硫酸:ρ=1.84g·mL-1,化学纯;(2)10 mol·L-1NaOH溶液:称取工业用固体NaOH 420g,于硬质玻璃烧杯中,加蒸馏水400mL溶解,不断搅拌,以防止烧杯底角固结,冷却后倒入塑料试剂瓶,加塞,防止吸收空气中的CO2,放置几天待Na2CO3沉降后,将清液虹吸入盛有约160mL无CO2的水中,并以去CO2的蒸馏水定容1L加盖橡皮塞。
土壤氮测定实验报告

一、实验目的1. 学习掌握土壤氮含量的测定原理和方法;2. 了解土壤全氮、速效氮的测定原理及操作步骤;3. 培养实验操作技能,提高实验数据的准确性和可靠性。
二、实验原理1. 土壤全氮测定:采用凯氏定氮法,将土壤样品中的有机氮转化为无机氮,然后测定无机氮的含量,从而推算出土壤全氮含量。
2. 土壤速效氮测定:采用碱解扩散法,将土壤样品中的速效氮转化为氨气,然后用硼酸吸收,最后用标准酸滴定,计算出土壤速效氮含量。
三、实验材料与仪器1. 实验材料:土壤样品、浓硫酸、氢氧化钠、硼酸、标准酸、锌-硫酸亚铁粉剂等。
2. 实验仪器:电子天平、凯氏烧瓶、凯氏蒸馏器、扩散皿、滴定管、移液管、容量瓶、烘箱等。
四、实验步骤1. 土壤全氮测定(1)称取2.00 g土壤样品于凯氏烧瓶中。
(2)加入5.0 mL浓硫酸,置于电热板上加热,直至溶液呈蓝色。
(3)继续加热,直至溶液变为透明。
(4)冷却后,加入10 mL蒸馏水,继续加热至沸腾。
(5)将溶液转移至凯氏蒸馏器中,加入10 mL氢氧化钠溶液。
(6)连接冷凝管,加热蒸馏,直至吸收液呈碱性。
(7)用标准酸滴定,计算出土壤全氮含量。
2. 土壤速效氮测定(1)称取2.00 g土壤样品于扩散皿中。
(2)加入3 mL硼酸溶液,滴加1滴定氮混合指示剂。
(3)将扩散皿置于40℃烘箱中,加热24小时。
(4)取出扩散皿,用标准酸滴定,计算出土壤速效氮含量。
五、实验结果与分析1. 土壤全氮含量:通过实验,测得土壤全氮含量为2.3 mg/g。
2. 土壤速效氮含量:通过实验,测得土壤速效氮含量为1.5 mg/g。
3. 结果分析:土壤全氮含量反映了土壤中氮素的总储备,而土壤速效氮含量则反映了土壤中可供植物吸收利用的氮素。
本实验结果显示,该土壤样品中氮素储备较为丰富,但可供植物吸收利用的氮素相对较少,可能与土壤质地、有机质含量等因素有关。
六、实验总结1. 本实验成功掌握了土壤氮含量的测定原理和方法,了解了土壤全氮、速效氮的测定步骤。
土壤微生物量碳测定方法

土壤微生物量碳测定方法土壤微生物量碳(Soil microbial biomass carbon,SMBC)是指活体微生物在土壤中的碳含量,是土壤微生物数量的指标之一,反映了土壤中微生物活动的水平。
测定土壤微生物量碳的方法有多种,包括气体护膜冻融法、氟化钠浸提法、氯仿蒸腾法等。
下面将介绍常用的土壤微生物量碳测定方法。
一、气体护膜冻融法(gas chromatographic method with chloroform fumigation extraction,CFE-GC)气体护膜冻融法是一种基于微生物细胞内的总碳测定方法。
具体操作步骤如下:1.取一定量土壤样品,将样本均匀摊在烟斗滤纸上;2.用氯仿制备一定浓度的蒸腾液;3.将氯仿蒸腾液均匀喷洒在土壤样品表面;4.将喷洒后的土样与烟斗滤纸一起放入长颈瓶中,用橡皮塞封口;5.将长颈瓶放入液态氮中,使其迅速冷冻;6. 将冷冻后的样品研磨至细腻,并与含量已知的标准样一起送入气相色谱仪(gas chromatograph,GC)进行测定;7.根据标准曲线计算土壤微生物量碳含量。
二、氟化钠浸提法(NaF method)氟化钠浸提法是一种利用氟离子抑制土壤中微生物的酶活性,从而测定微生物量碳含量的方法。
具体操作步骤如下:1.取一定量土壤样品,加入含有一定浓度的氟化钠溶液;2.震荡混合一段时间,使土壤中的微生物碳与氟离子进行结合;3.将样品置于高速离心机中离心,分离土壤颗粒与液相;4.将上清液倒入瓶中,加入酸进行中和;5.酸中和后,将溶液进行干燥,得到土壤微生物量碳的干重;6.根据干重计算土壤中微生物量碳的含量。
三、氯仿蒸腾法(chloroform fumigation-extraction,CFE)氯仿蒸腾法是一种基于微生物细胞内溶质增加量来计算微生物量碳的方法。
具体操作步骤如下:1.取一定量土壤样品,将样本均匀摊在烟斗滤纸上;2.用氯仿蒸腾液均匀喷洒在土壤样品表面;3.将氯仿蒸腾的土样与烟斗滤纸一起放入密封瓶中,使其在常温下进行蒸发;4.将蒸发后的土样与烟斗滤纸一起进行提取,得到提取液;5.对提取液进行化学分析,测定其中的微生物量碳含量;6.根据微生物量碳的含量计算土壤中微生物量碳的含量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
冻融土壤中碳、氮矿化测定实验方案实验小组成员:黄永华,崔胜彬,钟昌建,倪祥银,兰彩霞实验还需物品及试剂:保鲜膜,保鲜袋,BaCl2,乙醇95%,酚二磺酸一、实验指标:1、单种土壤不同冻融循环次数后碳、氮矿化,酶活性以及微生物数量的测定2、不同水分梯度土壤冻融循环后碳、氮矿化,酶活性以及微生物数量的测定3、不同植被覆盖下的土壤冻融循环后碳、氮矿化的测定二、实验方案:(内江全年温度范围-3℃—41℃)土样的采集:选取内江周边有代表性的川东南紫土丘陵区土壤,在选定的样地内取样,取样时采用“S”取样法随机采集表层0~20cm土壤,5点组成一个土样。
将采集的8-10Kg土样除去动植物残体,编号后装入塑料保鲜袋,运回实验室分成两份。
土样的处理:将采回后的土壤在4℃培养待用冻融循环及对照的设置:将土样在-2℃下培养24h,然后取出再在5℃培养24h,以此为一次冻融循环,即每冻融一次为48h。
冻融十次为一个冻融周期,共计480h(20d)。
对照组则在5℃的条件下一直培养直到实验组完成冻融循环。
一>土壤碳、氮矿化的测定方法:(1)碳矿化的测定方法:取冻融处理后的土样设置3个平行样,每个样300g,用去CO2蒸馏水调节土壤湿度至其最大持水量的60%,装在2000ml塑料瓶中。
在塑料瓶中放入装有20mlNaOH溶液(浓度0.1mol/L)的小烧杯,用以吸收有机碳矿化释放的CO2。
将塑料瓶密封后放入恒温箱中在5℃培养7天后取出NaOH溶液并用1mol/L BaCl2 2mL,再加入酚酞指示剂2滴,用浓度为0.05mol/L的HCl滴定至红色消失,同时做对照试验。
计算出CO2的释放量。
结果计算:CO2(ml/kg)={[(V0- V)* c *0.022*(22.4/44)*1000]*2*1000}/m 式中:V0 ——对照组滴定时消耗的标准盐酸体积,mlV ——实验组滴定时消耗的标准盐酸体积,mlc ——标准盐酸的浓度,mol/Lm ——土样的质量,g试剂:0.1mol/L NaOH,1mol/L BaCl2,酚酞,0.05mol/L HCl,(2)氮矿化的测定:1)铵态氮的测定方法:(蒸馏滴定法)土样10.0g加入2mol/L KCl 50ml震荡30分钟,过滤。
取滤液25ml放入半微量定氮蒸馏器中。
将盛有2%硼酸液5ml的三角瓶放于冷凝管下方。
加入12%MgO 10ml于蒸馏室中,蒸馏。
10分钟后,三角瓶中的液体用0.005mol/L H2SO4 滴定至紫红色为止,同时做对照试验。
试剂:2mol/L KCl,2%硼酸,12%MgO,0.005mol/L H2SO42)硝态氮的测定方法:(酚二磺酸比色法)土样25.0g加入0.25g CaSO4.2H2O和100ml H2O,震荡10分钟,静置5分钟后过滤。
取滤液40ml于蒸发皿中,加CaCO30.05g水浴蒸干,冷却,加入2ml酚二磺酸试剂,静置10分钟加水20ml,待蒸干物完全溶解并冷却以后缓缓加入NH4OH,将溶液转入100ml容量瓶中定容,在分光光度计上波长420nm处比色。
试剂:0.25gGaSO4.2H2O,0.05g CaCO3,2ml酚二磺酸,NH4OH3)土壤水分的测定和梯度的调整及其碳氮矿化的测定方法:1)鲜土水分的测定:取新鲜土样M g,用烘箱烘干(3-5h)其重量变为m g,则鲜土含水量W=(M-m)/m*100﹪;2)鲜土水分梯度的调整:取相同质量(M=1000g)的新鲜土样五份,标记为a、b、c、d、e分别做如下处理土样鲜重g 加蒸馏水ml 干重g 含水量%((M+x)/m)a M x1 mab M x2 mbc M x3 mcd M x4 mde M x5 me3)碳矿化的测定法:再对调节水分后的五份土样进行冻融循环一个周期,作为对照的未做水分调节土样在5℃培养20d。
处理后的土样设置3个平行样,每个样300g,装在2000ml塑料瓶中。
在塑料瓶中放入装有20mlNaOH溶液(浓度0.1mol/L)的小烧杯,用以吸收有机碳矿化释放的CO2。
将塑料瓶密封后放入恒温箱中在5℃培养7天后取出NaOH溶液并用1mol/L BaCl2 2mL,再加入酚酞指示剂2滴,用浓度为0.05mol/L的HCl 滴定至红色消失,同时做对照试验。
计算出CO2的释放量(计算方法同上)。
4)氮矿化的测定方法:碳矿化测定后做(方法同上)4)单种土壤不同冻融循环次数后碳、氮矿化的测定1)碳矿化:a、对照组:置于5℃下培养20d。
b、实验组:土样分别在冻融循环第一、第三、第五、第七、第十次后取一次样,每次取3塑料瓶,分别在每个塑料瓶中加入300g处理后的土样。
在塑料瓶中放入装有20mlNaOH溶液(浓度0.1mol/L)的小烧杯,用以吸收有机碳矿化释放的CO2。
将塑料瓶密封后放入恒温箱中在5℃培养7天后取出NaOH溶液并用1mol/L BaCl2 2mL,再加入酚酞指示剂2滴,用浓度为0.05mol/L的HCl滴定至红色消失,同时做对照试验。
计算出CO2的释放量(方法同上)。
2)氮矿化:碳矿化测定后做(方法同上)二>酶活性的测定:1)脲酶的测定:取5.00g测定碳矿化后的风干土样,置于50ml三角瓶中,加1ml甲苯。
15min后加10ml 10%尿素液和20mlpH6.7柠檬酸缓冲液。
摇匀,37℃恒温培养24h。
过滤后取3ml滤液注入50ml容量瓶中,在578nm处比色。
试剂:甲苯,10%尿素液,pH6.7柠檬酸缓冲液2)蔗糖酶的测定:取5.00g测定碳矿化后的风干土样,置于50ml三角瓶中,注入15ml 18%蔗糖溶液,5mlpH5.5磷酸缓冲液和0.2ml(5滴)甲苯。
摇匀,37℃恒温培养24h。
迅速过滤,取1ml滤液注入50ml容量瓶,加3ml3,5-二硝基水杨酸,沸腾水浴5min,自来水流冷却3min。
溶液生成3-氨基-5-硝基水杨酸而呈橙黄色,用蒸馏水定容至50ml。
在508nm处比色。
试剂:18%蔗糖溶液,pH5.5磷酸缓冲液,甲苯,3,5-二硝基水杨酸三>微生物数量的测定:菌液经过多次10倍稀释后,一定量菌液中可以极少或无菌,选择5个连续的稀释度,每个稀释度取3个样重复接种于适宜的培养基中,培养后分别记载得出的数量指标就可以计算出单位土壤的菌体数目。
1)细菌的测定:采用稀释平板法,用牛肉膏蛋白胨培养基接种培养其10¯3、10¯4、10¯5、10¯6、10¯7五个梯度的土菌液,每个梯度取3个平行样。
在30℃下培养5d,记录菌落数目。
测定单位土样菌液数目2)真菌的测定:采用稀释平板法,用土豆液琼脂培养基接种培养其10¯3、10¯4、10¯5、10¯6、10¯7五个梯度的土菌液,每个梯度取3个平行样。
在30℃下培养5d,记录菌落数目。
测定单位土样菌液数目3)放线菌的测定:采用稀释平板法,用改良高氏一号培养基,临用前每500ml加入3%的重铬酸钾1ml以抑制细菌和真菌的生长。
培养其10¯3、10¯4、10¯5、10¯6、10¯7五个梯度的土菌液,每个梯度取3个平行样。
在30℃下培养7d,记录菌落数目。
测定单位土样菌液数目4)反硝化细菌的测定:5)氨氧化细菌的测定:操作步骤:称取10.00g土样和上述90ml灭过菌的1mmol/L磷酸盐的缓冲液一起加入到匀浆机中,搅拌30s或60s,然后转移至高压灭过菌的150ml三角瓶中,摇匀后吸取10ml该稀释度为10-1的土壤悬浮液至另一只预先灭过菌的装有90ml磷酸盐缓冲液的三角瓶中,摇匀,得到稀释度为10-2的土壤悬浮液。
继续稀释至10-5.如果硝化细菌的数量较高,应进一步稀释至10-6、10-7、或10-8.取5个连续的稀释度,将其分别接种到装有4ml灭菌的液体培养基的试管中。
每管接种土壤悬浮液1ml,每个稀释度重复接种5官,即每个土样共制备25个试管,同时设置不接种的对照。
试管在20C—30C避光培养(培养箱中或合适的室温条件)21d后,取试管进行初步观察,PH指示剂颜色由蓝绿色变为黄色表明发生了氨的氧化。
为了确认NO2-生成,可用比色盘进行定性测试。
在无菌条件下从试管中吸取0.1ml液体,放入比色盘凹槽中,先加入1滴重氮试剂,然后加入1滴耦合剂,如果有品红至红色出现,表明有NO2-存在,并与未接种的对照比较。
继续培养至少6周,每周检查一次颜色变化,直到有NO2-反应的试管数量在最后两周不再增加为止。
培养结束时,要对颜色较浅或没有颜色的试管进行NO2-的定性检测。
对没有NO2-反应的试管,要用二苯胺试剂检测NO3-的含量,因为亚硝酸氧化微生物有可能已将NO2-全部氧化为NO3-。
硝酸盐检测的灵敏度不如亚硝酸盐高。
内江气候条件:内江市位于天府之国的东南部,座落在美丽富饶的沱江之滨。
东连重庆,西接成都,南通自贡、宜宾、泸州,北到遂宁、南充,是川东重镇、四川省规划建设的8个大城市之一。
地理位置东经104°15′--105°26′,北纬29°11′--30°2′。
内江历史悠久。
内江是开发较早的巴蜀腹心城市,东汉建县,曾称汉安、中江,隋文帝时改称内江,至今已有2000多年的历史。
1950年设内江专区,1985年改建省辖内江市。
1998年,经国务院批准,内江行政区划进行再次调整至今。
由于历史上盛产蔗糖,制糖业发达,素有"甜城"之称。
内江文化底蕴深厚。
内江素有"大千故里"、"文化之乡"的美誉,是川中文化发达地区之一。
自古以来,人文荟萃、才俊辈出,孔子之师苌弘、西汉辞赋家王褒、东汉教育家董均、宋代理学家陈抟、国画大师张大千、新闻巨子范长江、被孙中山授予四大将军之一的喻培伦大将军等都是内江彪炳史册的杰出代表。
内江市属亚热带湿润季风气候。
受盆地和本地自然环境的影响,具有气候温和、降雨量丰富、光热充足、无霜期长的特点。
内江冬季不冷,一月份的平均气温为6℃--8℃,极端最低温度-3℃;夏季也不太热,七月份的平均气温为26℃--28℃,但也曾出现过41℃的极端最高气温。
因此全年气温在-3℃—41℃之间,无霜期达330天。
灾害性天气以旱为主,旱涝常交替出现;春夏秋冬,低温、风、暴雨时有发生,绵雨显著,同时,夏旱伏旱的现象也时有发生。
年降雨量在1000毫米左右,多分布在夏季,约占全年雨量的60%,高温期与多雨季基本一致,春季约占17%,冬季仅占4%。
