有机化学课件第九章乙酰乙酸乙酯和丙二酸二乙酯
丙二酸二乙酯资料共33页

谢谢你的阅读
❖ 知识就是财富 ❖ 丰富你的人生
71、既然我已经踏上这条道路,那么,任何东西都不应妨碍我沿着这条路走下去。——康德 72、家庭成为快乐的种子在外也不致成为障碍物但在旅行之际却是夜间的伴侣。——西塞罗 73、坚持志伟大的事业需要始终不渝的精神。——伏尔泰 74、路漫漫其修道远,吾将上下而求索。——屈原 75、内外相应,言行相称。——韩非
丙二酸二乙酯资料
51、没有哪个社会可以制订一部永远 适用的 宪法, 甚至一 条永远 适用的 法律。 ——杰 斐逊 52、法律源于人的自卫本能。——英 格索尔
53、人们通常会发现,法律就是这样 一种的 网,触 犯法律 的人, 小的可 以穿网 而过, 大的可 以破网 而出, 只有中 等的才 会坠入 网中。 ——申 斯通 54、法律就是法律它是一座雄伟的大 夏,庇 护着我 们大家 ;它的 每一块 砖石都 垒在另 一块砖 石上。 ——高 尔斯华 绥 55、今天的法律未必明天仍是法律。 ——罗·伯顿
二羰基化合物详解演示文稿

CH3CH2 C OC2H5
草酸酯,无α-H
C H3 C H C O O C2H5 CO
- CO
C O O C2H5
CH3
(1)C2H5ONa
(2)
+
H
CH3CH
COOC2H5 COOC2H5
第22页,共53页。
④ 分子内的酯缩合反应 ——Dieckmann反应
C O O C 2H5
CH2CH2COOC2H5
烃基化反应;
(2)碳负离子与羰基化合物的反应,即羰基化合物和β-二羰 基化合物的缩合反应。当与酰卤或酸酐作用时可得酰基化产
物;
(3)碳负离子与α,β-不饱和羰基化合物的共轭加成(或
1,4-加成)。
第12页,共53页。
三、丙二酸二乙酯的合成及应用 1、丙二酸二乙酯的制法 2、丙二酸二乙酯在有机合成上的应用
四、乙酰乙酸乙酯的合成及应用
1、乙酰乙酸乙酯的合成——Claisen酯缩合反应
2、乙酰乙酸乙酯的性质
① 成酮分解 ② 成酸分解
OO CH3CCH2COC2H5
3、乙酰乙酸乙酯在合成上的应用
① 制备甲基酮
② 制备二元酮
第18页,共53页。
四、乙酰乙酸乙酯的合成及应用
1、乙酰乙酸乙酯的合成 ——Claisen酯缩合反应
O CH3C CH
O COC2H5
-
+
Na
O
O
RX CH3C CH COC2H5
一烃基乙酰乙酸乙酯
成酮
O
O
CH3C CH CO C2H5
5N % aO H
成酮分解
RO
+ + CH3C CH2 R
丙二酸二乙酯

O O O + CO2 H CH3C CHCOONa CH3C CHCOOH △ CH3C CH2CH2CH3 CH2CH3 CH2CH3
合成环状甲基酮 例三:合成
O CH C CH3
O O O O + 2NaNH2 CH3C CH2 C OC2H5 [CH3C C C OC2H5]2 Na
CH3 CH3CH2 CHCOOH
O O O O NaOC2H5 [H5C2O C CH C OC2H5 ] -Na+ H5C2O C CH2 C OC2H5
CH3CH2Br NaOC2H5 CH3CH2CH(COOC2H5)2 CH3CH2[C(COOC2H5)2]-Na+ △
CH3Br
CH3CH2 C(COOC2H5)2 CH3
O O CH3C-CH2-C-OC2H5 O CH3-C
H CH
O C-OC2H5
酮式
烯醇式
由分子内的原子或基团连接的位置 不同而产生的异构——互变异构
14.1.1 酸和碱对酮–烯醇平衡的影响 酸催化的酮–烯醇互变异构:
H O R C H C R' + H:B H
快
O H C R'
H
慢
O H C R' + H:B
Claisen 酯缩合反应机理:
O C2H5O-+CH3C OC2H5 O CH2 C OC2H5+CH3CH2OH O O CH3 C CH2 C OC2H5 OC2H5 O O CH3C OC2H5+CH2 C OC2H5
δ+
C2H5O-
O O O O C2H5ONa + CH3C CH C OC2H5] Na [ CH3C CH2 C OC2H5
有机化学二羰基化合物
碳氧双键处于共轭体系,发生了电子的离域,使体
系能量降低而趋于稳定。
:OH
H3C C CH
O C OC2H5
2024/7/26
4
第5页/共53页
影响烯醇式含量的其它因素:
① 活泼亚甲基上连有吸电子基团,烯醇式含 量↑,连有供电子基团,烯醇式含量↓。
O
O
O
O
H3C
C
CH
C OC2H5 > H3C
C
CH2
2+
Hg
+
H
OH CH CH2
O CH3C H
β-二羰基化合物的烯醇式结构稳定性:乙酰乙酸乙酯
实验事实:
① 能与NaHSO3、HCN等发生加成反应; ② 能与羟胺、苯肼反应,生成肟、苯腙等; ③ 能被还原成β-羟基酸酯; ④ 经水解、酸化后,可以脱羧生成丙酮。
O
O
H3C C CH2 C OC2H5
有羰基
O CH3C CH
O COC2H5
Na+
Br(CH2)4Br
O CH3C
C2H5ONa
COCH3
成酮分解
COOC2H5
O CH COC2H5 CH2(CH2)3Br
O
CCH3
2024/7/26
28
第29页/共53页
② 制二酮
2024/7/26
制β-二酮(1,3-二酮)
O CH3C CH
O COC2H5
第11页/共53页
三、丙二酸二乙酯的合成及应用
1、丙二酸二乙酯的制法 2、丙二酸二乙酯在有机合成上的应用
① 制备烃基取代乙酸 ② 制备二元羧酸
2024/7/26
乙酰乙酸乙酯及在合成上的应用ppt课件

该反应可由酰胺制备有机腈类化合物。
N + H2O
•脱羰反应-霍夫曼(Hofmann)降级反应
RCONH2 + Br2 + 4NaOH H2O
RNH2 + 2NaBr + Na2CO3 + 2H2O
该反应可由酰胺制备少一个碳原子的伯胺,产率较高.
•与亚硝酸的反应
RCONH2 + HNO2
RCOOH + N2 + H2O
该反应可用于酰胺的鉴别和定性分析。
•酰胺的水解
HCl
加热
RCOOH + NH4Cl
RCONH2 + H2O
NaOH RCOONa + NH3
加热
在有机合成上,氨基的酰化在水解,多用于氨基的保护。
•酰胺的酸碱性
酰胺是近中性化合物,这是由于氮原子上的未共用电子对与碳基 上的π电子形成共轭体系,电子云向羰基方向移动,降低了氮原 子上的电子云密度,使其结合质子的能力减弱。
目标要求
1.掌握几种类型的羧酸衍生物结构及命名 2.了解羧酸衍生物的物理性质及光谱性质 3.掌握羧酸衍生物的化学性质 4.掌握羧酸衍生物的亲核取代反应机理及反应活性 5.了解羧酸衍生物的相互转换 6.掌握乙酰乙酸乙酯、丙二酸二乙酯的性质及在合成中的应用 7.学会设计有机合成路线
一、羧酸衍生物结构和命名
'
R
反应可逆
-羰基酯
= =
= =
=
=
=
反应机理:
C2H5O
αH O
+ CH2 C OC2H5
O
C2H5OH
CH2 C OC2H5
O
O
O
乙酰乙酸乙酯 PPT

( 1 )金属钠遇水即燃烧爆炸,故使用时应严格防止钠 接触水或皮肤。钠的称量和切片要快,以免氧化或被空气 中的水气侵蚀。多余的钠片应及时放入装有烃溶剂(通常 二甲苯)的瓶中。
( 2 )摇钠为本实验关键步骤,因为钠珠的大小决定着 反应的快慢。钠珠越细越好,应呈小米状细粒。否则,应 重新熔融再摇。摇钠时应用干抹布包住瓶颈,快速而有力 地来回振摇,往往最初的数下有力振摇即达到要求。切勿 对着人摇,也勿靠近实验桌摇,以防意外。
H
H C COOC2H5 + OC2H5
H
(Ⅰ)
(Ⅱ)
H C COOC2H5 + HOC2H5 H
(Ⅲ)
H C C OC2H5 HO
2 、加成
O C2H 5 H CH 3 C O+ C CO O C2H 5
H
O C2H 5 H CH 3 C C CO O C2H 5
OH (Ⅳ )
3 、脱醇
-H O C 2 H 5 C H 3 C CC O O C 2 H 5 OH
2 、缩合和酸化。稍经放置钠珠沉于瓶底,将 二甲苯倾倒到二甲苯回收瓶中。迅速向瓶中加入 5.5mL 乙酸乙酯 ,装上冷凝管,并在其顶端装 一氯化钙干燥管。反应开始有氢气泡逸出。如反 应很慢时,可稍加温热。待激烈的反应过后,置 反应瓶于石棉网上小火加热,保持微沸状态,直 至所有金属钠全部作用完为止。此时生成的乙酰 乙酸乙酯钠盐为桔红色透明溶液(有时析出黄白 色沉淀)。待反应物稍冷后,在摇荡下加入 50% 的醋酸溶液,直到反应液呈弱酸性(约需3mL), 此时,所有的固体物质均已溶解。
性的。反应为平衡可逆反应,乙酸乙酯过量有利 于平衡向生成( III )的方向移动。
乙酰乙酸乙酯及丙二酸乙酯在有机合成的应用

生命科学与理学院乙酰乙酸乙酯、丙二酸乙酯在有机合成的应用专业:生物科学班级:2012级1班学号:姓名:张昆乙酰乙酸乙酯一、乙酰乙酸乙酯的性质物理性质无色液体,熔点<-45℃,沸点181℃,相对密度(20/4℃),折射率,蒸气压(20℃)。
与乙醇、乙醚、苯等一般有机溶剂混溶,易溶于水。
具有愉快的水果香气。
化学性质互变异构一般的乙酰乙酸乙酯是酮式和烯醇式互变异构体和平衡混合物,酮式占93%,烯醇式占7%。
酮式乙酰乙酸乙酯沸点为41℃(),不能与溴起加成反应,也不使三氯化铁显色,但能与酮试剂作用。
烯醇式乙酰乙酸乙酯沸点为33℃(),不与酮试剂作用,但能使三氯化铁显色,烯醇分子内发生氢键缔合,形成螯合环。
因此,烯醇式都以单分子形态存在,沸点较低。
乙酰乙酸乙酯的分解反应乙酰乙酸乙酯在不同条件下不同反应条件下发生不同类型的分解反应,生产酮或酸。
乙酰乙酸乙酯在稀碱作用下,发生酯的水解反应,受热后脱羧成酮,这种分解称为酮式分解。
+ CO 2在浓碱条件下,OH -浓度高,除了和酯作用外,还可以使乙酰乙酸乙酯中α-与β-碳原子之间的键断裂,生成两分子羧酸,这种分解称为酸式分解。
取代反应乙酰乙酸乙酯亚甲基上的氢受到相邻两个吸电子基的影响,变得非常活泼,1)5%NaOH2)H1)浓NaOH2)H +在金属钠或乙醇钠的作用下可以被烷基或酰基取代。
选择适当的烷基化试剂或酰基化试剂与乙酰乙酸乙酯反应,然后酮式分解或酸式分解就可以得到不同结构的酮或酸。
二、乙酰乙酸乙酯的合成乙酰乙酸乙酯(俗名三乙)具有典型的β-酮酸酯结构,可用于多种合成反应,是一种重要的有机及药用合成的中间体。
在医药上用于合成氨基吡啉、维生素B 等,还广泛用于配制草莓、苹果、杏、樱桃、桃等水果型和酒型(朗姆、威士忌等)香精。
在农药生产上用于合成有机磷杀虫剂蝇毒磷的中间体α-氯代乙酰乙酸乙酯、嘧啶氧磷的中间体,杀菌剂恶霉灵等,也是杀菌剂新品种嘧菌环胺、氟嘧菌胺、呋吡菌胺及植物生长调节剂杀雄啉的中间体。
第十一章丙二酸二乙酯和乙酰乙酸乙酯

二、丙二酸二乙酯的性质
丙二酸二乙酯是具有香味的无色液味, 熔点 -50℃,沸点 198.8℃。不溶于水,溶于乙 醇、乙醚等有机溶剂。丙二酸二乙酯是合成取 代乙酸和其他羧酸常用的试剂,在有机合成中 具有广泛用途。
三、 丙二酸二乙酯在有机合成的应用
丙二酸二乙酯的上述性质在有机合成上广泛用 于合成各种类型的羧酸(一取代乙酸,二取代乙酸, 环烷基甲酸,二元羧酸等)。 具有活泼亚甲基的化合物容易在碱性条件下形 成稳定的碳负离子,所以它们还可以和羰基发生一 系列亲核加成。 例如:由丙二酸二乙酯合成2-乙基-3-苯基丙酸
C H 2
例2:合成
引 CH 3 O CH 要 分 两 次 引 入 , 先 引 入 3 CH CH CH CH=CH 3C 2 2 C H C H = C H 再 引 入 2 2 原
O
O
CH3CCH2C 原 引
说明:乙酰乙酸乙酯合成法主要用其酮式分解 制取酮,酸式分解制酸很少用,制酸一般用丙二酸 二乙酯合成法。
第十一章丙二酸二乙酯和乙酰乙酸乙酯丙二酸二乙酯丙二酸单乙酯钾盐乙酰氨基丙二酸二乙酯2氟丙二酸二乙酯丙二酸单乙酯溴代丙二酸二乙酯甲基丙二酸二乙酯氨基丙二酸二乙酯丙二酸二乙酯结构式
第十一章 丙二酸二乙酯和乙酰 乙酸乙酯
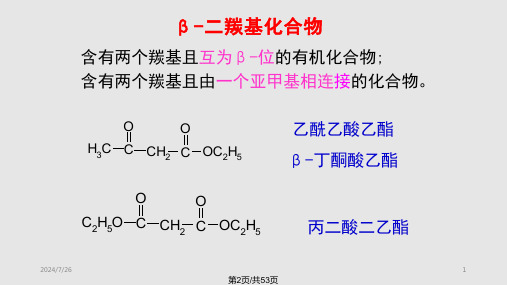
丙二酸二乙酯和乙酰乙酸乙酯是分子 中含有两个羰基,且两个羰基相隔一个亚 甲基的化合物,称为β二羰基化合物。
OO
乙酰乙酸乙酯又称β丁酮酸乙酯,简称三乙。 是无色透明具有果香味的液体,沸点180℃,微溶于 水,易溶于乙醇、乙醚等大多数有机溶剂中。
二、乙酰乙酸乙酯的性质
(1) 特性
①乙酰乙酸乙酯的互变异构现象
O O O H O C H C H C O C H 3C 2 5 C H C H O C H 3C 2C 2 5
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
O O
O O
-OH(稀)
水解
CH3C-CH2-COC2H5 CH3C-CH2-COH
O CH3C-CH3
-CO2
(一)乙酰乙酸乙酯的酮式分解和酸式分解
1、乙酰乙酸乙酯的酮式分解
乙酰乙酸乙酯在稀碱作用下,首先水解生 成乙酰乙酸,后者在加热条件下,脱羧生成酮。
2、乙酰乙酸乙酯的酸式分解 乙酰乙酸乙酯与浓碱共热,则在α-和β-碳原子间
CH3CH2OC CHCOCH2CH3 0.1%
O
O
OH CH3C
O
CH3CCH2CCH3 24%
CH CCH3 76%
三、乙酰乙酸乙酯在有机合成中的应用 (一)乙酰乙酸乙酯的酮式分解和酸式分解
1、乙酰乙酸乙酯的酮式分解 它与稀的NaOH溶 液发生水解反应,酸化生成乙酰乙酸,后者加热 则脱羧生成丙酮—称为乙酰乙酸乙酯的酮式分解。
酮 -H活泼
常用丙酮或其他甲基酮和酯缩合来合成 -二酮。 注意:与羟醛缩合反应不同(稀碱条件下,生成 ,-不饱和醛)。P163
CH3COCH2COOC2H5+C2H5ONa== CH3COCNaHCOOC2H5+C2H5OH CH3COCNaHCOOC2H5+CH3COOH== CH3COCH2COOC2H5+C2H5ONa
一般情况下,α-C上含H的酯,在乙醇钠 或其它碱性Cat.(如氨基钠)存在下, 都能进行克莱森酯缩合反应。具有α-H的 相同的酯,及一种含α-H,另一种不含αH的两种不同的酯反应时,具有制备意 义。例如下页:
O O EtOHC-OC 2H5 + H-CH2CCH 3
H2O
O O HC-CH2CCH 3
NaH
H2O
O O C-CH2CCH 3
合成练习题: 解:
O
O CH3
(1) C2H5ONa C2H5OH (2) C2H5Br
(1)以乙酰乙酸乙酯为原料合成 CH3CCHCH2CH3
O CH3CCHCOOEt C 2 H5
3
CH3CCH2COOEt
(1) C2H5ONa C2H5OH (2) CH3Br
O CH
(1) 稀 NaOH (2)H 3O+ (3)
CH3CCCOOEt C2 H5
T.M
苯甲酰基
合成练习题:
加热生成酯基
成环
二、乙酰乙酸乙酯的互变异构现象
它能与 HCN、亚硫酸氢钠发生加成反应,也 能与羟胺苯肼加成生成肟和苯腙,能被还原 成 β - 羟基酸酯。这些反应说明它具有酮式结 构。 酮式结构:CH3COCH2COOC2H5 但它还具有如下的特殊性质:它能使溴的乙 醇溶液退色,说明分子中具有C=C;与Na反 应放出 H ,生成钠的衍生物;与乙酰氯作用 生成酯。这些反应均说明分子中有 -OH 存在。 烯醇式结构:CH3C=CHCOOC2H5 OH
第九章 乙酰乙酸乙酯 和丙二酸二乙酯 第一节 乙酰乙酸乙酯 第二节 丙二酸二乙酯
西安石油化工技工学校 化工类教研室 李志藩
第一节 乙酰乙酸乙酯 一、克莱森酯缩合反应 二、乙酰乙酸乙酯的互变异构现象 三、乙酰乙酸乙酯在有机合成中的 应用 乙酰乙酸乙酯是具有愉快气味的 无色液体,沸点180℃,微溶于水, 易溶于乙醇、乙醚等有机溶剂。
一、克莱森酯缩合反应 ——乙酰乙酸乙酯的合成
1、乙酰乙酸乙酯的合成
两分子乙酸乙酯在乙醇钠作用下发生缩合, 脱去一分子乙醇:
轮胎切条机
乙酰乙酸乙酯 75%
2、克莱森酯缩合反应历程——亲核加成——消除
凡有 -H 原子的酯,在乙醇钠或其他碱性催化剂 (如氨基钠)存在下,都能进行克莱森酯缩合反应。
3、酮与酯在乙醇钠作用下的反应 类似克莱森酯缩合反应:
CH3C=CHCOOC2H5 OH
当与酮式试剂反应时,由于平衡移动,显示出为 酮式结构,在与溴水反应时为烯醇式结构。 烯醇式结构本来是不稳定的,但是在β -二羰基化合物 中是比较稳定的。用共轭效应和分子内氢键解释。 乙酰乙酸乙酯在不同溶剂中烯醇式和酮式比例不同, 溶剂极性越小,烯醇式比例越高。质子形极性溶剂易 于与酮式形成分子间氢键,酮式比例高;非极性溶剂 易于烯醇式分子内氢键的形成,所以在环己烷类非极 性溶剂中烯醇式比例高。 某些混合物的烯醇式含量SeeP162表9-1所示。
乙酰乙酸乙酯中的烯醇式较稳定,因为氢键会 形成稳定的六元环。见下页:
酮式-烯醇式互变异构式 (具有酮和烯醇的双重反应性)
O CH3CCH2COOC2H5 92.5% O H 7.5% O CH3 O C H O C OC2H5O
O
OH
O
CH3CH2OCCH2COCH2CH3 99.9%
高职高专有机化学各章
第一章 有机化合物概述 第二章 脂肪烃和脂环烃 第三章 芳香烃 第四章 对映异构体 第五章 卤代烃 第六章 醇、酚和醚 第七章 醛和酮 第八章 羧酸及其衍生物 第九章 乙酰乙酸乙酯和 丙二酸二乙酯 第十章 含氮有机化合物 第十一章 含杂原子有机化 合物 第十二章 生命有机化学 第十三章 有机化合物的波 谱知识简介 第十四章 有机化合物的分 离与纯化技术
一、克莱森酯缩合反应 具有α-H的乙酸乙酯在乙醇钠作用下,发生 缩合反应,脱去一分子乙醇,生成乙酰乙 酸乙酯的反应称为克莱森酯缩合反应。又 名β-丁酮酸酯,3-丁酮酸酯,简称三乙。它 也可以看做是乙酸乙酯的乙酰化产物。 乙酰乙酸乙酯的合成反应见下页: 克莱森酯缩合反应的总结果是一个碳负离子 的酰基化,生成了一个β-二羰基化合物, 因此这是一个合成β-二羰基化合物的方法。
乙酰乙酸乙酯实际上是酮式和烯醇式的混合物, 酮式和烯醇式混合物是互变异构体,两者处 于平衡状态,互相转换。在室温时,液态乙 酰乙酸乙酯是由约 7.5% 的烯醇式和 92.5% 的 酮式异构体组成的平衡混合物。这种能够互 相转变的两种异构体之间存在的动态平衡现 象就称为互变异构现象。
CH3COCH2COOC2H5
OO O EtOC2H5O-C-C-OC2H5 + H-CH2CCH3
O OO H2O C2H5O-C-C-CH2CCH 3
O O -CO C2H5O-C-CH2CCH3
O O C2H5O-C-OC2H5 + H-CH 2CCH3
NaH
H2O
O O C2H5O-C-CH2CCH3
O O C-OC2H5 + H-CH 2CCH3
