有机化学II16重氮化合物和偶氮化合物
(完整word版)重氮化合物和偶氮化合物

重氮化合物和偶氮化合物重氮化合物和偶氮化合物都含有—N=N —原子团。
该官能团的一端与烃基相连,另一端与非碳原子相连或不与其他的原子或原子团相连的化合物,称为重氮化合物。
如:氯化重氮苯 硫酸重氮苯(重氮苯盐酸盐) (重氮苯硫酸盐)-N=N-官能团两端都分别与烃基相连的化合物,称为偶氮化合物。
如:CH 3—N=N-CH 3 偶氮甲烷偶氮苯对羟基偶氮苯对二甲氨基偶氮苯一、偶氮化合物的制备在低温和强酸性水溶液中,芳香族伯胺和亚硝酸作用,生成重氮化合物,此反应称为重氮化反应。
如:+ NaNO 2 + HCl + H 2O + NaCl 重氮化反应的历程可能是铵盐先与亚硝酸作用,生成N —亚硝基化合物,然后发生重排,最后再脱水生成重氮盐。
重氮盐是重要的有机机合成中间体,生成的重氮盐不必分离,可直接在原溶液中进行下一步合成反应。
二、重氮盐的性质和应用重氮盐具有盐的性质,易溶于水,不溶于有机溶剂,其在水溶液中医药能解离为重氮盐正离子和负离子X —,因此水溶液能导电。
重氮盐的化学性质很活泼,可发生许多反应,主要有如下两类:一类是放氮反应,一类是不放氮的偶联反应。
N N Cl N N HSO 4N N N OH N N N (CH 3)2N NH 2N N Cl Cl NH 3N N Cl H H O N OH Cl H N N Cl N 0-5℃亚硝酸 重排-H 20(一)取代反应这是重氮基被其它原子或原子团取代,并在同时放出氮气的一类反应.重氮盐在亚铜盐的催化下,重氮基被氯、溴、氰基取代,分别生成氯苯,溴苯和苯腈,同时放出氮气,此反应称为桑德迈尔反应.将重氮盐加热,重氮基被羟基取代,生成苯酚并放出氮气。
例如:重氮硫酸盐和次磷酸或碱性甲醛水溶液作用,重氮基被氢原子取代并放出氮气.例如:+ N 2↑ (二)偶联反应重氮盐在低温下与苯酚或芳胺作用,生成有色的偶氮化合物的反应,称为偶联反应。
例如 :++偶联反应一般发生在对位,如对位已有基团占据,也可发生在邻位。
有机化学课件 16重氮化合物和偶氮化合物

• 由于中间体双游离基的碳碳单键能够旋转,所以最后 生成物有顺、反两种异构体:
• 碳烯与炔烃、环烯烃或苯的加成反应: 例1: H
例2:
例3:
(2)插入反应 • 单线态碳烯还可以插入C—H键之间,发生插入反应:
例如:丙烷与重氮甲烷在光照下作用:
• 单线态碳烯的插入反应无选择性,基本上是按统 计比例进行的。三线态卡宾的插入反应有选择性, 按C—H键反应性:3°> 2°> 1°= 7:2:1.
• 伽特曼反应——用铜粉作催化剂,产率低。 注意卤素一致
例如:
•希曼反应——(芳香族氟化物的制备) 必须将氟硼 酸加到重氮盐溶液中,使生成重氮盐氟硼酸沉淀,经 分离并干燥后再小心加热,即逐渐分解而得相应的芳 香族氟化物:
• 近来报导用重氮氟磷酸盐代替重氮氟硼酸盐,产率高:
(4)被氰基取代
例如:
• 氰基可以水解成羧酸,所以可以通过重氮盐在芳环 上引入羧基:
• 重氮盐中的重氮基可以被羟基、氢、卤素、氰基等 原子或基团取代,在反应中有氮气放出。 (1)被羟基取代 ——将重氮盐的酸性水溶液加热, 即发生水解,放出氮气,并有酚生成: 生成酚
• 在有机合成上常通过生成重氮盐的途径而使氨基转 变成羟基,由此来合成一些不能由芳磺酸盐碱熔而制 得的酚类. 例1:
溴会在碱熔时水解
N2 Cl
注意对应的酚、 胺的制备
•重氮盐与b-萘胺偶 合时,反应在1位上进 行 ,如 1 位 被 占 据 , 则 不发生反应.
• 反应介质的pH值对同时具有氨基或酚羟基的化合物 进行偶氮化合物和偶氮染料
• 偶氮化合物用适当的还原剂(SnCl2+HCl 或Na2S2O4)还原 成氢化偶氮化合物,继续还原则氮氮键断裂生成芳胺.
第十六章 重氮化合物和偶氮化合物
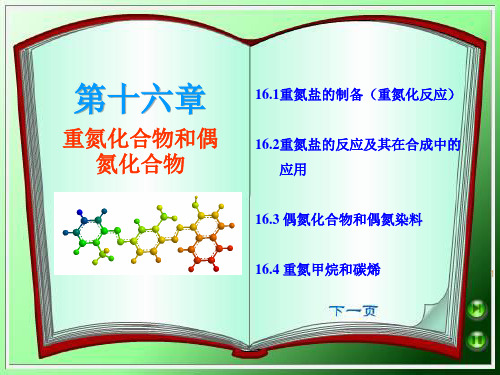
CH3COONa 0-5 C
。
NaO3S
N=N
N(CH3)2
甲基橙 (酸红碱黄,变色范围pH3.1-4.4)
能产生颜色的有机物一般都含有生色基和助色基。 能产生颜色的有机物一般都含有生色基和助色基。
27
生色基一般含有共轭体系, 生色基一般含有共轭体系,如:
11
例如:
从 OH
Br 溴会在碱熔时水解
NO2
NO2
Br2/Fe Fe+HCl
NH2 Br OH Br
解:
混酸
50 C
。
N2+ HSO4HNO2+过量H2SO4 0-5 C
。
H2O
Br
Br
12
例如: 由苯制取间硝基苯酚。 例如 由苯制取间硝基苯酚。
部分还原
13
、-Cl、- 、-I) ⑶重氮基被卤素取代 (X=-F、- 、- 、- - 、- 、-Br、-
近来报导用重氮氟磷酸盐代替重氮氟硼酸盐,产率高 近来报导用重氮氟磷酸盐代替重氮氟硼酸盐,产率高: 重氮氟磷酸盐代替重氮氟硼酸盐
16
例: 解: CH3
CH3 由
CH3 F
CH3
混酸
CH3 + NO2
CH3
Fe+HCl (CH3CO)2O
CH3 NHCOCH3
HNO2+过量H 2SO4 0-5 C
NO2
偶氮染料———苏丹红 苏丹红 偶氮染料
30
苏丹红,学名苏丹,分为Ⅰ 苏丹红,学名苏丹,分为Ⅰ、Ⅱ、Ⅲ、Ⅳ号,是一类合 成型偶氮染料, 主要用于溶剂、 成型偶氮染料 主要用于溶剂、油、蜡、汽油增色以及鞋和 地板等的增光。 地板等的增光。 在苏丹红事件中,包括30家企业的 家企业的88个食品样品先后被 在苏丹红事件中,包括 家企业的 个食品样品先后被 检出含有苏丹红Ⅰ 检出含有苏丹红Ⅰ号。中国检验检疫科学院食品安全研究所 副所长储晓刚表示,送检的几份(鸭蛋)样品里苏丹红Ⅳ 副所长储晓刚表示,送检的几份(鸭蛋)样品里苏丹红Ⅳ号 含量最高达到0.137mg/kg。国际癌症研究机构将苏丹 mg/kg。国际癌症研究机构将苏丹 含量最高达到 mg/kg。 号列为三类致癌物。 红Ⅳ号列为三类致癌物。
第十六章 重氮化合物和偶氮化合物

讨论: 讨论:
① 在强酸性介质(40%~50%硫酸)中进行, 以免偶联生成 在强酸性介质(40% 50%硫酸)中进行, ② 用硫酸盐而不用盐酸盐, 以免生成氯苯。 用硫酸盐而不用盐酸盐, 以免生成氯苯。 ③ 利用该反应可制备用其它方法难以得到的酚。 利用该反应可制备用其它方法难以得到的酚。
OH
N N OH
N2+Cl-
SnCl2, HCl or Na2SO3
NHNH2 HCl
苯肼盐 酸盐
OH-
NHNH2
苯肼
N2+Cl-
Zn, HCl
NH2 + NH3
(2) 偶合反应
定义: 重氮盐正离子可以作为亲电试剂与酚, 定义: 重氮盐正离子可以作为亲电试剂与酚, 芳胺等活泼的芳香 化合物进行芳环上的亲电取代 生成偶氮化合物, 化合物进行芳环上的亲电取代, 生成偶氮化合物, 这类反 亲电取代, 应称为偶联反应。 应称为偶联反应。
③ HNO2不能过量, 否则亚硝酸有氧化性, 促使重氮盐分解。 不能过量, 否则亚硝酸有氧化性, 促使重氮盐分解。
☆ 可用淀粉-KI试纸检验过量的HNO2;用尿素除去过量的HNO2。 可用淀粉-KI试纸检验过量的 试纸检验过量的HNO 用尿素除去过量的HNO
芳香族重氮化合物的结构: 芳香族重氮化合物的结构: [ArN+≡N]X- 或 ArN2+XN :
?
Br
NO2
HNO3 H2SO4 Br2,Fe 140℃ ℃
NO2
Fe + HCl
NH2
NaNO2,H2SO4 0~5℃ ℃
N2HSO4
H2O,H+
OH
Br
Br
Br
大学有机化学16 重氮化合物和偶氮化合物

¹¹±¹¹¹ ¹ á
NH2
+ HNO2 + H2SO4
¹¹H 2SO4 0-5 C
¹
N+
N HSO4- + 2H2O
¹¹±¹¹¹ ¹ò á
反应条件: A. 低温; B. 强酸; C. HNO2不过量。
二、重氮盐的性质及其在合成上的应用
(1)放出氮的反应——重氮基被取代的反应 (2)保留氮的反应——还原反应和偶合反应
KCN
CN
+ N2 COOH
Gattermann反 应 H 2O / H +
由于氰基可通过水解而成羧基,所以在有机合成 上可利用此反应在苯环上引入羧基。如:
由于在苯环上直接引入氰基是不可能的,所以 由重氮盐引入氰基是非常重要的。氰基可转化为羧 基、氨甲基等基团。如: CH CH
3 3
CH 2 NH
+ KHSO4
- Cl取 代
N 2C l
+ CuCl
HCl
Cl
+ N2
+ HCl
- B r取 代
N 2B r
+ Cu B r
HBr
Br
+ N2
+ H Br
S an dm eyer反 应
桑德迈尔反应
用途:制备一系列芳香族卤化物。
芳香族氟化物用此法制备- 希曼反应
(4)被氰基取代
N 2C l + CuCN
(一)取代反应 (放氮反应)
重氮基被-OH,-H,-X,-CN等取代,同时放出氮气
(1)被羟基取代
将重氮盐的酸性水溶液加热,即发生水解,放出氮气, 生成酚:
水解成酚时必须是强酸性条件,否则酚与重氮盐发生偶联,
16重氮化合物和偶氮化合物PPT精品文档39页
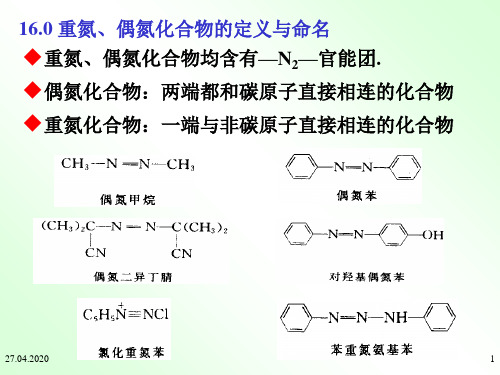
Br
Br
NO 2
NO 2
NO2
CN
COOH
COOH
CuCN Br
Br H3O+ Br
Br Fe
NaNO2 H3PO2
Br
Br
KCN
HCl
HCl
H2O
?
NO2
NO2
27.04.2020
9
③ 被卤原子取代 ◆ 碘代——重氮盐和KI加热。
N2Cl + KI
I + N2 + KCl
◆碘代反应属于SN1历程,这是苯环上引入I的有效方法.但此 法不能用来引进氯原子或溴原子。 Cl-,Br-亲核能力弱, 要引入Cl-、Br-常需要亚铜盐作为催化剂:
N2Cl +
OH-(pH=8) OH
低温
重氮组分 偶联组分
N=N
OH
NN
pH=5~6 N(CH3)2
N=N
N(CH3)2
◆重氮正离子进攻酚羟基或二甲氨基的对位,如对位已有其它
基团,则在其邻位发生偶合:
27.04.2020
15
OH
N2Cl +
•
弱碱 低温
OH N=N
CH3
CH3
◆重氮盐和酚的偶合一般在(pH=8-10)弱碱性溶液中进行;碱性
16.0 重氮、偶氮化合物的定义与命名
◆重氮、偶氮化合物均含有—N2—官能团. ◆偶氮化合物:两端都和碳原子直接相连的化合物
◆重氮化合物:一端与非碳原子直接相连的化合物
27.04.2020
1
16.1 重氮化反应—芳香族重氮盐的制备
◆伯芳胺在低温及强酸(主要是盐酸或硫酸)水溶液 中,与亚硝酸作用生成重氮盐的反应,称为重氮化反应:
有机化学-第十六章 重氮化合物与偶氮化合物10-文档资料
和偶氮化合物
-N2的两端都和基团碳原子直接相连的化合物为偶氮化合物。
如果-N2一端与非碳原子直接相连的化合物称为重氮化合物。
偶氮甲烷
偶氮苯
氯化重氮苯
苯重氮氨基苯
§16.1 重氮盐的制备—重氮化反应
伯胺在冷的强酸存在下与亚硝酸作用生成重氮化合物:
伯芳胺与酸比例为 1:2.5至1:3,以保持溶液的酸度,避免产生偶 联副反应。
Hale Waihona Puke 重氮化反应的终点可用KI-淀粉试纸测定
§16.2 重氮盐的性质及其在合成中的应用
其反应主要分为两大类: 留氮反应;放氮反应 一、放氮反应—重氮基被取代的反应 1、被羟基所取代 (P.393) : 将重氮盐的酸性水溶液加热,即发生水解,放出氮气,并有酚生成
应用:
在合成中可用于制备各种酚化合物,如合成间溴苯酚:
偶氮染料
生色基
对位红
甲基橙
助色基
刚果红
2. 重氮盐的偶合反应 (P.396)
重氮盐与含有强给电子基的芳香胺或酚反应,生成偶氮化合物的反 应称为偶联反应。反应一般发生在对位,对位已占据时发生在邻位。 重氮盐与芳香叔胺的反应:
对—(N,N-二甲氨基)偶氮苯(黄色)
§16.3 偶氮化合物(P.399)
还原反应
可用来推断偶氮 化合物的结构
可用HPF6代 替
应用:
4、被氰基取代 (P.396)
桑德迈尔Sandmeyer反应 Gattermann反应
应用:在苯环上引入一个羧基:
二、保留氮的反应(P.396)
1、还原反应
重氮盐可被SnCl2、Sn/HCl、Zn/HAc、Na2SO3、 NaHSO3还 原为苯肼:
有机化学II-16重氮化合物和偶氮化合物
N
(I)
-OH、-NH2(NHR、NR2)都是很强的第一类定位基,
N
N
(II)
N+
在偶合反应中,极限结构(Ⅱ)作为亲电试剂,进攻芳环而 发生亲电取代反应:
N N
+
+
G -H+
N N H N N
G
G = OH, NH2,NHR,NR2
G
由于重氮正离子中氮原子上的正电荷可以离域到苯环 上,因此它是一个很弱的亲电试剂,只能与高度活化的苯 环才能发生偶合反应。 可以预料:
N N N
+
N
按共振论的观点,重氮正离子是下列极限共振结构的 共振杂化体:
N N N N
当苯环上连有强吸电子时,重氮正离子的稳定性将↑。
重氮化反应机理如下:
-H2O
HO
N O
H2O N O
N O
[N
O
O
N O]
亚硝酰正离子
Ar NH2
+
Ar
NH2 N
-H+
Ar
NH N O
互变异构
-H2O
H+
Ar
Ar N
OH
H+
OH2
+
NR2
H+
NR2 H
+
而在强碱介质中,重氮盐正离子与碱作用,可生成重 氮酸或其盐。
:
Ar N
+
N:
Ar N
N:
+
NaOH
Ar N
N OH
NaOH
Ar N
N O Na
+
重氮盐
重氮酸
重氮化合物和偶氮化合物的区别
偶氮化合物和重氮化合物的主要区别是:术语偶氮化合物是指存在N=N基团,而重氮化合物是指在有机化合物的末端存在偶氮基团。
在偶氮化合物中,N=N官能团出现在化合物的中间,其中官能团的两个末端与一些其它取代基相连,相反,在重氮化合物中,官能团出现在化合物的末端。
1、什么是偶氮化合物?
偶氮是指存在N=N官能团。
在有机化合物中,该官能团以RN=N-R'的形式出现,其中R和R'是烷基或芳基,偶氮这个名字来源于术语azote,它指的是氮的法语名称。
芳基偶氮化合物比烷基偶氮化合物相对稳定,它们通常以结晶形式存在。
烷基化合物含有与偶氮官能团相连的烷基,我们可以称为脂肪族偶氮化合物。
2、什么是重氮化合物?
重氮是指存在连接到有机化合物末端的两个氮原子。
这类化合物的一般结构式为2C=+=−。
简单的重氮化合物的一个例子是重氮甲烷,它具有连接到甲烷分子的偶氮官能团。
重氮化合物可以在环加成反应中充当1,3-偶极子,此外它们可以作为卡宾生产的前提,还可以在亲核加成反应中作为亲核试剂反应。
16重氮化合物和偶氮化合物
芳香族重氮盐的重氮基能与芳环共轭,在0~50~5℃℃比较稳定比较稳定。
•重氮正离子主要的共振结构重氮正离子主要的共振结构::1 1 重氮化合物重氮化合物N 2+ X -O 22活化活化、、定位作用活化能力的控制转换转换、、占位作用G I-OH-COOH-X 制备间位制备间位或或临位的苯衍生物G II芳香重氮盐在合成中的应用1.3.2 重氮盐的化学性质- 重氮盐的化学性质-还原 还原A. 用锌粉盐酸还原为苯胺B. 用SnCl2 / HCl等还原为苯肼1.3.3 重氮盐的化学性质-偶联反应 偶联反应: 偶联反应: 亲电取代反应定义 重氮盐正离子可以作为亲电试剂与 重氮盐正离子可以作为亲电试剂与酚 芳胺 重氮盐正离子可以作为亲电试剂与酚 酚、 芳胺等活泼的芳香化合物 等活泼的芳香化合物 重氮盐正离子可以作为亲电试剂与酚 、芳胺等活泼的芳香化合物 芳胺等活泼的芳香化合物进行芳环 进行 芳环 上的亲电取代 生成偶氮化合物 这类反应称为偶联反应 进行芳环 芳环上的亲电取代 上的亲电取代, ,生成偶氮化合物, 生成偶氮化合物, ,这类反应称为偶联反应。
这类反应称为偶联反应。
。
进行芳环上的亲电取代 芳环上的亲电取代, 上的亲电取代, 生成偶氮化合物, 这类反应称为偶联反应。
+ N N Cl- +Y Y = OH , NR2N NY•示例H3C N2Cl + NH2 H3C N N NH2H2N N2Cl + NH2H2N N N NH2思考题: 思考题:CH3 NH2H3CNH21.3.3 重氮盐的化学性质----偶联反应偶联反应主要在对位, 偶联反应主要在对位,对位被占领时在邻位发生。
对位被占领时在邻位发生。
OH NH2萘胺和萘酚 与重氮盐的 偶联反应的 位置OH (NH2) OH (NH2)SO3Na1.3.3 重氮盐的化学性质----偶联反应同时具有氨基和羟基的萘的衍生物与重氮盐进行偶联反 应时, pH值对反应位置选择很重要 值对反应位置选择很重要, 例如: 应时 ,pH 值对反应位置选择很重要 ,例如 :PH = 5~77NH2 OH2PH = 8~9HO3SH-酸SO3HpH=5~7 弱酸性, 弱酸性,在氨基的邻位发生 氨基的邻位发生; 的邻位发生; pH=8~9, pH=8~9,为弱碱性, 为弱碱性,酚以酚氧负离子存在, 酚以酚氧负离子存在,这个环 活泼, 羟基的邻位发生反应 活泼,在羟基的邻位发生反应2 重氮甲烷和碳烯(自学) 2.1 重氮甲烷 (CH2N2)— 黄色气体, 黄色气体,剧毒易爆炸。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碘化物的生成最容易,只需用KI与重氮盐一起共热
即可,且收率良好。
可以通过Schiemann反应将氟原子引入芳环,例 如:
N+2Cl-
N+2BF4-
HBF4 CH3 或NaBF4
CH3
1)过滤,干燥 2)
F
+ N2 + BF3
CH3
4) 被氰基取代
通过Sandmeyer或Gattermann反应,重氮基也可被氰
+
_ H+
OH2
OH
苯基正离子轨道图
+
如:
Cl
Cl
HO
Cl
Cl
分析:该目标分子的合成若用磺化碱融法的问题 在于有对碱敏感的基团-X。而采用重氮盐法效果很 好。
Cl
HNO3 Fe H2SO4 HCl Cl
Cl
NH2 NaNO2
Cl
H0~25SoOC4
H+ H2O
Cl OH
Cl
3) 被卤原子取代
在氯化亚铜的盐酸溶液作用下,芳香族重氮盐分 解,放出氮气,同时重氮基被氯原子取代。该反应 称Sandmeyer 反应。(若用溴化重氮盐和溴化亚铜, 则得到相应溴化物,用CuI或CuF无法进行此反应)
氮盐的水解反应是分步进行的:
N2+ N2
H2O
+
Cl
+
O H2
H+
OH
C l (副产物)
2.水解反应中生成的酚容易与末反应重氮盐发生 偶合反应,硫酸可以抑制该反应,并提高了水 解反应温度,使水解反应更彻底。
重氮盐的水解反应是典型的单分子亲核取代反 应(SN1),其反应历程如下:
N2+
+ + N2
+ + H2O
重氮化合物和偶氮化合物
定义: 两个烃基分别连在-N=N-基两端的化合物称为偶氮 化合物。通式为:R-N=N-R’,例如:
CH2=CHCH2 N=N CH2CH2CH3
烯丙基偶氮丙烷
(CH3)2C N N C(CH3)2
CN
CN
偶氮二异丁腈
NN
偶氮苯
NN
NHCH3
对甲氨基偶氮苯
如果 -N=N- 基只与一个烃基相连,而另一个基团 不是烃基,这样的化合物称为重氮化合物。
H3PO2 H2O
Br
Br
Br
CH3
再如: NH2 分析:(1) 先引入一个基团,但无论是先引入-
CH3(为邻、对位基)还是先引入-NO2都不行(不能进行酰 基化)。
(2) 考虑苯环上有两个取代基,成功引入第三个取代 基后再去掉一个基团。这里有两种情况:
NO2
NH2 CH3
NH2 CH3
NO2
HNO3 Fe H2SO4 HCl
CN
Ni
H2O,H+ CH3
NH2 (CH3CO)2O
NHCOCH3 CH3Br
AlBr3
NHCOCH3 CH3 +
NHCOCH3 CH3
HNO3 H2SO4
NHCOCH3 CH3 +
NO2
NHCOCH3 NO2 H3O+
CH3
NH2 CH3
NaNO2 HCl
NO2
H3PO2 H2O
CH3 NO2
Fe + HCl
CH3
NH2
2) 被羟基取代
基取代。
N+2HSO4- CuCN,KCN
CN
O2N
Cl
O2N
Cl
由于在苯环上直接引入氰基是不可能的,所以由重氮
盐引入氰基是非常重要的。氰基可转化为羧基、氨甲基等 基团。
这在有机合成上有重要意义,例如:
CH3
CH3
CH3
NaNO2,HCl
CuCN,KCN
0~5 oC
NH2
+N2Cl- CH3 H2
此反应在有机合成上有重要的用途。
如:
Br
Br
Br
分析:根据定位效应,解决这一问题的最好办法是首 先在环上引入一个强的邻、对位定位基,待完成引入溴原 子的任务后,再被H原子取代。
HNO3 H2SO4
NO2 Fe
HCl
NH2
NH2
3Br2 Br
Br
NaNO2 HCl
Br
0~5oC
N2+Cl-
Br
Br
Br
CH3
CH3
NH2 NaNO2,HBr
N+ 2 B r - C u ·粉,
Br
注意:制备溴化物时,可用硫酸代替氢溴酸进行重氮
化,但不宜用盐酸代替,否则将得到氯化物和溴化物的混 合物。
加热重氮盐的碘化钾溶液,可以得到相应的芳基碘。
NH2
N+2Cl-
INaNO2,HCl来自0~7oC
KI, 温热 74%~76%
加热芳香族重氮硫酸盐,即有氮气放出,同时生 成酚,故又称重氮盐的水解反应。
N+2HSO4- H2O,H+
OH + N2 + H2SO4
该法主要用来制备没有异构体的酚和用磺化碱熔等 其它方法难以得到的酚。
重氮盐制备酚时,常在硫酸中进行,主要因为:
1.若采用盐酸溶液,体系中的Cl-可以作为亲核试 剂与苯基正离子反应,生成副产物氯苯。
NN
+
NN
按共振论的观点,重氮正离子是下列极限共振结构的 共振杂化体:
NN
NN
当苯环上连有强吸电子时,重氮正离子的稳定性将↑。
重氮化反应机理如下:
HO N O
Ar NH2 + N O
H2O N
Ar
-H2O
O
NH2 N
[N O
N O]
亚硝酰正离子
O -H+
互变异构
Ar NH N O
亚硝基胺
-H2O
Ar N N OH2
其中重氮盐尤为重要。
N N NH
苯重氮氨基苯
+
N NCl
N N NH
CH3
苯重氮氨基对甲苯
+
N
NHSO-4
+
N
NBF4-
氯化重氮苯 α-萘基重氮硫酸盐 苯重氮氟硼酸盐 (苯重氮盐酸盐)
重氮盐的制备----重氮化反应
芳香族伯胺在低温(一般为0~5℃)和强酸溶液中 与亚硝酸钠作用,生成重氮盐的反应称为重氮化反应。
H3C
NH2 NaNO2,HCl H3C 0 oC
NH2
+_ N2Br
N2+Cl-
CuCl HCl
H3C
Cl
(70%~79%)
Br
Cl NaNO2,HBr
Cl CuBr
Cl
10 oC
HBr
(89%~95%)
用铜粉代替氯化亚铜或溴化亚铜,也可得到相应卤化
物,此反应称为Gattermann反应。
CH3
NH2+ NaNO2+HCl 0~5oC
N+2Cl-
NH2
OCH3+ NaNO2 + HCl 0oC
N+2ClOCH3
重氮盐具有盐的典型性质,绝大多数重氮盐易溶于水
而不溶于有机溶剂。芳香族重氮盐所以稳定,是因为其重 氮盐正离子中的C-N-N键呈线型结构,π 轨道与芳环的 π 轨道构成共轭体系的结果。
Ar
Ar N
NN
N
H+
OH
Ar N N
重氮盐的性质及其在合成上的应用
1 放出氮的反应 1) 被氢原子取代
ArN+2Cl- + H3PO2 + H2O
Ar_H + H3PO3 + N2 + HCl
ArN2+SO4- + C2H5OH
Ar_H + CH3CHO + N2 + H2SO4
这两种方法中,以次磷酸还原为好;而以乙醇还原产 率则不高,因往往有副产物Ar-OC2H5生成。
