免疫印迹(WB)实验操作具体步骤及详细说明
免疫印迹步骤
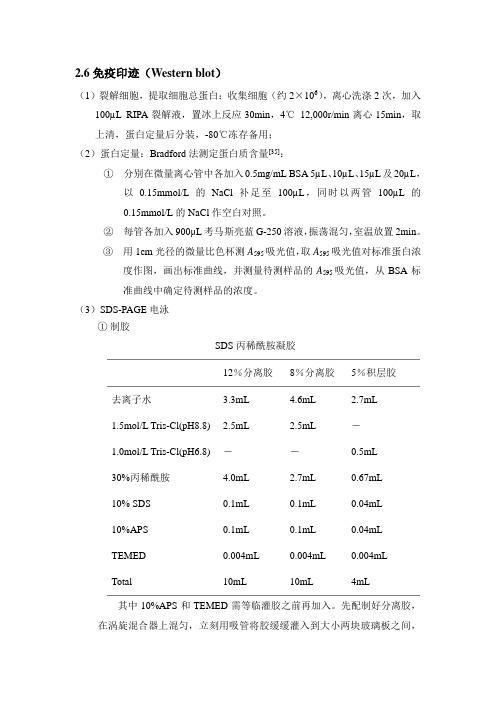
2.6 免疫印迹(Western blot)(1)裂解细胞,提取细胞总蛋白:收集细胞(约2×106),离心洗涤2次,加入100µL RIPA裂解液,置冰上反应30min,4℃12,000r/min离心15min,取上清,蛋白定量后分装,-80℃冻存备用;(2)蛋白定量:Bradford法测定蛋白质含量[35]:①分别在微量离心管中各加入0.5mg/mL BSA 5µL、10µL、15µL及20µL,以0.15mmol/L的NaCl补足至100µL,同时以两管100µL的0.15mmol/L的NaCl作空白对照。
②每管各加入900μL考马斯亮蓝G-250溶液,振荡混匀,室温放置2min。
③用1cm光径的微量比色杯测A595吸光值,取A595吸光值对标准蛋白浓度作图,画出标准曲线,并测量待测样品的A595吸光值,从BSA标准曲线中确定待测样品的浓度。
(3)SDS-PAGE电泳①制胶SDS丙稀酰胺凝胶12%分离胶8%分离胶5%积层胶去离子水 3.3mL 4.6mL 2.7mL1.5mol/L Tris-Cl(pH8.8)2.5mL 2.5mL -1.0mol/L Tris-Cl(pH6.8) --0.5mL30%丙稀酰胺 4.0mL 2.7mL 0.67mL10% SDS 0.1mL 0.1mL 0.04mL10%APS 0.1mL 0.1mL 0.04mLTEMED 0.004mL 0.004mL 0.004mLTotal 10mL 10mL 4mL其中10%APS和TEMED需等临灌胶之前再加入。
先配制好分离胶,在涡旋混合器上混匀,立刻用吸管将胶缓缓灌入到大小两块玻璃板之间,至胶的最上缘距玻璃板顶端3cm左右。
再用去离子水覆盖在分离胶的上层,封闭空气使胶易于凝固。
室温静置1h左右可看到去离子水和胶之间由于折射率不同而出现一条界限,说明胶已经凝好,可用注射器小心吸出上层的去离子水。
免疫印迹(WB)实验操作具体步骤及详细说明

免疫印迹(WB)实验操作具体步骤及详细说明免疫印迹(WB)实验操作具体步骤及详细说明一、试剂和溶液转印缓冲液:0.025M Tris base , 0.187 M 甘氨酸, 25%甲醇氨基黑溶液:0.1% 酸性黑10B 1×TBST:25mM Tris-HCl ( pH 8.0 ) , 0.2 M NaCl , 0.1%Tween 20 封闭液:TBST 配制的5%牛奶抗体稀释液:TBST 配制的5%牛奶显色系统:ECL 显色二、实验步骤1.电泳:将裂解液进行SDS-PAGE 电泳,80v,30 分钟,120v,90 分钟;2.转膜:PVDF 膜在甲醇中浸泡约30 秒左右,滤纸浸泡在转印缓冲液预湿,半干法转印到PVDF 膜上,10v,150 分钟;3.染色:氨基黑染色5 分钟,甲醇褪去背景色,观察条带;4.膜活化:将PVDF 膜置于甲醇活化1min,用纯水洗膜2 次后再用TBST 洗涤3 次;5.封闭:将膜条置于5%牛奶或2% BSA 中,室温混摇2h;6.一抗孵育:将待检抗体用3%牛奶或2% BSA 稀释到合适浓度(参照抗体说明书,根据客户预实验结果,稀释度上下浮动一个数量级都为正常),将膜放入对应的已稀释待检样品中,置4℃混摇孵育过夜;7.洗涤:取出膜放在TBST 中洗涤3×5min;8.二抗孵育:将膜取出放入稀释好的HRP 标记的二抗(参照二抗说明书进行稀释)中,室温混摇2h;9.洗涤:取出膜放在TBST 中洗涤3×5min;10.ECL 显色:将膜取出放入混匀的ECL 显色液中,孵育3min,将膜取出贴在有荧光角标的胶片上,迅速用保鲜膜包好;11.曝光:把底片放在暗盒中,根据荧光强度分别对X 光胶片作不同时间段的曝光,曝光结束后,将底片取出,1min 显影,30s 清洗,1min 定影,30s 清洗,晾干;12.结果分析:用扫描仪将曝光后的X 光胶片扫描,做后续结果分析。
免疫印迹(immunoblotting)

免疫印迹(immunoblotting)免疫印迹(immunoblotting)又称蛋白质印迹(Western blotting),是根据抗原抗体的特异性结合检测复杂样品中的某种蛋白的方法。
该法是在凝胶电泳和固相免疫测定技术基础上发展起来的一种新的免疫生化技术。
由于免疫印迹具有SDS-PAGE 的高分辨力和固相免疫测定的高特异性和敏感性,现已成为蛋白分析的一种常规技术。
免疫印迹常用于鉴定某种蛋白,并能对蛋白进行定性和半定量分析。
主要实验步骤如下:1.蛋白质抽提a.实验对象为组织样品,取适量(250~500mg)新鲜组织样品或正确保存的组织样品,加1ml含蛋白酶抑制剂的总蛋白抽提试剂(或核蛋白抽提试剂),匀浆后抽提总蛋白(或核蛋白)。
b.实验对象为细胞样品,每份样品取1×106~1×107细胞,PBS清洗细胞,去PBS加0.1ml~1ml含蛋白酶抑制剂的总蛋白抽提试剂(或核蛋白抽提试剂)抽提总蛋白(或核蛋白)。
2.蛋白质定量:按KCTMBCA蛋白质定量试剂盒操作说明操作,测定样品浓度。
3.变性聚丙烯酰胺不连续凝胶电泳(SDS-PAGE)将准备好的样品液和生物素标记的蛋白质分子量标准分别上样,标准加进第一个孔中,电泳分离蛋白。
4.蛋白质转移到硝酸纤维膜或PVDF膜按Bio-Rad蛋白转移装置说明组装滤纸凝胶纤维素夹层,30mA恒流条件下,4°C转移过夜。
5.膜的封闭和抗体孵育a.膜在5%BSA溶液中室温孵育1小时以封闭膜上的非特异结合。
b.封闭过的膜加入一级抗体室温孵育1.5小时,抗原抗体结合。
c.加入HRP标记的二级抗体以结合一级抗体及HRP标记的抗生物素抗体以结合分子量标准,室温孵育膜1小时。
加入HRP标记的GAPDH抗体可同时检测GAPDH含量。
6.结果检测:化学发光法检测,膜与化学发光底物孵育,经X胶片曝光显影。
图片扫描保存为电脑文件,并用ImageJ分析软件将图片上每个特异条带灰度值的数字化。
免疫印迹实验操作具体步骤及详细说明

免疫印迹实验操作具体步骤及详细说明免疫印迹(Western Blotting,简称WB)是一种常用的分子生物学技术,主要用于检测和鉴定蛋白质的存在以及其在不同样本中的表达水平。
下面将详细介绍WB实验的具体步骤。
1.细胞裂解和蛋白质提取:首先将待检测的组织样本或细胞样本通过离心将其收集,并添加适量的裂解缓冲液。
使用超声波或机械破碎手段将细胞打乱,使蛋白质溶解在裂解缓冲液中。
再通过离心去除细胞碎片和细胞核等。
2.蛋白质浓度测定:根据实验需要,采用BCA法、Lowry法或Bradford法等方法测定蛋白质浓度,以确定后续实验的载体中待加载的蛋白质量。
3.蛋白质电泳:将相同量的蛋白质样品加入SDS-凝胶槽中,进行电泳。
电泳时蛋白质在凝胶中向阴极迁移,分子量小的蛋白质迁移速度较快,分子量大的较慢。
电泳结束后,将凝胶转移到膜上。
4.膜上瞬时染色:在转移至膜上后,可以使用Ponceau S染色或其他瞬时染色方法,以确认蛋白质在膜上的存在和转移效果。
5.阻断:在膜上的蛋白质检测之前,需要对膜进行阻断处理,以防止非特异性结合。
常用的方法是在膜上加入牛血清蛋白或脱脂奶粉的溶液,进行阻断。
6.一抗反应:加入已稀释好的一抗抗体,与目标蛋白质特异性结合。
一抗的选择要根据待检测蛋白的特异性来确定。
7.清洗:一抗反应后,用TBST或PBS等缓冲液进行多次清洗,以去除未结合的一抗抗体。
8.二抗反应:9.清洗:二抗反应后,用TBST或PBS等缓冲液进行多次清洗,以去除未结合的二抗抗体。
10.显色和成像:使用显色剂(如ECL)使膜上的蛋白质发生化学发光反应,然后将膜放入X射线片中,进行曝光。
最后使用化学显影废片机或Gel Doc System等设备进行成像。
11.数据分析:使用专业的成像软件分析成像结果,计算蛋白质的相对表达水平,并与内参蛋白进行比较。
需要注意的是,在进行WB实验的过程中,要严格操作,避免污染和交叉反应的出现。
同时,应根据实验需求选择适当的试剂和抗体,并进行标记、保存和储存等操作。
蛋白质免疫印迹(Western Blot )实验步骤和原理及注意事项

蛋白质免疫印迹(Western Blot )实验步骤和原理及注意事项1.收集蛋白样品(Protein sample preparation)可以使用适当的裂解液。
收集完蛋白样品后,为确保每个蛋白样品的上样量一致,需要测定每个蛋白样品的蛋白浓度。
根据所使用的裂解液的不同,需要采用适当的蛋白浓度测定方法。
因为不同的蛋白浓度测定方法对于一些去垢剂和还原剂等的兼容性差别很大。
BCA法。
2. 电泳(Electrophoresis)(1) SDS-PAGE凝胶配制(2) 样品处理在收集的蛋白样品中加入适量浓缩的SDS-PAGE蛋白上样缓冲液。
例如2X或5X的SDS-PAGE蛋白上样缓冲液。
使用5X的SDS-PAGE蛋白上样缓冲液可以减小上样体积,在相同体积的上样孔内可以上样更多的蛋白样品。
100℃或沸水浴加热3-5分钟,以充分变性蛋白(根据蛋白分子的大小,煮沸时间可适当变化,一般不低于5min。
煮沸只是变性蛋白,而不是分解,一般加了抑制酶不会分解。
煮沸对于SDS-PAGE凝胶电泳是必须的,只有煮沸,才能消除蛋白质的立体二级结构,伸展为一维线性结构,所以一般来讲二聚体都会解体,才能完全按照分子量跑电泳,加的蛋白Marker才有指示分子量的意义。
蛋白样品变性后与SDS充分结合,SDS使每个氨基酸带相同的电荷,使整个蛋白呈线性结构. 抗体因为要是线性表位结合的,100度煮10min 后13000,离心5分钟,取上清电泳,因为沉淀会导致拖尾.也可以取上清到另一管,4度可以放一周备再次电泳)。
(3)电泳i.清洗玻璃板:一只手扣紧玻璃板,另一只手蘸点洗衣粉轻轻擦洗。
两面都擦洗过后用自来水冲,再用蒸馏水冲洗干净后立在筐里晾干。
ii.灌胶与上样(1)玻璃板对齐后放入夹中卡紧。
然后垂直卡在架子上准备灌胶。
(操作时要使两玻璃对齐,以免漏胶。
)(2)配10%分离胶,加入TEMED后立即摇匀即可灌胶。
灌胶时,可用10 ml枪吸取5 ml胶沿玻璃放出,待胶面升到绿带中间线高度时即可。
western blot 免疫印迹方法

Western blot一、S DS-聚丙烯凝胶电泳二、转膜1.准备好转膜用的物品:转膜夹、剪刀、镊子、纤维素膜、滤纸,盘子,盒子,玻璃棒,甲醇,转膜液(不加SDS,有气泡)2.将滤纸侵泡于盘中的转膜液,赶走气泡,将膜剪去一角做标记,侵泡于甲醇中,根据黑胶白膜原则叠好,保证无气泡后夹紧放入电泳槽中,黑对黑原则放入电泳槽,槽内放入冰袋,盖好电泳槽盖。
3.于冰上或者冰箱中低温转膜,恒流300mA,50min三、封闭(正面朝上)TBS洗5min配5%脱脂奶粉-TBS摇几分钟4℃过夜。
四、加一抗,倒去封闭液,用TBS冲洗一次,TBST 5min×3次(大概10ml),加入用2.5%脱脂奶粉-TBST稀释的一抗(1:10),室温摇2h五、加二抗:倒去一抗或回收(TBST,5mi n×3次)用2.5%脱脂奶粉-TBST按2000:1稀释二抗(鼠抗人IgE抗体),室温摇2h(有的已经与HRP结合的,如若没有,后面加HRP),TBST洗5mi n×3次,然后TBS洗5mi n×3。
六、化学发光,显影,定影(1)将A和B两种试剂在保鲜膜上等体积混合;1min后,将膜蛋白面朝下与此混合液充分接触;1min后,将膜移至另一保鲜膜上,去尽残液,包好,放入X-光片夹中。
(2)在暗室中,将1×显影液和定影液分别到入塑料盘中;在红灯下取出X-光片,用切纸刀剪裁适当大小(比膜的长和宽均需大1cm);打开X-光片夹,把X-光片放在膜上,一旦放上,便不能移动,关上X-光片夹,开始计时;根据信号的强弱适当调整曝光时间,一般为1min或5min,也可选择不同时间多次压片,以达最佳效果;曝光完成后,打开X-光片夹,取出X-光片,迅速浸入显影液中显影,待出现明显条带后,即刻终止显影。
显影时间一般为1~2min(20~25℃),温度过低时(低于16℃)需适当延长显影时间;显影结束后,马上把X-光片浸入定影液中,定影时间一般为5~10min,以胶片透明为止;用自来水冲去残留的定影液后,室温下晾干。
免疫印迹分析流程

免疫印迹分析流程
免疫印迹分析(Western Blot)是一种常用的蛋白质分析方法。
它的基本流程包括:
1. 样品制备:提取并定量蛋白质样本。
常用的方法有细胞裂解、组织匀浆等。
2. 电泳分离蛋白:使用SDS-PAGE凝胶电泳分离蛋白质。
根据分子量的不同,蛋白质会在凝胶上分离成不同的条带。
3. 转膜:将凝胶中的蛋白转移到NC膜或PVDF膜上。
4. 滤膜:使用5%脱脂奶粉或BSA在室温封闭1小时,以阻断膜胶的非特异性结合位点。
5. 一抗反应:加入特异性的一抗,孵育过夜。
一抗与目标蛋白特异性结合。
6. 二抗反应:洗涤后加入连接HRP的二抗,孵育1-2小时。
二抗与一抗结合。
7. ECL显色:滴加显影液,HRP催化发光底物氧化产生发光信号。
8. 凝胶成像:曝光、扫描和记录结果。
目标蛋白会出现特异性的条带。
9. 数据分析:通过条带的位置和强度分析目标蛋白的相对分子量和表达量。
以上是免疫印迹分析的基本流程。
根据实验目的,可以选择不同的样品制备方法、凝胶系统、转膜系统等,从而实现对蛋白质的分离、定量和功能分析。
WB实验操作流程

Western Blot即蛋白质印迹法(免疫印迹试验),是分子生物学、生物化学和免疫遗传学中常用的一种实验方法。
其基本原理是通过特异性抗体对凝胶电泳处理过的细胞或生物组织样品中的特定蛋白进行显影。
通过分析显影的位置和显影深度获得特定蛋白质在所分析的细胞或组织中表达情况的信息。
实验流程主要包括以下几个步骤:样品制备;SDS-PAGE凝胶电泳;转膜;封闭;免疫杂交;显影。
实验器材操作步骤样品制备准备进行western blot的样品可分为细胞、组织、免疫沉淀或亲和纯化后的蛋白等。
样品为蛋白溶液时不需要进行提取,而样品为细胞、组织或包埋组织等则需要根据样品的特性对其进行提取。
根据需求不同还可针对于细胞亚结构进行提取。
(1)以体外培养的贴壁细胞样本为例,对其进行总蛋白提取:1、倒掉培养液,并将瓶倒扣在吸水纸上使吸水纸吸干培养液(或将瓶直立放置一会儿使残余培养液流到瓶底然后再用移液器将其吸走)。
2、每瓶细胞加3ml 4℃预冷的PBS(0.01M pH7.2~7.3)。
平放轻轻摇动1min洗涤细胞,然后弃去洗液。
重复以上操作两次,共洗细胞三次以洗去培养液。
将PBS弃净后把培养瓶置于冰上。
3、按1ml裂解液加10 μl PMSF(100mM),摇匀置于冰上。
(PMSF要摇匀至无结晶时才可与裂解液混合。
)4、每瓶细胞加400 μl含PMSF的裂解液,于冰上裂解30min,为使细胞充分裂解培养瓶要经常来回摇动。
5、裂解完后,用干净的刮棒将细胞刮于培养瓶的一侧(动作要快),然后用枪将细胞碎片和裂解液移至1.5ml离心管中。
(整个操作尽量在冰上进行。
)6、于4℃下12000rpm离心5min。
(提前开离心机预冷)7、将离心后的上清分装转移倒0.5min的离心管中放于-20℃保存。
(2)以哺乳动物组织样本为例,对其进行总蛋白提取:1. 将100 mg 组织剪切成小块,加入适量的冰冷PBS 洗涤两次后,4℃,700×g(3000 rpm) 离心3 min,弃上清。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
免疫印迹(WB)实验操作具体步骤及详细说明
一、试剂和溶液
转印缓冲液:0.025M Tris base , 0.187 M 甘氨酸, 25%甲醇氨基黑溶液:0.1% 酸性黑10B 1×TBST:25mM Tris-HCl ( pH 8.0 ) , 0.2 M NaCl , 0.1%Tween 20 封闭液:TBST 配制的5%牛奶抗体稀释液:TBST 配制的5%牛奶显色系统:ECL 显色
二、实验步骤
1.电泳:将裂解液进行SDS-PAGE 电泳,80v,30 分钟,120v,90 分钟;
2.转膜:PVDF 膜在甲醇中浸泡约30 秒左右,滤纸浸泡在转印缓冲液预湿,
半干法转印到PVDF 膜上,10v,150 分钟;
3.染色:氨基黑染色5 分钟,甲醇褪去背景色,观察条带;
4.膜活化:将PVDF 膜置于甲醇活化1min,用纯水洗膜2 次后再用TBST 洗
涤3 次;
5.封闭:将膜条置于5%牛奶或2% BSA 中,室温混摇2h;
6.一抗孵育:将待检抗体用3%牛奶或2% BSA 稀释到合适浓度(参照抗体说
明书,根据客户预实验结果,稀释度上下浮动一个数量级都为正常),将膜放入对应的已稀释待检样品中,置4℃混摇孵育过夜;
7.洗涤:取出膜放在TBST 中洗涤3×5min;
8.二抗孵育:将膜取出放入稀释好的HRP 标记的二抗(参照二抗说明书进行
稀释)中,室温混摇2h;
9.洗涤:取出膜放在TBST 中洗涤3×5min;
10.ECL 显色:将膜取出放入混匀的ECL 显色液中,孵育3min,将膜取出贴在
有荧光角标的胶片上,迅速用保鲜膜包好;
11.曝光:把底片放在暗盒中,根据荧光强度分别对X 光胶片作不同时间段的曝
光,曝光结束后,将底片取出,1min 显影,30s 清洗,1min 定影,30s 清洗,晾干;
12.结果分析:用扫描仪将曝光后的X 光胶片扫描,做后续结果分析。
