2018届高考化学大一轮:第十九单元 物质结构与性质 含解析
2018年高考真题物质结构与性质汇编

(5)Fe(H2O)6]2+与 NO 反应生成的 Fe(NO)(H2O)5]2+中,NO 以 N 原子与 Fe2+形成配位键。 请在 Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体。
(2018.海南卷 19) 19-I(6 分)下列元素或化合物的性质变化顺序正确的是 A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI C.晶格能:NaF>NaCl>NaBr>NaI D. 热 稳 定 性 : MgCO 3>CaCO3>SrCO 3>BaCO 3
ZnCl2、ZnBr2、ZnI2 能够溶于乙醇、乙醚等有机溶剂,原因是_____________。 (4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表
面创伤。ZnCO3 中,阴离子空间构型为________________,C 原子的杂化形式为 ________________。 (5)金属 Zn 晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六
Li2O 晶格能为_______kJ·mol-1。
(5)Li2O 具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为 0.4665nm,阿伏加
德罗常数的值为 NA,则 Li2O 的密度为_____________g·cm-3(列出计算式)。
(2018.全国 II 卷 35)硫及其化合物有许多用途,相关物质的物理常数如下表所示:
19-Ⅱ(14 分) 黄铜矿石主要的炼铜原料,CuFeS2 是其中铜的主要存在方式。回答下列问题:
(1)CuFeS2 中存在的化学键类型是_________。下列基态原子或离子的价层电子排布图 正确的是__________(填标号)。
(word完整版)2018全国高考理综1卷(化学试题(卷)部分)答案解析和分析

2018年全国高考理综(Ⅰ)卷化学试题部分参考答案一、选择题:每小题6分,在每小题给出的四个选项中,只有一选项是符合题目要求的。
7.磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误..的是A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠【答案分析】D。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8.下列说法错误的是A.蔗糖、果糖和麦芽糖均为双糖B.酶是一类具有高选择催化性能的蛋白质C.植物油含有不饱和脂肪酸甘油酯,能使Br2/CCl4褪色D.淀粉和纤维素水解的最终产生均为葡萄糖【答案与分析】A。
果糖属于单糖。
9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是A B C D【答案与分析】D。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法是用分液法,而不饱和碳酸钠溶液乙醇、冰醋酸浓硫酸正极片碱溶2溶液LiFePO4滤渣H2SO4/HNO3含Li、Fe、P炭黑等滤渣碱溶沉淀滤液Na2CO3含锂沉淀能采用加热蒸发结晶法,10.N A是阿伏加得罗常数的值,下列说法正确的是A.16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1N AB.22.4L(标准状况下)氩气含有的质子数为18N AC.92.0g甘油(丙三醇)中含有羟基数为1.0N AD.1.0molCH4与Cl2在光照下反应生成CH3Cl分子数为1.0N A【答案与分析】B。
盐类水解的程度是很小的,A不对;隋性气体属于单原子分子,1mol的氩气在标准状况下所占的体积为22.4L,所含的电子数和质子数相等,均为18mol,B正确;1mol甘油(丙三醇)中含有3N N的羟基,C错误;CH4与CL2在光照的条件下反应生成的产物中含有CH3Cl、CH2Cl2、CHCl3及CCl4,则生成物中含有的CH3Cl少于1mol,D不对。
2018年高考全国卷1理综化学试题解析(精编版)(原卷版)(2021年整理)

(完整)2018年高考全国卷1理综化学试题解析(精编版)(原卷版)(word版可编辑修改)编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望((完整)2018年高考全国卷1理综化学试题解析(精编版)(原卷版)(word版可编辑修改))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为(完整)2018年高考全国卷1理综化学试题解析(精编版)(原卷版)(word版可编辑修改)的全部内容。
绝密★启用前注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe56 I 127一、选择题1. 磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是A。
合理处理废旧电池有利于保护环境和资源再利用B. 从“正极片”中可回收的金属元素有Al、Fe、LiC. “沉淀”反应的金属离子为Fe3+D. 上述流程中可用硫酸钠代替碳酸钠2。
下列说法错误的是A。
蔗糖、果糖和麦芽糖均为双糖B。
酶是一类具有高选择催化性能的蛋白质C。
植物油含不饱和脂肪酸酯,能使Br₂/CCl4褪色D。
淀粉和纤维素水解的最终产物均为葡萄糖3。
在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是A. AB. B C。
2018高考化学真题和模拟类编_专题18_物质结构和性质(选修)

1.【2018新课标1卷】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。
回答下列问题:(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标号)。
A. B.C. D.(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是______。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是______、中心原子的杂化形式为______。
LiAlH4中,存在_____(填标号)。
A.离子键 B.σ键 C.π键 D.氢键(4)Li2O是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。
可知,Li原子的第一电离能为________kJ·mol−1,O=O键键能为______kJ·mol−1,Li2O晶格能为______kJ·mol−1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。
已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为N A,则Li2O的密度为______g·cm−3(列出计算式)。
【答案】 D C Li+核电荷数较大正四面体 sp3 AB 520 498 2908【解析】分析:(1)根据处于基态时能量低,处于激发态时能量高判断;(2)根据原子核对最外层电子的吸引力判断;(3)根据价层电子对互斥理论分析;根据物质的组成微粒判断化学键;(4)第一电离能是气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,据此计算;根据氧气转化为氧原子时的能量变化计算键能;晶格能是气态离子形成1摩尔离子晶体释放的能量,据此解答;(5)根据晶胞中含有的离子个数,结合密度的定义计算。
点睛:本题考查核外电子排布,轨道杂化类型的判断,分子构型,电离能、晶格能,化学键类型,晶胞的计算等知识,保持了往年知识点比较分散的特点,立足课本进行适当拓展,但整体难度不大。
2018年高考真题——化学(江苏卷) 含解析 已整理
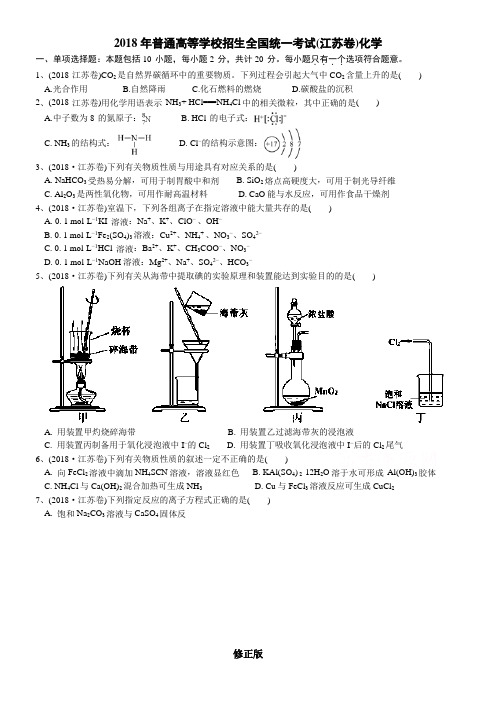
2018年普通高等学校招生全国统一考试(江苏卷)化学一、单项选择题:本题包括10 小题,每小题2 分,共计20 分。
每小题只有一个....选项符合题意。
1、(2018·江苏卷)CO2是自然界碳循环中的重要物质。
下列过程会引起大气中CO2含量上升的是( )A.光合作用B.自然降雨C.化石燃料的燃烧D.碳酸盐的沉积2、(2018·江苏卷)用化学用语表示NH3+ HCl===NH4Cl中的相关微粒,其中正确的是( )A.中子数为8 的氮原子:B. HCl 的电子式:C. NH3的结构式:D. Cl−的结构示意图:3、(2018·江苏卷)下列有关物质性质与用途具有对应关系的是( )A. NaHCO3受热易分解,可用于制胃酸中和剂B. SiO2熔点高硬度大,可用于制光导纤维C. Al2O3是两性氧化物,可用作耐高温材料D. CaO能与水反应,可用作食品干燥剂4、(2018·江苏卷)室温下,下列各组离子在指定溶液中能大量共存的是( )A. 0. 1 mol·L−1KI 溶液:Na+、K+、ClO− 、OH−B. 0. 1 mol·L−1Fe2(SO4)3溶液:Cu2+、NH4+、NO3−、SO42−C. 0. 1 mol·L−1HCl 溶液:Ba2+、K+、CH3COO−、NO3−D. 0. 1 mol·L−1NaOH溶液:Mg2+、Na+、SO42−、HCO3−5、(2018·江苏卷)下列有关从海带中提取碘的实验原理和装置能达到实验目的的是( )A. 用装置甲灼烧碎海带B. 用装置乙过滤海带灰的浸泡液C. 用装置丙制备用于氧化浸泡液中I−的Cl 2D. 用装置丁吸收氧化浸泡液中I−后的Cl2尾气6、(2018·江苏卷)下列有关物质性质的叙述一定不正确的是( )A. 向FeCl2溶液中滴加NH4SCN溶液,溶液显红色B. KAl(SO4) 2·12H2O溶于水可形成Al(OH)3胶体C. NH4Cl与Ca(OH)2混合加热可生成NH3D. Cu与FeCl3溶液反应可生成CuCl27、(2018·江苏卷)下列指定反应的离子方程式正确的是( )A. 饱和Na2CO3溶液与CaSO4固体反应:CO32−+CaSO4CaCO3+SO42−B. 酸化NaIO3和NaI的混合溶液:I− +IO3−+6H+===I2+3H2OC. KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3===2FeO42−+3Cl−+4H++H2OD. 电解饱和食盐水:2Cl−+2H+Cl2↑+ H2↑8、(2018·江苏卷)短周期主族元素X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。
2018全国高考理综1卷(化学试题部分)答案与解析和分析范文
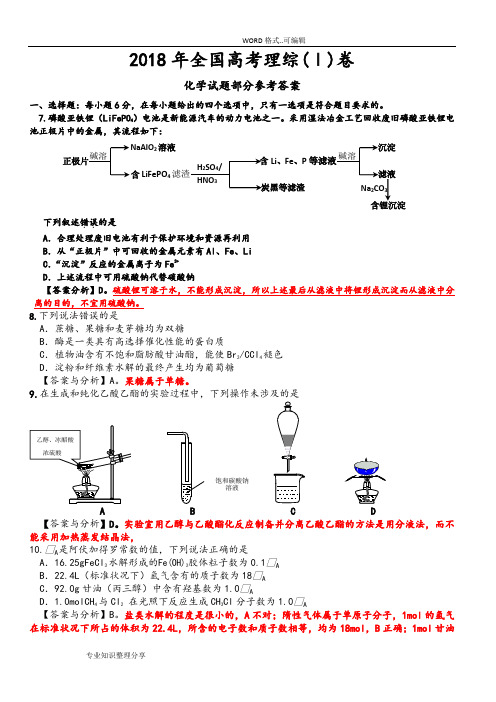
2018年全国高考理综(Ⅰ)卷化学试题部分参考答案一、选择题:每小题6分,在每小题给出的四个选项中,只有一选项是符合题目要求的。
7.磷酸亚铁锂(LiFePO 4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误..的是 A .合理处理废旧电池有利于保护环境和资源再利用 B .从“正极片”中可回收的金属元素有Al 、Fe 、Li C .“沉淀”反应的金属离子为Fe 3+ D .上述流程中可用硫酸钠代替碳酸钠【答案分析】D 。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8.下列说法错误的是A .蔗糖、果糖和麦芽糖均为双糖B .酶是一类具有高选择催化性能的蛋白质C .植物油含有不饱和脂肪酸甘油酯,能使Br 2/CCl 4褪色D .淀粉和纤维素水解的最终产生均为葡萄糖 【答案与分析】A 。
果糖属于单糖。
9.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是A B C D【答案与分析】D 。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法是用分液法,而不能采用加热蒸发结晶法, 10. 是阿伏加得罗常数的值,下列说法正确的是A.16.25gFeCl 3水解形成的Fe(OH)3胶体粒子数为0.1 B .22.4L (标准状况下)氩气含有的质子数为18 C .92.0g 甘油(丙三醇)中含有羟基数为1.0D .1.0molCH 4与Cl 2 在光照下反应生成CH 3Cl 分子数为1.0【答案与分析】B 。
盐类水解的程度是很小的,A 不对;隋性气体属于单原子分子,1mol 的氩气在标准状况下所占的体积为22.4L ,所含的电子数和质子数相等,均为18mol ,B 正确;1mol 甘油饱和碳酸钠 溶液2溶液LiFePO 4Li 、Fe 、P滤液 Na 2CO 3 含锂沉淀(丙三醇)中含有3的羟基,C 错误;CH 4与CL2在光照的条件下反应生成的产物中含有CH 3Cl 、CH 2Cl 2、CHCl 3及CCl 4,则生成物中含有的CH 3Cl 少于1mol ,D 不对。
2018年全国高考理综1卷(化学试题部分)答案与分析69925
2018年全国高考理综(Ⅰ)卷化学试题部分参考答案一、选择题:每小题6分,在每小题给出的四个选项中,只有一选项是符合题目要求的。
7.磷酸亚铁锂(LiFePO 4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误..的是 A .合理处理废旧电池有利于保护环境和资源再利用 B .从“正极片”中可回收的金属元素有Al 、Fe 、Li C .“沉淀”反应的金属离子为Fe 3+ D .上述流程中可用硫酸钠代替碳酸钠【答案分析】D 。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8.下列说法错误的是A .蔗糖、果糖和麦芽糖均为双糖B .酶是一类具有高选择催化性能的蛋白质C .植物油含有不饱和脂肪酸甘油酯,能使Br 2/CCl 4褪色D .淀粉和纤维素水解的最终产生均为葡萄糖 【答案与分析】A 。
果糖属于单糖。
9.A B C D【答案与分析】D 。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法是用分液法,而不能采用加热蒸发结晶法,10.N A 是阿伏加得罗常数的值,下列说法正确的是A .16.25gFeCl 3水解形成的Fe(OH)3胶体粒子数为0.1N AB .22.4L (标准状况下)氩气含有的质子数为18N AC .92.0g 甘油(丙三醇)中含有羟基数为1.0N AD .1.0molCH 4与Cl 2 在光照下反应生成CH 3Cl 分子数为1.0N A【答案与分析】B 。
盐类水解的程度是很小的,A 不对;隋性气体属于单原子分子,1mol 的氩气在标准状况下所占的体积为22.4L ,所含的电子数和质子数相等,均为18mol ,B 正确;1mol 甘油(丙三醇)中含有3N A 的羟基,C 错误;CH 4与CL2在光照的条件下反应生成的产物中含有CH 3Cl 、CH 2Cl 2、CHCl 3及CCl 4,则生成物中含有的CH 3Cl 少于1mol ,D 不对。
2018届高考化学一轮 复习课件专题十八 物质结构与性质(选修3)(含17高考真题及解析) (共146张PPT)
学霸有招 考点56 考点57 考点58
高手洞考
高手锻造
试做真题 透析真题 高手必备 萃取高招 对点精练
图(a) 图(b) (3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。 ①从结构角度分析,R中两种阳离子的相同之处为 ,不同之 处为 。(填标号) A.中心原子的杂化轨道类型 B.中心原子的价层电子对数 C.立体结构 D.共价键类型
学霸有招 考点56 考点57 考点58
高手洞考
高手锻造
试做真题 透析真题 高手必备 萃取高招 对点精练
②R 中阴离子N5 中的 σ 键总数为 个。 分子中的大 π 键可用符 ������ 号Π������ 表示,其中 m 代表参与形成大 π 键的原子数,n 代表参与形成大
6 π 键的电子数(如苯分子中的大 π 键可表示为Π6 ),则N5 中的大 π -
学霸有招
高手洞考
高手锻造
高考 考查内容 高考示例 考点 1.原子结构与元素的性质 (1)了解原子核外电子的能 2017 课标 级分布,能用电子排布式表 全国Ⅰ 56. 示常见元素(1— 36 号)原子 35; 原 核外电子的排布。了解原 2017 课标 子 子核外电子的运动状 全国Ⅱ 结 态;(2)了解元素电离能的 35; 构 含义,并能用以说明元素的 2017 课标 与 某些性质;(3)了解原子核 全国Ⅲ 性 外电子在一定条件下会发 35; 2016 课标 质 生跃迁,了解其简单应 全国 用;(4)了解电负性的概念, 知道元素的性质与电负性 Ⅰ,37; 的关系
学霸有招
高手洞考
高手锻造
第六部分 选考模块
学霸有招
高手洞考
高手锻造
专题十八 物质结构与性质(选修3)
学霸有招
2018年全国高考理综1卷[化学试题部分]答案及分析范文
2018年全国高考理综<Ⅰ>卷化学试题部分参考答案一、选择题:每小题6分,在每小题给出的四个选项中,只有一选项是符合题目要求的。
7.磷酸亚铁锂〔LiFePO 4电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误..的是 A .合理处理废旧电池有利于保护环境和资源再利用 B .从"正极片"中可回收的金属元素有Al 、Fe 、Li C ."沉淀"反应的金属离子为Fe 3+D .上述流程中可用硫酸钠代替碳酸钠[答案分析]D 。
硫酸锂可溶于水,不能形成沉淀,所以上述最后从滤液中将锂形成沉淀而从滤液中分离的目的,不宜用硫酸钠。
8.下列说法错误的是A .蔗糖、果糖和麦芽糖均为双糖B .酶是一类具有高选择催化性能的蛋白质C .植物油含有不饱和脂肪酸甘油酯,能使Br 2/CCl 4褪色D .淀粉和纤维素水解的最终产生均为葡萄糖 [答案与分析]A 。
果糖属于单糖。
9.A B C D[答案与分析]D 。
实验室用乙醇与乙酸酯化反应制备并分离乙酸乙酯的方法是用分液法,而不能采用加热蒸发结晶法, 10.是阿伏加得罗常数的值,下列说法正确的是A .16.25gFeCl 3水解形成的Fe<OH>3胶体粒子数为0.1B .22.4L 〔标准状况下氩气含有的质子数为18C .92.0g 甘油〔丙三醇中含有羟基数为1.0饱和碳酸钠 溶液乙醇、冰醋酸 浓硫酸正极片碱溶2溶液 LiFePO 4滤渣H 2SO 4/ HNO 3含Li 、Fe 、P炭黑等滤渣碱溶沉淀滤液Na 2CO 3 含锂沉淀D.1.0molCH4与Cl2在光照下反应生成CH3Cl分子数为1.0[答案与分析]B。
盐类水解的程度是很小的,A不对;隋性气体属于单原子分子,1mol的氩气在标准状况下所占的体积为22.4L,所含的电子数和质子数相等,均为18mol,B正确;1mol甘油〔丙三醇中含有3的羟基,C错误;CH4与CL2在光照的条件下反应生成的产物中含有CH3Cl、CH2Cl2、CHCl3及CCl4,则生成物中含有的CH3Cl少于1mol,D不对。
2018高考化学真题和模拟类编_专题18_物质结构和性质(选修)
1.【2018新课标1卷】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。
回答下列问题:(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标号)。
A. B.C. D.(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是______。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是______、中心原子的杂化形式为______。
LiAlH4中,存在_____(填标号)。
A.离子键 B.σ键 C.π键 D.氢键(4)Li2O是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。
可知,Li原子的第一电离能为________kJ·mol−1,O=O键键能为______kJ·mol−1,Li2O晶格能为______kJ·mol−1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。
已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为N A,则Li2O的密度为______g·cm−3(列出计算式)。
【答案】 D C Li+核电荷数较大正四面体 sp3 AB 520 498 2908【解析】分析:(1)根据处于基态时能量低,处于激发态时能量高判断;(2)根据原子核对最外层电子的吸引力判断;(3)根据价层电子对互斥理论分析;根据物质的组成微粒判断化学键;(4)第一电离能是气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,据此计算;根据氧气转化为氧原子时的能量变化计算键能;晶格能是气态离子形成1摩尔离子晶体释放的能量,据此解答;(5)根据晶胞中含有的离子个数,结合密度的定义计算。
点睛:本题考查核外电子排布,轨道杂化类型的判断,分子构型,电离能、晶格能,化学键类型,晶胞的计算等知识,保持了往年知识点比较分散的特点,立足课本进行适当拓展,但整体难度不大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十九单元 物质结构与性质测试时间:90分钟满分:120分 1.[2016·全国卷Ⅰ](15分)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。
回答下列问题:(1)基态Ge 原子的核外电子排布式为[Ar]________,有________个未成对电子。
(2)Ge 与C 是同族元素,C 原子之间可以形成双键、三键,但Ge 原子之间难以形成双键或三键。
从原子结构角度分析,原因是_________________________________________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________________________________。
(4)2424是该反应的良好催化剂。
Zn 、Ge 、O 电负性由大至小的顺序是____________。
(5)Ge 单晶具有金刚石型结构,其中Ge 原子的杂化方式为________,微粒之间存在的作用力是________。
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置。
如图为Ge单晶的晶胞,其中原子坐标参数A 为(0,0,0);B 为⎝ ⎛⎭⎪⎫12,0,12;C 为⎝ ⎛⎭⎪⎫12,12,0。
则D 原子的坐标参数为________。
②晶胞参数,描述晶胞的大小和形状。
已知Ge 单晶的晶胞参数a =565.76 pm ,其密度为________g·cm -3(列出计算式即可)。
答案 (1)3d 104s 24p 2(1分) 2(1分)(2)Ge 原子半径大,原子间形成的σ单键较长,p-p 轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键(2分)(3)GeCl 4、GeBr 4、GeI 4的熔、沸点依次增高。
原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强(2分)(4)O>Ge>Zn(2分)(5)sp 3(1分) 共价键(1分)(6)①⎝ ⎛⎭⎪⎫14,14,14(2分) ②8×736.02×565.763×107(3分) 解析 (1)在元素周期表中,锗位于硅正下方,锗的原子序数为14+18=32,基态原子的核外电子排布式为1s 22s 22p 63s 23p 63d 104s 24p 2或[Ar]3d 104s 24p 2,由于4p 能级有3个能量相同的轨道,根据洪特规则,4p 上2个电子分别占据两个轨道且自旋方向相同,故未成对电子数为2。
(2)本题从单键、双键、三键的特点切入,双键、三键中都含有π键,难以形成双键、三键,实质是难以形成π键,因为锗的原子半径较大,形成单键的键长较长,p-p 轨道肩并肩重叠程度很小。
(3)根据表格数据得出,三种锗卤化物都是分子晶体,其熔、沸点分别依次增高,而熔、沸点的高低与分子间作用力强弱有关,分子间相互作用力强弱与分子量大小有关。
(4)锌、锗位于同周期,同一周期从左至右元素的电负性逐渐增大(除稀有气体元素外),而氧位于元素周期表右上角,电负性仅次于氟,由此得出氧、锗、锌的电负性依次减小。
(5)类比金刚石,晶体锗是原子晶体,每个锗原子与其周围的4个锗原子形成4个单键,故锗原子采用sp 3杂化。
微粒之间的作用力是共价键。
(6)①对照晶胞图示、坐标系以及A 、B 、C 点坐标,选A 点为参照点,观察D 点在晶胞中位置⎝ ⎛⎭⎪⎫体对角线14处,由B 、C 点坐标可以推知D 点坐标。
②类似金刚石晶胞,1个晶胞含有8个锗原子,ρ=8×736.02×565.763×107 g·cm -3。
2.[2016·全国卷Ⅱ](15分)东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。
回答下列问题:(1)镍元素基态原子的电子排布式为________________,3d 能级上的未成对电子数为________。
(2)硫酸镍溶于氨水形成[Ni(NH 3)6]SO 4蓝色溶液。
①[Ni(NH 3)6]SO 4中阴离子的立体构型是________。
②在[Ni(NH 3)6]2+中Ni 2+与NH 3之间形成的化学键称为________,提供孤电子对的成键原子是________。
③氨的沸点________(填“高于”或“低于”)膦(PH 3),原因是____________________________________;氨是________分子(填“极性”或“非极性”),中心原子的轨道杂化类型为________。
(3)单质铜及镍都是由________键形成的晶体;元素铜与镍的第二电离能分别为:I Cu =1958 kJ·mol -1、I Ni =1753 kJ·mol -1,I Cu >I Ni 的原因是______________________________________________________。
(4)某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为________。
②若合金的密度为d g·cm -3,晶胞参数a =________nm 。
答案 (1)1s 22s 22p 63s 23p 63d 84s 2(或[Ar]3d 84s 2)(2分) 2(1分)(2)①正四面体(1分) ②配位键(1分) N(1分) ③高于(1分) NH 3分子间可形成氢键(1分) 极性(1分) sp 3(1分)(3)金属(1分) 铜失去的是全充满的3d 10电子,镍失去的是4s 1电子(1分)(4)①3∶1(1分) ②⎝ ⎛⎭⎪⎫2516.02×1023×d13 ×107(2分)解析 (1)Ni 元素原子核外有28个电子,电子排布式为1s 22s 22p 63s 23p 63d 84s 2或[Ar]3d 84s 2。
3d 能级上有2个未成对电子。
(2)①SO 2-4中S 无孤电子对,立体构型为正四面体。
②[Ni(NH 3)6]2+为配离子,Ni 2+与NH 3之间为配位键。
配体NH 3中提供孤电子对的为N 。
③NH 3分子间存在氢键,故沸点比PH 3高。
NH 3中N 有一个孤电子对,立体构型为三角锥形,因此NH 3为极性分子,N 的杂化轨道数为3+1=4,杂化类型为sp 3。
(3)单质铜及镍都是由金属键形成的晶体,Cu 、Ni 失去一个电子后电子排布式分别为[Ar]3d 10、[Ar]3d 84s 1,铜的3d 轨道全充满,达到稳定状态,所以Cu 的第二电离能相对较大。
(4)①Cu 原子位于面心,个数为6×12=3,Ni 原子位于顶点,个数为8×18=1,铜原子与镍原子的数量比为3∶1。
②以该晶胞为研究对象,则64×3+59N Ag =d g·cm -3×(a ×10-7cm)3,解得a =3251×107。
6.02×1023×d3.[2016·全国卷Ⅲ](15分)砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。
回答下列问题:(1)写出基态As原子的核外电子排布式______________。
(2)根据元素周期律,原子半径Ga________As,第一电离能Ga________As(填“大于”或“小于”)。
(3)AsCl3分子的立体构型为________,其中As的杂化轨道类型为________________。
(4)GaF3的熔点高于1000 ℃,GaCl3的熔点为77.9 ℃,其原因是__________________________________________________________。
(5)GaAs的熔点为1238 ℃,密度为ρg·cm-3,其晶胞结构如图所示。
该晶体的类型为____________,Ga与As以________键键合。
Ga和As的摩尔质量分别为M Ga g·mol-1和M As g·mol-1,原子半径分别为r Ga pm和r As pm,阿伏加德罗常数值为N A,则GaAs晶胞中原子的体积占晶胞体积的百分率为________。
答案(1)[Ar]3d104s24p3(1分)(2)大于(2分)小于(2分)(3)三角锥形(1分)sp3(1分)(4)GaF3为离子晶体,GaCl3为分子晶体(2分)(5)原子晶体(2分)共价(2分)4π×10-30N A ρ(r 3Ga +r 3As )3(M Ga +M As )×100%(2分) 解析 (1)根据构造原理可写出基态As 原子的核外电子排布式。
(2)同周期主族元素从左到右,原子半径逐渐减小,第一电离能呈增大趋势,且As 的4p 能级处于半充满状态,稳定性强。
Ga 的原子半径大于As ,Ga 的第一电离能小于As 。
(3)AsCl 3的中心原子(As 原子)的价层电子对数为(5+1×3)/2=4,所以是sp 3杂化。
AsCl 3的立体构型为三角锥形。
(4)根据晶体类型比较熔点。
一般来说,离子晶体的熔点高于分子晶体的熔点。
(5)根据晶胞结构示意图可以看出,As 原子与Ga 原子形成了空间网状结构的晶体,结合GaAs 的熔点知GaAs 是原子晶体。
首先用均摊法计算出1个晶胞中含有As 原子的个数:8×1/8+6×1/2=4,再通过观察可知1个晶胞中含有4个Ga 原子。
4个As 原子和4个Ga 原子的总体积V 1=4×⎝ ⎛⎭⎪⎫43π×10-30×r 3As +43π×10-30×r 3Ga cm 3;1个晶胞的质量为4个As 原子和4个Ga 原子的质量之和,即⎝ ⎛⎭⎪⎫4M As N A+4M Ga N A g ,所以1个晶胞的体积V 2=4ρN A ·(M As +M Ga ) cm 3。
最后由V 1/V 2即得结果。
4.[2016·宜昌期中](15分)A 、B 、C 、D 、E 均为元素周期表前四周期元素,原子序数依次增大。
A 元素原子核外电子分占3个不同能级,且每个能级上排布的电子数相同;B 元素的简单气态氢化物与最高价氧化物的水化物反应生成盐;C 元素为非金属元素且基态原子的p 能级上电子数比s 能级上电子数多1;D 是前四周期元素中基态原子中含单电子数最多的元素;E 元素位于周期表中的第11纵行。
(1)D 属于________区的元素,其基态原子的核外电子排布式为____________________。
