气体(实际气体和气体液化)
《液化》PPT课件

量小水珠
露也是由空气中的水蒸ห้องสมุดไป่ตู้液化 而成的,×
C.所有气体在温度降到足够低时都
能液化 √
D.用压缩体积的办法可以使所有气
体液化
单纯用压缩体积的方法并不能使所有的气体 液化,有些气体必须采用降低温度和压缩体
积相结合的方法才能使它们液化,×
知识点3 汽化吸热、液化放热
[想一想]把塑料袋从热水中拿出,凉一 会儿,塑料袋变瘪,并且有酒精液滴产 生,这过程说明了什么?
水蒸气遇到温度较 低的蒸格、装食物 的餐具、食物和锅 盖就会液化,并放 出大量的热.
对蒸锅不断加热,开水就不停地变成水蒸 气,水蒸气再液化放热,食物就弄熟了.
我们再来了解一下电冰箱的 构造和原理.
冰箱中热的“搬运工”是一种既容易 汽化又容易液化的物质(工作物质). 液态的工作物质经过很细的毛细管进 入冰箱冷冻室的管子汽化、吸热,使 冰箱内温度降低.然后汽化的蒸气被 压缩机压入冷凝器,在这里液化并把 从冰箱内带来的热通过冰箱壁上的管 子放出.工作物质这样循环流动,冰 箱冷冻室里就可以保持很低的温度.
先熟,对于这种现象解释正确的是( D ) A.上面的包子个头小 B.水蒸气上升过程温度变高 C.上面的蒸笼保温效果好 D.水蒸气到达最上面蒸笼后会液化放热
思路提示:高温的水蒸气遇到冷的蒸笼盖,会变成水 滴,由气态变成液态,是液化现象.气体液化时,要 放热,从而使上面的包子先熟.
汽化和液化 现象及应用
知识点2 气体液化的两种方式
所有气体在温度降到足够低时都可以液化, 这是液化的一种途径.在一定的温度下,压缩体 积也可以使气体液化,这是液化的第二种途径.
家中用的液化气,就是 在常温下用压缩体积的 办法使石油气变成液体 后装入钢瓶的.
液化及措施

液化及措施
一、液化定义
物质由气态变为液态的过程叫做液化。
气态物质液化时所需能量要远大于气态变成固态所需能量,这是因为液态分子之间的空隙比固态分子之间的空隙要大,液态分子之间的相互作用力也比固态的少。
所以,要使物质由气态变为液态,需要克服分子之间的引力做功,因此液化过程需要施加大量的外力。
二、液化方法
使气体液化的方法有降低温度和压缩体积两种。
1.降低温度(Cooling): 通过降低气体的温度,使其达到露点温度以下,气
体便会液化。
日常生活中,我们常常可以看到,当气温下降时,空气中的水蒸气会凝结成水滴,这就是液化现象。
2.压缩体积(Compression): 通过增加气体的压力,使其达到压力露点,也
可以使气体液化。
例如,液化石油气就是在常温下通过压缩体积的方法装入钢罐的。
三、实际应用
1.液化石油气:在常温下利用压缩体积的办法,把石油气液化装在钢罐里。
2.气体打火机:里面的丁烷、煤气罐里面的煤气,也是在常温下利用压缩体
积的办法使气体液化的。
3.低温技术:很多气体在常温下很容易被液化,对部分沸点较低的气体,如
乙醚,使用化学手段也可以使之液化。
在工业上,低温液化技术的应用十分广泛,如液化空气、液氧、液氮、液氢等都在各个领域发挥着重要的作用。
综上所述,液化是物质由气态变为液态的过程,可以通过降低温度和压缩体积两种方法实现。
液化在实际生产和生活中应用非常广泛,深入理解液化的原理和应用对推动科学技术的发展和人类社会的进步具有重要意义。
2实际气体

Tc、pc、Vc 统称为物质的临界参数。 统称为物质的临界参数。
是物性参数 不易测定
超临界态是指温度大于临界温度,压力大于临界 超临界态是指温度大于临界温度, 压力的状态。 压力的状态。
返回
上一内容
下一内容
回主目录
3. 真实气体的 p -Vm 图及气体的液化
l´1 ´ l´2 ´
T1<T2<Tc<T3<T4
返回
T1<T2<Tc<T3<T4
p
c
l2 l1 g2 g1
T4 T3 Tc T2 g´ ´ T1 2
g´1 ´
l
g
Vm 图1.3.1真实气体 p –Vm 等温线示意图 真实气体
上一内容 下一内容 回主目录
返回
若甲烷在203 K,2533.1 kPa 条件下服 例1.4.1 若甲烷在 , 从范德华方程, 从范德华方程,试求其摩尔体积 解:范德华方程可写为: 范德华方程可写为: Vm3 - (b+RT/p) Vm2 + (a/p)Vm - ab/p = 0 + 甲烷: = 甲烷 a=2.283×10-1 Pa⋅m6⋅mol-2, × ⋅ b=0.4728 ×10- 4 m3⋅mol - 1 = Tc=190.53 K T > Tc,解三次方程应得一个实根, 解三次方程应得一个实根, 以上数据代入范德华方程: 二个虚根将 以上数据代入范德华方程: Vm3-7.091 ×10- 4 Vm2+9.013 ×10- 8 Vm-3.856 ×10-12 =0 解得: 解得:Vm = 5.606 × 10 - 4 m3⋅mol-1
• 对理想气体 PVm=RT 可理解为: 可理解为: (气体分子所受的总压力 (1mol分子的自由活动 气体分子所受的总压力) 气体分子所受的总压力 分子的自由活动 空间)=RT 空间 • 理想气体 气P(外压 外压) 外压 1mol分子的自由活动空间 m 分子的自由活动空间=V 分子的自由活动空间
气化和液化的概念

汽化和液化的概念液化和汽化是物质的两种基本状态,液化是把气体变为液体的过程,汽化则是把液体变为气体的过程。
液化和汽化在化学、物理、工程和生产等领域都有着广泛的应用。
一、液化液化指气体经过压缩、冷却等方式被转化为液态状态的过程。
液化主要是通过控制温度和压力来改变气体的物态,使得气体的分子间距离减小,从而发生相变。
1.液化的条件压力和温度是影响气体液化的两个主要因素,气体的液化需要满足定的条件。
首先,在固定的温度下,气体的压力越大,分子间的距离越小相变的可能性就越大,因此较高的压力是气体液化的必要条件。
另外,在固定的压力下,气体的温度越低,气体分子的总能量越小,分子之间的相互作用力增强,气体液化的可能性就越大,因此温度的降低也是液化的必要条件。
2.液化的方法液化的过程中,可以通过多种方式来降低气体的温度和增加气体的压力以实现液化。
液化的方法主要包括以下几种:(1)压缩法:通过对气体进行压缩,使气体的压力增加,分子之间的距离变小,进而增加相互作用力,从而实现液化。
(2) 冷却法:通过将气体的温度降低到气体的临界温度以下,使得气体的相变点下降,可以实现液化。
一些惰性气体,如氨、氢等,只需要将温度降到4K以下,就可以液化。
(3) 混合物分离法:通过调节混合物的温度和压力,使得混合物中的不同气体液化点不同,可以通过液化分离的方式分离出不同品种的气体二、汽化汽化(Vaporization) 是指在一定条件下,液体变为气体状态的过程。
汽化主要涉及到能量的转化问题,液体的汽化主要包括蒸发、沸腾和升华三种方式。
1.汽化的条件相较于液化,液体的汽化条件更易控制。
液体汽化需要满足以下几个条件:(1)液体和气体之间的界面存在。
(2)液体距离其相变点较近。
(3)液体表面的蒸气压力足够大。
(4)液体的表面积足够大,可以满足蒸发、沸腾、升华的需要。
2.汽化的方式液体的汽化主要有三种方式,包括蒸发、沸腾和升华。
这三种汽化方式分别适用于不同的条件和情况。
真实气体的液化及临界参数
1.液体的饱和蒸气压苯乙醇水表不同温度的水、乙醇和苯的饱和蒸气压表不同温度的水、乙醇和苯的饱和蒸气压●同一物质,蒸气压随温度的升高而增大●大气中水蒸气的压力达到其饱和蒸气压时,称为相对湿度为100%2. 临界参数如图势能曲线所示,随着分子间距的缩小,分子间力将从吸引转为排物质的饱和蒸气压随温度的升高而急速增大,温度越高,使气体液化所一种纯气体的温度超过某一定值以后,靠加压来缩小分子间距使其液3. 真实气体的p-V图及气体的液化cm饱和曲线西安电子科技大学技大学图1.1.3真实气体的p-V m等温线技大学 技大学 技大学 西安电子科技大学西安电子科技大学西安电子科技大学超临界流体气和风味。
采用超临界流体技术脱除咖啡因,可避免以上缺点。
mm技大学 技大学西安电子科技大学西安电子科技大学9理想气体p V m /J ·m o l -1p V mp V m /J ·m o l -1m -p 图技大学 技大学 西安电子科技大学西安电子科技大学技大学 技大学 技大学 西安电子科技大学西安电子科技大学西安电子科技大学m <RT )范德华方程()a ⎛⎞技大学 技大学 技大学 西安电子科技大学西安电子科技大学西安电子科技大学★设分子A 、B 是半径为r 的圆球,当两个分子相碰时,质心间的最短距离x = 2r 。
★把分子B 看成是位于其球心处的质点,这个质点不能进入以分子A 为圆心、2r 为半径的球形禁区内,球形禁区的体积等于②b 是lmol 硬球气体分子本身体积的4倍★由于是两个分子碰撞,这个体积属于两个分子。
对每个分子来说,不能进入的体积为331444233x r ππ⎛⎞⎛⎞×=×⎜⎟⎜⎟⎝⎠⎝⎠即相当于分子本身体积的4倍。
3344(2)833r r ππ⎛⎞=×⎜⎟⎝⎠即等于分子本身体积的8倍。
技大学 技大学 西安电子科技大学西安电子科技大学27过饱和蒸汽过饱和液体方法,为以后建立更准确的真实气体状态方程,奠定了基础。
01第一章理想气体-2

4. 其他重要方程举例 (略)
2011-08 20
§1.5 对应状态原理及普遍化压缩因子图
1. 压缩因子
引入压缩因子Z来修正理想气体状态方程,
描述实际气体的 pVT 性质:
pV = ZnRT 或 pVm= ZRT
Z =
2011-08
(Vm:实际气体摩尔体积)
压缩因子的定义为:
• Br2(g)冷却发生液化. 液 化现象表明 Br2分子在 气相时就不具有零体积.
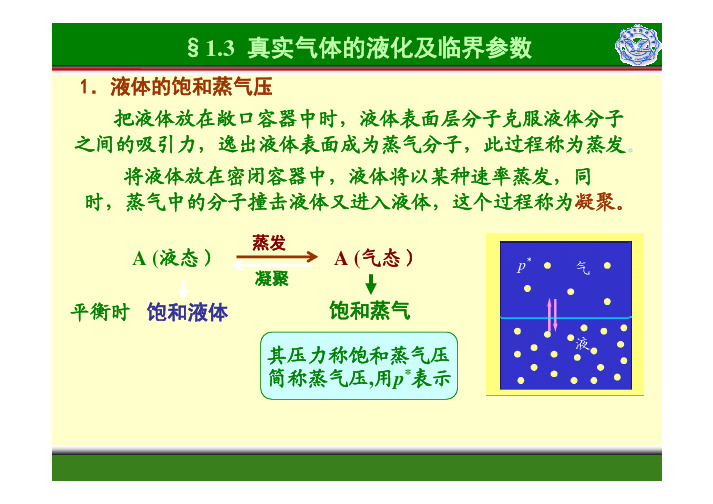
1. 液体的饱和蒸气压
理想气体不会液化(因为分子间没有相互作用力)
实际气体:在一定T、p 时,气-液可共存达到平衡. 气-- 液平衡时: 气体称为饱和蒸气; 液体称为饱和液体; 压力称为饱和蒸气压 p**。
图1.3.1 气-液平衡示意图
2011-08
( pV lim p 0 p
m
) = 0 TB
14
每一种气体均有自己的波义尔温度; TB一般为Tc的2 ~ 2.5 倍; T= TB时,气体在几百 kPa 的压力范围内
符合理想气体状态方程
2. 范德华方程 (1) 范德华方程 理想气体状态方程 pVm=RT
实质为:
(分子间无相互作用力时气体的压力)× (1 mol 气体分子的自由活动空间)=RT
2011-08 15
实际气体:
1) 分子间有相互作用力
器 壁
内部分子
靠近器壁的分子
分子间相互作用减弱了分子对器壁的碰撞, 所以: p = p理-p内
p内= a / Vm2
2011-08
p理= p + p内= p + a / Vm2
2011-08 24
压缩因子示意图
八年级物理上册第三章第3节汽化和液化第2课时液化导学案(附模拟试卷含答案)

第2课时液化课巩固教师引导学生复习上一节内容,并讲解布置的作业(教师可针对性地挑选部分汽化和液化现象及应用新气体液化的两种方式汽化吸热、液化放热. .本节课我们学习了液化和汽化的相关知识,知道气体液化的两种形式——降低2019-2020学年八上物理期末试卷一、选择题1.如图题图所示,向两支同样的试管中注入质量相等的甲、乙两种液体,发现液面在同一水平线上,比较甲、乙两种液体对试管底部的压强A.甲大 B.乙大 C.一样大 D.无法确定2.a、b两个实心物体的体积与质量的关系如图所示。
下列说法正确的是A.a物质的密度比b的大B.b物质的密度是a的2倍C.b物质的密度是2×103kg/m3D.a、b的密度与它们的质量、体积有关3.在儿童乐园,摄影师给卡通人物照相.在对焦时,发现毛玻璃上卡通人像的位置如图甲所示.为了使毛玻璃上卡通人像的位置如图乙所示,摄像师应当将镜头适当地A.向下并且向右移B.向下并且向左移C.向上并且向左移D.向上并且向右移4.人眼好像一架照相机,晶状体和角膜的共同作用相当于凸透镜,如图甲所示表示的是来自远处的光经小丽眼球折光系统得光路示意图。
下列分析正确的是A.小丽是近视眼B.小丽是远视眼C.应利用凸透镜矫正D.以上说法都不对5.如图所示是在镜中看到的钟面指针位置,则实际时刻是A.9:30 B.2:30 C.6:15 D.12:15 6.太阳光通过校园林荫道旁树叶的缝隙,在路面上形成了许多光斑,这些光斑A.是圆形的,它是太阳的虚像B.是树叶形的,它是太阳的实像C.是圆形的,它是太阳的实像D.是树叶缝隙形的,它是太阳的影子7.如图所示的图象中,属于晶体熔化图象的是A.C.8.下列一些关于生活中的物理现象及原因分析,错误的是( ) A .用冰袋给高热病人降温,原因是冰熔化要吸热B .使用高压锅,食物容易被煮熟,原因是锅内气体压强大,液体沸点高C .水沸腾时壶口冒出的“白气”是空气中的水蒸气液化形成的D .衣柜里的樟脑丸变小了,原因是樟脑丸发生了升华现象9.为了减少高速行驶的车辆产生的噪声对高速公路两侧单位、居民的干扰,常在高速公路两侧立有一定高度的隔声板,这种减弱噪声的措施属于( ) A .在声源处减弱噪声 B .在传播过程中减弱噪声 C .在人耳处减弱噪声 D .以上说法都不正确10.今年5月,世博会在我国上海顺利举行,为向全世界充分展示“城市,我们的美好生活”这一主题,上海建设越来越注重以人为本。
教科版八年级物理上册汽化和液化课件教科版_图文

时间 /min
… 6 7 8 9 10 11 12 13 14 15 …
温度/℃ … 95 96 97 98 98 98 95 98 98 98 …
(1)从记录数据看出,某一次观察记录中明显错误的是第 12 min时的数据; (2)此时水沸腾的温度为 98 ℃;
(3)在水沸腾过程中要 吸热 (选填“吸热”或“放热”).
5 67
102 102 102
温度/℃
沸腾 108
沸点:102 98
液体沸腾时的 温度叫沸点。
想一想:
该曲线与 88 晶体的熔
化曲线有
什么不同?
78 0
1
23
4
5
6
7 时间/min
观察水的沸腾
观察阶段
观察要求
水在沸腾前
水在沸腾时
气泡
出现少量气泡,上 升过程中由大变小
内部出现大量气 泡,上升,变大
温度 逐渐升高 保持不变
教科版八年级物理上册汽化和液化课件教科版 _图文.ppt
一.汽化 液化 1.定义:物质由液态变成气态的过程,称为汽化
物质由气态变为液态的过程,称为液化
2.汽化的两种方式:
蒸发 和 沸腾
只在液体表面进行的汽化现象叫蒸发。 在液体表面和内部同时发生的剧烈的汽化 现象叫沸腾
烧开水时如果不断加热会发现锅里的水会有下面的现象,这不再
(4) 如下图是小组同学作出的水的沸腾图像,其中正确的是(D )
8、当烧杯中的水沸腾时,试管甲中的酒 精是否沸腾?试管乙中的水是否沸腾? 为什么?
甲乙
烧杯
6.小李把同样水饺放水中煮和放在油中 炸,经过一段时间取出水饺,发现在油炸 的水饺发黄变焦了,而在水中煮的水饺没 有发黄变焦,这说明…………( C ) A.水是无色的,油是黄的 B.油的传热性能比水强 C.油的沸点比水的沸点高 D.油没有沸点,水有沸点
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
按范德华
方程计算 的体积/ ×10-6m3
压力/kPa
实际体积 /×10-6m3
按理想气 体状态方 程计算的 体积/ ×10-6m3
按范德华
方程计算 的体积/ ×10-6m3
100 1000
9
25574.0 25705.0 25597.0 50×100 380.0 2449.0 2571.0 2471.3 100×100 69.3
的摩尔分数及分压;(2)计算水煤气的平均
摩尔质量和在该条件下的相对密度。
4
2021/3/6
整理ppt
气体——实际气体和气体液化
【问题3-6】按照理想气体状态方程式计算 40℃时CO2的摩尔体积,与实际测得的实际体 积比较。
5
2021/3/6
整理ppt
CO2在40℃、不同压力下按理想气体状态方程计 算的摩尔体积与实际体积的对比
压力/kPa
Байду номын сангаас
实际体积 /×10-6m3
按理想气 体状态方 程计算的 体积/ ×10-6m3
pV nRT
请比较两个公式有什么不同?
7
2021/3/6
整理ppt
(p a)V ( b)RT V2
b——是1mol气体分子的等效体积
• a——是气体内压力与气体体积平方成反比的 比例系数
• (1)不是把气体分子看成质点,而是看成具有 一定的体积,减去有效体积。
• (1)考虑分子间作用力对体积和压力的影响, 加上内部压力。
513.0 256.7
整理ppt
395.0 88.9
【问题3-7】请查阅我国“西气东输”的管道压力是 采用什么方法计算的。
首先,“西气东输”管道要有较高的压力
使用理想气 体状态方程?
10
使用范德华 方程计算?
整理ppt
二、压缩因子
Z pVm pV RT nRT
对于理想气体,Z=1
若某气体Z≠1,则该气体与理想气体发生了偏差
什么能够达到冷冻的目的? 2.盛装不同气体的钢瓶颜色和标识是不尽相同
的,请搜集.查找并记录统计。
19
2021/3/6
整理ppt
课后任务
作业:
1、23℃,100kPa时3.24×10-4 kg某理想气 体的体积为2.8×10-4m3,试求该气体在 100kPa,100℃时的相对密度。
2.水煤气的体积百分数分别为H2 ,50%;CO , 38%;N2 , 6.0%;CO2, 5.0%;CH4, 1.0% 。在25℃,100kPa下,(1)求各组分
《化学基础》
1
2021/3/6
整理ppt
第三章 物质的聚集状态 主要内容
2
2021/3/6
整理ppt
学习目标
3
整理ppt
学习内容
物质的相态——相和相图;饱和蒸汽压和 温度
气体——理想气体、混合气体、实际气体 溶液——稀溶液依数性;非电解质溶液气
液平衡;电解质的电解 胶体——胶体的特殊性质;物质的表面特征
3、临界状态——物质在临界温度、临界压力下状态
4、临界状态——一旦温度降低或压力降低,将迅速 气化。
15
图3-5 二氧化碳压力-体积图 整理ppt
临界参数
由表1.3.1可知:p*=f (T)
T ,p*
当T=Tc 时,液相消失,加压不再可使气体液化。
临界温度Tc :使气体能够液化所允许的最高温度 临界温度以上不再有液体存在, p*=f (T) 曲线终止于临界温度; 临界温度 Tc 时的饱和蒸气压称为临界压力
,多使用二氧化碳:一时它的临界点温度容易达到, 17 成本低,二是萃取后不会产生二次污染问整理题ppt。
内容总结
1. 理解实际气体与理想气体的区别;
2.了解范德华方程、压缩因子计算过程;
3.理解气体液化的过程和状态变化;
4.理解气体液化的有关应用。
18
2021/3/6
整理ppt
课后任务
作业: 1.医院里做冷冻用的液化气体是那种气体,为
Z>1 时,pVm>RT ,气体的可压缩性比理想气体小 ——难压缩
Z<1 时, pVm<RT ,气体的可压缩性比理想气体好
——容易压缩
11
整理ppt
Z pVm pV RT nRT
Z p R V T m p R c V T m c ,cp T r V rrZ cp T r V rr
压缩因子法公式简单工程计算常用
对于不同的气体,压缩因子Z的数值是不一定相同的。
压缩因子Z的数值可以通过每种气体的临界参 数通过计算和查找压缩因子图而得到。
混合气体的压缩因子Z的数值可以通过每种气
体的压缩因子按照体积分数计算得到。
12
整理ppt
三、气体的液化
气体在某温度下加压,体积会不断缩小,到 一定程度会产生液化现象。
请考虑,是在所有温度下加压都可以使气 体液化吗?
临界压力 pc : 在临界温度下使气体液化所需的最低压力 临界摩尔体积Vm,c:在Tc、pc下物质的摩尔体积
Tc、pc、Vc 统称为物质的临界参数
16
16 整理ppt
气体的液化有哪些应用
1、得到液态气体,例如:液氧、液氮等。
这些液态气体便于储存和携带,例如:液氧。 一旦减压会迅速气化、吸热,起到瞬间冷冻的效果,并 对人体无害,例如:液氮。 工业上已有很成熟的工艺将空气压缩、降温,将氧和氮 分离并液化。 2、超临界流体萃取——一制药和食品工业采用较多
8
整理ppt
在压力为几兆帕的范围内,使用范德华方程 往往可得到比理想气体状态方程好的结果,但 压力更高时,范德华方程的计算结果同实验值 存在比较大的偏差。:
CO2在40℃不同压力下按范德华方程计算的摩 尔体积与实际体积对比关系
压力/kPa
实际体积 /×10-6m3
按理想气 体状态方 程计算的 体积/ ×10-6m3
压力/kPa
实际体积 /×10-6m3
按理想气 体状态方 程计算的 体积/ ×10-6m3
100
25574.0
10×100 2449.0
25705.0 50×100 380.0 2571.0 100×100 69.3
513.0 256.7
6
2021/3/6
整理ppt
一、范德华方程
(p a)V ( b)RT V2
还是看看实际测定的气体的不同温度下的压 力和体积的关系变化吧!
13
整理ppt
图 真实气体p-Vm等温线示意图
① AB段(除B点) 只有气相存在。
② BD水平段 l-g两相平衡共存。
③ DE段(除D点) 只有液相存在。
14
整理ppt
1、临界温度——每种气体液化的最高温度 2、临界参数——临界温度、临界压力和临界体积
