有机化学 有机化学 胺和生物碱
第十一章胺和生物碱

O
[
S O
NR H
]
-
Na+
S
O
O S O
+
R 2N H
S O
N R 2 N aOH
不溶解
Cl
+
R N
3
不反应
(三)与亚硝酸的反应 不同类型的胺与HNO2反应,生成不 同的产物。由于亚硝酸不稳定,在反应中 用NaNO2与 HCl(或H2SO4)作用产生。 1. 伯胺
芳香伯胺若在低温强酸性溶液与亚
硝酸反应,生成重氮盐,称为重氮化反应。
2-甲基-3-氨基戊烷
CH3 CH3CHCHNHCH3 CH3
2-甲基-3-甲氨基丁烷
4.季铵盐和季铵碱(命名同无机铵类化 合物) [(CH3)3NC2H5 ]+Br [(CH3)4N]+OH氢氧化四甲基铵
溴化三甲基乙基铵
必须注意“氨、胺、铵”字的用法, 氨用来表示气态氨(NH3)或基团,如氨
基(—NH2),亚氨基( NH);胺用来
2. 仲胺
脂肪仲胺与芳香仲胺与亚硝酸反应,
都是在氮上进行亚硝化,生成N-亚硝基
胺类化合物,强致癌物。
CH3CH2NHCH2CH3 + HNO2 CH3CH2 N CH2CH3 + H2O N O N-亚硝基二乙胺(黄色油状)
N=O NHCH3 + HNO2 N CH3 + H2O
N-甲基苯胺
N-甲基-N-亚硝基-苯胺
的性质。
1. 氧化反应 芳胺很容易被氧化,氧化的产物很复
杂,这取决于氧化剂的性质和反应的条件。
NH2 MnO2 + H2SO4 O
O
对苯醌
2. 亲电取代反应 由于氨基使苯环活化,所以苯胺很 容易发生亲电取代反应。
本科五年制 基础 有机化学第12章 胺
N
N
N
N
OH
ONa
无偶联 能力
② 酚或胺:
OH
OH -
偶联慢
NH 2
H+
O-
偶联快
NH 3+
H+ OH-
能偶联
不能偶联
偶联的条件为:低温、弱酸或弱碱。
思考题
重氮盐稳定存在的条件是什么?为什么? 为什么重氮盐被羟基取代要强酸条件,而偶 联反应要弱酸、弱碱?
生物碱 (Alkaloid) 一、生物碱的概念及临床应用
胺
脂肪胺 芳香胺 R-NH2 Ar-NH2
3、根据分子中氨基的数目分类
胺 一元胺 多元胺
CH3CH2NH2 H2NCH2CH2NH2
注:芳香胺为N原子 直接连在芳香环上 的胺,如果不是直 接连在芳香环上, 即使有芳香环也不 属于芳香胺。
4、季铵盐和季铵碱
氢氧化铵或铵盐分子中四个氢原子完全被烃基取代而 成的化合物分别称为季铵碱或季铵盐。
MDMA
2-(2-氯苯基)-2-(甲氨基)环己酮 氯胺酮(K粉)
苯丙胺为中枢神经兴奋剂, 是国家严格管制的精神类药品。 甲基苯丙胺俗称“冰毒”, 属于联合国规定的苯丙胺类毒品。 MDMA 属于致幻剂类毒品,是“摇头丸”的主要成分。 氯胺酮俗称K粉。临床上用作麻醉剂或麻醉诱导剂, 有精神 依赖性,其致幻作用是导致被滥用的主要原因。
R R' N H OH2 "R
R R' H OH 2 H OH 2
< <
N
<
H OH 2 R N H OH 2 H OH 2
H OH2 H2O H N H OH2 H OH2
有机化学的基础知识点归纳总结5篇

有机化学的基础知识点归纳总结5篇篇1一、概述有机化学是研究含碳化合物及其衍生物的化学分支。
本篇文章旨在归纳总结有机化学的基础知识点,以帮助读者更好地理解和掌握有机化学的核心内容。
二、基本概念1. 有机化学定义:研究碳基化合物的化学称为有机化学。
2. 有机化合物的特点:主要由碳和氢组成,具有同分异构现象,可发生化学反应等。
三、有机化合物的分类1. 烃类:仅由碳和氢组成的有机化合物。
如:烷烃、烯烃、炔烃、芳香烃等。
2. 醇类:含有羟基(-OH)的有机化合物。
3. 酮类:含有羰基(-CO-)的有机化合物。
4. 羧酸类:含有羧基(-COOH)的有机化合物。
5. 其他类别:包括醚、酯、醛、胺等。
四、共价键与分子结构1. 共价键:原子间通过共用电子对形成的化学键。
2. 分子结构:有机化合物的分子由原子通过共价键连接而成。
3. 立体异构:包括构型异构和构象异构,如异构体的命名和判断。
五、有机反应类型1. 取代反应:原子或原子团替代有机分子中的某些原子或原子团。
2. 加成反应:简单物质与有机化合物中的不饱和键进行加合。
3. 消除反应:从有机化合物中消除某些原子或原子团,生成不饱和键。
4. 氧化与还原反应:涉及有机化合物中电子转移的反应。
六、有机化学反应机制1. 反应速率:描述化学反应快慢的物理量。
2. 反应机理:描述反应如何进行的途径和步骤。
3. 速率定律与活化能:阐述反应速率与反应物浓度之间的关系及反应的活化能要求。
七、光谱分析与结构鉴定1. 光谱分析:利用物质对光的吸收、发射等特性进行物质分析的方法。
2. 结构鉴定:通过光谱数据、化学性质等推断有机化合物的结构。
八、有机合成与设计1. 有机合成:通过有机反应合成有机化合物。
2. 合成设计:根据目标产物设计合适的合成路线和方法。
九、应用与实例1. 医药:药物的设计与合成是有机化学的重要应用领域。
2. 材料科学:高分子材料、功能材料等需要有机化学的知识。
3. 农业:农药、化肥等的设计与合成离不开有机化学。
有机化学(第9版)第十三章 胺和生物碱

降低毒 副作用:
有机化学 (第9版)
四、化学性质
(三)磺酰化反应
伯胺、仲胺能与磺酰氯作用生成磺酰胺。常用的磺酰化试剂是苯磺酰氯和对甲基苯 磺酰氯。 兴斯堡试验(Hinsberg test):鉴别三类胺
有机化学 (第9版)
四、化学性质
(四)与亚硝酸的反应
伯胺与亚硝酸的反应 脂肪伯胺与HNO2反应定量放出氮气,常用于氨基酸和多肽的定量分析。
重点难点
掌握 胺的命名、结构和化学性质;胺的碱性及其影响因 素;芳香重氮化合物的化学性质;生物碱的通性。
熟悉 胺的分类、不同类型胺的鉴别;酰基化反应、芳香 重氮盐在有机合成上的应用。
了解 胺的物理性质;芳香重氮盐的结构;生物碱(常见) 的结构和生理活性及临床应用。
配套题库请下载 医学猫 APP,执业、三基、规培、主治、卫生资格、正副高等题库都已入库。
有机化学 (第9版)
四、化学性质
(二)酰化反应
伯胺、仲胺易与酰氯或酸酐等酰基化剂反应生成酰胺。可用于改善胺的脂溶 性、降低毒性、保护氨基。
有机化学 (第9版)
四、化学性质
(二)酰化反应
保护氨基:
CH3 CH3COCl
NH2
CH3 [O]
NHCOCH3
COOH
OH H2O NHCOCH3
ห้องสมุดไป่ตู้
COOH NH2
烈的致癌作用。
有机化学 (第9版)
四、化学性质
(四)与亚硝酸的反应
叔胺与亚硝酸的反应 脂肪叔胺与亚硝酸反应生成不稳定的季铵盐,碱性条
件下分解为原来的胺。芳香叔胺酸中与亚硝酸反应生成桔 黄色的盐,用碱中和后得到翠绿色的C-亚硝基化合物。
二乙胺、三乙胺、N,N,-二 甲基苯胺与亚硝酸反应结果
有机化学有机化学胺以及生物碱
H3C H3C
三
47nm
01nm
.9。 .9。
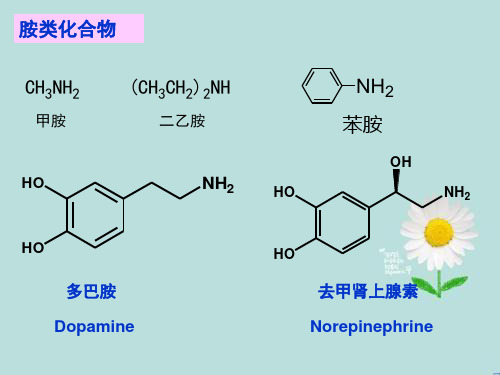
键长:C-N 0.147nm
H3C N H3C
CH3 键角: C-N-C 108。
三甲胺
N
❖苯胺分子中,苯环上所有未参与杂化的p轨道所形成 的大π键可以和氮原子的未参与成键的 sp3杂化轨道形 成部分共轭体系
胺的物理性质
❖ 物态: 低级胺为无色气体或者易挥发的液体,有氨味或鱼腥
HO-N=O + NaCl
亚硝酸
❖脂肪伯胺与HNO2反应生成极不稳定的脂肪重氮盐。
R-NH2
NaNO2 HCl
R
+
N
N Cl-
脂肪重氮盐
N2 ↑ + R+ + Cl-
醇、烯、卤烃等混合物
➢ 该重氮盐即使在低温下也会立即分解放出氮气,并有醇、烯 及卤代烃等混合物的形成。
❖ 芳香伯胺与 HNO2 在低温(一般<5℃)及过量强 酸水溶液中反应生成芳香重氮盐,这个反应称为
从电性效应看,碱性顺序应为: R3N > R2NH > RNH2
2.水的溶剂化效应
H
H
OH
OH
H
+
R NH
H
H O
H
OH H
R+H N
RH
R+ R NH R OH H
H O
H
溶剂化效应越强,氨离子越稳定。
碱性强弱顺序为:伯胺>仲胺>叔胺
3. 空间效应
❖ N 原子上连接的基团越多越大,对 N 上孤对电子的屏蔽作 用越大, N 上孤对电子与 H+ 结合就越难, 碱性就越弱。从空间 效应看碱性顺序为伯胺>仲胺>叔胺
第十二章 胺、酰胺和生物碱(ok)

chapter 12
3
胺
脂肪胺 伯 胺 CH3NH2 甲胺
NH2
芳香胺
(CH3)2CHNH2 异丙胺
CH2NH2
苯胺
苄胺 N attached to aryl group 芳
N attached to alkyl group 脂肪
chapter 12
4
胺的分类和命名 (伯胺 RNH2: one carbon directly attached to N) 伯胺
chapter 12
25
胺的碱性
电子效应的影响(与溶剂化效应相反) 电子效应的影响(与溶剂化效应相反) N上的电子云密度 ,接受质子的能力↑,碱性↑ 上的电子云密度↑,接受质子的能力 ,碱性 上的电子云密度 脂肪叔胺 > 仲胺 > 伯胺 > NH3 > 芳香胺 NH3 4.8 NH2-NH2 6.1 NH2-OH 8.2
叔丁醇(叔醇 叔醇) 叔丁醇 叔醇
伯胺) 叔丁基胺(伯胺 叔丁基胺 伯胺
chapter 12
8
胺的分类和命名
-NHCH3 甲氨基 -N(CH3)2 二甲氨基
1 2 3 4 5 CH3-CH-CH2-CH-CH3 - - CH3 NH2
2-甲基 氨基戊烷 甲基-4-氨基戊烷 甲基
CH3-CH-CH2CH2CH2CH3 - NHCH3
2-甲氨基己烷 甲氨基己烷
chapter 12
9
胺的分类和命名
When all four atoms attached to N are carbon, the ion is called a quaternary ammonium ion(季铵离子) and salts (季铵离子) that contain it are called quaternary ammonium salts. 季铵盐 NH4Br 溴化铵 (CH3)2N(C2H5)2Br 溴化二甲二乙铵 二甲二乙 溴化二甲二乙铵 季铵碱 NH4OH 氢氧化铵 (CH3)4NOH 氢氧化四甲 四甲铵 氢氧化四甲铵
有机化学重点整理

有机化学重点整理第二章:烷烃和环烷烃甲烷methane 己烷hexane 庚菀heptane乙烷ethane 丙烷propane 辛烷octane 丁烷butane 壬烷nonane 戊烷pentane 癸烷decane正normal n- 异iso- 新neo- 优先次序:异丙基>异丁基>丁基>丙基>乙基>甲基构象conformation ——由于碳碳单键的旋转,导致分子中原子或原子团在空间的不同排列方式构象异构体conformational isomer因单键的旋转而产生的异构体(构象异构属于立体异构)稳定性:对位交叉式>邻位交叉式>部分重叠式>全重叠式交叉式—稳定的优势构象烷烃的物理性质:bp、mp、密度:随C原子数↑而↑ 2.烷烃支链↑bp ↓正烷烃密度<0.8g.cm-3甲烷的卤代反应属于自由基的链反应:链引发、链增长、链终止三个阶段①链引发(形成自由基)②链增长(延续自由基,形成产物)③链终止(消除自由基)活性顺序:F2 > Cl2 > Br2 > I2 叔氢> 仲氢> 伯氢离解能越小,自由基越稳定,越易形成R3C > R2CH>RCH2> CH3环烷烃稳定性影响因素:环张力(角张力、扭转张力、空间张力)环丙烷、环丁烷——易开环发生加成,不与KMnO4反应(所有的环烷烃)开环发生在连氢原子最多和连氢原子最少的两个碳原子之间。
氢卤酸中的氢原子加在连氢原子较多的碳原子上,卤原子加在连氢原子较少的碳原子上。
椅式构象是最稳定的优势构象,较大基团在e键的构象是稳定构象(横E竖A),e键取代基最多的构象是优势构象第三章:烯烃和炔烃ζ键和π键的主要特点:ζ键:可以单独存在,存在于任何共价键中。
成键轨道沿键轴“头碰头”重叠,重叠程度较大,键能较大,键较稳定。
电子云呈柱状,对键轴呈圆柱形对称。
电子云密集于两原子之间,受核的约束大,键的极化性(度)小。
有机化学名词解释

一、化合物类名无机酸酯:醇与含氧无机酸反应失去一分子水后的生成物称为无机酸酯。
双烯烃:碳碳双键数目最少的多烯烃是二烯烃或称双烯烃。
可分为三类:两个双键连在同一个碳原子上的二烯烃称为累积二烯烃,两个双键被两个或两个以上单键隔开的二烯烃称为孤立二烯烃,两个双键被一个单键隔开的二烯烃称为共轭二烯烃。
内酯:分子内的羧基和羟基失水形成的产物称为内酯。
内酰胺:分子内的羧基和胺(氨)基失水的产物称为内酰胺。
四级铵碱:四级铵盐在强碱(KOH,NaOH)作用下生成的产物称为四级铵碱。
生物碱:从动植物体内得到的一类有强烈生理效能的含氮有机化合物。
游离生物碱绝大多数是固体,难溶于水,易溶于乙醇等有机溶剂。
天然的生物碱多半是有左旋光的手性化合物。
半缩醛或半缩酮:醇具有亲核性,在酸性催化剂如对甲苯磺酸、氯化氢的作用下,很容易和醛酮发生亲核加成,一分子醛或酮和一分子醇加成的生成物称为半缩醛或半缩酮。
有机化合物:除一氧化碳、二氧化碳、碳酸盐等少数简单含碳化合物以外的含碳化合物。
多肽:一个氨基酸的羧基与另一分子氨基酸的氨基通过失水反应,形成一个酰氨键,新生成的化合物称为肽,肽分子中的酰氨键叫做肽键。
二分子氨基酸失水形成的肽叫二肽,多个氨基酸失水形成的肽叫多肽。
杂环化合物:在有机化学中,将非碳原子统称为杂原子,最常见的杂原子是氮原子、硫原子和氧原子。
环上含有杂原子的有机物称为杂环化合物。
分为两类,具有脂肪族性质特征的称为脂杂环化合物,具有芳香特性的称为芳杂环化合物。
因为前者常常与脂肪族化合物合在一起学习,所以平时说的杂环化合物实际指的是芳杂环化合物。
杂环化合物是数目最庞大的一类有机物。
多环烷烃:含有两个或多个环的环烷烃称为多环烷烃。
共轭烯烃:单双键交替出现的体系称为共轭体系,含共轭体系的多烯烃称为共轭烯烃。
纤维二糖:是由两分子葡萄糖通过1,4 两位上的羟基失水而来的,纤维二糖是B-糖苷。
纤维素:由多个纤维二糖聚合而成的大分子。
多稀烃:含有多于一个碳碳双键的烯烃称为多稀烃。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Methylethylamine
对于芳香胺来说,如果氮原子上连有脂肪烃基,命名时在烃 基前标上N
2
仲胺
(CHNH 3)2NH 2
NHCH 3 N-甲基苯胺
N-methylaniline
苯 胺 二甲胺
aniline
复杂的胺则以烃作为母体,氨基作为取代基。
CH3 NH2 CH3-CH-CH2-CH-CH2-CH3
胺的化学性质
(一) 胺的碱性
CH3NH 2 + HCl CH3NH2· HCl 甲胺盐酸盐
CH3NH3Cl
NH 2 + HCl
-
氯化甲铵
苯 胺 盐 酸 盐
NH 2· HCl
NH 3Cl-
氯 化 苯 铵
医药上利用胺的碱性,将难溶于水的胺类药物制成盐, 增加它的水溶性和稳定性。例如
H2N
COOCH2CH2N(C 2H5)2 + HCl 普鲁卡因 H2N
NH2
+ HNO2 + H2SO4
¼¼H 2SO4 0-5 C
¼
N+
N HSO4- + 2H2O
¼¼ª ¼¼ ò ¼ á ¼
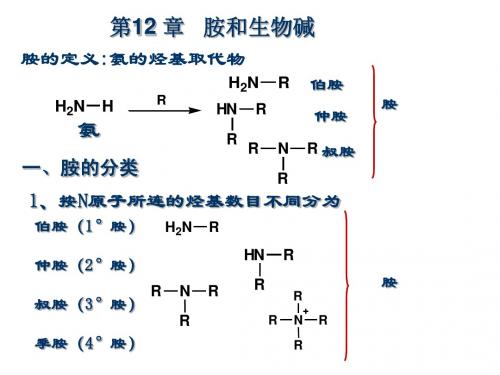
芳香重氮盐的化学反应
重氮盐的化学性质很活泼,主要发生两大类反应: 放出N2的反应;(取代反应) 保留N2的反应;(还原和偶合)
放出氮的反应
¨ ¼¼¼ N2+Cl- + Z
(HSO4 )
命名
(CH3)2NH 简单胺一般以胺为母体,先写出直接与氮原子相连的烃 二甲胺 基的数目和名称,再以胺为结尾。
R2NH 仲胺
CH3NH2
¬© ¼ «
(CH3CH2)2NH
¼¼© «
CH3CH2NHCH (HOCH 3 2CH2)
¼© ª « 甲乙胺 ¼¼¼© «
NH2
methylamine
diethylamine
脂肪仲胺和芳香仲胺与亚硝酸反应,都是在氮 上进行亚硝化, 生成 N-亚硝基化合物。
(CH3CH2)2N-H + HO-NO
(C2H5)2N-NO + H2O
N-亚硝基二乙胺
NHCH3 + HNO2
N=O N CH3 + H2O N-甲基-N-亚硝基苯胺
N-亚硝基胺为中性的黄色油状物或固体,绝大多数不溶于 水而溶于有机溶剂。现已被列为化学致癌物。
+
氯 化 四 甲 铵
C12H25
Br消毒宁
CH3
十二烷基-二甲基-2-苯氧乙基溴化铵
黄连素
抗菌,消炎
生物碱
NHCOCH3
CH3O
CH3O OCH 3 O OCH3
秋水仙碱
抗肿瘤,抗痛风
重氮盐和偶氮化合物
NaNO2 / HCl 0 - 5oC
N N+Cl-
Ar
NH NH 22
Ar
N2 Cl
重氮盐
NaO3S
2-¼ ¬¼ ù -4-© ª¼ ù ¼¼ é
CH3 CH3 CH3-CH-CH2-CH-N-CH2-CH3 CH2-CH3
2-¼ ¬¼ ù -4-(¼ ¼¼© ª¼ ù )¼ ì ¼ é
胺的结构
7N
1s 2s 2p
2
2
3
4个sp 轨道
3
H
N H
H
四面体结构
键长: C-N
0.147nm 0.101nm
成部分共轭体系
胺的物理性质
物态: 低级胺为无色气体或者易挥发的液体,有氨味或鱼腥 味,高级胺为固体。芳胺为高沸点的液体或者固体,有 毒! 水溶解度:胺可与水分子形成氢键,随着烃基在分子中 的比例增大,溶解度下降。因此低级胺可溶于水,高级 胺不溶于水。 熔沸点:胺是极性化合物,而且胺分子之间还可以通过 氢键缔合(叔胺除外),所以胺的熔点和沸点比分子量相近 的非极性化合物高。
N2Cl + H
N(CH3)2
CH3COONa 0-5 C
¼
NaO3S
N=N
N(CH3)2
¼¼ ¬ ù ¼ ¨¼ ¼ á ¼ ì ¼¼¼¼ ª¼« ¼¼ §pH3.1-4.4¼ ¼
偶氮化合物
胺和生物碱
胺类化合物
胺的分类和命名
胺的结构 胺的物理性质 胺的化学性质
分类
按照与氮原子直接连接的烃基的种类可分为 RNH2 脂肪胺(aliphatic amine), ArNH2 芳香胺 (aromatic amine); 按照与氮原子所连接的烃基的数目可分为 RNH2 伯胺primary amine; R2NH 仲胺secondary amine;R3N 叔胺tertiary amine 按照氨基数目的多少可分为 RNH2 一元胺, H2NRNH2 二元胺
+ CuBr
HBr
Br
+ N2 + HBr
Sandmeyer反应
(2)被氰基取代
N2Cl
KCN
+ CuCN
CN
+ N2 COOH
COOH
Gattermann反应
H2O/H+
应用:
H3C
NH2
HOOC
NH2 CH3
N2Cl
HNO2+¼ ¼¼HCl 0-5 C
CN
KCN+CuCN H2O/H+
COOH
O S N(C2H5)2(不溶) O
(C2H5)2NH
由伯胺生成的磺酰胺氮上的氢受磺酰基影响呈弱酸性,可与 碱成盐而溶于水;仲胺形成的磺酰胺氮上无氢,不与碱成盐而 呈固体析出。常利用此反应鉴别三类胺,称为Hinsberg (兴斯堡) 试验法。
磺胺类抗菌药物
N H2N
磺胺嘧啶
SO2NH N
N H 2N SO2NH S
胺类化合物
3 2
H 2 伯胺 CH NH
¬© ¼ «
CH CH NH 3 2 2 (CH3CH2)2NH 乙 胺 ¼ ¼© « CH2NH NH 2
2
NH2
¼© ª «
NH (HOCH 2 2CH2)3N
¼¼¼© «
OH
苯 胺
HO
HO
NH2
苄 胺
HO
HO
多巴胺 Dopamine
去甲肾上腺素 Norepinephrine
季铵盐类
(C2H5)4N OH
+ (C H ) N OH 2氧 5 4 氢 化 四 乙 铵
+ -
CH3 H3 C
O CH3 OH-
N+ CH2CH2O C CH3
乙酰胆碱
氢 氧 化 四 乙 铵 氢氧化四乙铵
(CH3)4N+Cl+ (CH ) N Cl 3四 4甲 氯 化 铵
氯化四甲铵
CH3 PhOCH 2CH2 N
局部麻醉药
COOCH2CH2N(C 2H5)2· HCl 盐酸普鲁卡因
脂肪胺中,伯胺,仲胺,叔胺谁的碱性最强?N上的 R取代基越多,碱性越大?
事实是,在水溶液中,碱性最强的是仲胺。
脂肪胺的碱性强弱是电子效应、立体效应和溶剂 化效应共同综合作用的结果。 1. 电性效应
脂肪胺中的烷基是供电子基, 它使 N 上的电子云密度增 大,而且连接的烃基越多, 电子云密度就越高, 碱性增强。 从电性效应看,碱性顺序应为: R3N > R2NH > RNH2
2.水的溶剂化效应
H O H O H H
H
R N H H
+
H
R R
N
+
H H
O H
R + R N H R
O
H H
O H H
O
H H
溶剂化效应越强,氨离子越稳定。 碱性强弱顺序为:伯胺>仲胺>叔胺
3. 空间效应
N 原子上连接的基团越多越大,对 N 上孤对电子的屏蔽作 用越大, N 上孤对电子与 H+ 结合就越难, 碱性就越弱。从空间 效应看碱性顺序为伯胺>仲胺>叔胺
磺胺噻唑
(五)与亚硝酸的反应
NaNO2 + HCl
HO-N=O + NaCl
亚硝酸
脂肪伯胺与HNO2反应生成极不稳定的脂肪重氮盐。
R-NH2 NaNO2 HCl
R N N Cl
脂肪重氮盐
+
-
N2 ↑ + R+ + Cl醇、烯、卤烃等混合物
该重氮盐即使在低温下也会立即分解放出氮气,并有醇、烯 及卤代烃等混合物的形成。
KMnO4
COOH
¼
CH3
CH3
CH3
COOH
(3)被OH 取代(重氮盐的水解)
H2O / H+
Ar
机理:
N2 X
Ar
OH +
N2
Ar
N2 X
Ar
+ N2 H2O
+
X OH2 - H+ Ar OH
Ar
一般为副反应
可用作制备酚类(产率不高,用 ArN2 SO4H 较好)
(4)被氢原子取代
N2+ Cl+ H3PO2 + H2O
H H
N
甲胺
N-H
。 键角: C-N-H 112.9 C H 3C
三
47nm
01nm
键长: C-N 0.147nm
。 .9 。 .9
H3C H3C
N
CH3
键角: C-N-C
。 108
三甲胺
N
苯胺分子中,苯环上所有未参与杂化的p轨道所形成 的大π键可以和氮原子的未参与成键的 sp3杂化轨道形
肾上腺素
