氨分解制氢课件
氨分解(精)

氨分解制氢
液氨加热至800~850℃,在镍基催化剂作用下,将氨进行分解, 可以得到含75%H2、25%N2的氢氮混合气体: 用此法制得的气体是一种良好的保护气体,可以广泛地应用于半 导体工业、冶金工业,以及需要保护气氛的其他工业和科学研究中。 有汽化器内,电加热元件,氨气减压阀,等主要不部件组成, 用液氨分解来制取保护气体,在工业上是很容易实现的,这是因 为: 1、氨易分解:常压,800~850℃在催化剂作用下,即使空速较 大,氨分解度仍可超过99%。 2、气体精制容易:作为液氨纯度是很高的,其中挥发性杂质只 有少是惰性气体和水分,特别值得注意的是其中含O2极微,同时, 氨分解时不可能有副反应发生。由此可见,氨分解后气体只要设法除 去比较容易除去的少量水分就能得到精制了,半导体工业上所不希望 存在的金属离子cl、CO2等问题都不存在了。 3、原料液氨容易得到。价格低廉,而且原料消耗也比较少(每 公斤氨可产生2.6M3混合气体
气体保护站
氨分解
氨分解气体发生装置以液氨为原料,经汽化后将氨气 加热到一定温度,在催化剂作用下,氨发生分解成氢氮混 合气体,氨分解的化学方程式如 氨分解制氢下:2NH3=3H2+N2-22080卡 即在标 准状况下,1千摩尔氨完全分解可产生氢氮混合气体 44.8Nm,并吸收热量11040千卡。也就是1kg液氨完全分 解能产生2.64Nm氢氮混合气体,根据化学方程式,分解 气体由75%H2,和25%N2组成。 氨分解制氢装置是根 据氨气发生分解反应的基本原理进行精心设计制作的组合 装置。 氨分解在工业装置条件下不可能100%完全分 解,存在微量的残余氨,工业液氨中含有少量的水,配套 使用气体纯化器,可脱除混合气中的残余氨和水分,获得 满意的保护气体,满足工业生产的需要(如对杂质氧有较 高要求,还可在纯化器中增加除氧器)。 以该产品 气的混合气氛直接作还原保护气氛,是需要氢气作保护气 氛场合最经济的方法。该产品也可作为富氢原料气,提取 纯氢,是一种经济的制氢方法。
《制氢学习》课件

3 化石燃料重整法
利用化石燃料进行重整反应产生氢气。
4 生物制氢法
利用微生物或酶的作用产生氢气。
制氢的应用
加氢制氢
将氢气与其他物质反应,如加 氢裂解重油。
催化制氢
利用催化剂加速制氢反应速率, 提高氢气产量。
燃料电池等领域中的 应用
介绍燃料电池、氢能源汽车等 领域中氢气的应用。
制氢的发展前景
1
国内外制氢的现状和发展趋势
分析国内外制氢技术的现状和未来发展趋势。
2
制氢技术的市场前景及产业化
探讨制氢技术在市场上的潜力和产业化的可能性。
3
结语
总结制氢技术的应用前景,并展望未来制氢技术的发展。
《制氢学习》PPT课件
# 制氢学习
制氢的概述
制氢的意义和现状
探索制氢技术的重要性及全球现状,解决能源和环境问题。
制氢的分类和原理
介绍制氢方法的分类和基本原理,如热分解法、电解法等。
制氢的方法
1 热分解法
通过高温加热将物质分解产生氢气,适用于 可性材料。
2 电解法
利用电流将水分解成氢气和氧气,是最常用 的制氢方法。
氨分解制氢工艺技术规程
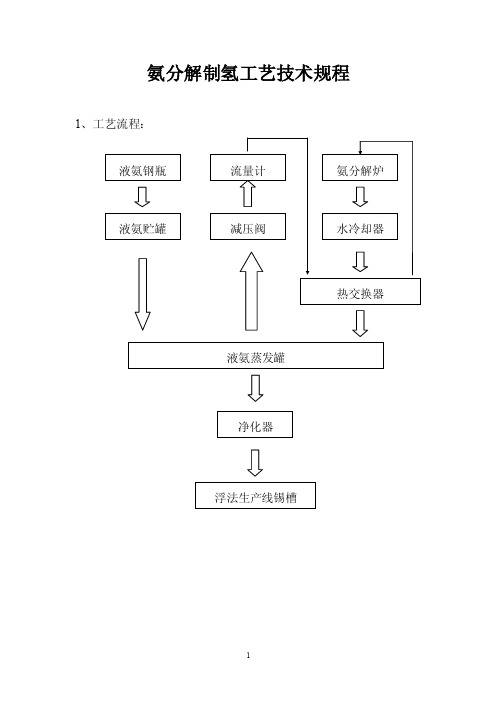
氨分解制氢工艺技术规程1、工艺流程:2.工艺技术指标:2.1氢气送往锡槽的压力~0.20Mpa2.2氢气送往锡槽的流量0~90m3/h(分解气 0~120 m3/h)2.3氢气残氧量≤5ppm2.4氢气残氨量≤2ppm2.5氢气露点温度≤-60℃3.工艺技术要求:3.1原料液氨必须符合GB536-65液体合成氨的一级品纯度的要求。
3.1.1液氨(NH3)≥99.8%3.1.2水分、油含量≤0.2%3.2脱硫器、净化器应装满吸附剂。
脱硫吸附剂应采用活性炭,净化吸附剂采用5A分子筛。
3.3分解炉应装满催化剂,催化剂采用镍基催化剂。
3.4工艺系统所有的容器及管路应无焊渣、铁锈、油污。
耐压强度试验和气密性试验应达到要求。
3.5安全阀以及报警系统、自控系统、电器、仪表、仪器、机器、装置应能正常工作。
3.6空置的液氨系统在充注液氨前应用纯度为≥99.9%的氮气吹扫置换里面的空气,当各吹扫出口的氮气纯度≥99.9%时为合格。
3.7工艺气路系统在开车前或停车后应用纯度≥99.9%的氮气吹扫置换,当各吹扫出口的氮气纯度≥99.9%时为合格。
3.8分解系统的冷却器在开车前要同入冷却水,冷却水出口应有适量的水流出。
运行中不能中断冷却水。
冬季如果停车时间较长,要放净冷却器的存水。
3.9液氨容器灌装液氨量最多不能超过容器的80%,在密闭状态下,其周围环境温度最高不能超过50℃,容器中压力最高不能超过1.96Mpa。
3.10液氨系统在工作时,压力应控制在0.3~0.7Mpa,氨气减压阀后的压力应控制在0.20 Mpa.3.11分解炉的工作温度应控制在800~850℃之间。
3.12新催化剂在第一次使用前要经过还原活化,活化可在分解炉内用纯度≥99.8%的氨气或钢瓶氢气进行。
3.13在还原活化催化剂时,要严格控制气体流量和升温速度,以保证催化剂充分活化。
具体事项按表1的技术要求进行。
表13.14出分解炉的气体残氨量应≤1000ppm(V)。
制氢技术ppt课件
2.5 其他制氢方法
烃类分解生成氢气和炭黑
生成的炭黑可以用于橡胶工业、着色剂、抗静电剂、复 印色粉及黑色染料等。 ❖ 热裂解法
CnHm----n C + m/2 H2 ❖ 等离子体法 a. 采用氢气为等离子体气。 b. 原料的适应性强,几乎所有的烃都可作制氢原料。 c. 过程的热量可回收发电,能耗有所降低。
床气化炉和Texaco加压气流床气化炉。制得的氢主要 用于合成氨工业。 2)煤炭地下气化生产原料气 将地下的煤直接进行有控制地燃烧,通过对煤的热作用及 化学作用而产生可燃气体。集建井、采煤、地面气化 三大工艺为一体,省去庞大的工艺设备。“第二代采 煤方法”
气体原料制氢
❖ 天然气水蒸气重整制氢 CH4+H2O----CO+3H2-206KJ CO+H2O----CO2+H2+41KJ 需要吸收大量的热,反应温度为650~850度,反应管出口
第二章 制氢
L/O/G/O
目前的制氢方法有哪些?
热化学 制氢
化石能 源制氢
电解水制 氢
氢气
其它制氢 方法
生物质 制氢
2.1 氢气的实验室制法
2.1 氢气的实验室制法
2.2 用水制氢
❖ 水电解制氢目前占总产量的4%,工艺过程简单,无污染,但 消耗电量大,每立方米氢气电耗为4.5—5.5 kWh,电解水制氢 主要用于工业生产中要求纯度高,用氢量不多的工业企业。
1)开发新的热源---热化学制氢过程需要消耗水和热,热 源是关键。核能是今后最有希望的热源;太阳能亦可 产生600-800℃ 的高压过热蒸汽。
2)热化学制氢面临的技术挑战 反应过程的控制,以及中间产物的分离。 3)热化学制氢的材料难题——耐酸以及高温材料的研究
氨分解说明书

氨分解说明书(总7页) -CAL-FENGHAI.-(YICAI)-Company One1-CAL-本页仅作为文档封面,使用请直接删除第一部分氨分解部分一、化工原理:1摩尔氨气在一定的压力和温度及镍触媒催化作用下可分解为1.5摩尔的氢气和0.5摩尔的氮气并吸收一定的热量。
气化学方程式如下。
2NH3→3H2+N2-Q二、氨分解制氢的优点:用此法制得的气体是一种良好的保护气,可以广泛的应用于半导体工业,冶金工业及需要保护气氛的其他工业中。
氨分解制取保护气体在工业上是很容易实现的,这是因为1、氨易分解,压力不高,在触媒催化作用下,温度控制在800~850度时,氨可大部分分解。
2、气体精炼容易:作为原料的液态氨纯度很高,其中挥发性杂质只有溶解在液氨中的少量惰性气体和水分,几乎不含氧,同时,在此条件下,氨分解是不可逆的,由此可见,氨分解后采取适当的方法就可除去少量水分得到精制的氢氮混合气。
3、在我国,原料氨容易得到。
价位低廉,而且分解氨耗电比较少。
三、工艺流程:氨瓶中氨经过氨阀控制后通过气化器气化,进入热交换器与分解气进行热交换后送入分解炉,分解炉内装有活化过的镍触媒,在800~850度下氨分解成氢,氮混合气体,分解后的高温混合气体进入热交换器内与气态氨进行热交换,此时分解气降温,同时气态氨回收热量并升温,热交换后的分解气经冷凝器冷却后送往干燥气四、技术指标:1、额定产气量: 50立方米/小时2、气体纯度露点≤-103、分解炉操作温度 800~850C4、分解炉额定功率 45kw5、额定氨耗 20kg/h6、冷却耗量 2.5立方米/小时7、电源 50Hz 380V8、设备总重 3500kg五、操作方法:1 、原始开车:1)仔细阅读使用说明书,熟悉设备的原理和构造。
2)检查气,电各系统是否通畅,消除泡,冒,点,漏,并接通电源。
3)镍触媒的活化:分解炉内装的镍触媒在出厂时已经还原,但因设备在运输,库存期间总有水分,氧气等介入,触媒活性略有下降,因此原始开车时要进行触媒的活化。
制氢工艺技术PPT课件

-
17
-
15
低变催化剂
低变催化剂主要组分为Cu0,添加Zn0、Al203,、Cr203等。 催化剂毒物主要是硫、氯,水、氨也有影响。硫主要来自 原料气,它会与催化剂活性表面的铜晶粒发生化学吸附和 反应而影响活性。研究表明,氯比硫的毒害严重,氯离子 来自蒸汽和原料气,对低变催化剂的毒害是与Cu、Zn0生 成了Cu7Cl4(OH)10(H2O)、ZnCl2·4Zn(OH)2等组成的低熔 点而有挥发性的表面化合物,使Zn0失去间隔体作用,铜 微晶迅速长大,破坏了催化剂的结构,使活性大大下降。 加之生成的氯化物易溶于水,在湿气条件下,氯化物会沿 床层迁移,毒害更多催化剂。凝聚水和氨可以使催化剂中 铜微晶生成铜氨络合物,使催化剂中毒和侵蚀
-
14பைடு நூலகம்
中温变换催化剂
中变催化剂化学组分为Fe2O3、Cr203、K2O, 使用时被还原为有活性的Fe3O4,催化剂
毒物为硫、磷、硅等。但中变催化剂受毒 物影响较小,如原料气硫含量达到0.1%时 才使Fe3O4转变为FeS,使活性稍有下降, 为新剂的70%~80%。工艺蒸汽中含杂质
过多时会与原料气组分反应,使催化剂结 皮而降低活性
-
5
氢气的化学性质
氢能与很多物质进行化学反应,在进行化学反 应形成化合物时其价键具有特征。氢原子失去 其ls电子就成为H+离子,实际上就是氢原子核 或质子。质子的半径比氢原子的半径要小许多 倍,使质子有相对很强的正电场。因此它总是 同别的原子或分子结合在一起形成新的物质。 如加氢反应就是将氢气加到各种化合物上的反 应。如甲烷化反应:
-
16
甲烷化催化剂
催化剂的主要化学组分为Ni0、Al203,使用时还原为金 属镍。主要毒物为硫、砷、钒、碳酸钾和羰基镍等。对 于甲烷化催化剂,硫是永久性毒物,这是因为操作温度 较低,活性镍一旦与硫化氢生成Ni2S3后,即使除去H2S, 也无法被氢气再还原为活性状态。研究表明,甲烷化催 化剂中吸硫达到0.15%~0.2%时活性丧失50%,若达到 0.5%则活性全部丧失。希望进甲烷化催化剂的原料气中 硫含量越低越好,一般要小于0.1ppm。甲烷化工序设在 脱碳之后,各种脱碳液带入均会造成不同的毒害。砷是 永久性毒物,催化剂中砷含量达到0.1%时便严重失活。 甲烷化催化剂在150℃以下操作时,活性镍与一氧化碳 会反应生成羰基镍Ni(CO)4,这是对人剧毒的挥发物, 还造成催化剂中镍的流失,严重降低活性。因此,在床 层降温至150℃以下时不能再通工艺气,应改用氮、氢 气氛
《制氢工艺技术》课件

目 录
• 制氢工艺技术概述 • 制氢工艺的主要类型 • 制氢工艺技术的经济性分析 • 制氢工艺技术的发展趋势与展望
01
制氢工艺技术概述
氢气的性质与用途
氢气的性质
氢气是一种轻质、易燃易爆、无色无 味的可燃气体,具有很高的热值和能 量密度。
氢气的用途
氢气是重要的工业原料,广泛应用于 化工、石油、冶金等领域,同时也是 燃料电池的主要燃料。
环境压力
传统化石能源的使用对环境造成了巨大的压力, 发展制氢技术有助于减少温室气体排放,缓解环 境压力。
产业升级
制氢技术的发展对于推动相关产业升级和转型具 有重要意义,能够带动一系列产业链的发展。
02
制氢工艺的主要类型
天然气制氢
天然气蒸汽转化制氢
将天然气与水蒸气在高温下反应,通过转化反应将天然气转 化为氢气和一氧化碳的混合气体,再通过一氧化碳变换反应 进一步制取高纯度氢气。
制氢技术的经济性评价方法
投资回收期法
通过计算投资回报率来评估技术的经济性。
净现值法
考虑资金的时间价值,通过比较不同方案的 净现值来选择最优方案。
内部收益率法
计算投资方案的内部收益率,以评估其盈利 能力。
制氢工艺技术的经济性比较与选择
1
比较不同制氢技术的成本与效益,选择经济性更 优的方案。
2
考虑环境影响,权衡经济效益与环境成本。
开发新型反应器结构
研究新型反应器结构,提高反应器的传热、 传质性能。
加强副产物的回收与利用
副产物分离与回收
研究高效的副产物分离和回收技术, 提高副产物的回收率。
副产物资源化利用
将副产物转化为有价值的资源,实现 副产物的资源化利用。
氢的制备与储存技术ppt演示课件

5.各种化工过程副产氢气的回收
多种化工过程如电解食
盐制碱工业、发酵制酒 工艺、合成氨化肥工业、 石油炼制工业等均有大 量副产氢气,如能采取 适当的措施进行氢气的 分离回收,每年可得到 数亿立方米的氢气。这 是一项不容忽视的资源, 应设法加以回收利用。
氢回收工厂
13
二、氢的储存
14
氢可以气态、液态和固态3种方式进 行储存。
氢储存装置
16
3、而利用吸氢材料与氢气反应生成固溶体和 氢化物的固体储氢方式,能有效克服气、 液两种储存方式的不足,而且储氢体积密 度大、安全度高、运输方便、操作容易, 特别适合于对体积要求较严格的场合,如 在燃料电池汽车上的使用。
17
目前,有希望达到或接近该要求的材 料有3大系列: a.镁基合金材料; b.碳基材料; c.络合物储氢材料。
7
(3)以重油为原料部份氧化法制取 氢气
重油原料包括有常压、
减压渣油及石油深度加 工后的燃料油。重油与 水蒸汽及氧气反应制得 含氢气体产物。
该法生产的氢气产物成
本中,原料费约占三分
之一,而重油价格较低,
故为人们重视。
我国建有大型重油部份
氧化法制氢装置,用于
氢气氨分解炉
制取合成氨的原料。
8
3.生物质制氢
生物质资源丰富,是重要的可再生能源。 生物质可通过气化和微生物制氢。
9
(1)生物质气化制氢
将生物质原料如薪柴、锯未、麦秸、稻草 等压制成型,在气化炉(或裂解炉)中进 行气化或裂解反应可制得含氢燃料气。
10
(2)微生物制氢
利用微生物在常温常压下进行酶催化反应 可制得氢气。
11
4.其它含氢物质制氢
1、气态方式较为简 单方便,也是目前储 存压力低于17 MPa 氢气的常用方法,但 体积密度较小是该方 法最严重的技术缺陷, 另外气态氢在运输和 使用过程中也存在安 全隐患。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
生产过程中的危险、有害因素
1、火灾爆炸
氨分解制氢生产过程中存在的氢气火灾危险性分类为甲 类,氨的火灾危险性分类为乙类,这些物质与氧化剂接触 遇到火源时有发生火灾爆炸的危险,引火源包括明火、高 热、摩擦或撞击火花、电气火花、静电火花、雷电等。存 在氨(液氨)、氢气的设备、管道、阀门损坏或法兰连接 处密封不严造成氢气、氨气的泄漏;开停车过程中若设备 及管道未用惰性气体置换,或置换不合格;装置无防雷防 静电接地设施或设施有缺陷;操作人员进入作业场所穿化 纤衣物、带铁钉鞋或用钢质工具敲打设备;电气设施、电 缆电线出现过负荷、过电流、过热、漏电、短路等情形, 均有可能引发火灾、化学爆炸事故。
氨分解制氢 安全生产知识
培训
张会林 河北国泰安全评价有限公司
氨分解
氨(气态)在一定温度下,经催化剂作用下裂解为 75%的氢气和25%的氮气,并吸收21.9千卡热量,其 主要反应为: 2NH3→3H2+N2-21.9千卡
整个过程因是吸热膨胀反应,提高温度有利于氨裂解 ,同时它又是体积扩大的反应,降低压力有利于氨的 分解,氨分解制氢设备为使用最佳状态。
(2)与氧化剂、酸类、卤素、食用化学品分开 存放,切忌混储。储罐远离火种、热源。采用 防爆型照明、通风设施。禁止使用易产生火花 的机械设备和工具。储存区应备有泄漏应急处 理设备。
(3)液氨气瓶应放置在距工作场地至少 5m 以 外的地方,并且通风良好。
(4)注意防雷、防静电,厂(车间)内的氨气储罐 应按《建筑物防雷设计规范》(GB 50057)的 规定设置防雷、防静电设施。
12
4、灼烫
灼烫包括化学灼伤、高温烫伤、低温冻伤等。
生产过程中使用液氨如发生泄漏接触或进入人体, 会使皮肤、器官、眼睛受到化学灼伤的伤害。
氨分解炉内温度高达870℃,若隔热保温措施不 良或高温物料泄漏,有可能造成人员高温烫伤事 故。
液氨发生泄漏接触人体会因其温度较低且气化时 吸收热量造成局部过冷导致人员低温冻伤。
3、中毒和窒息 氨分解制氢原料氨,属于有毒物质,低浓度氨对粘 膜有刺激作用,高浓度氨可造成组织溶解坏死,可 引起发射性呼吸停止。如果生产装置、设备、容器、 管道密封不良或违章检修、操作失误等造成氨外溢、 泄漏、若通风不良、防护不当或处理不及时,则有 可能发生中毒、窒息事故。 生产过程中产生的氮气属于窒息性气体,若发生大 量泄漏致使作业环境空气重氮浓度过高时,可能发 生功能作业人员窒息事故。
避免与氧化剂、酸类、卤素接触。 生产、储存区域应设置安全警示标志。在传送过程中,钢瓶和
容器必须接地和跨接,防止产生静电。搬运时轻装轻卸,防止钢 瓶及附件破损。禁止使用电磁起重机和用链绳捆扎、或将瓶阀作 为吊运着力点。配备相应品种和数量的消防器材及泄漏应急处理 设备。 【特殊要求】 【操作安全】 (1)严禁利用氨气管道做电焊接地线。严禁用铁器敲击管道与阀 体,以免引起火花。
(2)在含氨气环境中作业应采用以下防护措施: ——根据不同作业环境配备相应的氨气检测仪及
防护装置,并落实人员管理,使氨气检测仪及 防护装置处于备用状态; ——作业环境应设立风向标; ——供气装置的空气压缩机应置于上风侧; ——进行检修和抢修作业时,应携带氨气检测仪 和正压式空气呼吸器。 (3)充装时,使用万向节管道充装系统,严防 超装。 【储存安全】 (1)储存于阴凉、通风的专用库房。远离火种、 热源。库房温度不宜超过 30℃。
工作场所浓度超标时,操作人员应该佩戴过滤式防毒 面具。可能接触液体时,应防止冻伤。
储罐等压力容器和设备应设置安全阀、压力表、液位计、温度
计,并应装有带压力、液位、温度远传记录和报警功能的安全装 置,设置整流装置与压力机、动力电源、管线压力、通风设施或 相应的吸收装置的联锁装置。重点储罐需设置紧急切断装置。
涉及的主要设备
1、液氨储罐(或者液氨钢瓶) 2、 气化器 3、氨分解制氢炉
氨分解制氢装置的用途
1、应用于黑色、有色、机械行业的板带材、线材盘管 材和标准件等材料的光亮退火中的保护气。
2、应用于粉末冶金、钨钼材料、硬质合金、电子材料 等的烧结工序。
3、应用于浮法玻璃生产中锡槽保护气。 4、应用于高温耐火材料烧结。 5、应用于化工行业中作还原气。
2020/3/2
安全标准化
14
事故案例
(1)事故经过 2010年7月24日,某公司氮化使用的液氨气体发生泄漏, 现场操作人员试图关闭液氨气瓶阀门,但刚接近泄漏区 域,即感到眼睛受到强烈刺激,无法呼吸,因此而无法 将仍在漏出液氨气体的气瓶阀门关闭,使得液氨继续向 外泄漏,情况万分危急,因为液氨气瓶所处位置是在生 产厂房内部,离泄漏点不足10米处便是热处理加热电炉, 连续产生明火,一旦泄漏的液氨气体达到爆炸浓度,遇 到明火便会发生剧烈爆炸,后果将不勘设想。这时,操 作人员便立即报告了公司领导,公司领导也试图进入现 场关闭阀门,无奈根本无法接近,见此情景,公司领导 立即拨打总公司消防队电话,并讲明了事态的情况,要 求携带空气呼吸器进行救援,三分钟之内,消防队赶到 现场,消防队员带上空气呼吸器进入泄漏现场实施关闭 阀门作业,但由于对阀门结构不熟悉而失败,便将空气 呼吸器由操作人员佩戴进入现场将气瓶阀门关闭,从而 制止了液氨气体的进一步泄漏,避免了一起重大爆炸事 故的发生。
涉及的危险化学品
氨的理化性质:
外观与性状:无色有刺激性恶臭的气体。
熔点(℃): -77.7
相对密度(水=1): 0.82(-79℃) 沸点(℃): -33.5
相对密度(空气=1): 0.6 饱和蒸汽压(kPa):06.62(4.7℃)
燃烧热(kJ/mol): 无资料
临界温度(℃): 132.5
临界压力(MPa): 114.0
2、物理爆炸 氨分解制氢生产过程中涉及的压力容器或压力管 道有可能因操作失误或设备故障发生超压导致物 理爆炸。如冷却水系统发生故障(水压小、断水、 管路结垢堵塞等),使氨分解炉不能及时冷却从 而造成超温超压可能导致爆炸事故;液氨储罐、 液氨中间罐、氨气化器、净化装置吸附桶等压力 容器上安全阀、压力表等安全附件失灵,致使使 用压力超过设计工作压力或储罐充装量过大时可 能导致容器爆炸;液氨钢瓶暴晒,造成压力过高, 也能发生爆炸;系统停电或温度控制系统失灵等 原因致使液氨剧烈气化导致压力迅速升高从而导 致容器爆炸;选材不当或存在焊接缺陷、腐蚀、 疲劳超期使用等致使容器承压能力降低可能造成 容器超压爆炸。
2020/3/2
氮的理化性质:
外观与性状:无色无臭气体。 熔点(℃): -209.8 相对密度(水=1): 0.81(-196℃) 沸点(℃): -195.6 相对密度(空气=1): 0.97 饱和蒸汽压(kPa):1026.42(-173℃) 临界温度(℃): -147 临界压力(MPa): 3.40 溶解性:微溶于水、乙醇。
闪点(℃):气体。低于0℃下闪点不确定;有时难以点燃 。 引燃温度(℃): 651
爆炸下限[%(V/V)]: 15.7 爆炸上限[%(V/V)]:温常压下1体积水可 溶解700倍体积氨。
氢的理化性质:
外观与性状:无色无臭气体。 熔点(℃): -259.2 相对密度(水=1): 0.07(-252℃) 沸点(℃): -252.8 相对密度(空气=1): 0.07 饱和蒸汽压(kPa): 13.33(-257.9℃) 燃烧热(Kj/mol): 241.0 临界温度(℃): -240 临界压力(MPa): 1.30 引燃温度(℃): 400 爆炸下限[%(V/V)]: 4.1 爆炸上限[%(V/V)]: 74.1 最小点火能(mJ): 0.019 最大爆炸压力(MPa): 0.720 溶解性:不溶于水,不溶于乙醇、乙醚。
④未装设减压阀;
⑤事故发生时正值夏季高温季节,当天使用的气瓶又是刚换 的满瓶,后经调查,气瓶存在过量充装情况,二者叠加, 气瓶内部压力会显著增高,也是事故发生的诱因;
⑥连接胶管人员不熟悉连接技术,未可靠固定连接点。
(3)事故的纠正与预防措施 1)使用专用高压软管,采取螺纹连接的方式,使连接可 靠。 2)按取用气相气体的要求放置气瓶,并妥善固定。事故 发生后,对液氨钢瓶的结构进行了仔细的研究,D800液氨 钢瓶的结构如图(见下图6.2-2)所示,图中钢瓶的一端有 二只阀门,分别与钢瓶内部二根导气管相连接,图中上部 的一根为气相导管,下部的一根为液相导管,因此,在气 瓶放置时,必须使两只阀门的连线与地面垂直,并且取用 气体的连接管接在上部阀门上,这样从气瓶供出的气体即 为气相气体,而下部阀门为液相气体,如果气瓶位置旋转 90度,二只阀门连线与地面呈水平状态时,其供出的气体 将均为液相气体。 3)在气瓶气体输出阀门之后安装液氨专用减压阀,降低 气体输出压力。 4)实施管道连接时应有专人负责,避免不熟悉人员连接 时产生连接缺陷。
重点监管的危险化学品措施
1、氨
【一般要求】 操作人员必须经过专门培训,严格遵守操作规程,熟
练掌握操作技能,具备应急处置知识。 严加密闭,防止泄漏,工作场所提供充分的局部排风
和全面通风,远离火种、热源,工作场所严禁吸烟。 生产、使用氨气的车间及贮氨场所应设置氨气泄漏检
测报警仪,使用防爆型的通风系统和设备,应至少配备两 套正压式空气呼吸器、长管式防毒面具、重型防护服等防 护器具。戴化学安全防护眼镜,穿防静电工作服,戴橡胶 手套。
2020/3/2
安全标准化
19
安全技术措施
主要依据: 《液氨泄漏的处理处置方法》HGT 4686-2014 《爆炸危险环境电力装置设计规范》GB 50058-2014 《石油化工可燃气体和有毒气体检测报警设计规范》
GB 50493-2009 《工作场所有毒气体检测报警装置设置规范》GBZT
223-2009 《重点监管的危险化学品名录》2013年版 《国务院安委会关于深入开展涉氨制冷企业液氨使 用专项治理的通知》
5)将气瓶搬离主厂房,设置气瓶专用间,设置雾化 喷淋系统,一旦泄漏可开启水雾喷淋,以吸收氨气。
