高中化学必修二第一章复习课件 PPT
合集下载
人教版高中化学必修二课件:1.1《元素周期表》(共37张PPT)

2KI+Br2 = I2+2KBr 静置后,液体分层, 氧化性: Br2 > I2
上层 无色 ,
下层 紫色 。
结论
氧化性:Cl2 > Br2 > I2 还原性:I - > Br - > Cl 小结: 氧化性:F2> Cl2> Br2>I2 还原性:F-> Cl- > Br- > I-
氧化性:F2> Cl2> Br2>I2。 Cl2可从溴、碘的盐 溶液中置换出相应的卤素单质,F2与氯、溴、 碘的盐溶液可以置换出相应的卤素单质吗?
H2+F2 = 2HF H2+Cl2 = 2HCl 暗处剧烈反应并爆炸;HF很稳定 光照或点燃反应;HCl较稳定
H2+Br2 = 2HBr
H2+I2
加热500℃ ,HBr不稳定
2HI 需不断加热,HI同时分解
■都能跟氢气反应,体现相似性 反应通式:H2 + X2 = 2HX (X= F、Cl、Br、I) ■单质氧化性减弱,体现递变性
① 除9、10、18纵行(列序)外,族序数=列序个位数。(记忆方法) ②18个纵行,只16个族;0族和第VIII族不属主族,也不属副族。
一、碱金属元素结构和化学性质的相似性和递变性
Li Na K Rb Cs
1.相似性:
最外层上都只 有一个电子 2.递变性: 核电荷数↑ 电子层数↑ 原子半径↑ 失电子能力↑ 化学性 质相似
3.请在下面的线框中用色笔画出周期表的轮廓。并标出族序数,写
出七个主族元素(可参考课本)和 0族元素的元素符号。
周期 ⅠA ⅡA ⅢB ⅣB ⅤB ⅥB VIIB
IB IIB ⅢA ⅣA ⅤA Ⅵ AⅦA 0 种类
人教版高中化学必修二第一章第三节《化学键》课件(共38张PPT)
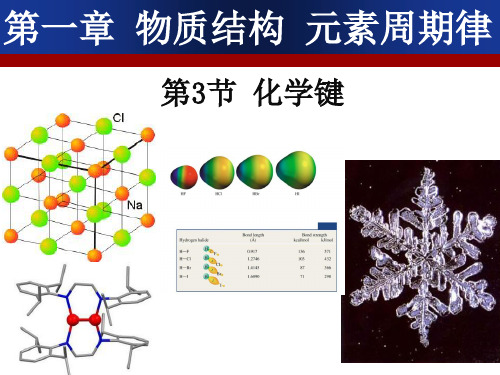
活泼的金属元素和酸根离子形成的盐 把NH4+看作是活泼的金属阳离子
金属氧化物:Na2O,Al2O3等
强碱:NaOH Ba(OH)2等
如何表示氯化钠的形成过程--电子式
•资料卡片
电子式 为方便起见,我们在 元素符号周围用“ · ”或 “×”来表示原子的最外 层电子(价电子)。这种 式子叫做电子式。例如:
归纳:分子间作用力与化学键的比较
作用微粒 作用力大小
意义
化学键 相邻原子间 作用力大 范德华力 分子之间 作用力小
影响化学性质和 物理性质
影响物理性质 (熔沸点等)
一些氢化物的沸点
讨论: 为什么HF、H2O和NH3的沸点会反
常呢?
2.氢键
1)形成条件:原子半径较小,非金属性很强的 原子(N、O、F)与H原子形成强极性共价键 ,与另一个分子中的半径较小,非金属性很强 的原子Y (N、O、F),在分子间H与Y产生
1.原子、离子都要标出最外层电子,离子须标明 电荷;
2.阴离子要用方括号括起来;
3.相同的原子可以合并写,相同的离子要单个写 ;
4.不能把“→”写成“====”;
⑴ 用电子式表示氧化镁的形成过程 ⑵ 用电子式表示硫化钾的形成过程
氢气在氯气中燃烧
写出该过程的化学方程式和实验现象 思考:活泼的金属元素和活泼非金属元素化 合时形成离子键。请思考,非金属元素之间 化合时,能形成离子键吗?为什么?
较强的静电吸引,形成氢键
2)表示方法:X—H…Y—H(X.Y可相同或不 同,一般为N、O、F)。
3)氢键能级:比化学键弱很多,但比分子间作 用力稍强
特征:具有方向性。
氢键作用:使物质有较高的熔沸点(H2O、HF 、 NH3) 使物质易溶于水
金属氧化物:Na2O,Al2O3等
强碱:NaOH Ba(OH)2等
如何表示氯化钠的形成过程--电子式
•资料卡片
电子式 为方便起见,我们在 元素符号周围用“ · ”或 “×”来表示原子的最外 层电子(价电子)。这种 式子叫做电子式。例如:
归纳:分子间作用力与化学键的比较
作用微粒 作用力大小
意义
化学键 相邻原子间 作用力大 范德华力 分子之间 作用力小
影响化学性质和 物理性质
影响物理性质 (熔沸点等)
一些氢化物的沸点
讨论: 为什么HF、H2O和NH3的沸点会反
常呢?
2.氢键
1)形成条件:原子半径较小,非金属性很强的 原子(N、O、F)与H原子形成强极性共价键 ,与另一个分子中的半径较小,非金属性很强 的原子Y (N、O、F),在分子间H与Y产生
1.原子、离子都要标出最外层电子,离子须标明 电荷;
2.阴离子要用方括号括起来;
3.相同的原子可以合并写,相同的离子要单个写 ;
4.不能把“→”写成“====”;
⑴ 用电子式表示氧化镁的形成过程 ⑵ 用电子式表示硫化钾的形成过程
氢气在氯气中燃烧
写出该过程的化学方程式和实验现象 思考:活泼的金属元素和活泼非金属元素化 合时形成离子键。请思考,非金属元素之间 化合时,能形成离子键吗?为什么?
较强的静电吸引,形成氢键
2)表示方法:X—H…Y—H(X.Y可相同或不 同,一般为N、O、F)。
3)氢键能级:比化学键弱很多,但比分子间作 用力稍强
特征:具有方向性。
氢键作用:使物质有较高的熔沸点(H2O、HF 、 NH3) 使物质易溶于水
人教版高中化学必修二第一章完整ppt课件

第一章 物质结构 元素周期律 第一节 元素周期表
ppt精选版
1
第1课时 元素周期表
ppt精选版
2
学习目标
1.简单了解元素周期表的发展历程。 2.了解元素周期表的编排规则及结构。 3.能描述元素在元素周期表中的位置。
ppt精选版
3
一、元素周期表的完善历程 1. 第一张元素周期表 (1)时间 1869 年,俄国化学家门__捷__列__夫__绘制出第一张元素周期 表,是化学发展史上的重要里程碑。 (2)编排原则 ①将元素按照_相__对__原__子__质__量_____由小到大依次排列。 ②将_化__学__性__质_相似的元素放在一个纵行。
答案:C
ppt精选版
28
解析:考查元素周期表的结构。对主族元素,其族序数 等于最外层电子数,但副族则不是;18 列构成 16 个族,其 中第Ⅷ族包含 3 列。
ppt精选版
29
3. 已知某离子的结构示意图为 的是( )
A. 该元素位于第二周期第ⅡA 族 B. 该元素位于第二周期第Ⅷ族 C. 该元素位于第三周期第ⅡA 族 D. 该元素位于第三周期 0 族
ppt精选版
18
4. 确定该元素在周期表中的位置,形式为“第几周期第 几族”,要注意分清主族、副族、0 族、第Ⅷ族
在应用上述方法推断元素的族序数时,要特别注意第 六、七周期第ⅢB 族的锕系和镧系元素,它们的每个空格都 有 15 种元素,其后的元素需再减去 14,然后定位。
ppt精选版
19
例 2 俄罗斯科学家用含 20 个质子的钙的一种原子轰击 含 95 个质子的镅原子,结果 4 次成功合成 4 个第 115 号元 素的原子。这 4 个原子生成数微秒后衰变成第 113 号元素。 下列有关叙述正确的是( )
ppt精选版
1
第1课时 元素周期表
ppt精选版
2
学习目标
1.简单了解元素周期表的发展历程。 2.了解元素周期表的编排规则及结构。 3.能描述元素在元素周期表中的位置。
ppt精选版
3
一、元素周期表的完善历程 1. 第一张元素周期表 (1)时间 1869 年,俄国化学家门__捷__列__夫__绘制出第一张元素周期 表,是化学发展史上的重要里程碑。 (2)编排原则 ①将元素按照_相__对__原__子__质__量_____由小到大依次排列。 ②将_化__学__性__质_相似的元素放在一个纵行。
答案:C
ppt精选版
28
解析:考查元素周期表的结构。对主族元素,其族序数 等于最外层电子数,但副族则不是;18 列构成 16 个族,其 中第Ⅷ族包含 3 列。
ppt精选版
29
3. 已知某离子的结构示意图为 的是( )
A. 该元素位于第二周期第ⅡA 族 B. 该元素位于第二周期第Ⅷ族 C. 该元素位于第三周期第ⅡA 族 D. 该元素位于第三周期 0 族
ppt精选版
18
4. 确定该元素在周期表中的位置,形式为“第几周期第 几族”,要注意分清主族、副族、0 族、第Ⅷ族
在应用上述方法推断元素的族序数时,要特别注意第 六、七周期第ⅢB 族的锕系和镧系元素,它们的每个空格都 有 15 种元素,其后的元素需再减去 14,然后定位。
ppt精选版
19
例 2 俄罗斯科学家用含 20 个质子的钙的一种原子轰击 含 95 个质子的镅原子,结果 4 次成功合成 4 个第 115 号元 素的原子。这 4 个原子生成数微秒后衰变成第 113 号元素。 下列有关叙述正确的是( )
人教版高中化学必修二第一章第一节 《元素周期表 》课件(共15张PPT)

B.原子的核外电子数
C.原子核内的质子数
√D.原子的中子数
1.原子序数为 x 的元素位于第IA族,那么原子序 数为 x+2 的元素肯定不会在( )
√ A.第 IA 族 B.第ⅢB族 C.第ⅢA族 D.0族
【提示】若x为氢元素,则A正确;若x为锂或钠, 则C正确;若x在第4、5、6、7周期,则B项正确。 故答案为D。
3.第ⅠA族和0族元素的原子序数
4.每周期元素的种数
一、元素周期表的结构 “三短”“四长”;“七主”“七副”“0族和Ⅷ族” 二、元素原子结构与其在周期表中位置的关系.
周期序数=电子层数 主族序数=最外层电子数
原子序数
核外电子排布
周期表中位置
1.不能作为元素周期表中元素排列顺序的依据是
A.原子的核电荷数
螺旋式元素周期表
金字塔式元素周期表
1869年,俄国化学家门捷列夫将 元素按照相对原子质量由小到大 依次排列,制出了第一张元素周 期表,这就是现代元素周期表的 雏形。
第一章 物质结构 元素周期律
第一节 元素周期表
【思考与交流】
周期表的结构
阅读教材P4、5页并结合周期表,讨论以下问题
1.元素周期表的编排原则是什么?周期表有多 少横行,多少纵行,多少族?
A.若X是氢,则Y是氦
√C.若X是氟,则W是硫
B.若Y是氦,则Z是钠 D.若Y是氟,则Z是铝
例.已知某主族元素的原子结构示意图如下,判断 其位于第几周期,第几族?
【提示】X为第4周期,第ⅠA族;Y为第5周期,第 ⅦA族。
【记一记】
周期表的结构
1.原子序数=核电荷数=质子数=核外电子数
2.周期序数=电子层数 主族序数=最外层电子数
高中化学:第一二章章节复习课件 人教版必修2

D2.0、常甲温、时乙,两A能种从非酸金中属置元换素出:(氢1,)甲而的B最不能高价氧化物对应的水 化物酸性比乙的最高价氧化物对应的水化物酸性强;(2)
甲比乙更容易与H2化合;(3)甲单质能与乙的阴离子反 应生成乙单质;(4)与金属反应时,等物质的量的甲 原子得电子数比乙原子得电子数多;(5)甲的单质熔 沸点比乙的低。能说明甲比乙的非金属C性强的是
16.下面的判断,错误的是( A)D
A.稳定性:HF<HCl<HBr<HI
B.砹是一种固体,HAt很不稳定,AgAt是难溶于水且感光性很 强的固体
C.硫酸锶(SrSO4)是一种难溶于水的白色固体 D.硒化氢(H2Se)是比H2S稳定的气体
第十九页,共44页。
• 466、458
第二十页,共44页。
17.对于核电荷数为37的元素,下列描述正确的是
第二十一页,共44页。
457、456
第二十二页,共44页。
金属性和非金属性强弱判断依据
1、金属性强弱的判断依据:
(1) 金属单质与水反应快慢
(2) 金属单质与酸反应快慢
(3) 最高价氧化物的水化物的碱性强弱 (4) 金属与盐溶液发生的金属间的置换反应 2、非金属性强弱判断依据:
(1) 非金属 单质与氢气反应的难易
子键. 成键的微粒: 阴离子、阳离子
成键的本质(作用力):静电作用(吸引和排斥) 成键的条件: 活泼金属和活泼非金属之间. (2)离子化合物: 通过离子键而形成的化合物 一般来说活泼金属 IA和和活II泼A族非金属 VIA和VI之IA间族可形成离子化合物(简单离子化合物)。
第二十六页,共44页。
(3)离子化..合物形成过程.的. 表示—电子式
③阴离子的电子式 ④离子化合物的电子式
甲比乙更容易与H2化合;(3)甲单质能与乙的阴离子反 应生成乙单质;(4)与金属反应时,等物质的量的甲 原子得电子数比乙原子得电子数多;(5)甲的单质熔 沸点比乙的低。能说明甲比乙的非金属C性强的是
16.下面的判断,错误的是( A)D
A.稳定性:HF<HCl<HBr<HI
B.砹是一种固体,HAt很不稳定,AgAt是难溶于水且感光性很 强的固体
C.硫酸锶(SrSO4)是一种难溶于水的白色固体 D.硒化氢(H2Se)是比H2S稳定的气体
第十九页,共44页。
• 466、458
第二十页,共44页。
17.对于核电荷数为37的元素,下列描述正确的是
第二十一页,共44页。
457、456
第二十二页,共44页。
金属性和非金属性强弱判断依据
1、金属性强弱的判断依据:
(1) 金属单质与水反应快慢
(2) 金属单质与酸反应快慢
(3) 最高价氧化物的水化物的碱性强弱 (4) 金属与盐溶液发生的金属间的置换反应 2、非金属性强弱判断依据:
(1) 非金属 单质与氢气反应的难易
子键. 成键的微粒: 阴离子、阳离子
成键的本质(作用力):静电作用(吸引和排斥) 成键的条件: 活泼金属和活泼非金属之间. (2)离子化合物: 通过离子键而形成的化合物 一般来说活泼金属 IA和和活II泼A族非金属 VIA和VI之IA间族可形成离子化合物(简单离子化合物)。
第二十六页,共44页。
(3)离子化..合物形成过程.的. 表示—电子式
③阴离子的电子式 ④离子化合物的电子式
鲁科版高中化学必修二课件同课异构课件1:1.1.2核外电子排布.pptx

⒉根据Na、Mg、O、Cl原子在反应中失去或得到电子的 数目和该原子的最外层电子数目,推断其氧化物和氯化物 中元素的化合价,将结果填入下表:一些元素的原子得失 电子的情况
课堂练习1
1.下列原子结构示意图中,正确的是:
A.
B.
C.
D.
2.某元素原子的原子核外有三个电子层,最外层有4个电子,该原子 核内的质子数为:
道尔顿原子模型
原子是组成物质的基本粒子,它们是坚实的、不可再 分的实心球。
汤姆生原子模型
原子是一个平均分布着正电荷的粒子,其中镶 嵌着许多电子,中和了正电荷,从而形成了中 性原子。
卢瑟福原子模型
原子中心有一个带正电荷的核,它的质量几乎等于原子的全部 质量,电子在它的周围沿着不同的轨道运转,就象行星环绕太 阳运转一样。
答案:1.AC2.B3.D
波尔原子模型
电子在原子核外空间的一定轨道上绕核做 高速的圆周运动。
电子云模型
现代物质结构学说。波粒二象性。
根据原子光谱和理论分析 核电荷数为1~20的元素原子核外电子层排布
K Ca
+35 28187
Br
补充练习1
1.某元素原子核外L层电子数是其它层电子数之和的2倍,则 该元素的核电荷数为:
A.6B.8C.12D.16
A.14B.15C.16D.17 3.下列叙述正确的是: A.电子在原子核外作高速圆周运动 B.电子云示意图中的小黑点表示一个电子 C.次外层电子数一定是2或8 D.最外层只有一个电子的原子不一定是碱金属元素的原子
答案:1.B2.A3.D
课堂练习2
1.根据下列叙述,写出元素名称并画出原子结构示意图。
答案:1.(1)硫284(2)硼23(3)氖282.NaF
课堂练习1
1.下列原子结构示意图中,正确的是:
A.
B.
C.
D.
2.某元素原子的原子核外有三个电子层,最外层有4个电子,该原子 核内的质子数为:
道尔顿原子模型
原子是组成物质的基本粒子,它们是坚实的、不可再 分的实心球。
汤姆生原子模型
原子是一个平均分布着正电荷的粒子,其中镶 嵌着许多电子,中和了正电荷,从而形成了中 性原子。
卢瑟福原子模型
原子中心有一个带正电荷的核,它的质量几乎等于原子的全部 质量,电子在它的周围沿着不同的轨道运转,就象行星环绕太 阳运转一样。
答案:1.AC2.B3.D
波尔原子模型
电子在原子核外空间的一定轨道上绕核做 高速的圆周运动。
电子云模型
现代物质结构学说。波粒二象性。
根据原子光谱和理论分析 核电荷数为1~20的元素原子核外电子层排布
K Ca
+35 28187
Br
补充练习1
1.某元素原子核外L层电子数是其它层电子数之和的2倍,则 该元素的核电荷数为:
A.6B.8C.12D.16
A.14B.15C.16D.17 3.下列叙述正确的是: A.电子在原子核外作高速圆周运动 B.电子云示意图中的小黑点表示一个电子 C.次外层电子数一定是2或8 D.最外层只有一个电子的原子不一定是碱金属元素的原子
答案:1.B2.A3.D
课堂练习2
1.根据下列叙述,写出元素名称并画出原子结构示意图。
答案:1.(1)硫284(2)硼23(3)氖282.NaF
(鲁科版)高中化学必修二:1.1原子结构【第一课时+第二课时】课件
化学 必修2
第1章 原子结构与元素周期律
自主预习区 互动探究区 巩固训练区 课时作业
已知R2+离子核外有a个电子,它含有b个中子。 表示R原子符号正确的是( )
解析:
R2+的电子数为a―→R原子的质子数为a+
N=b 2――→A(R)=a+2+b。
答案: C
化学 必修2
第1章 原子结构与元素周期律
自主预习区 互动探究区 巩固训练区 课时作业
二、核素
[填一填]
1.元素 质子数(或核电荷数) 的同一类原子 (1)定义:具有相同______________________
的总称。
原子核内的质子数 。 (2)决定元素种类的微粒:_____________________ 2.核素 质子 和一定数目______ 中子 的一种原 (1)定义:具有一定数目_____ 子。
1 1H 2 1H 3 1H
名称 俗称 符号
氕 ____
氘 ____ 重氢 ______
氚 ____ 超重氢 ________ T ____
H ____
D ___
化学 必修2
第1章 原子结构与元素周期律
自主预习区 互动探究区 巩固训练区 课时作业
4.几种重要的核素 (1)作为相对原子质量和阿伏加德罗常数测定用的标准原
12 14 6C ;考古中常测量______ 子为______ 6C 的数量来推断生物体的存
在年代。
2 3 H 1 1H 。 (2)制造氢弹的原料为_____、_____
235 92 U (3)原子弹、核反应堆的燃料:_____
自主预习区 互动探究区 巩固训练区 课时作业
自主预习区 互动探究区 巩固训练区 课时作业
人教版高中化学必修二第一章第一节《元素周期表》第一课时 (共23张PPT)

_________________________________________________________ (3)写出单质Z与钠反应的化学方程式:_________________。
最后,给一个任务:记忆前20号元素名称 原子 序数 1 2 3 4 5 6 7 8 9 10 元素 名称 氢 氦 锂 铍 硼 zxxk __ __ __ __ __ 原子 序数 11 12 13 14 15 16 17 18 19 20 元素 名称 __ __ __ __ __ __ __ 氩 钾 钙
有相差1, 有相差11, 有相差25。
3.A、B分别为同周期ⅡA、ⅢA族的元素,则下列A、B
的原子序数关系不正确的是( C )
A.A+1=B
B.A+11=B
C.A+18=B
D.A+25=B
4.(双选)某元素X,它的原子最外层电子数是次外层电
子数的2倍,则X在周期表中位于 (AC )
A.第二周期 B.第三周期
(3)主族序数与最外层电子数的关系: 主族序数 = 最外层电子数
(4)一些族的别称
ⅠA称为_______碱__金__属___元素 ⅦA称为_____卤__族_______元素 零族称为___稀__有__气__体_____元素 第ⅢB~ⅡB族为_____过__渡___元素
元素周期表
一、元素周期表
(一)元素周期表的结构 数一数,每一个周期有多少种元素?
①主族:在罗马数字后标A表示:
ⅠA、Ⅱ___A_、___Ⅲ__A__、___Ⅳ__A__、__Ⅴ___A__、__Ⅵ__A__、___Ⅶ__A________
②副族:在罗马数字后标B表示:
ⅠB、__Ⅱ__B__、__Ⅲ___B__、__Ⅳ__B__、___Ⅴ__B__、__Ⅵ__B__、___Ⅶ__B_______
最后,给一个任务:记忆前20号元素名称 原子 序数 1 2 3 4 5 6 7 8 9 10 元素 名称 氢 氦 锂 铍 硼 zxxk __ __ __ __ __ 原子 序数 11 12 13 14 15 16 17 18 19 20 元素 名称 __ __ __ __ __ __ __ 氩 钾 钙
有相差1, 有相差11, 有相差25。
3.A、B分别为同周期ⅡA、ⅢA族的元素,则下列A、B
的原子序数关系不正确的是( C )
A.A+1=B
B.A+11=B
C.A+18=B
D.A+25=B
4.(双选)某元素X,它的原子最外层电子数是次外层电
子数的2倍,则X在周期表中位于 (AC )
A.第二周期 B.第三周期
(3)主族序数与最外层电子数的关系: 主族序数 = 最外层电子数
(4)一些族的别称
ⅠA称为_______碱__金__属___元素 ⅦA称为_____卤__族_______元素 零族称为___稀__有__气__体_____元素 第ⅢB~ⅡB族为_____过__渡___元素
元素周期表
一、元素周期表
(一)元素周期表的结构 数一数,每一个周期有多少种元素?
①主族:在罗马数字后标A表示:
ⅠA、Ⅱ___A_、___Ⅲ__A__、___Ⅳ__A__、__Ⅴ___A__、__Ⅵ__A__、___Ⅶ__A________
②副族:在罗马数字后标B表示:
ⅠB、__Ⅱ__B__、__Ⅲ___B__、__Ⅳ__B__、___Ⅴ__B__、__Ⅵ__B__、___Ⅶ__B_______
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学必修二第一章复习课件
第一章
物质结构 元素周期律
单元复习
一.原 子 结 构 1、原子结构
天才来自于勤奋
原 质子-决定元素种类 决定质量数
子 核
中子-决定元素的同位素
(近似原子量)
原
子
核 外 电 子
决定 元素 的性 质
电子层-决定所在周期 最外层电子-决定主族序数
2、原子结构的表示方法
(1)原子结构示意图
5、金属性和非金属性强弱判断依据
金属性强弱的判断依据:
(1) 金属单质与水或者酸反应快慢
。
(2) 最高价氧化物的水化物的碱性强弱 。
(3) 金属与盐溶液发生的金属间的置换反。应
非金属性强弱判断依据: (1)非金属 单质与氢气反应的难易 。
(2)气态氢化物的稳定性强弱
。
(3)最高化氧化物的水化物的酸性强。弱
Rb I 37铷 53碘
Cs At 55铯 85砹
最外层电子数__相__同 从上到下 核电核数_增__多__ 电子层数__增__多__
原子半径__增__大__ 原子核对最外层电子吸引力__减__弱_ 失电子能力__增__强_ 单质的还原性__增__强__元素金属性增__强__
得电子能力_减__弱__ 单质氧化性_减__弱___元素非金属_减__弱___
核外电子排布的一般规律
归纳为:一低四不超
即
核外电子总是尽先排布在 能量最低 的电子层里 每层电子不能超过 2n2 个 最外层电子不能超过 8 个(K层是最外层时不超过 2个) 次外层电子不能超过 18 个 倒数第三层电子不能超过 32 个。
课堂练习
1、质量数为B的Xn-阴离子含有a个电子,
则中子数为( )A
D、氡在常温是固体。
二.元素周期律与元素周期表
1.编排原则
短周期 第1、2、3周期
元
周期 长周期 第4、5、6周期 不完全周期 第7周期
素
周 2.结构
期
表
族
主族:IA~VIIA 副族:IB~VIIB 0族::
电子层数=周期序数
最外层电子数=主族序数=最高正价数
同一周期元素(稀有气体除外)
Na Mg Al Si P S Cl Ar 11钠 12镁 13铝 14硅 15磷 16硫 17氯 18氩
同一周期,电子层数_相__同____ 从左到右,原子半径逐渐__减__小_,失电子 能力逐渐 _减__弱___,得电子能力逐渐__增__强 金属性逐渐_减__弱____非金属性逐渐__增__强__ 金属性越强,最高价氧化物对应水化物碱性_越__强____ 非金属性越强,最高价氧化物对应水化物酸性_越__强__ 单质与氢气反应条件越__越__容__易 生成的氢化物稳定性_越__强___
A、B-a+n
B、2B
C、B-a-n
D、2a
2、已知Rn-离子的质量数为35,中子数 为18,核外电子总数为18,则该离子
是: A
A、Cl- B、F - C、S2- D、Br
巩固试题:
1、核电荷数分别为16和6的元素的原
子相比较,前者的下列数据是后者的
4倍的是(D )
A、电子数
B、最外层电子数
C、电子层数 D、次外层电子数
2、氡(Rn)是放射性元素,某些建筑材料中含有氡,人 居住其中健康将受到危害。已知222Rn来自镭,称为镭 射气;220Rn来自钍,称为钍射气;219Rn来自锕,称为锕
射气。下列关于氡的说法中,正确的是( B )
A、氡气的化学性质活泼,对人体有害
B、“锕射气”是氡的同位素原子
C、氡原子有8个电子层,最外层有8个电子
比较微粒大小的依据(三看)
一看电子层数:电子层数越多半径越大 Na>Na+,K>Na
二看核电荷数:电子层数相同时,核电荷数 越大半径越小。
S2->Cl->K+>Ca2+; O2->F->Na+>Mg2+>Al3+
三看电子数:电子层和核电荷数都相同时, 电子数越多半径越大。 Cl->Cl; Fe2+>Fe3+
元素的种类是由_质__子__数_决定的。 核素的种类是由_质__子_数__和_中__子__数_决定的。 元素的同位素是由_中__子_数__决定的。 原子的质量数是由_质_子__数__和_中__子_数__决定的,近似等
于_相__对_原__子_质__量_ 元素的化学性质是由_最__外_层__电_子__数_决定的。 元素在同期表中的位置是由电__子__层_数__和_最__外_层__电__子_数_ 决定的。
变化 (1~8)
元素同期律反应的就是元素的位、构、性的关系
1.下面的判断,错误的是(AD ) A.稳定性:HF<HCl<HBr<HI B.砹是一种固体,HAt很不稳定,AgAt是难溶于水且 感光性很强的固体 C.硫酸锶(SrSO4)是一种难溶于水的白色固体 D.硒化氢(H2Se)是比H2S稳定的气体
(4)非金属单质间的置换反应
。
概念: 元素的性质(原子半径、主要化合价、元素的金
6、 属性非金属性)随着原子序数的递增而呈周期性的变化 元 规律。
素
规律:原子半径同周期从左到右渐小,同族从上到下渐
周 大。主要化合价:+1 +2 +3 +4 +5 +6 +7 0
期
-4 -3 -2 -1
律
原因:核外电子排布随着原子序数的递增而呈周期性的
2、
37 17
Cl-中的
质子数是
17
,中子数
是 20 ,核外电子数是 18 ,质量数
是 37 。
大家有疑问的,可以询问和交流
可以互相讨论下,但要小声点
课堂练习
1、人类探测月球发现,在月球的土壤中含有较丰富的质量 数为3的氦,它可以作为未来核聚变的重要原料之一。氦
的该种同位素应表示为(B)
A、34 He B、23 He C、24 He D、33 He
(2)原子组成表示式 A X Z
原子(
A Z
X)中,质子有_Z_个,中子有_A-_Z个,
核外电子有__Z_个。
3、相互关系
(1) 质量数= 质子数+中子数 (2) 原子中:质子数= 核电荷数=核外电子数
(3) 阳离子中:
质子数= 核电荷数=离子的核外电子数+离子电荷数
四“素”的概念不同
几个决定:
最高正价数+/最低负价/=8
某元素最高正价氧化物对应的水化物的 化学式是H2XO4,这种元素的气态氢化物 的化学式为(B )
A. HX B. H2X C. XH3 D. XH4
4、元素的性质与元素在周期表中位置的关系
同一主族元素,结构相似,性质相似
Li F 3锂 9氟
Na Cl 11钠 17氯
K Br 19钾 35溴
第一章
物质结构 元素周期律
单元复习
一.原 子 结 构 1、原子结构
天才来自于勤奋
原 质子-决定元素种类 决定质量数
子 核
中子-决定元素的同位素
(近似原子量)
原
子
核 外 电 子
决定 元素 的性 质
电子层-决定所在周期 最外层电子-决定主族序数
2、原子结构的表示方法
(1)原子结构示意图
5、金属性和非金属性强弱判断依据
金属性强弱的判断依据:
(1) 金属单质与水或者酸反应快慢
。
(2) 最高价氧化物的水化物的碱性强弱 。
(3) 金属与盐溶液发生的金属间的置换反。应
非金属性强弱判断依据: (1)非金属 单质与氢气反应的难易 。
(2)气态氢化物的稳定性强弱
。
(3)最高化氧化物的水化物的酸性强。弱
Rb I 37铷 53碘
Cs At 55铯 85砹
最外层电子数__相__同 从上到下 核电核数_增__多__ 电子层数__增__多__
原子半径__增__大__ 原子核对最外层电子吸引力__减__弱_ 失电子能力__增__强_ 单质的还原性__增__强__元素金属性增__强__
得电子能力_减__弱__ 单质氧化性_减__弱___元素非金属_减__弱___
核外电子排布的一般规律
归纳为:一低四不超
即
核外电子总是尽先排布在 能量最低 的电子层里 每层电子不能超过 2n2 个 最外层电子不能超过 8 个(K层是最外层时不超过 2个) 次外层电子不能超过 18 个 倒数第三层电子不能超过 32 个。
课堂练习
1、质量数为B的Xn-阴离子含有a个电子,
则中子数为( )A
D、氡在常温是固体。
二.元素周期律与元素周期表
1.编排原则
短周期 第1、2、3周期
元
周期 长周期 第4、5、6周期 不完全周期 第7周期
素
周 2.结构
期
表
族
主族:IA~VIIA 副族:IB~VIIB 0族::
电子层数=周期序数
最外层电子数=主族序数=最高正价数
同一周期元素(稀有气体除外)
Na Mg Al Si P S Cl Ar 11钠 12镁 13铝 14硅 15磷 16硫 17氯 18氩
同一周期,电子层数_相__同____ 从左到右,原子半径逐渐__减__小_,失电子 能力逐渐 _减__弱___,得电子能力逐渐__增__强 金属性逐渐_减__弱____非金属性逐渐__增__强__ 金属性越强,最高价氧化物对应水化物碱性_越__强____ 非金属性越强,最高价氧化物对应水化物酸性_越__强__ 单质与氢气反应条件越__越__容__易 生成的氢化物稳定性_越__强___
A、B-a+n
B、2B
C、B-a-n
D、2a
2、已知Rn-离子的质量数为35,中子数 为18,核外电子总数为18,则该离子
是: A
A、Cl- B、F - C、S2- D、Br
巩固试题:
1、核电荷数分别为16和6的元素的原
子相比较,前者的下列数据是后者的
4倍的是(D )
A、电子数
B、最外层电子数
C、电子层数 D、次外层电子数
2、氡(Rn)是放射性元素,某些建筑材料中含有氡,人 居住其中健康将受到危害。已知222Rn来自镭,称为镭 射气;220Rn来自钍,称为钍射气;219Rn来自锕,称为锕
射气。下列关于氡的说法中,正确的是( B )
A、氡气的化学性质活泼,对人体有害
B、“锕射气”是氡的同位素原子
C、氡原子有8个电子层,最外层有8个电子
比较微粒大小的依据(三看)
一看电子层数:电子层数越多半径越大 Na>Na+,K>Na
二看核电荷数:电子层数相同时,核电荷数 越大半径越小。
S2->Cl->K+>Ca2+; O2->F->Na+>Mg2+>Al3+
三看电子数:电子层和核电荷数都相同时, 电子数越多半径越大。 Cl->Cl; Fe2+>Fe3+
元素的种类是由_质__子__数_决定的。 核素的种类是由_质__子_数__和_中__子__数_决定的。 元素的同位素是由_中__子_数__决定的。 原子的质量数是由_质_子__数__和_中__子_数__决定的,近似等
于_相__对_原__子_质__量_ 元素的化学性质是由_最__外_层__电_子__数_决定的。 元素在同期表中的位置是由电__子__层_数__和_最__外_层__电__子_数_ 决定的。
变化 (1~8)
元素同期律反应的就是元素的位、构、性的关系
1.下面的判断,错误的是(AD ) A.稳定性:HF<HCl<HBr<HI B.砹是一种固体,HAt很不稳定,AgAt是难溶于水且 感光性很强的固体 C.硫酸锶(SrSO4)是一种难溶于水的白色固体 D.硒化氢(H2Se)是比H2S稳定的气体
(4)非金属单质间的置换反应
。
概念: 元素的性质(原子半径、主要化合价、元素的金
6、 属性非金属性)随着原子序数的递增而呈周期性的变化 元 规律。
素
规律:原子半径同周期从左到右渐小,同族从上到下渐
周 大。主要化合价:+1 +2 +3 +4 +5 +6 +7 0
期
-4 -3 -2 -1
律
原因:核外电子排布随着原子序数的递增而呈周期性的
2、
37 17
Cl-中的
质子数是
17
,中子数
是 20 ,核外电子数是 18 ,质量数
是 37 。
大家有疑问的,可以询问和交流
可以互相讨论下,但要小声点
课堂练习
1、人类探测月球发现,在月球的土壤中含有较丰富的质量 数为3的氦,它可以作为未来核聚变的重要原料之一。氦
的该种同位素应表示为(B)
A、34 He B、23 He C、24 He D、33 He
(2)原子组成表示式 A X Z
原子(
A Z
X)中,质子有_Z_个,中子有_A-_Z个,
核外电子有__Z_个。
3、相互关系
(1) 质量数= 质子数+中子数 (2) 原子中:质子数= 核电荷数=核外电子数
(3) 阳离子中:
质子数= 核电荷数=离子的核外电子数+离子电荷数
四“素”的概念不同
几个决定:
最高正价数+/最低负价/=8
某元素最高正价氧化物对应的水化物的 化学式是H2XO4,这种元素的气态氢化物 的化学式为(B )
A. HX B. H2X C. XH3 D. XH4
4、元素的性质与元素在周期表中位置的关系
同一主族元素,结构相似,性质相似
Li F 3锂 9氟
Na Cl 11钠 17氯
K Br 19钾 35溴
