恩诺沙星可溶性粉(100g5g)说明书
恩诺沙星可溶性粉

恩诺沙星可溶性粉说明书兽用处方药【兽药名称】通用名称:恩诺沙星可溶性粉商品名称:无英文名称:Enrofloxacin Soluble Powder汉语拼音:Ennuoshaxing Kerongxingfen【主要成分】恩诺沙星【性状】本品为白色或淡黄色粉末。
【药理作用】药效学恩诺沙星属于动物专用的杀菌性广谱抗菌药物。
对大肠杆菌、沙门氏菌、克雷伯氏杆菌、布鲁氏菌、巴氏杆菌、胸膜肺炎放线杆菌、丹毒杆菌、变形杆菌、黏质沙雷氏菌、化脓性棒状杆菌、败血波特氏菌、金黄色葡萄球菌、支原体和衣原体等均有良好作用,对铜绿假单胞菌和链球菌的作用较弱,对厌氧菌作用微弱。
本品对大多数菌株的MIC均低于1µg/ml。
对敏感菌有明显的抗菌后效应(PAE)。
本品的抗菌机制是作用于细菌细胞的DNA旋转酶,干扰细菌DNA的复制、转录和修复重组,细菌不能正常生长繁殖而死亡。
其作用有明显的浓度依赖性,血药浓度大于8倍MIC时可发挥最佳治疗效果。
药动学大多数动物内服本品能很好吸收,犬内服的生物利用度约为80%,为环丙沙星的2倍,内服后15分钟可达峰浓度的50%,1小时内达峰。
胃内食物可延迟药物吸收速率,但不影响吸收数量。
内服的生物利用度,绵羊为65%~75%,鸡为62.2%~84%,猪和未反刍犊牛为80%~100%,反刍动物低于10%。
【药物相互作用】①本品与氨基糖苷类或广谱青霉素类合用,有协同作用。
②Ca2+、Mg2+、Fe3+和Ab3+等重金属离子可与本品发生螯合,影响吸收。
③与茶碱、咖啡因合用时,由于蛋白结合率改变,血浆蛋白结合率降低,,血中茶碱、咖啡因的浓度异常升高,甚至出现茶碱中毒症状。
④本品有抑制肝药酶作用,可使主要在肝脏中代谢的药物的清除率降低,血药浓度升高。
【适应证】用于禽细菌性和支原体感染,如大肠杆菌病、鸡白痢、禽霍乱、鸡慢性呼吸道病等;犬、猫敏感菌所致消化系统、呼吸系统、泌尿系统及皮肤软组织的各种感染,如肠炎、气管支气管炎、肺炎、鼻炎等。
恩诺沙星可溶性粉成品检验记录

检查
装量
样品号
1
2
3
药+包装重
包装重
药重
平均
标准规定
每袋装量不得少于标示量,平均装量不得少于标示量
项目结论
溶解性
取本品1.0g,加水50ml,搅拌,应全部溶解
检验结果:
干燥
失重
天平室温度℃湿度%
干燥条件
105℃干燥至恒重
检品号
1
2
复核人:检验人:
有限公司
成品检验记录附页
文件编号:00第2页共3页
检验项目标准规定检验结果项目结论
1、性状应符合规定规定
2、鉴别应与对照品的规定
主斑点相同
3、装量应符合规定
规定
4、溶解性应符合规定规定
5、干燥失重减失重量不得过10.0%规定
6、含量测定:
含恩诺沙星应为
标示量的90.0%-110.0%规定
检验结论:
本品按<<恩诺沙星可溶性粉内控质量标准(半成品)>>检验,结果
规定。
备注:
负责人:复核人:检验人:
有限公司
成品检验报告单
文件编号: 00第3页共3页
检品名称
恩诺沙星可溶性粉
检验单号
批号
规格
请验车间
西药粉剂车间
取样地点
西药待包间
取样数量
取样人
送检日期
年月日
报告日期
年月日
检验依据
<<恩诺沙星可溶性粉内控质量标准(半成品)>>
检验项目标准规定检验结果项目结论
1、性状应符合规定规定
对照品制备:
取105℃干燥至恒重的恩诺沙星对照品,按上法同样操作。
10%恩诺沙星可溶性粉生产工艺规程+内控标准检验操作规程

10%恩诺沙星可溶性粉生产工艺规程目录1、产品概述2、处方和依据3、工艺流程图4、制剂工艺过程及工艺条件5、原辅材料质量标准和检查方法6、中间体质量标准和检查方法7、成品质量标准和检查方法8、包装规格、包装材料质量标准9、说明书、产品文字说明和标志10、工艺要求11、设备一览表和主要设备生产能力12、技术安全与劳动保护13、劳动组织与产品生产周期14、原辅料消耗定额15、包装材料消耗定额16、动力消耗定额17、环境保护18、编制说明1 产品概述:1.1 产品特点:1.1.1性状:本品为、白色或淡黄色粉末。
1.1.2药理作用:恩诺沙星为兽医专用的第三代氟喹诺酮类,有广谱杀菌作用,对静止期和生长期的细菌均有效。
本品对多种革兰氏阴性杆菌有良好的抗菌作用,包括绿脓杆菌、肠杆菌属、弯曲杆菌属、志贺氏菌属、沙门氏菌属、气单胞菌属、嗜血杆菌属、耶尔森菌属、沙雷氏菌属、弧菌属、变形杆菌等。
对布鲁氏菌属、巴斯德氏菌属、丹毒丝菌、博德特氏菌、葡萄球菌、支原体属和衣原体也有效。
本品禽内服吸收迅速,分布容积大,在体内广泛分布,消除半衰期较长。
1.1.3适应症:主治禽的沙门氏菌、大肠杆菌、巴斯德氏菌、嗜血杆菌、葡萄球菌、链球菌及各种支原体所引起的感染。
1.1.4用法用量:混饮每lL水鸡25~75mg(以恩诺沙星计),一日两次,连用3-5天。
1.1.5 休药期鸡8日,产蛋鸡禁用。
1.1.6 规格:100g:10g(恩诺沙星)1.1.7 贮藏:遮光、密封、在干燥处保存。
1.1.8有效期:二年1.1.9批准文号:2 处方和依据2.1处方:100g恩诺沙星10g(折纯) 无水碳酸钠 5.0g 无水葡萄糖:85g2.2处方依据:《兽药国家标准化学药品、中药卷》第一册3工艺流程图4制剂工艺过程及工艺条件4.1总述:按生产指令单领取恩诺沙星原料药、无水碳酸钠和无水葡萄糖。
分别过80目筛后(剩余少量不合格同批原辅料汇总粉碎处理过80目筛),按处方量将恩诺沙星和无水碳酸钠混合均匀后与葡萄糖粉按等两递加法混合均匀,定量分装即可。
恩诺沙星可溶性粉(半成品)内控质量标准
制药GMP管理文件
一、目的:制定恩诺沙星可溶性粉(半成品)的内控标准,规范公
司恩诺沙星可溶性粉的生产。
二、适用范围:适用于恩诺沙星可溶性粉的生产与检验。
三、责任者:生产部、检验员、仓库保管员
四、正文:
恩诺沙星可溶性粉
本品为恩诺沙星与助溶剂及葡萄糖配制而成,含恩诺沙星应为标示量的92.0%~109.0%.
【性状】本品为白色或淡黄色的粉末。
【鉴别】(1)取含量测定项下的供试品溶液,照分光光度法测定,在271、322和334nm波长处有最大吸收。
(2)取本品适量,加水制成每1ml含0.4mg的溶液,作为供试品溶液,另取恩诺沙星对照品10mg,加0.1mol/L氢氧化钠溶液4ml使溶解,加水至25ml,作为对照品溶液,照薄层色谱法试验,吸取上述两种溶液各2ul,分别点于同一硅胶G薄层板上,以氯仿-甲醇-苯-二乙胺-水(15:20:10:7:4)为展开剂,展开后,晾干,置紫外光灯下检视,供试品
所显主斑点的荧光和位置应与对照品的主斑点相同。
【检查】pH值取溶解性项下的溶液,依法测定,pH值应为8.5-10.5. 溶解性取本品1.0g,加水50ml,搅拌,应全部溶解。
干燥失重取本品,在60℃减压干燥4小时,减失重量不得过8.0%.
装量按最低装量检查法检查,应符合规定.
【含量测定】取本品适量,精密称定,置500ml量瓶中,加氢氧化钠溶液(0.1mol/L)10ml,,振摇使溶解,加水稀释至刻度,摇匀,精密量取10ml,置100ml量瓶中,加水稀释至刻度,摇匀,照分光光度法,在271nm 波长处测定吸收度,另取在105℃干燥至恒重的恩诺沙星对照品按上法同样测定;计算,即得。
5%恩诺沙星可溶性粉工艺规程

9.2.2含量均匀度:
包装验证的目的是证明5%恩诺沙星可溶性粉成品的均一性及其装量符合要求。即分别在分装的不同时间段进行随机抽取样品,从第一袋及最后一袋进行采样,中间均匀地采样8袋,共10袋。分别称重及取样送检。
4.6.3外包好的药品应先寄于库中并贴上状态标志,经检验合格后填写入库通知单才能入库。
4.6.4清场时按《外包清场岗位操作规程》进行。
5、工艺卫生和环境卫生
5.1工艺卫生:全部生产过程在30万级洁净区内进行。
5.1.1物流程序:原辅料前处理(物净、脱包)原料暂存粉碎过筛室称量配料室混合室中间站内包室外包室入库
(3)本品的红外光吸收图谱应与对照图普一致
(4)应呈正反应
(1)应呈正反应
(2)应符合规定
(3)本品的红外光吸收图谱应与对照图普一致
(4)应呈正反应
检查
酸度
PH值应为3.0—5.0
PH值应为3.0—5.0
氟喹啉酸
应符合规定
应符合规定
环丙沙星
应符合规定
应符合规定
氟
含氟量不得少于5.0%(按干燥品计)
含氟量不得少于5.0%(按干燥品计)
4.5.3注意内包装袋应清洁,进行物料平衡计算,99.0≤限度≤100%。收率不小于98.0%。包好的小包装应转入下一道工序。
4.5.4清场按《内包清场岗位操作规程》进行。
4. 6外包
4.6.1药品外包时严格按《外包岗位操作规程》进行操作,
恩诺沙星说明书(简化版)

恩诺沙星检测试剂盒说明书酶联免疫法定量检测恩诺沙星产品简介RIDASCREEN® Enrofloxacin/Quinolones(订货号:R3113R)恩诺沙星检测试剂盒,采用竞争性酶联免疫法定量测定尿液、血清种的恩诺沙星药物残留。
试剂盒中含有酶联免疫检测所需的所有试剂,包括标准品。
试剂盒足够进行96次检测(包括标准测定)。
定量分析需要使用微孔板酶标仪。
检测时间:样品制备(以10个样品为例).................大约30 分钟检测过程(孵育时间)....................大约1小时15分钟检测限:尿液、血清.................................................5ppb回收率:80 - 110 %(与标准品对应)特异性:RIDASCREEN® Enrofloxacin/Quinolones恩诺沙星检测试剂盒的特异性根据与相关物质的交叉反应确定。
恩诺沙星........................................................... 100 %诺氟沙星,麻保沙星,氧氟沙星...................... > 100 %达氟沙星............................................................... 67 %环丙沙星............................................................... 41 %沙氟沙星................................................................. 9 %1. 用途RIDASCREEN® Chinolone恩诺沙星检测试剂盒采用了竞争性酶联免疫法定量测定鸡蛋、牛肉、猪肉、羊肉、鸡肉、火鸡、鱼和虾中的恩诺沙星药物残留。
恩诺沙星可溶性粉使用说明

恩诺沙星可溶性粉使用说明【兽药名称】通用名:恩诺沙星可溶性粉英文名:Enrofloxacin 汉语拼音:Ennuoshaxing Kerongxingfen【主要成份】包被恩诺沙星、功能佐剂、增效剂等。
【性状】本品为白色或淡黄色粉末。
【药理作用】广谱抗菌药。
作用于细菌细胞的DNA旋转酶,干扰细菌DNA的复制,并穿透细菌的细胞壁,从而破坏细胞壁,使细菌细胞破裂、不能正常生长繁殖而死亡;功能佐剂可增加抗生素的抗菌效果,恢复病畜食欲,促进疫病康复,提高治愈率。
【适应症】抗菌药。
对胸膜肺炎放线杆菌、猪副嗜血杆菌、大肠杆菌、沙门氏菌、巴氏杆菌、枝原体、衣原体等均有强大抵抗作用。
适用于禽畜各种病原微生物所引起的禽支原体、大肠杆菌病、心包炎、肝周炎、气囊炎、腹膜炎、肺炎球菌、猪副嗜血杆菌病、胸膜肺炎放线杆菌、链球菌等。
临床适用于病禽咳嗽、呼噜、张口喘气,肿头、肿眼,闭目呆立,羽毛逆立,拉白色稀便,肺脏淤血,发黑,肝肿大、关节肿大及猪肺疫、喘气病等呼吸系统疾病。
【用法用量】1、拌料:本品每50g拌料50~100㎏,一日1~2次,连用2~3 天,治疗量加倍。
2、混饮:本品每50 g兑水50~80㎏,注意饮药水前1小时断水,一日1~2次,连用2~3天;重症可酌加量。
【注意事项】蛋鸡产蛋期慎用。
【不良反应】暂无规定【停药期】禽8日,猪10日,牛、羊14日。
【规格】50g:恩诺沙星5g【贮藏】密闭,遮光,在干燥处保存。
【执行标准】《兽药质量标准》2003年版【批准文号】兽药字(2009)200282526【生产批号】、【生产日期】、【有效期至】见打印。
【生产企业】照氟苯尼考粉50克的袋。
恩诺沙星标准
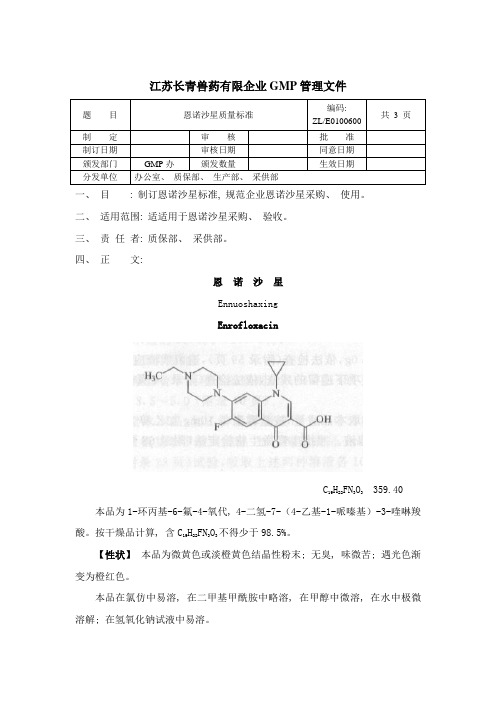
江苏长青兽药有限企业GMP管理文件题目恩诺沙星质量标准编码:ZL/E0100600共3 页制定审核批准制订日期审核日期同意日期颁发部门GMP办颁发数量生效日期分发单位办公室、质保部、生产部、采供部一、目: 制订恩诺沙星标准, 规范企业恩诺沙星采购、使用。
二、适用范围: 适适用于恩诺沙星采购、验收。
三、责任者: 质保部、采供部。
四、正文:恩诺沙星EnnuoshaxingEnrofloxacinC19H22FN3O3359.40本品为1-环丙基-6-氟-4-氧代, 4-二氢-7-(4-乙基-1-哌嗪基)-3-喹啉羧酸。
按干燥品计算, 含C19H22FN3O3不得少于98.5%。
【性状】本品为微黄色或淡橙黄色结晶性粉末; 无臭, 味微苦; 遇光色渐变为橙红色。
本品在氯仿中易溶, 在二甲基甲酰胺中略溶, 在甲醇中微溶, 在水中极微溶解; 在氢氧化钠试液中易溶。
熔点本品熔点(附录34页)为221~226℃。
熔融时同时分解。
【性状】(1)取本品约50mg, 加稀醋酸10ml, 使溶解, 加碘化铋钾试液数滴, 即生成橘红色沉淀。
(2)取本品约50mg, 置干燥表面皿中, 加丙二酸约50mg与醋酐1ml, 在水浴上加热5~10分钟, 即显红棕色。
(3)取本品, 加0.1mol/L氢氧化钠溶液制成每1ml中约含5μg溶液, 照分光光度法(附录17页)测定, 在271nm、 322nm和334nm波优点有最大吸收。
(4)本品红外光吸收图谱应与对照图谱一致。
【检验】氟取本品约40mg, 精密称定, 照氟检验法(附录53页)测定, 按干燥品计算, 含氟量不得少于5.0%。
氟喹啉酸取本品, 加0.1mol/L氢氧化钠溶液溶解并制成每1ml中约含10mg溶液, 作为供试品溶液; 另取氟喹啉酸对照品, 加0.06mol/L氨溶液制成每1ml中约含0.1mg溶液, 再将此溶液加水制成每1ml中约含0.01mg和0.02mg 溶液, 作为对照品溶液(1)和对照品溶液(2)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
兽用
恩诺沙星可溶性粉使用说明书
【兽 药 名 称】
通 用 名:恩诺沙星可溶性粉 商 品 名:
英 文 名:Enrofloxacin Soluble Powder 汉语拼音:Ennuoshaxing Kerongxing Fen
本品主要成分及化学名称:恩诺沙星,1-环丙基-6-氟-4-氧代-1,4-二氢-7-(4-乙基-1-哌嗪基)-3-喹啉羧酸 结构式:
分子式:C 19H 22FN 3O 3 分子量:359.40 【性 状】本品为白色或淡黄色粉末。
【药理作用】
药 效 学:本品是动物专用的杀菌性广谱抗菌药物。
对大肠杆菌、沙门氏菌、
克雷伯氏杆菌、布鲁氏菌、巴氏杆菌、胸膜肺炎放线杆菌、丹毒杆菌、变形杆菌、粘质沙雷氏菌、化脓性棒状杆菌、败血波特氏菌、金黄色葡萄球菌、支原体、衣原体等均有良好作用,对绿脓杆菌、链球菌作用较弱,对厌氧菌作用微弱。
本品对大多数菌株的MIC 均低于1μg/ml 。
对敏感菌有明显的抗菌后效应(PAE )。
本类药物的抗菌机制是作用于细菌细胞的DNA 旋转酶,干扰细菌的DNA 的复制、转录和修复重组,细菌不能正常生长繁殖而死亡。
其作用有明显的浓度依赖性,血药浓度大于8倍MIC 时可发挥最佳治疗效果。
本品适用于牛、猪、禽、犬、猫和水生动物的敏感细菌及支原体
所致的消化系统、呼吸系统、泌尿系统及皮肤软组织的各种感染性疾病。
主要用于支原体病、巴氏杆菌病、大肠杆菌病、沙门氏菌病、链球菌病等。
药 动 学:大多数单胃动物内服本品能很好吸收,0.5~2小时血药浓度达高
峰,胃内食物可延迟药物吸收速率,但不影响吸收数量。
内服的
生物利用度 ,鸡62.2%~84%,犬、猪、未反刍犊牛80%~100%,反刍动物低于10%。
肌注吸收迅速而完全,生物利用度猪91.9%,奶牛82%,骆驼92%。
在动物体内广泛分布,能很好进入组织、体液(包括骨骼和前列腺),出了脑脊液的浓度只有血清浓度的6%~10%外,几乎所有组织的药物浓度均高于血浆,能在白细胞蓄积达血浆浓度的140倍。
在犬的表观分布容积为2.8L/kg ,血浆蛋白结合率为27%。
肝脏代谢主要是脱去7-位哌嗪环的乙基生成环丙沙星,其次为氧化及葡萄糖醛酸结合。
消除主要通过肾脏(以肾小管分泌和肾小球滤过)排泄,15%~50%以原形从尿中排泄。
半衰期在不同种属动物和不同给药途径有较大差异,如静注半衰期为牛1.7~2.3小时,马4.4小时,猪3.5小时,鸡5.3~10.3小时,犬2.4小时;肌注半衰期为奶牛5.9小时,马9.9小时,猪4.6小时;内服半衰期猪6.9小时,犬3.7~5.8小时,鸡9.1~14.2小时。
【适 应 症】用于鸡大肠杆菌病、鸡白痢、鸡巴氏杆菌病和鸡败血性支原体病
等。
【注意事项】1、蛋鸡产蛋期禁用。
2、本品不适用于8周龄前的犬。
3、对中枢系统有潜在兴奋作用,诱导癫痫发作,患癫痫的犬用。
4、肉食动物与肾功能不良患畜慎用,可偶发结晶尿。
5、本品耐药菌株成增多趋势,不应在亚治疗剂量下长期使用。
【用法与用量】以恩诺沙星计。
混饮:每1L 水,鸡50~75mg ,连用3~5日。
【不良反应】本品毒性较小,临床使用安全。
主要不良反应有:1、可使幼龄
动物软骨发生变性,引起跛行及疼痛。
2、消化系统反应有呕吐、腹痛、腹胀。
3、皮肤反应有红斑、瘙痒、荨麻疹及光敏反应等。
【休 药 期】鸡8日。
【规 格】100g :5g
【包 装】100g 或250g 或500g 或1kg 或5kg/袋 【贮 藏】遮光,密封,在干燥处保存。
【有 效 期】二年 【批准文号】 【生产企业】
N N N O H 3C OH F
O。
