专题04 氧化还原反应-2020年高考和模拟题化学分项汇编(解析版)
2020-2021全国高考化学氧化还原反应的综合高考模拟和真题分类汇总含答案解析

2020-2021全国高考化学氧化还原反应的综合高考模拟和真题分类汇总含答案解析一、高中化学氧化还原反应1.硫酰氯(SO2Cl2)和亚硫酰氯(SOCl2)都是重要的化工试剂,均易水解。
(1)甲同学在实验室利用SO2和Cl2在活性炭催化作用下制取SO2Cl2,装置如图所示。
①B装置中冷凝管进水口是___。
(填“m”或“n”),B中干燥管盛有的物质是___。
②欲制取少量SO2Cl2,选择图中的装置(可以重复选用),其连接顺序为:a、___、h。
③去除C装置会降低SO2和Cl2的利用率,可能的原因是___(用化学方程式表示)。
(2)SOCl2水解后无残留物,较SO2Cl2是更好的脱水剂。
乙同学设计实验利用SOCl2和ZnCl2•xH2O制取无水ZnCl2。
①解释SOCl2在该实验中的作用是___(写出两点)。
②实验室常用NaOH溶液吸收SOCl2,该反应的离子方程式是___。
(3)乙同学认为SOCl2还可用作由FeCl3•6H2O制取无水FeCl3的脱水剂,但丙同学认为该实验可能发生副反应使产品不纯。
①可能发生的副反应的化学方程式是___。
②两同学设计如下实验判断该反应的可能性:取少量SOCl2和FeCl3•6H2O反应后的混合物于试管中,加水溶解,将溶液平分至五支试管,分别进行以下实验,其中能得出合理结论的是___。
A.加入过量稀HNO3,再滴加几滴AgNO3溶液B.加入少量稀HNO3,再滴加几滴BaCl2溶液C.滴加几滴BaCl2溶液D.滴加几滴酸性KMnO4溶液E.滴加几滴KSCN溶液后,再滴加几滴氯水【答案】m 碱石灰 fgdebced SO2+Cl2+2H2O=H2SO4+2HCl SOCl2作脱水剂,与水反应生成HCl可以抑制氯化锌的水解 SOCl2+4OH-=SO32-+2Cl-+2H2OSOCl2+2FeCl3•6H2O=FeSO4+6HCl+FeCl2+9H2O BCD【解析】【分析】冷凝管中冷凝水的流向要对流,下进上出;干燥管中根据要求一般填装碱石灰或无水氯化钙,碱石灰同时具有干燥和吸收酸性气体功能,无水氯化钙只有吸水性。
高考化学专题练习-氧化还原反应(含解析)

高考化学专题练习-氧化还原反应(含解析)一、单选题1.对于反应3Cl2+6NaOH ==5NaCl+NaClO3+3H2O,以下叙述正确的是()A. Cl2是氧化剂,NaOH是还原剂B. 被氧化的Cl原子和被还原的Cl原子的物质的量的比为5∶1C. Cl2既是氧化剂又是还原剂D. 每生成1mol的NaClO3转移6mol的电子2.下列反应中既属于化合反应又属于氧化还原反应的是()A. SO3+H2O=H2SO4B. 2Na+Cl22NaClC. Fe+CuSO4=FeSO4+CuD. K2SO4+BaCl2=BaSO4↓+2KCl3.常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+→2Fe3++2H2O、2Fe3++H2O2→2Fe2++O2↑+2H+,下列说法不正确的是()A. H2O2的氧化性比Fe3+强,其还原性比Fe2+强B. 在H2O2分解过程中,Fe2+和Fe3+的总量保持不变C. 在H2O2分解过程中,溶液的pH逐渐下降D. H2O2生产过程要严格避免混入Fe2+4.一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3═2HNO3+4N2↑+9H2O,在反应中被氧化与被还原的氮原子数之比为()A. 5:3B. 5:4C. 1:1D. 3:55.下列实验中,现象和结论都正确的是()实验现象结论A. 将SO2通入BaCl2溶液,然后滴入稀硝酸产生白色沉淀,白色沉淀不消失所得沉淀为BaSO3,后转化为BaSO4B. 将浓硫酸滴入含少量水的蔗糖中,并搅拌得黑色蓬松的固体及刺激性气味气体该过程中浓硫酸仅体现吸水性和脱水性C. 用黄豆粒大小的金属钠分别与水、乙醇反应前者反应更剧烈羟基的活动性:水>乙醇D. 向10mL0.1mol/LNaOH溶液中加入1mL0.1mol/L MgCl2溶液,再向混合液中滴加0.1mol/L CuCl2溶液产生蓝色沉淀Cu(OH)2比Mg(OH)2更难溶A. AB. BC. CD. D6.过氧化氢在下列三个反应中:①H2O2+H2S═2H2O+S↓、②2H2O22H2O+O2↑、③H2O2+Cl2═2HCl+O2,所起的作用是()A. 起相同作用B. 起不同作用C. 只起氧化剂的作用D. 只起还原剂的作用7.Fe3O4可表示为FeO•Fe2O3,是一种性能优良的新型磁性材料.水热法制备Fe3O4纳米级颗粒的反应为3Fe2++2S2O32﹣+O2+xOH﹣=Fe3O4+S4O62﹣+yH2O.下列说法中,不正确的是()A. 每生成1mol Fe3O4,反应转移的电子总数为4mol B. 该反应中,氧化剂与还原剂物质的量之比为1:5C. 3mol Fe2+被氧化时,消耗O2标准状况下的体积约为22.4LD. x=48.明代宋应星著的《天工开物》中有关于“火法”冶炼锌的工艺记载:“炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。
2020-2021全国高考化学氧化还原反应的综合高考模拟和真题分类汇总附答案

2020-2021全国高考化学氧化还原反应的综合高考模拟和真题分类汇总附答案一、高中化学氧化还原反应1.亚氯酸钠(NaClO2)是二氧化氯(ClO2)泡腾片的主要成分。
实验室以氯酸钠(NaClO3)为原料先制得ClO2,再制备NaClO2粗产品,其流程如图:已知:①ClO2可被NaOH溶液吸收,反应为2ClO2+2NaOH=NaClO3+NaClO2+H2O。
②无水NaClO2性质稳定,有水存在时受热易分解。
(1)反应Ⅰ中若物质X为SO2,则该制备ClO2反应的离子方程式为___。
(2)实验在如图-1所示的装置中进行。
①若X为硫磺与浓硫酸,也可反应生成ClO2。
该反应较剧烈。
若该反应在装置A的三颈烧瓶中进行,则三种试剂(a.浓硫酸;b.硫黄;c.NaClO3溶液)添加入三颈烧瓶的顺序依次为___(填字母)。
②反应Ⅱ中双氧水的作用是___。
保持反应时间、反应物和溶剂的用量不变,实验中提高ClO2吸收率的操作有:装置A中分批加入硫黄、___(写出一种即可)。
(3)将装置B中溶液蒸发可析出NaClO2,蒸发过程中宜控制的条件为___(填“减压”、“常压”或“加压”)。
(4)反应Ⅰ所得废液中主要溶质为Na2SO4和NaHSO4,直接排放会污染环境且浪费资源。
为从中获得芒硝(Na2SO4·10H2O)和石膏(水合硫酸钙),请补充完整实验方案:___,将滤液进一步处理后排放(实验中须使用的试剂和设备有:CaO固体、酚酞、冰水和冰水浴)。
已知:CaSO4不溶于Na2SO4水溶液;Na2SO4的溶解度曲线如图−2所示。
【答案】2ClO3-+SO2═2ClO2+SO42- cab 作还原剂水浴加热时控制温度不能过高(或加一个多孔球泡等)减压向废液中分批加入适量CaO固体并搅拌,用冰水浴控制反应温度,对浊液取样并滴加酚酞,至溶液呈浅红色时停止加入CaO。
静置后过滤,用水洗涤沉淀2-3次得到石膏;滤液蒸发浓缩,冷却结晶至32.4℃以下,接近0℃,过滤,所得晶体用冰水洗涤2-3次,低温干燥得到芒硝【解析】【分析】用二氧化硫将NaClO3还原制得ClO2,ClO2和NaOH反应制得NaClO3和NaClO2,再用过氧化氢将NaClO3还原成NaClO2制得NaClO2粗品。
2020高考化学试题分类汇编氧化还原反应、离子反应、化学反应中的能量变化 word版含答案

2020高考化学试题分类汇编氧化还原反应1、(2020全国理综Ⅱ)10、已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2 → H2O IO3- → I2 MnO4-→ Mn2+ HNO3→ NO如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是:A. H2O2B. IO3-C. MnO4-D. HNO32、(2020广东)13下列反应中,氧化剂与还原剂物质的量的关系为1∶2的是A.O3+2KI+H2O==2KOH+I2+O2B.2CH3COOH+C a(ClO)2==2HClO+Ca(CH3COO)2C.I2+2NaClO3==2NaIO3+Cl2D.4HCl+MnO2==MnCl2+Cl2↑+2H2O3、(2020江苏)3物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关。
下列各组物质:①Cu与HNO3溶液②Cu与FeCl3溶液③Zn与H2SO4溶液④Fe与HCl溶液由于浓度不同而能发生不同氧化还原反应的是A.①③B.③④C.①②D.①③④4、(2020全国理综Ⅱ)28(15分)以下一些氧化物和单质之间可以发生如下图所示的反应:其中,氧化物(I)是红棕色固体,氧化物(II)、(III)、(IV)在反应条件下都是气体。
(1)氧化物(I)的化学式(分子式)是。
氧化物(II)的化学式(分子式)是。
(2)反应①的化学方程式是 。
反应②的化学方程式是反应③的化学方程式是28、(15分)⑴ Fe 2O 3 CO (6分)⑵ ① Fe 2O 3 + 3 CO高温 2 Fe + 3 CO 2 ② CO + H 2O高温 CO 2 + H 2 ③ C + H 2O 高温CO + H 2 (如写可逆号,同样给分) (9分)5、 (2020天津理综)29(14分)2gCu2S和CuS的混合物在酸性溶液中用400mL0.2022020mol/LKMnO4溶液处理,发生反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL0.1mol/L(NH 4)2Fe(SO 4)2溶液完全反应。
2020-2021全国高考化学氧化还原反应的综合高考模拟和真题分类汇总及答案
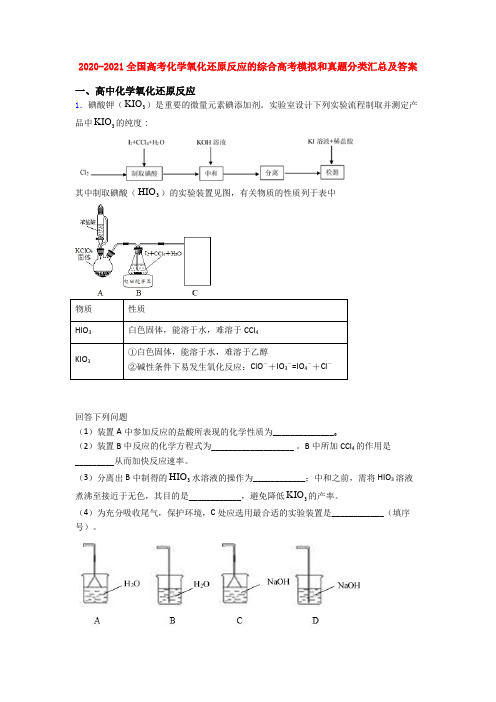
2020-2021全国高考化学氧化还原反应的综合高考模拟和真题分类汇总及答案一、高中化学氧化还原反应1.碘酸钾(3KIO)是重要的微量元素碘添加剂。
实验室设计下列实验流程制取并测定产品中3KIO的纯度:其中制取碘酸(3HIO)的实验装置见图,有关物质的性质列于表中物质性质HIO3白色固体,能溶于水,难溶于CCl4KIO3①白色固体,能溶于水,难溶于乙醇②碱性条件下易发生氧化反应:ClO-+IO3-=IO4-+Cl-回答下列问题(1)装置A中参加反应的盐酸所表现的化学性质为______________。
(2)装置B中反应的化学方程式为___________________ 。
B中所加CCl4的作用是_________从而加快反应速率。
(3)分离出B中制得的3HIO水溶液的操作为____________;中和之前,需将HIO3溶液煮沸至接近于无色,其目的是____________,避免降低3KIO的产率。
(4)为充分吸收尾气,保护环境,C处应选用最合适的实验装置是____________(填序号)。
(5)为促使3KIO 晶体析出,应往中和所得的3KIO 溶液中加入适量的___________。
(6)取1.000g 3KIO 产品配成200.00mL 溶液,每次精确量取20.00mL 溶液置于锥形瓶中,加入足量KI 溶液和稀盐酸,加入淀粉作指示剂,用0.1004mol/L 223Na S O 溶液滴定。
滴定至终点时蓝色消失(2--2-22346I +2S O =2I +S O ),测得每次平均消耗223Na S O 溶液25.00mL 。
则产品中3KIO 的质量分数为___(结果保留三位有效数字)。
【答案】还原性、酸性 22235CI +I +6H O==2HIO +10HCl 充分溶解2I 和2Cl ,以增大反应物浓度 分液 除去2Cl (或-ClO ),防止氧化3KIO C 乙醇(或酒精) 89.5%。
高考化学复习《氧化还原反应》知识点解析及练习题含答案
1.了解氧化还原反应的本质是电子转移。
2.了解氧化剂、还原剂、氧化产物和还原产物等概念。
3.能够利用得失电子守恒进行有关氧化还原反应的计算。
4.了解常见的氧化剂和还原剂及常见的氧化还原反应。
知识点一、氧化还原反应的基本概念及相互关系1.氧化还原反应的实质是电子的得失或电子对的偏移,特征是反应前后元素化合价的升降;判断某反应是否属于氧化还原反应可根据反应前后化合价是否发生了变化这一特征。
2.基本概念(1)氧化反应:失去电子(化合价升高)的反应。
(2)还原反应:得到电子(化合价降低)的反应。
(3)氧化剂(被还原):得到电子的物质(所含元素化合价降低的物质)。
(4)还原剂(被氧化):失去电子的物质(所含元素化合价升高的物质)。
(5)氧化产物:还原剂失电子后对应的产物(包含化合价升高的元素的产物)。
(6)还原产物:氧化剂得电子后对应的产物(包含化合价降低的元素的产物)。
3.氧化还原反应的表示方法高考化学复习《氧化还原反应》知识点解析及练习题含答案(1)双线桥法箭头必须由反应物指向生成物,且两端对准同种元素。
箭头方向不代表电子转移方向,仅表示电子转移前后的变化。
在“桥”上标明电子的“得”与“失”,且得失电子总数应相等。
(2)单线桥法箭头必须由还原剂中失电子的元素指向氧化剂中得电子的元素。
箭头方向表示电子转移的方向。
在“桥”上标明转移的电子总数。
1.氧化还原反应与四种基本反应类型的关系(1)有单质参加的化合反应一定是氧化还原反应;(2)有单质生成的分解反应一定是氧化还原反应;(3)置换反应一定是氧化还原反应;(4)复分解反应一定不是氧化还原反应。
2.常见的氧化剂和还原剂重要的氧化剂一般有以下几类:(1)活泼的非金属单质,如Cl2、Br2、O2等。
(2)元素(如Mn等)处于高化合价时的氧化物,如MnO2等。
(3)元素(如S、N等)处于高化合价时的含氧酸,如浓H2SO4、HNO3等。
(4)元素(如Mn、Cl、Fe等)处于高化合价时的盐,如KMnO4、KClO3、FeCl3等。
【附20套精选模拟试卷】2020高考化学一轮精选题库:1.4氧化还原反应(含答案)

第四单元氧化还原反应一、选择题1.氧化还原反应在生产、生活中广泛存在,下列生产、生活中的实例不含有氧化还原反应的是( )。
A.金属冶炼 B.燃放鞭炮 C.食物腐败 D.点制豆腐解析豆腐的点制属于胶体的聚沉,是物理变化。
答案 D2.已知:①向MnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉I试纸上,试纸变蓝色。
下列判断正确的是( )。
A.上述实验证明氧化性:MnO-4>Cl2>Fe3+>I2B.上述实验中,共有两个氧化还原反应C.实验①生成的气体不能使湿润的淀粉I试纸变蓝D.实验②证明Fe2+既有氧化性又有还原性解析根据题意知①中生成了氯气,则Cl-被氧化成Cl2,MnO4作氧化剂,Cl2为氧化产物。
②中FeCl2被Cl2氧化成FeCl3,③中I-被FeCl3氧化生成了I2。
根据氧化还原反应规律知:氧化性:MnO-4>Cl2>Fe3+>I2,A正确;上述三个反应都是氧化还原反应,Cl2也可以氧化I而生成I2,实验②只能说明Fe2+有还原性。
答案 A3.已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。
下列反应在水溶液中不可能发生的是( )A.3Cl2+6FeI2===2FeCl3+4FeI3B.Cl2+FeI2===FeCl2+I2C.Co2O3+6HCl===2CoCl2+Cl2↑+3H2OD.2Fe3++2I-===2Fe2++I2解析本题考查利用氧化性强弱判断反应的发生,由于Co2O3、Cl2、FeCl3、I2的氧化性依次减弱,故Cl2可将Fe2+、I-氧化生成 Fe3+、I2,且先氧化I-,Co2O3可将Cl-氧化生成Cl2,Fe3+可将I-氧化生成I2,故A不正确。
答案 A4.已知I-、Fe2+、SO2、Cl-、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<I-<SO2,则下列反应不能发生的是 ( )。
2020年高考化学复习 氧化还原反应(含答案)

2020年高考化学复习氧化还原反应一、选择题1、取软锰矿石(主要成分为MnO2)116g跟足量浓盐酸发生如下反应(杂质不参与反应) MnO2+4HCl(浓)MnCl2+Cl2 ↑+2H2O,制得22.4L Cl2 (标准状况)。
下列有关说法中不正确的是A.这种软锰矿石中MnO2的质量分数为75%B.被氧化的HCl的物质的量为4molC.参加反应的HCl的质量为146gD.被还原的MnO2的物质的量为1mol2、实验室为监测空气中汞蒸气的含量,通常悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化的时间来判断空气中汞的含量,其反应为4CuI+Hg===Cu2HgI4+2Cu。
以下有关该反应的说法正确的是( )A.产物Cu2HgI4中,Hg的化合价为+1B.CuI既是氧化剂,又是还原剂C.Hg与Cu均发生氧化反应D.Cu是还原产物3、某同学在做实验时引发了镁失火,她立即拿起二氧化碳灭火器欲灭火,却被实验老师及时制止。
原因是CO2可以支持镁燃烧,发生反应:2Mg+CO22MgO+C,下列关于该反应的判断正确的是( )A.Mg的化合价由0升高到+2,所以MgO是还原产物B.由此反应可以判断氧化性:CO2>MgO,还原性:Mg>CC.CO2作氧化剂,表现出氧化性,发生氧化反应D.Mg原子失去的电子数目等于氧原子得到的电子数目4、下列化学反应中电子转移的表示方法正确的是( )5、下列反应中的氨与反应4NH3+5O2===4NO+6H2O中的氨作用相同的是( )①2Na+2NH3===2NaNH2+H2↑②2NH3+3CuO===3Cu+N2+3H2O③4NH3+6NO===5N2+6H2O④3SiH4+4NH3===Si3N4+12H2A.①② B.②③C.③④ D.①④6、已知在碱性溶液中可发生如下反应:2R(OH)3 + 3ClO-+ 4OH-===2RO+3Cl-+5H2O。
则RO中R的化合价是( )A.+3 B.+4C.+5 D.+67、下列反应中,硫元素的化合价升高的是( )A.Zn+H2SO4===ZnSO4+H2↑B.C+2H2SO4(浓) CO2↑+2SO2↑+2H2OC.Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2OD.S+O2点燃,SO28、已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题04 氧化还原反应
1.【2020年7月浙江选考】反应MnO2+4HCl(浓)加热MnCl2+Cl2↑+2H2O中,氧化产物与还原产物的物质的量之比是( )
A.1:2 B.1:1 C.2:1 D.4:1
【答案】B
【解析】由反应方程式可知,反应物MnO2中的Mn元素的化合价为+4价,生成物MnCl2中Mn元素的化合价为+2价,反应物HCl中Cl元素的化合价为-1价,生成物Cl2中Cl元素的化合价为0价,故MnCl2是还原产物,Cl2是氧化产物,由氧化还原反应中得失电子守恒可知,n(Cl2):n(MnCl2)=1:1,B符合题意;答案选B。
2.【2020山东(新高考)】下列叙述不涉及氧化还原反应的是
A.谷物发酵酿造食醋B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒D.大气中NO2参与酸雨形成
【答案】B
【解析】A.涉及淀粉水解成葡萄糖,葡萄糖氧化成乙醇,乙醇氧化成乙酸,涉及氧化还原反应,A不符合题意;
B.小苏打即NaHCO3,NaHCO3受热分解产生无毒的CO2,因此可用小苏打作食品膨松剂,不涉及氧化还原反应,B符合题意;
C.利用含氯消毒剂的强氧化性消毒杀菌,涉及氧化还原反应,C不符合题意;
D.NO2与水反应有HNO3产生,因此NO2参与了硝酸型酸雨的形成,涉及氧化还原反应,D不符合题意。
答案选B。
3.(浙江省金华十校2020届高三4月模拟考试)下列变化中,气体被还原的是
A.水蒸气使CuSO4固体变蓝B.氯气使浅绿色FeC12溶液变黄
C.H2使灼热CuO 固体变红D.氨气使A1Cl3溶液产生白色沉淀
【答案】B
【解析】A .水蒸气使 CuSO 4固体变蓝,发生了反应:CuSO 4+5H 2O= CuSO 4∙5H 2O ,不是氧化还原反应,故A 不选;
B .氯气使浅绿色 FeC12 溶液变黄,发生了反应:
Cl 2+2FeCl 2=2FeCl 3,Cl 2中0价的Cl 反应后降低到了FeCl 3中的-1价,被还原,故B 选;
C .H 2使灼热CuO 固体变红,发生了反应:H 2+CuO
∆Cu+H 2O ,H 2中H 的化合价从0价升高到了水中的
+1价,被氧化,故C 不选;
D .氨气使A1Cl 3溶液产生白色沉淀,发生了反应:AlCl 3+3NH 3∙H 2O=Al(OH)3↓+3NH 4Cl ,不是氧化还原反应,故D 不选;
故选B 。
4.(北京市顺义区2020届高三第一次模拟)常温下,向22H O 溶液中滴加少量243Fe (SO )溶液,反应原理如图所示。
关于该反应过程的说法正确的是
A .该反应过程中,M 是3Fe M'+,是2Fe +
B .当有21molO 生成时,转移2mol 电子
C .在22H O 分解过程中,溶液的pH 逐渐降低
D .22H O 的氧化性比3Fe +强,还原性比2Fe +弱【答案】B
【解析】
【分析】根据反应原理图,H 2O 2+M+H +→H 2O+Mˊ的过程中H 2O 2被还原成H 2O ,Mˊ+H 2O 2→M+O 2+H +的过程中H 2O 2被氧化成O 2,根据氧化还原反应的特点,M 为Fe 2+,Mˊ为Fe 3+,据此分析作答。
【详解】A .根据分析, M 是2Fe +,Mˊ是3Fe +,故A 错误;
B .图示中生成O 2的反应为2Fe 3++H 2O 2=2Fe 2++O 2↑+2H +,反应过程中O 元素的化合价由-1价升至0价,因此当有21molO 生成时,转移2mol 电子,故B 正确;
C .图示中的反应为2Fe 3++H 2O 2=2Fe 2++O 2↑+2H +、2Fe 2++H 2O 2+2H +=2Fe 3++2H 2O ,则总反应为2H 2O 2=催化剂2H 2O+O 2↑,在22H O 分解过程中生成了H 2O ,溶液变稀,则溶液的pH 会逐渐增大,故C 错误;
D .根据2Fe 3++H 2O 2=2Fe 2++O 2↑+2H +说明H 2O 2的还原性强于Fe 2+,2Fe 2++H 2O 2+2H +=2Fe 3++2H 2O 说明H 2O 2的氧化性强于Fe 3+,故D 错误;
综上所述,答案为B 。
5.(2020届济南市实验中学高三下学期2月份阶段检测)已知酸性 K 2Cr 2O 7 溶液可与 FeSO 4 溶液反应生成 Fe 3+和 Cr 3+。
现将硫酸酸化的 K 2Cr 2O 7 溶液与 FeSO 4 溶液混合,充分反应后再向所得溶液中加入KI 溶液,混合溶液中Fe 3+
的物质的量随加入的 KI 的物质的量的变化关系如图所示,下列不正确的是
A .图中A
B 段的氧化剂为 K 2Cr 2O 7
B .开始加入的 K 2Cr 2O 7 为 0.25 mol
C .图中 BC 段发生的反应为 2Fe 3++2I -=2Fe 2++I 2
D .混合之前,K 2Cr 2O 7 与 FeSO 4的物质的量之比为1∶6
【答案】D
【解析】【分析】将硫酸酸化的 K 2Cr 2O 7 溶液与 FeSO 4 溶液混合,发生如下反应:+2-2+3+3+27214H +Cr O +6Fe =6Fe +2Cr +7H O ,向所得溶液中加入KI 溶液,混合溶液中Fe 3+的物质的量
随加入的 KI 的物质的量的变化关系如图,可知在AB 段发生反应:
+2--3+
272214H +Cr O +6I =3I +2Cr +7H O ,在BC 段发生反应:2Fe 3++2I -=2Fe 2++I 2。
据此解答。
【详解】A .在AB 段发生反应:+2--3+272214H +Cr O +6I =3I +2Cr +7H O ,氧化剂是K 2Cr 2O 7,故A 正确; B .根据图像可知,在BC 段,消耗I -
0.9mol ,由反应对应的关系3+Fe I 0.9 0.9-
~,推知在混合时生成了0.9mol Fe 3+, 2-3+27Cr O 6Fe 0.150.9
,消耗K 2Cr 2O 7物质的量为0.15mol ;又AB 段有对应关系:消耗I -0.6mol ,2--
27Cr O 6I 0.1 0.6
~,消耗K 2Cr 2O 7物质的量为0.1mol ;共消耗K 2Cr 2O 7物质的量为0.15+0.1=0.25mol ,故B 正确;。
