有机化学炔烃
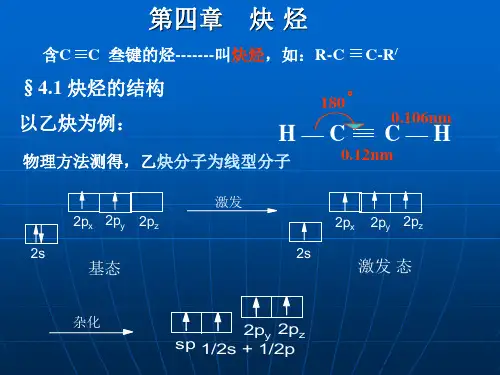
有机化学 第四章 炔烃
R-C
C-Na + NH3↑
R-C≡C-Na + R/X R/X/
6、聚合反应
Cu2Cl2 2 CH CH NH Cl H2O CH2 CH 4
CH CH CH2 CH Cu2Cl2 NH 4Cl H 2O
C CH
C
C CH CH2
增碳
例: 以乙炔为原料合成下列化合物: (1)Z-3-己烯; (3)醋酸乙烯脂; (2)E-3-己烯;
2) 和卤化氢加成
RC
注:
CH
HX
HgCl2
R
C X
CH2 HX
HgCl2
R
X C X
CH3
① 反应可以停留在卤代烯烃阶段; ② 在催化剂汞盐或铜盐存在时,叁键与HX反应 活性比双键大; ③ 不对称炔烃与HX加成符合马氏规则,对于HBr 有过氧化物效应。
3) 和水加成
RC CH + H2O
HgSO4 H 2SO4 ) (稀
5 4 3 2 1
CH3-CH = CH-C
CH
3-戊烯-1-炔
(不叫 2-戊烯-4-炔)
如对称,优先考虑双键。
HC CCHCH=CH 2 CH 3
6 5 4 3 2 1
3-甲基-1-戊烯-4-炔
HC C-CH2-CH2-CH=CH2
1-己烯-5-炔
§4.3 物理性质(自学) §4.4 化学性质 1、氢化反应 1)催化氢化
RC CR' + H2
催化加氢反应活性:炔烃>烯烃
Ni(Pt , Pd)
RCH
CHR'
Ni(Pt, Pd)
H2
RCH2CH2R'
RC
炔烃的结构通式

炔烃的结构通式炔烃是一类具有碳碳三键的有机化合物。
根据碳原子数的不同,炔烃可以分为乙炔、丙炔、丁炔等。
下面将分别对这些炔烃的结构通式进行介绍。
1. 乙炔(C2H2):乙炔是最简单的炔烃,由两个碳原子和两个氢原子组成。
其结构通式为CH≡CH。
乙炔是一种无色、有刺激性气味的气体,在室温下可以燃烧。
乙炔常被用作燃料和原料,广泛应用于金属切割和焊接等领域。
2. 丙炔(C3H4):丙炔由三个碳原子和四个氢原子组成。
其结构通式为HC≡CCH3。
丙炔是一种无色液体,在室温下能够燃烧。
丙炔常被用作溶剂和化学合成的原料。
3. 丁炔(C4H6):丁炔由四个碳原子和六个氢原子组成。
其结构通式为HC≡CCH2CH3。
丁炔是一种无色液体,在室温下能够燃烧。
丁炔常被用于化学合成和有机合成的反应中。
炔烃具有碳碳三键的特点,使其在化学反应中具有独特的反应性。
炔烃可以发生加成反应、氧化反应、卤化反应等。
其中,加成反应是炔烃最常见的反应类型之一,其反应产物是由两个反应物的分子结合而成的。
例如,乙炔可以和氢气发生加成反应,生成乙烯(C2H4)。
这种反应是一个重要的工业反应,用于合成乙烯。
除了加成反应,炔烃还可以发生氧化反应。
氧化反应是指炔烃与氧气发生反应,生成二氧化碳和水。
例如,乙炔可以在适当的条件下与氧气反应,生成二氧化碳和水。
这种反应是乙炔燃烧的过程,释放出大量的热能。
炔烃还可以发生卤化反应。
卤化反应是指炔烃与卤素发生反应,生成相应的卤代烃。
例如,乙炔可以和氯气发生反应,生成氯代乙烯(C2H2Cl2)。
这种反应常用于合成有机化合物和制备化学试剂。
炔烃是一类具有碳碳三键的有机化合物。
乙炔、丙炔和丁炔是常见的炔烃。
炔烃具有独特的反应性,可以发生加成反应、氧化反应和卤化反应。
炔烃在工业生产和化学合成中有着广泛的应用。
大学有机化学-炔烃

顺式聚乙炔
反式聚乙炔
问题:
→ CH3(CH2)2C≡CCH2CH3
KMnO4
(CH3(CH2)2COOH) + (CH3CH2COOH)
HOOCCH3
乙酸锌—活性炭 160-165 oC
CH2 CHOOCCH3 乙酸乙烯酯
炔烃亲核加成机理:
CH3C CH CH3O-
CH3 C CH-
OCH3
CH3OH
CH3O-
CH3 C CH2 OCH3
碳负离子稳定性与C+相反!
(四)硼氢化的氧化反应
H5C2C
CC2H5
B2H6, 0 oC 二甘醇二甲醚
H5C2
C2H5
CC
B
H
3
→ H2O2
NaOH RCH2CHO
(4)聚合反应 (a)低聚
乙烯基乙炔
CuCl NH4Cl 2HC CH
HC CH
CH2 CH C CH CuCl NH4Cl
(b)高聚
CH2 CH C C CH CH2
二乙烯基乙炔
n HC CH TiCl4 Al(C2H5)3
CH CH n 聚乙炔
内的最长的链作为主链,按最低序列原则给碳 碳双键或碳碳三键尽可能降低位次。
CH3CH CH C CH 3-戊烯 - 1-炔
CH3C CCHCH2CH CH2 C2H5
4- 乙基 -1-庚烯 -5-炔
若双键和三键处于相同的位次供选择时, 优先给双键 最低编号。
HC C CH CH2 CH3C CCHCH2CH CHCH3
RC≡CH+NaNH2 RC≡CNa+NH3
炔化钠时非常重要的有机合成中间体, 常利用与(RX)反应来合成炔烃同系物。例 如:
有机化学第五章炔烃(陈青)-幻灯片

Na
C3 C H2 C HCC 2 C3 H H 液 NH3
CH3CH2 C
H
H C
CH2CH3
18
机理:
Na
RCCR
R C C R Na
负离子自由基
NH3
R
CC
H
R
乙烯型自由基
R
CC
H
R
反式 稳定
R
R
CC H
顺式
R CC
Na
H
R
乙烯型自由基
R
NH3
CC
H
R
乙烯型负离子
R
H
CC
H
R
反式烯烃
② 炔烃用LiAlH4还原得反式烯烃。 ③ 炔烃硼氢化,醋酸处理得顺式烯烃。
3
异构:由于炔烃是个直线形分子,故没有几何异构, 它具有碳链异构和官能团位置异构。 碳链不同
叁键位置不同
1—戊炔
碳链位置异构
3—甲基—1—丁炔
2—戊炔 官能团位置异构
6
命名:系统命名 (IUPAC) 命名原则
炔烃的系统命名原则与烯烃相同,无顺反异构,只将烯字改 为“炔”字即可(英文词尾ene改为yne,乙炔英文名称采用 俗名acetylene)。
乙炔中的碳为SP杂化,轨道中S成分较大,核对电子的束缚
14
能力强,电子云靠近碳原子,使乙炔分子中的C-H键 δ- δ+
极性增加: HCCH 氢具有酸性。
(2)炔化物的生成
①乙炔或 RCCH可和NaNH2、RLi、RMgX反应
RCCH+ NaNH2 RCCH+ n-C4H9Li
RC CNa+ NH3
19
有机化学第六章 链烃——炔烃
聚合,催化剂
[ CH2-CH ]n
OC2H5 粘合剂
CH2=CHOC2H5
CHCH + HCN
聚合,催化剂
CuCl2H2O, 70℃
[ CH2-CH ]n CN
人造羊毛
CH2=CH -CN
(四)氧化反应
R C C R'
KMnO4
H+
OH
O3 H2O
O
R C OH +
羧酸
O HO C R'
羧酸
R CCH
Cl
4-Chloro-4-methyl-2-pentyne
CH3
Br
CH3 CH C C CHCH2CH3
2-甲基-5-溴-3-己炔 5-Bromo-2-methyl-3-heptyne
CH3CH=CHC CH 3-戊烯-1-炔
3-penten-1-yne
1 23 4 5 CH2 CHCH2C CH
在Hg++催化下,叁键比双键易水合。(故烯炔水合时烯键可被保留)
H2C CH C CH
H2O, HgSO4 H2SO4
O H2C CH C CH3
甲基乙烯基酮
➢ 炔烃的水合机理
R C CH
Hg++
亲电加成
H2O d+
R C CH Hg++
p络合物 (汞化物)
OH2 R C CH
Hg +
-H+
OH
H+
H C
R'
(二) 叁键上的亲电加成反应
1.炔烃与X2 、HX的亲电加成
XX R C CH
R C
X
有机化学-炔烃

b.London 5/22/1912 d.IN,US 12/20/2004
“For their development of use of boron and phosphorus-containing compounds,respectively, into important reagents in organic synthesis"
1500oC HC CH + 3H2
3) CH4 + O2 1500oC HC CH + CO + H2O
2. 由烯烃制备:
CH3CH2 HC
Br2 CH2
CCl4
CH3CH2 HC CH2 Br Br
NaNH2
Mineral Oil 110-160oC
NH4Cl CH3CH2 C CH
R Cl + Mg ether
R Mg Cl
R C CH + CH3CH2MgBr
R C CMgBr
炔格氏试剂
R C CMgBr + R' Cl
R C C R'
炔烃制备
四、炔烃的制备
1. 乙炔的制备:
1) CaO + C
CaC2 + CO
CaC2 + H2O
HC CH + Ca(OH)2
2) 2CH4
“For their development and use of molecules with structure-specific interactions of high selectivity"
3) 控制加氢------反式加氢
有机化学 第04章 炔烃
例 2:
H
C
C
H
异戊二烯 反合成分析
HO HO H3 C C O C + 醇 脱水 CH CH3
•合成路线
NaNH2 H C C H HC C Na
O
1. H3C 2. H2O
Al2O3
C
CH3
HO H3C CH3
H2 Lindlar催化剂 催
HO
CH2
H 3C CH3
(醇 脱 水试 剂 )
例 3: H
第四章 炔烃和二烯烃 炔烃和二烯烃
主要内容
炔烃的几种制备方法 炔烃的亲电加成(加成类型,加成取向), ),在合成中 炔烃的亲电加成(加成类型,加成取向),在合成中 的应用 炔烃的两种还原方法及在合成中的应用( 炔烃的两种还原方法及在合成中的应用(顺、反烯烃 的制备) 的制备) 末端炔烃的特殊性质及在合成中的应用
E2消除 消 R C C R'
C
H NH2 or OH
由偕二卤代烃制备
H R C H X C X R' 2 NaNH2 R C C R'
机理:两次E2消除 机理:两次E2消除
NH2 H R C H X H
E2消除 消
C X NH2 R' R C C X R'
E2消除 消 R C C R'
由四卤代烃制备
2. H2O
CH3CH2
C
C
CH2CH2OH
H2 Lindlar催化剂 催
CH3CH2 C H C
CH2CH2OH H
末端炔烃的特征反应
Ag(NH3)2+ / OH R R C C H Cu(NH3)2+ / OH R C C Cu C C Ag
有机化学基础知识点炔烃的命名和结构
有机化学基础知识点炔烃的命名和结构炔烃是有机化合物中的一类,它们的分子结构中含有碳-碳叁键。
炔烃可以进一步分为单炔烃和多炔烃两类。
在本文中,我们将详细介绍炔烃的命名规则以及结构特点。
一、单炔烃的命名单炔烃是指分子中只含有一个碳-碳叁键的炔烃。
根据命名规则,单炔烃的命名分为三个步骤:首先确定烃的主链,其次标记炔烃叁键的位置,最后确定炔烃的名称。
为了更好地理解单炔烃的命名规则,我们以乙炔为例进行说明。
乙炔是由两个碳原子构成的炔烃,它的分子式为C₂H₂。
首先,我们确定主链长度为两个碳原子,因此它的名称为“乙”。
接下来,我们需要标记炔烃叁键的位置,乙炔中的碳原子编号为1和2,其中编号1上连接有炔烃叁键,因此我们用数字1来标记它的位置。
最后,将这两步结果结合起来,乙炔的名称就是“1-乙炔”。
二、多炔烃的命名多炔烃指的是分子中含有两个以上碳-碳叁键的炔烃。
与单炔烃的命名类似,多炔烃的命名也分为三个步骤:确定主链、标记叁键位置和确定名称。
以丙炔为例来介绍多炔烃的命名规则。
丙炔是由三个碳原子构成的炔烃,其分子式为C₃H₄。
首先,我们确定主链长度为三个碳原子,因此它的名称为“丙”。
接下来,我们需要标记叁键的位置。
丙炔中的碳原子编号为1、2和3,其中编号1和3上连接有炔烃叁键。
我们用数字1和3来标记这两个位置。
最后,将这两步结果结合起来,丙炔的名称就是“1,3-丙炔”。
三、炔烃的结构特点炔烃的分子结构中含有碳-碳叁键,这赋予了它们许多特殊的化学性质。
与其他有机化合物相比,炔烃的化学反应更为活泼,更容易发生加成反应、消除反应和取代反应。
由于叁键的存在,炔烃的分子间相互作用力较弱,使其具有较低的沸点和熔点。
这也导致了炔烃在常温下多呈现为气体或液体的状态。
在物理性质方面,炔烃还具有较强的燃烧性和较高的燃烧热。
由于炔烃分子中碳原子间含有叁键,燃烧时叁键的断裂释放了大量的能量,因此炔烃是优良的燃料。
此外,炔烃还常用于合成其他有机化合物,如合成橡胶、塑料和医药品等。
化学炔烃有机知识点总结
化学炔烃有机知识点总结炔烃是一类碳氢化合物,具有碳-碳三键结构。
它们通常具有较高的反应活性,因此在有机合成和工业生产中具有重要的地位。
炔烃的命名和结构特征,其物理性质和化学性质,以及它们在有机合成和工业中的应用都是化学研究的重要方面。
一、炔烃的结构和命名1. 结构特征炔烃分子中含有碳-碳三键,因此它们的通式为CnH2n-2,其中n表示碳原子数。
炔烃的分子中每个碳原子都含有一个sp杂化轨道,这种轨道的方向是线性的,使得碳-碳三键是直线的。
2. 命名规则炔烃的命名采用IUPAC命名法。
对于直链炔烃,根据主链的碳原子数和三键的位置进行命名。
对于支链炔烃,可以使用取代基的位置和数量来进行命名。
在有多个炔基的化合物中,可以采用前缀表示多个炔基的位置。
二、炔烃的物理性质1. 物态性质炔烃通常是无色气体或液体,但也有一些炔烃是固体。
它们的密度比空气大,通常不溶于水,但可以溶于非极性溶剂。
2. 燃烧性质炔烃非常易燃,在氧气或空气中燃烧时释放大量热能。
因此,在工业生产中会用作燃料,例如乙炔常用作切割和焊接金属。
三、炔烃的化学性质1. 加成反应炔烃中的碳-碳三键具有较高的活性,在存在适当的条件下可以发生加成反应,通常在存在催化剂的情况下进行。
例如,炔烃可以和氢气发生加成反应,生成烯烃。
此外,炔烃还可以和卤素发生加成反应,生成1,2-二卤代烷烃。
2. 氢化反应炔烃还可以发生氢化反应,将碳-碳三键还原为碳-碳双键或单键。
这通常需要催化剂的存在,例如,乙炔可以和氢气在钯催化剂的作用下发生氢化反应,生成乙烯。
3. 卤素化反应炔烃可以和卤素发生卤素化反应,生成1,2-二卤代炔烃。
这种反应通常需光照或热量的存在。
4. 炔烃的自发聚合反应炔烃中的双键具有较高的活性,因此可以发生聚合反应,生成高聚物。
例如,乙炔可以发生自发聚合反应,生成聚乙炔。
四、炔烃在有机合成中的应用1. 炔烃可以作为合成原料,用于合成其他有机化合物,例如,乙炔可以和醇反应,生成醛。
有机化学第四章 炔烃
4.4.2
氧化反应
乙炔通入高锰酸钾溶液中 ,即可被氧化成CO2 和 H2O ,同时KMnO4溶液褪色并生成MnO2沉淀。因 反应现象非常明显,常用于炔烃的定性鉴别。
3HC≡CH+10KMnO4+2H2O→6CO2↑+10KOH+10 MnO2↓
此反应若在酸性条件下反应,则无二氧化锰沉淀产生。 但无论在什么条件下反应,炔烃都会被氧化成羧酸。 根据炔烃的氧化产物,可以方便地推断出炔烃的结构。
炔烃的异构可由碳链的结构及官能团位置变化引 起。 由于碳最高只有4价,叁键碳只能连有一个烃基, 所以炔烃不存在顺反异构体,炔烃的异构体数因 此较相应碳数烯烃的异构体要少。 例:丁烯与丁炔相比
丁烯有三个构造异构体及两个顺反异构体。 而丁炔只有1-丁炔和2-丁炔两个异构体。
炔烃 4
有机化学
炔烃=C
H Br
(P71)有错
有机化学 炔烃 23
4.4.1.3 亲电加成
(3)
加H2O
乙炔在高汞盐(5%HgSO4)催化下,通入10%稀 H2SO4中,可发生乙炔直接与水加成的反应,得 到乙醛,这是工业上合成乙醛的重要方法。
H2O , HgSO4
H2C H C O H
HC
CH
H
C
C
H
0.1203nm
有机化学
炔烃
9
C-sp杂化
乙炔分子这样的形状,与碳原子采用的杂化方式 是密切相关的,在乙炔中不饱和碳原子采用sp杂 化方式。
激 发
2p
2p 2s
杂 化
sp
2p
2s
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Cu2Cl2 NH4Cl 3 HC CH
(C6H5)3PNi(CO)2 600C
CH2 = CH-C CH 乙烯基乙炔
CH2 = CH-C
二乙烯基乙炔
C-CH = CH2
4 HC
CH
Ni(CN)4
28
第五节
炔烃的制备
一、用邻二卤代烷和偕二卤代烷制备
CH3CHBr-CHBrCH3 CH3CH2-CBr2CH3
CCH2CH3 CCH2CH3
2C2H5Br
C2H5-C
C-C2H5
乙炔二钠
2、 CH CH +Na 110℃ HC CNa CH3I C-CH3 110℃ Na NaC C-CH3 HC
乙炔钠
C2H5-C C-CH3 C2H5Br
乙炔三键两端所连基团不同时,须分步连接, 否则将得到三种不同产物的混合物,无实验室 制备价值。
CH
1、与卤素加成
Br R C C R
Br2 CCl4
Br C Br R
R
C Br
C Br
R
Br2 CCl4
R
C Br
加成为反式进行,控制条件可停留在烯烃阶段,得到 反式烯烃。 Br HC
Br2
3
-20℃ CH3C CCH3 2Br2 25℃
C=C
Br
CH3
Br Br CH3 C-C CH3 BrBr
CH3CH2CH2CH=CH2 KOH 乙醇
Br2
CH3CH2CH2CHCH2Br Br CCH3
CH3CH2C
二、炔化钠与伯卤代烷反应
R-C CH NaNH2 RC CNa R`-X R-C C΄R
30
例如:
CH CH 合成 1、CH3CH2C 2、CH3C
1、 CH CH +Na 190℃ NaC CNa
H C C C2H5
17
顺 式
C2H5 H
反 式
用Na-NH3(液)还原得反式烯烃。 催化氢化用: Lindlar催化剂:Pd-CaCO3/Pb(AcO)2 Cram 催化剂:Pd-BaSO4/喹啉 Ni3B (P-2)催化剂:都得到顺式烯烃 催化氢化反应活性:炔>烯
CH3(CH2)2C≡C(CH2)4CH=CH2 Pd-Pb LindLar催化剂: H CH3(CH2)2 C=C H2 (CH2)4CH=CH2 H
O RCH2CH
HgSO4,H2SO4
RC CH2 OH
乙醛 酮 酮
RC CH
总结:
重排
O RCCH3
H2O
HC CH
RC CH
RC CR
HgSO4,H2SO4 H2O
HgSO4,H2SO4 H2O HgSO4,H2SO4 H2O
HC CH
RC CH
RC CR
1.BH3 THF 2. H2O2OH
乙醛
KOH-C2H5OH or NaNH2 矿物油 <100oC
KOH-C2H5OH, >150oC
CH3CCCH3
NaNH2 KOH-C2H5OH
CH3CH=CCH3 Br
NaNH2 矿物油 , 150-160o C
CH3CH2CCH
29
O CCH3 PCl5 吡啶
Cl CCH3 Cl NaNH2 C CH
12
第四节
炔烃的化学性质
乙烯的π电子云 乙炔的π电子云 炔烃和烯烃具有相似的结构,也具有相似的 性质,在学习炔烃的性质时,要有意将炔烃的性 质与烯烃进行比较,要注意它们的相同点,更 要注意它们的不同点. 13
一、炔氢的酸性: 碳原子类型 杂化方式 杂化轨道中 s 成分含量 电 负 性 ≡CH sp 1/2 3.29 =CH2 sp2 1/3 2.75
18
三键为线性构型,更容易被催化剂表面吸附.
三.炔烃的亲电加成反应
乙烯的π电子云
乙炔的π电子云
1、两个π键电子云浑然一体成圆柱状对称分 布难以极化。 2、炔碳原子电负性大对核外电子控制较牢π 电子不易给出。 3、故反应活性: 烯>炔
19
CH2 = CH-CH2-C
CH + Br2(1mol)
CH2-CH-CH2C Br Br
CH
sp3 1/4 2.48
14
化合物
pKa
HC
乙烷
~50
乙烯 氨 炔氢 乙醇 水
~44 35
110°
25
16 15.7
CNa + H2
1、与Na反 应
CH + Na HC
乙炔钠
HC CH + Na
190°
NaC
CNa + H2
乙炔二钠
用途:主要用于由低级炔烃合成高级炔烃.
15
2、重金属炔化物的生成 HC ≡CH RC ≡CH RC ≡CR
CH3CH2 C C H OH
Hale Waihona Puke 重排CH3CH2 C C H CH2CH3 3B
HAc
CH2CH3
CH3CH2 C C H H CH2CH3
O CH3CH2CH2CCH2CH3
将炔烃转化为顺式烯烃
24
注意:
RC CH
重排
BH3 THF
R C C H
H H O OH 2 2 3B
R C C H
H OH
1
第一部分
炔烃讲授提要
第一节:碳原子的sp杂化与乙炔分 子的形成 第二节:炔烃的命名 第三节:炔烃的物理性质 第四节:炔烃的化学性质 第五节:炔烃的制备
2
第一节 碳原子的sp杂化与 乙炔分子的形成
用现代物理方法测得:
H 0.120nm C C H 0.108nm
1800 据此认为乙炔分子中的碳原子进行的是sp杂化:
16
二、还原反应
R__C C__R΄ + H2
Pd or Ni
R__CH2__CH2__R΄
若控制条件,可使反应停留在烯烃阶段:
C2H5C CC2H5 + H2
Pd-Pb(CH3COO)2/CaCO3 或:Pd-BaSO4/喹啉 或Ni3B (P-2)
Na-NH3(液)
C2H5 C H C
C2H5 H
CH≡CCH2CH=CH2
1-戊烯-4-炔 对
4-戊烯-1-炔 错 CH2=CHCH=CHC≡CH 1,3-己二烯-5- 炔
11
第三节
炔烃的物理性质
炔烃分子的极性比烯烃稍强,故其熔、沸 点比同碳原子数的烯烃较高. 炔烃难溶于水,易溶于乙醚、苯、四氯 化碳等有机溶剂。在丙酮中溶解度: 25℃ 0.1MPa下1体积丙酮可溶解29.8L 乙炔,1.2MPa下则可溶解300L乙炔.
Ag(NH3)2
+
AgC≡CAg (白) R-C ≡CAg (白) ×
CuC≡CCu (红) Cu(NH3)2 R-C ≡CCu (红) × 重金属炔化物干燥时受热或受震易发生爆炸, 实验完毕后应用酸将其分解:
+
AgC≡CAg RC≡CCu
HNO3 HCl
HC≡CH + AgNO3 RC≡CH + Cu2Cl2
激发
杂化
2p 2s
基 态
2p 2s
激发态
p sp
3
碳 原 子 sp 杂 化 示 意 图
4
碳原子上的两个sp杂化轨道
乙炔分子中的σ键
5
乙炔分 子中π 键的形 成与π 电子云 的分布
6
sp杂化及乙炔π-键电子分布要点:
1、杂化后形成两个完全等同的sp杂化轨 道,彼此间的夹角为180°。 2、碳原子上还保留两个相互垂直的p轨 道。 3、两个π-键电子云相互作用浑然一体呈 园柱状对称分布,分不出单个的π-键.
31
32
1.BH3 THF 2. H2O2OH 1.BH3 THF 2. H2O2OH
醛
酮
25
5、炔烃的亲核加成
CHCH + CH3COOH
聚合
__
Zn (OAc)2 150-180oC
CH3COOCH=CH2
醋酸乙烯酯
[ CH2 CH ] n OCCH3 聚醋酸乙烯酯 O
H2O
[ CH2__ CH ] n OH 聚乙烯醇
=
H
重排
O
O C CH +H2O Hg2+
[
C=CH OH
]
O
CCH3
CH3(CH2)5C
CH +H2O
Hg
2+
CH3(CH2)5CCH3 91%
注: 在炔烃的水合反应中,除乙炔的水合得 到乙醛外,其它炔烃的水合都得到酮.
23
4. 硼氢化反应
炔烃和硼烷试剂反应,得到三烯基硼。
CH3CH2C CCH2CH3 BH3 THF H2O2 OH
Br nC4H9CCH3 Br Br
HBr nC4H9CH2CH 过氧化物 Br21 Br
3、炔烃的水合(库歧洛夫反应)
HC CH + H2O
HgSO4 H2SO4
H2C
CH OH
CH3 C
历程:
H H H
烯醇式
O-H H H OH H -H
酮 式
O CH3C H
C=C
[
H
C-C H
]
在室温下以动态平衡同时存在且相互转化 的构造异构体叫互变异构体,这种现象叫互 变异构现象. 22
9
2、烯炔的命名
(1)、分子中同时含有双、三键时,应尽可能 使二者编号之和最小.
CH3CH=CHC≡CH
