卟啉化合物的合成及物理化学性质
卟啉的化学性质

卟啉的化学性质一、卟啉的来源与分类1。
卟啉的来源:以卟啉为基础合成新药物已进入研究阶段。
这些卟啉大多从天然药物或合成药物中提取,如从植物根中提取具有强心作用的亚油酸等;从某些动物内脏如猪肝、牛心、羊肾、牛胆、猪肾等中提取具有抗癌作用的卟啉。
2。
卟啉的分类:目前世界上应用较广泛的卟啉有三种,分别是1, 2, 4-三羟基卟啉(TMA)及其衍生物: 2, 5-双(四甲基-2, 3, 5, 6-五吡啶基)卟啉(TMB); 2, 4-双( 2, 4-二甲氧基- 6-吡啶基)卟啉(TMC); 3, 2, 4-双( 4, 5-二甲氧基-6-吡啶基)卟啉(TMD)。
这些卟啉都可通过化学方法合成。
2。
第一节卟啉的来源和性质二、卟啉的结构性质,了解第二节环系的概念。
三、掌握第四节含有不饱和键的环的鉴定方法。
四、第六节共轭多烯的环系特征及重要的共轭多烯药物的合成原则。
五、掌握第八节单环β-D-吡喃类化合物的性质。
第一节卟啉的来源和性质一、卟啉的来源天然药物及合成药物1。
第三节卟啉的性质第二节环系的概念一、了解环系的基本概念。
13。
含有不饱和键的环1)环是大分子的骨架。
环的稳定性取决于:含双键的环体系,环的稳定性取决于:环的主体部分越大越稳定,但在有氢键时稳定性降低,分子内或分子间存在着氢键时环的稳定性增加。
含有不饱和键的环体系,环的稳定性增加。
环的稳定性主要由成环反应来维持。
环的类型:稳定性分级:级别环数(数目越多越稳定)环的类型稳定性分级稳定性分级二、卟啉的结构性质,掌握第二节环系的基本概念。
熟悉各类环系的特征。
三、掌握第六节共轭多烯的环系特征。
共轭多烯环系:共轭多烯化合物的性质与主链相似。
四、第七节单环β-胡喃类化合物的性质。
单环β-胡喃类化合物的性质。
单环β-胡喃类化合物的鉴定。
主要反应有:酸碱反应:酯化反应:氧化反应:取代反应:硝化反应:消去反应:还原反应:酰化反应:醚化反应:其他反应:主要用途:抗菌药、消炎药、抗病毒药及调节蛋白质水平药等。
金属卟啉化合物的合成及应用

金属卟啉化合物的合成及应用金属卟啉化合物一直以来都备受关注,它们不仅在生物领域中发挥重要作用,还在材料科学、催化化学等领域有着广泛的应用。
本文将重点探讨金属卟啉化合物的合成方法及其在不同领域中的应用。
金属卟啉化合物是一类含有卟啉结构的化合物,其中金属离子与卟啉环上的四个氮原子形成配位键。
合成金属卟啉化合物的方法多种多样,常见的方式包括金属盐与卟啉类配体的配位反应、金属卟啉前体的合成及后续处理等。
其中,金属盐与卟啉类配体的配位反应是一种比较常见的合成方法。
通过合理选择金属离子和卟啉类配体的配比、反应条件等因素,可以合成出不同金属中心的卟啉化合物。
此外,金属卟啉前体的合成也是一种重要的合成途径。
例如,通过对卟啉类化合物进行改进,引入不同官能团,可以在后续反应中方便地将金属离子引入到卟啉环中,得到期望的金属卟啉化合物。
金属卟啉化合物在生物领域中有着重要的应用。
其中,血红蛋白和肌红蛋白是含有铁卟啉结构的蛋白质,在传递氧气和电子传递过程中发挥着关键作用。
此外,金属卟啉化合物还被广泛用作生物标记物、光敏剂等。
例如,卟啉类化合物可用于磁共振成像、光动力疗法等。
此外,金属卟啉化合物还可以用于合成人造光合色素等生物医学材料,具有巨大的应用潜力。
除了在生物领域中的应用,金属卟啉化合物还在材料科学、催化化学等领域中发挥重要作用。
例如,金属卟啉化合物常被用作催化剂,参与氧化反应、甲醛氧化等过程。
此外,在光电子器件、光催化水裂解等方面也有广泛的应用。
金属卟啉化合物因其优良的光电性能、催化活性等特点,被认为是一类具有潜力的功能材料。
综上所述,金属卟啉化合物的合成方法和应用具有重要的实际意义。
通过不断深入研究金属卟啉化合物的合成及性质,可以拓展其在生物医学、材料科学、催化化学等领域的应用,推动相关领域的发展。
金属卟啉化合物作为一类具有潜力的功能材料,必将在未来的研究和应用中发挥越来越重要的作用。
新型卟啉化合物的合成及性质

一
CHO + P ro y rl
Байду номын сангаас
r P o ine / r p o i -
:
”
M WI
A
R —C b HO +P ro +Z ( O) yrl nAe 2
C2 CO2 Ae Hs H, OH
:
u
Nir e z n e u tob n e erf x l
B
S h me 1 S n h ss r u e fc m p u d a d B c e y t e i o t o o o n s A n s
0 1 .5mL吡 咯置于 2 L烧 瓶 中混合 均 匀 .装 上 冷 凝 管 , 入 微 波 炉 中 ,以 60 W 功 率 分 多 次 辐射 0m 放 0 1 i.反应 完毕后 自然 冷却 , 5mn 加入 4 0mL乙醇 过夜 .抽 滤 ,用 乙醇 洗 至滤 液无 色 , 水 M S 干燥 , 无 gO
参 照 文献 [ 1 的方 法 ,采 用 微 波 辐 照 法 合 成 目标 化 合 物 A.将 07 C O、适 量 的丙 酸 及 1] .1gR .H
收稿 日期 : 0 61-5 2 0 —22 . 基金项 目:吉林省科技发展计划( 准号 : 04 59 和教育部高校博 士学科点专项科研基金 ( 批 2 0 06 ) 批准号 : 0 5 140 ) 20 0 8 0 2 资助
断, 即齐聚苯乙烯撑 ( P ) O V 结构单元.所以在卟啉大 仃键 的芳香体系——卟啉环的中位上引入具有供 电子兼助溶的基团( P O V结构单元) 可使分子具有更大的共轭性 , , 因而使其具有更好的光电性能和其 它 物理性质 . 本文对带有 O V取代基的卟啉配体和锌配合物的合成和性能进行 了研究, 中 O V取代基的卟 P 其 P
卟啉化合物的合成及物理化学性质
卟啉化合物的合成及物理化学性质周彬 ,张文 ,曾琪 ,张智(武汉大学 化学与分子科学学院 ,武汉 430072)【摘要】利用中位-四[对羟基苯基]卟啉和四水合乙酸钴在DMF 中搅拌加热至100℃回流30min 合成了金属钴卟啉。
然后再用柱层析分离得到纯净的金属卟啉产物。
利用电导率仪研究了金属卟啉金属钴卟啉的电迁移性质。
通过金属钴卟啉配合物与咪唑配位动力学的研究证实了其轴向上存在配位作用。
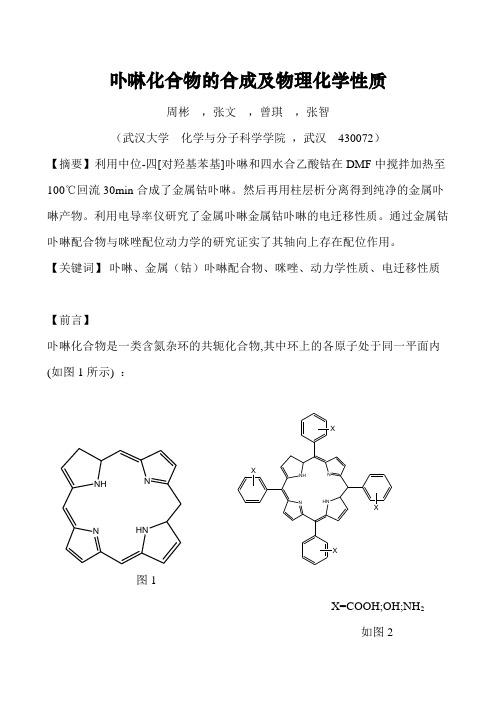
【关键词】 卟啉、金属(钴)卟啉配合物、咪唑、动力学性质、电迁移性质【前言】卟啉化合物是一类含氮杂环的共轭化合物,其中环上的各原子处于同一平面内(如图1所示) :NHNHNNNHNHNNXXXX图1X=COOH;OH;NH 2如图2卟啉环中含有四个吡咯环,每两个吡咯环在2位与5位之间由一个次甲基桥连,在5,10,15,20,位上也可键合四个取代苯基(如图2),形成四取代苯基卟啉。
卟啉环中有交替的单键和双键,有18个π电子组成的共轭体系,具有芳香性。
当两个氮原子上的质子电离后,其形成的空腔中可以容纳Fe,Co,Mg,Cu,Zn,等金属离子而形成金属配合物,并且这些金属配合物都具有一些生理上的作用。
卟啉化合物具有对光,热的良好稳定性。
它的这种稳定性,大的可见光消光系数和它在电荷转移过程中的特殊作用,使得它在光电领域中的应用受到高度重视,它被用于气体传感器,太阳能的贮存,生物模拟氧化反应的催化剂,生物大分子探针,还可以作为模拟天然产物的母体,金属卟啉配合物被广泛的应用于微量分析等领域。
本实验合成并提纯了卟啉配合物,采用电导仪测定金属配合物在溶液中的电迁移性质,还就其与有机碱的轴向配位反应进行动力学的测定。
【实验部分】⒈试剂与仪器:1.1试剂卟啉,醋酸钴,DMF(二甲基甲酰胺),无水乙醇,无水乙醚,二氯甲烷,丙酮,环己烷,薄层层析硅胶,柱层析硅胶,氢氧化钠,咪唑,1.2仪器紫外-可见分光光度仪,傅立叶变换红外光谱仪,DD3001电导率仪,分析天平,电磁搅拌器,减压蒸馏装置,旋转蒸发仪,抽滤装置,真空干燥器.⒉实验步骤:2.1金属(钴)卟啉配合物的合成与分离在25 ml两口烧瓶中加入0.1540g中位-四(对羟基苯基)卟啉与8mlDMF,搅拌加热,至100o C时加入卟啉量的10倍摩尔量的四水和乙酸钴(0.5606g),继续加热至回流,并保持回流状态20-30min。
卟啉化合物的合成、理化性质及其应用

2012.11.27-2010.12.10卟啉化合物的合成、理化性质及其应用(苏州大学材料与化学化工学部09级化学类)摘要:为了了解卟啉化合物,用郭灿城等人提出新方法合成TPPH2和CoTPP,并利用红外、紫外与荧光光谱分析其结构。
关键词:TPPH2、CoTPP、合成Abstract:To understand the synthesis and token of Porphyrins,we synthetise TPPH2and CoTPP with new method proposed by Cancheng Guo et al,and characterized by FT-IR,UV and fluorescence spectrum.Keywords:TPPH2、CoTPP、synthetize1.前言卟啉(porphyrins)是卟吩(porphine)外环带有取代基的同系物和衍生物的总称,当其氮上2个质子被金属离子取代后即成金属卟啉配合物(metalloporphyrins)。
自然界中存在许多天然卟啉及其金属配合物,如血红素、叶绿素、维生素B12、细胞色素P-450、过氧化氢酶等。
天然卟啉化合物具有特殊的生理活性。
人工合成卟啉来模拟天然卟啉化合物的各种性能一直是人们感兴趣和研究的重要课题。
由于卟啉化合物独特的结构、优越的物理、化学及光学特征,使得卟啉化合物在仿生学、材料化学、药物化学、电化学、光物理与化学、分析化学、有机化学等领域都具有十分广阔的应用前景,正吸引着人们对卟啉化学不断深入地研究。
本实验采用郭灿城等人提出的合成四苯基卟啉的新方法,合成TPPH2和CoTPP,并利用红外、紫外与荧光光谱分析其结构。
2.实验部分2.1、仪器与药品仪器:烧杯(50mL×2、100mL×1)、量筒(50mL)、三颈烧瓶(250mL,19#×1/14#×2)、双颈烧瓶(50mL,19#×2)、茄形瓶(250mL,24#)、恒压滴液漏斗(14#)、球形冷凝管(19#)、干燥管(19#)、空心塞(19#×2、14#×2)、布氏漏斗及抽滤瓶、色谱柱(24#)、调压变压器、旋转蒸发仪、温度计(300℃)、油浴、磁力搅拌器、回流装置。
金属卟啉化合物的合成和应用

金属卟啉化合物的合成和应用金属卟啉化合物是一类重要的有机金属化合物,具有广泛的应用领域。
本文将从合成方法、结构特点和应用三个方面进行探讨。
一、合成方法金属卟啉化合物的合成方法主要有两种:直接合成和间接合成。
直接合成是指通过金属离子与卟啉配体直接反应得到金属卟啉化合物。
这种方法操作简单,反应时间短,适用于合成一些常见的金属卟啉化合物。
例如,将金属离子与卟啉配体在溶剂中反应,通过控制反应条件和配体的选择,可以合成出具有不同金属中心和配位结构的金属卟啉化合物。
间接合成是指通过先合成卟啉配体,再与金属离子反应得到金属卟啉化合物。
这种方法适用于合成一些特殊的金属卟啉化合物,例如含有稀有金属的卟啉化合物。
通过设计合成卟啉配体的结构,可以调控金属卟啉化合物的性质和应用。
二、结构特点金属卟啉化合物的结构特点主要体现在两个方面:金属中心和卟啉配体。
金属中心是金属卟啉化合物的核心,其性质直接影响着化合物的性质和应用。
金属中心的选择可以根据需求来确定,常见的金属中心有铁、铜、锌等。
不同金属中心具有不同的电子结构和配位能力,从而影响了金属卟啉化合物的光电性能和催化性能。
卟啉配体是金属卟啉化合物的配位基团,其结构决定了金属卟啉化合物的稳定性和反应性。
卟啉配体通常由四个吡啶环和一个呋喃环组成,通过改变吡啶环的取代基和呋喃环的取代基,可以调控金属卟啉化合物的溶解性、光谱性质和催化活性。
三、应用领域金属卟啉化合物在多个领域具有广泛的应用。
以下列举几个典型的应用领域:1. 光电材料:金属卟啉化合物具有良好的光电性能,可以作为光电转换材料、光敏材料和光催化材料。
例如,某些金属卟啉化合物可以作为太阳能电池的光敏材料,将光能转化为电能。
2. 生物医药:金属卟啉化合物具有抗氧化、抗菌和抗肿瘤等生物活性,可以应用于药物研发和医学诊断。
例如,某些金属卟啉化合物可以作为抗肿瘤药物,用于治疗肿瘤疾病。
3. 催化剂:金属卟啉化合物具有良好的催化活性和选择性,可以用于有机合成反应和环境保护。
镍配合物卟啉
镍配合物卟啉是一种具有独特结构和性质的化合物,其在多个领域都有着广泛的应用前景。
以下是对镍配合物卟啉的详细介绍。
一、结构与性质镍配合物卟啉由镍离子和卟啉配体组成。
卟啉是一种四吡咯类化合物,具有一个由四个氮原子和四个吡咯环组成的共轭体系。
镍离子与卟啉配体中的氮原子形成配位键,从而形成了稳定的镍配合物。
镍配合物卟啉具有多种优良的性质,如良好的热稳定性、光稳定性、电化学性质等。
此外,其独特的电子结构和光学性质使其在光电器件、催化剂、生物传感器等领域具有广泛的应用价值。
二、合成方法镍配合物卟啉的合成方法多种多样,常见的有模板法、溶剂热法、微波辅助法等。
这些方法各有优缺点,可以根据具体需求选择合适的合成方法。
三、应用领域1.光电器件:镍配合物卟啉具有良好的光电性能,可用于制备太阳能电池、发光二极管等光电器件。
2.催化剂:镍配合物卟啉在催化领域也表现出优异的性能,可用于催化氧化、还原、氢化等反应。
3.生物传感器:由于镍配合物卟啉具有良好的生物相容性和光学性质,因此可用于制备生物传感器,如检测生物分子、细胞等。
四、前景展望随着科学技术的不断发展,镍配合物卟啉在各个领域的应用将会越来越广泛。
未来,我们可以期待在以下方面取得更多突破:1.提高镍配合物卟啉的性能,如光电转换效率、催化活性等;2.开发新的应用领域,如生物医学、环境监测等;3.优化合成方法,降低生产成本,提高产量。
总之,镍配合物卟啉作为一种具有独特结构和性质的化合物,其在多个领域都有着广泛的应用前景。
随着研究的深入和技术的进步,相信镍配合物卟啉将会为我们的生活带来更多惊喜和便利。
卟啉化合物-综合实验
气/水界面上组装蜂窝状结构
非水溶液中组装得到的囊泡结构
卟啉化合物的合成原理(一步法)
Hale Waihona Puke 丙酸吡咯meso-四苯基卟啉
CHO
CHO
+
COOH
+ N H
1 : 3 :4
丙酸
N H
N
N
H N
HOOC
卟啉化合物的分离
柱层析(俗称过柱子) 采用的淋洗液选择依据:极性由小到大 卟啉的淋洗液:氯仿,用甲醇或者乙醇调极
强吸收峰(soret带),另外还有四个小的 Q带吸收峰
2.红外光谱分析: 利用KBr压片的方法,分析谱图中出现的主 要振动吸收峰
性 1.卟啉1:用纯氯仿淋洗 2.卟啉2:先用氯仿淋洗下第一色带,再用
CHCl3:CH3OH(v/v)=95:1淋洗第二色带 (即产物)
详细的合成步骤:
• (1)H2TPP的合成:
取75mL丙酸和2mL(0.02mol)苯甲醛置于250mL 三口圆底烧瓶中,搅拌并加热(~100V),当溶液开始 沸腾时用恒压滴液漏斗将1.4mL(0.04mol)吡咯 逐滴加入,~10min加完,继续回流30min,冷却至 室温,抽滤,得紫色晶体。先用无水乙醇洗涤,后 蒸馏水洗涤2~3次,再用无水乙醇洗涤2-3次,抽 干,转移到表面皿上置于真空干燥器中~10h以除 去吸附的丙酸,得产品0.7g,产率~20%。
具体分离方法:
将所得产品用最少量的氯仿溶解后,用 200-300目的硅胶过柱分离,收集红色溶液, 用减压蒸出氯仿(注意回收!不要乱倒! 有毒!!!),将所得固体再用极少量的 氯仿溶解,沿着器壁慢慢加入少量甲醇, 静置,重结晶,得亮紫色的固体。
两种卟啉的表征
• 1.紫外-可见光谱分析: • 普带特征:大约在420nm处有一个尖锐的
卟啉化合物的合成及光电性能
卟啉化合物的合成及光电性能卟啉是一种重要的天然有机化合物,其分子结构为四个吡啶环通过甲烷桥相连而成,是许多生物体内重要的分子构建块。
因其具有独特的光电性能,广泛应用于光电领域。
本文主要探讨卟啉化合物的合成方法以及其在光电领域的性能表现。
首先,卟啉化合物的合成可通过多种途径实现。
其中,自然界中往往通过生物合成途径产生,而在实验室中,化学合成是常见的方法之一。
通过闭环合成法,可以较为高效地合成卟啉化合物。
闭环合成是指通过碳环的闭合反应,在不断逐步构建分子骨架的过程中,最终合成目标产物。
这种方法具有较高的选择性和效率,是实验室合成卟啉化合物的常用手段之一。
其次,卟啉化合物在光电领域中表现出色的性能。
由于其分子结构的特殊性质,卟啉具有较好的光吸收和电子传输性能。
在太阳能电池中,卟啉化合物可以作为光敏染料,吸收阳光的能量转化为电能。
此外,在光导纤维和光合成中也起到重要作用。
卟啉还可以通过与不同金属配合形成卟啉金属络合物,拓展了其在光电领域的应用领域。
最后,通过对卟啉化合物的研究和合成,可以不断拓展其在光电领域的应用。
通过调控卟啉分子结构,改善其光电性能,提高其在光伏和光催化领域的效率。
同时,进一步研究卟啉与金属的配合反应,探索新的卟啉金属络合物的光电性能,为光电材料的开发提供新的思路和途径。
总的来说,卟啉是一种重要的有机化合物,其在光电领域的应用潜力巨大。
通过合成方法的不断改进和性能研究的深入探索,将为卟啉化合物在光电领域的应用提供更为广阔的前景。
希望未来能够有更多的研究者加入到这一领域,共同推动卟啉化合物的应用与发展。
卟啉类化合物的合成与性质研究
卟啉类化合物的合成与性质研究卟啉类化合物是一类具有特殊结构和重要应用价值的有机化合物。
它们由四个吡咯环通过共享碳原子构成,并且在一个或多个环上含有金属原子。
卟啉类化合物在生物学、材料科学和光电子学等领域具有广泛的应用。
本文将探讨卟啉类化合物的合成方法和性质研究。
一、卟啉类化合物的合成方法卟啉类化合物的合成方法多种多样,其中最常见的方法是通过酸催化的缩合反应合成。
这种方法利用吡咯环上的氨基和醛基或酮基之间的反应,生成卟啉环。
此外,还可以通过金属催化的反应合成卟啉类化合物。
金属催化反应的优势在于反应条件温和,产率高,适用范围广。
二、卟啉类化合物的性质研究卟啉类化合物具有许多独特的性质,其中最引人注目的是它们的光学性质。
由于卟啉环中的共轭双键结构,卟啉类化合物具有很强的吸收和发射光谱。
这使得它们在光电子学领域有着广泛的应用,如光敏染料、光电转换器件等。
此外,卟啉类化合物还具有良好的电子传输性质。
由于卟啉环中的共轭结构,电子在分子内可以自由传输,使得卟啉类化合物成为一种优良的电子传输材料。
这一性质使得卟啉类化合物在有机电子器件中有着广泛的应用,如有机太阳能电池、有机场效应晶体管等。
此外,卟啉类化合物还具有较强的配位性质。
由于卟啉环上的氮原子可以与金属形成配位键,卟啉类化合物可以与金属离子形成稳定的配合物。
这些配合物在生物学和催化领域有着重要的应用,如血红素和维生素B12等。
三、卟啉类化合物的应用前景卟啉类化合物由于其独特的结构和多样的性质,具有广泛的应用前景。
在生物学领域,卟啉类化合物被广泛应用于光动力疗法、荧光探针和生物传感器等。
在材料科学领域,卟啉类化合物可用于制备光电材料、催化剂和分子电子器件等。
在光电子学领域,卟啉类化合物可用于制备光电转换器件、光敏染料和有机发光二极管等。
总之,卟啉类化合物的合成与性质研究对于推动生物学、材料科学和光电子学等领域的发展具有重要意义。
通过不断深入研究,我们可以进一步了解卟啉类化合物的结构与性质之间的关系,为其应用提供更加可靠的理论基础。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
卟啉化合物的合成及物理化学性质
周彬 ,张文 ,曾琪 ,张智
(武汉大学 化学与分子科学学院 ,武汉 430072)
【摘要】利用中位-四[对羟基苯基]卟啉和四水合乙酸钴在DMF 中搅拌加热至100℃回流30min 合成了金属钴卟啉。
然后再用柱层析分离得到纯净的金属卟啉产物。
利用电导率仪研究了金属卟啉金属钴卟啉的电迁移性质。
通过金属钴卟啉配合物与咪唑配位动力学的研究证实了其轴向上存在配位作用。
【关键词】 卟啉、金属(钴)卟啉配合物、咪唑、动力学性质、电迁移性质
【前言】
卟啉化合物是一类含氮杂环的共轭化合物,其中环上的各原子处于同一平面内(如图1所示) :
NH
N
HN
N
NH
N
HN
N
X
X
X
X
图1
X=COOH;OH;NH 2
如图2
卟啉环中含有四个吡咯环,每两个吡咯环在2位与5位之间由一个次甲基桥连,在5,10,15,20,位上也可键合四个取代苯基(如图2),形成四取代苯基卟啉。
卟啉环中有交替的单键和双键,有18个π电子组成的共轭体系,具有芳香性。
当两个氮原子上的质子电离后,其形成的空腔中可以容纳Fe,Co,Mg,Cu,Zn,等金属离子而形成金属配合物,并且这些金属配合物都具有一些生理上的作用。
卟啉化合物具有对光,热的良好稳定性。
它的这种稳定性,大的可见光消光系数和它在电荷转移过程中的特殊作用,使得它在光电领域中的应用受到高度重视,它被用于气体传感器,太阳能的贮存,生物模拟氧化反应的催化剂,生物大分子探针,还可以作为模拟天然产物的母体,金属卟啉配合物被广泛的应用于微量分析等领域。
本实验合成并提纯了卟啉配合物,采用电导仪测定金属配合物在溶液中的电迁移性质,还就其与有机碱的轴向配位反应进行动力学的测定。
【实验部分】
⒈试剂与仪器:
1.1试剂
卟啉,醋酸钴,DMF(二甲基甲酰胺),无水乙醇,无水乙醚,二氯甲烷,丙酮,环己烷,薄层层析硅胶,柱层析硅胶,氢氧化钠,咪唑,
1.2仪器
紫外-可见分光光度仪,傅立叶变换红外光谱仪,DD3001电导率仪,分析天平,电磁搅拌器,减压蒸馏装置,旋转蒸发仪,抽滤装置,真空干燥器.
⒉实验步骤:
2.1金属(钴)卟啉配合物的合成与分离
在25 ml两口烧瓶中加入0.1540g中位-四(对羟基苯基)卟啉与8mlDMF,搅拌加热,至100o C时加入卟啉量的10倍摩尔量的四水和乙酸钴(0.5606g),继续加热至回流,并保持回流状态20-30min。
然后,将产物倒入300ml冰水中,陈化2小时,抽滤,并将得到的固体在烘箱中烘干。
在陈化过程中制作薄板层析硅胶板,并与柱层析硅胶一并活化,在120C的条件下活化2小时。
利用薄板层析法选择二氯甲烷:丙酮为3:1的比例作为合适的淋洗剂。
然后进行柱层析,收集金属卟啉配合物,旋转蒸发,置于干燥器中干燥,备用。
2.2金属(钴)卟啉配合物的电迁移性质测定
⑴准确称取2.8mg的钴卟啉,倒入10ml的容量瓶中,用无水乙醇溶解并稀释至刻度,准确配制约10-2mol/l的氢氧化钠乙醇溶液。
⑵调节电导率仪的恒温水槽至25o C,取3.0ml钴卟啉溶液于一支干净的试管中,测量其电导率,并记录。
再逐次加入5μL的氢氧化钠溶液,测量其电导率至30次,并分别记录每一次的电导率值。
最后,用3ml的无水乙醇溶液作空白实验,依次测量加入5μL的氢氧化钠溶液的电导。
绘制电导-氢氧化钠的体积曲线。
2.3金属(钴)卟啉配合物与咪唑配位动力学测定
⑴准确称取0.1756g咪唑溶于适量无水乙醇中,待溶解后转入一个25ml 的容量瓶中,并用乙醇稀释到刻度。
配成浓度为约0.100mol/L的咪唑乙醇溶液,标记为1号。
再从1号瓶中吸取12.5ml的溶液于另一个干净的25ml 的容量瓶中,并稀释到刻度,标记为2号。
从1号瓶中吸取2.5ml的溶液于另一25ml的容量瓶中,稀释到刻度,标记为3号。
从3号瓶中吸取2.5ml
溶液于另一个干净的25ml的容量瓶中,用乙醇稀释到刻度,标记为4号。
⑵称取2.1mg卟啉钴,转入一个25ml的容量瓶中,加入无水乙醇溶解并
稀释到刻度。
⑶在定性模式中安装ABS为0—2;λ为480—380nm;显示模式为叠加
式的测量参数。
用双池无水乙醇作空白参比,校正波长和ABS零基线。
⑷装入3.6ml定性扫描寻找纯卟啉溶液的最大吸收波长值。
打印纯卟啉
的定性扫描图谱和吸光度—波长值数据表。
⑸在定性扫描模式中以1:1的比例(1.8ml卟啉和1.8ml咪唑)于石英
比色皿中,测混合物在413nm和436nm时的配位反应过程的ABS值。
每一分钟切换一次413nm和436nm波长值并记录相应的ABS值。
每5分钟扫描一次所测溶液的叠加式定性扫描谱图,15分钟打印一次。
⑹按⑸的方法测量其他几个浓度(由低到高)的咪唑配位溶液在两个不
同波长值下的ABS值并记录。
2.4 作钴卟啉化合物的红外光谱图。
【数据处理与结果讨论】
⑴电迁移分析
实验数据见下表:
序号.NaOH体积
(μL)
卟啉电导(μ
s/cm)
空白电导(μ
s/cm)
净电导(μ
s/cm)
1 0 2.790.438 2.352
2 5 3.69 1.356 2.334
3 10 4.58 2.37 2.21
4 1
5 5.43 3.38 2.05
5 20 6.29 4.3
6 1.93
6 25 7.14 5.3
7 1.77
7 30 8.03 6.28 1.75
8 35 9.017.39 1.62
9 40 9.698.23 1.46
10 45 10.479.28 1.19
11 50 11.1410.170.97
12 55 11.9611.010.95
13 60 12.7311.810.92
14 65 13.712.770.93
15 70 14.4213.570.85
16 75 15.3914.60.79
17 80 16.1915.510.68
18 85 16.8516.390.46
19 90 17.5417.120.42
20 95 18.518.10.4
21 100 19.0518.860.19
22 105 19.77 19.64 0.13 23 110 20.5 20.4 0.1 24
115
21.3
21.3
根据数据作电导—NaOH 体积图:
电导(μs /c m )
V NaOH (μL)
图3 卟啉钴的电迁移分析
从电导-氢氧化钠溶液体积曲线上可发现有四个拐点,而所制得的卟啉钴上刚好有四个酚羟基,说明所合成的四取代苯基卟啉可在碱溶液中呈离子态。
⑵金属卟啉与有机碱轴向配位动力学分析 实验数据见下表:
不同浓度咪唑配位后的A(波长=413nm)
log((Ai-2. 9850)/(0. 8279-Ai))= logKb+m logC ;logKb= 2.84611, m= 0.66975;Kb= 701.633
l o g ((A i -2. 9850)/(0. 8279-A i ))
logC
反应中,随着咪唑浓度的增加,钴卟啉的轴向逐渐被满配位,紫外415.8处的吸收强度逐渐减弱,而438.8处的吸收强度逐渐增强。
每两分子咪唑与一分子钴卟啉配位。
⑶红外光谱分析
红外光谱图上可以看到: 在3361.0cm -1出现强,宽吸收带,分析为多聚态酚羟基伸缩振动,有于内氢键存在,使γ
OH
向低波数移动。
在1600—1450cm -1
处有若干峰,说明含有苯环或杂芳环的骨架伸缩振动。
符合金属(钴)卟啉配合物的结构。
【参考文献】
[1]胡宏纹.有机化学.高等教育出版社,1990
[2]游效曾.配位化合物的结构和性质,科学出版社,1992 [3]JJ Zupancic,S L Pttey Weeks,A patent5,018,380,1991 [4]R Aroca,H Bolourchi,D Battisti,K ngmuir.1993,9,3183
[5]A Lmoore,D Gary,G Devens,T A Moore.Photochem.Photobiol,1980,32(5),691
[6]L R Milgron.J.Chem.Soc.Perkin Trans,1983,10,2535
[7]JJ Van Hemmen.Radiat.Res.,1978,75(2),410
[8]W D Horrocks Jr,C Pwang.J.Am.Chem.Soc,1976,98,7157
[9]J W Buchler.in”Porphyris and Metalloporphyrins”,ed. Kevin M Smith,Elsevier Scientific Publishing Company. Amster dam.The Netherland,1975,157
[10] 李早英,黄杰生.有机化学,1997,17,203
[11]周晓海等,武汉大学学报(自然科学版),1994,3,79
[12]周晓海等,科学通报,1995,40(21),1958
[13]《综合化学实验》武汉大学化学与分子科学学院实验中心,武汉大学出版社,2003。
