葡萄糖酸钙钙含量测定分析报告
2024年葡萄糖酸钙市场调查报告

2024年葡萄糖酸钙市场调查报告1. 引言葡萄糖酸钙是一种常见的补充钙的营养品,被广泛应用于食品、药品和饲料等行业。
本报告旨在对葡萄糖酸钙市场进行调查和分析,以揭示该市场的现状、发展趋势和竞争态势。
2. 市场规模和增长趋势根据调查数据显示,葡萄糖酸钙市场在过去几年里持续增长。
2018年,全球葡萄糖酸钙市场规模约为XX亿美元,预计到2025年将达到XX亿美元。
市场增长主要受到增加的需求和不断发展的应用领域的推动。
葡萄糖酸钙作为一种重要的钙补充剂,其在医药领域的应用前景广阔,这也是市场增长的重要驱动力之一。
3. 市场分析3.1 主要应用领域葡萄糖酸钙广泛应用于食品、药品和饲料等行业。
在食品领域,葡萄糖酸钙常用于乳制品、糕点和饼干等产品中,以增加钙的含量。
在药品领域,葡萄糖酸钙常用于制剂、保健品和钙片等产品中,以补充钙质。
在饲料领域,葡萄糖酸钙主要用于饲料添加剂,提高动物的饲料健康水平。
3.2 地区分布根据市场调查,葡萄糖酸钙市场在全球范围内分布广泛。
亚太地区是该市场的主要消费地区,占据全球市场份额的XX%。
其次是欧洲和北美地区,占据市场份额的XX%和XX%。
其他地区的市场份额相对较低。
3.3 竞争态势目前,葡萄糖酸钙市场存在着激烈的竞争。
全球范围内有多家企业参与市场竞争,其中包括XX公司、XX公司和XX公司等。
这些企业在产品质量、价格和品牌影响力等方面具有一定的竞争优势。
为了在市场中保持竞争力,企业需要不断提高产品质量和技术创新能力,同时寻求更为广阔的市场拓展和合作机会。
4. 市场前景随着人们对健康意识的不断提高和生活水平的提升,葡萄糖酸钙市场有望继续保持良好的发展势头。
未来几年里,市场需求将进一步增加,特别是在医药领域的应用前景非常广阔。
同时,随着全球经济的发展和食品安全意识的增强,葡萄糖酸钙市场的国际贸易也将持续增长。
5. 结论综上所述,葡萄糖酸钙市场在全球范围内持续增长。
市场规模不断扩大,主要受到增加的需求和不断发展的应用领域的推动。
葡萄糖酸钙含量的测定

mL 的 EDTA 标 准 溶
第 2 份:
第 3 份:
填写下表:
编号
1
EDTA 溶液的浓度 cEDTA(mol/L)
EDTA 溶液浓度的平均值 cEDTA(mol/L) 相对偏差(%)
2.葡萄糖酸钙含 量计算 第Ⅰ份:
第Ⅱ份:
第Ⅲ份:
填写下表:
样品编号
Ⅰ
葡萄糖酸钙含量( g/mL)
葡萄糖酸钙含量平均值( g/mL)
相对偏差(%)
三、实训结果讨论 分析:
2
3
Ⅱ
Ⅲ
四、思考题: 1、标定 EDTA 标准溶液的基准物有哪些?选择时应注意什么?
2、用铬黑 T 做指示剂,为什么要控制在 pH≈10?
锌标准溶液的浓度(mol/L) 锌标准溶液的体积(mL)
滴定消耗 EDTA 溶液的体积(mL)
4.葡 萄 糖 酸 钙 含 量 的 测 定
样品的体积(mL) 滴定样品消耗 EDTA 溶液的体积(mL)
二、实训结果计算 : 1 . EDTA 标准溶液的浓 度
g, 加入
mL1+1 盐酸,用
定容,
g, 配 成 1
贺州学院
项 目 实 训(验)报 告
Training Item Report
评
语
Comment
姓名 Name 项目编号 Item No. 课程名称 Course
成绩 Score
教师签字
日期
Signature of Tutor______________Date:_______
学时 Time
学号
Student No.
14
项目名称
Item
分析化学
班级 Class
葡萄糖酸钙实验报告

一、实验目的1. 了解葡萄糖酸钙的理化性质。
2. 掌握葡萄糖酸钙含量的测定方法。
3. 熟悉实验操作流程,提高实验技能。
二、实验原理葡萄糖酸钙是一种白色结晶性粉末,无臭,有甜味,易溶于水,微溶于醇。
本实验采用滴定法测定葡萄糖酸钙含量,利用葡萄糖酸钙与氢氧化钠反应生成葡萄糖酸钠和氢氧化钙,通过滴定氢氧化钠溶液消耗的体积计算出葡萄糖酸钙的含量。
三、实验仪器与试剂1. 仪器:电子天平、滴定管、烧杯、玻璃棒、锥形瓶等。
2. 试剂:葡萄糖酸钙标准溶液、氢氧化钠标准溶液、酚酞指示剂、蒸馏水等。
四、实验步骤1. 准备工作:将葡萄糖酸钙样品在105℃下干燥至恒重,准确称取0.1g干燥样品,放入锥形瓶中。
2. 配制溶液:准确移取25.00mL葡萄糖酸钙标准溶液于烧杯中,加入50mL蒸馏水,用玻璃棒搅拌使其溶解。
3. 滴定:向锥形瓶中加入2滴酚酞指示剂,用氢氧化钠标准溶液进行滴定,直至溶液由无色变为浅红色,记录消耗的氢氧化钠标准溶液体积。
4. 计算结果:根据滴定消耗的氢氧化钠标准溶液体积,计算葡萄糖酸钙含量。
五、实验数据与结果1. 样品干燥后质量:0.1g2. 滴定消耗氢氧化钠标准溶液体积:V1 mL3. 葡萄糖酸钙含量计算公式:C(葡萄糖酸钙)=(C(氢氧化钠)×V1×M)/m其中,C(氢氧化钠)为氢氧化钠标准溶液的浓度,V1为滴定消耗的氢氧化钠标准溶液体积,M为葡萄糖酸钙的摩尔质量,m为样品干燥后的质量。
六、实验结果与分析1. 根据实验数据,计算得到葡萄糖酸钙含量为X mg/g。
2. 分析:实验过程中,滴定终点判断准确,实验操作规范,结果可靠。
通过实验,掌握了葡萄糖酸钙含量的测定方法,提高了实验技能。
七、实验总结1. 本实验成功测定了葡萄糖酸钙的含量,达到了实验目的。
2. 通过实验,掌握了葡萄糖酸钙的理化性质,了解了实验原理。
3. 提高了实验操作技能,为今后实验工作奠定了基础。
八、实验注意事项1. 实验过程中,注意安全操作,防止实验事故发生。
葡萄糖酸钙含量的测定

葡萄糖酸钙含量的测定实验目的:1.强化滴定法的操作2.强化分析天平,容量瓶移液管,吸量管,滴定管 ,锥形瓶 ,溶液配制及转移容量仪器的洗涤干燥,滴定分析操作实验原理:)/(1000)()()(22L mmol V EDTA V EDTA C ca C ⨯⨯=+水样1,EDTA 是常用的螯合滴定剂,可滴定多种金属离子,与金属离子按1:1的比例结合2.在待测液中加入钙红指示剂(蓝色) 它与钙离子配位呈红色3.滴定时,EDTA 先与游离钙离子配位,然后夺取已和指示剂配位的钙离子,从而使指示剂被释放出来,达终点时,溶液由红色变为蓝色,此时可根据EDTA 标准溶液消耗量计算出钙离子的含量仪器与试剂:仪器:分析天平,100ml 容量瓶,5ml 吸量管 滴定管,锥形瓶 ,烧杯,滴定台,药勺,洗耳球,玻璃棒,胶头滴管试剂:待测葡萄糖酸钙粉末,钙红指示剂,蒸馏水,0.05 mol/L 的EDTA 标准溶液实验步骤:1,用分析天平称量3g葡萄糖酸钙粉末2.将葡萄糖酸钙粉末溶于10ml50~60℃的蒸馏水中3. 将葡萄糖酸钙溶液转移到100ml容量瓶中,用胶头滴管加入蒸馏水至刻度线4.从容量瓶中取出部分溶液到烧杯中,用吸量管吸取20.00ml溶液到锥形瓶中,0.05mol/L的EDTA标准溶液加入到滴定管中,记下初始读数,6.开始滴定,当溶液由红色变成蓝色时停止滴定,记下此时读数,7.再重复滴定两次数据记录与结果分析日期:温度:结实验编号 1 2 3 葡萄糖酸钙溶液V(EDTA)/mlV初(EDTA)/ml平均(EFTA)/ml相对平均偏差 /%葡萄糖酸钙含量/%讨论。
电位滴定法测定葡萄糖酸钙的含量
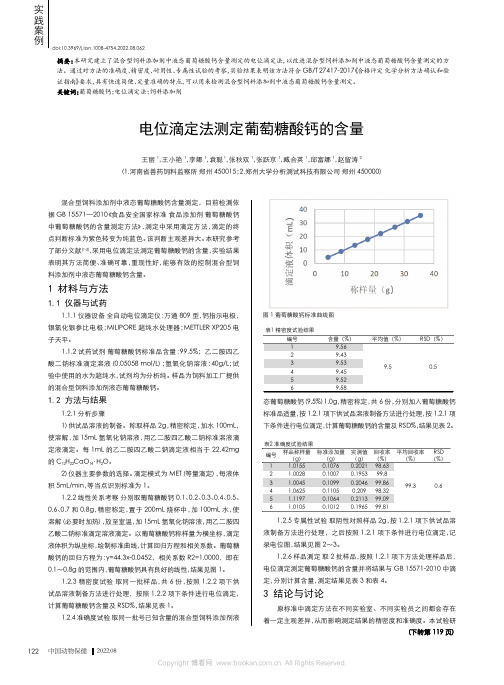
中国动物保健2022.08实践案例电位滴定法测定葡萄糖酸钙的含量王丽1,王小艳1,李娜1,袁聪1,张秋双1,张跃京1,臧合英1,邱富娜1,赵留涛2(1.河南省兽药饲料监察所郑州450015;2.郑州大学分析测试科技有限公司郑州450000)研究建立了混合型饲料添加剂中液态葡萄糖酸钙含量测定的电位滴定法,以改进混合型饲料添加剂中液态葡萄糖酸钙含量测定的方法。
通过对方法的准确度、精密度、耐用性、专属性试验的考察,实验结果表明该方法符合GB/T 27417-2017《合格评定化学分析方法确认和验证指南》要求,具有快速简便、定量准确的特点,可以用来检测混合型饲料添加剂中液态葡萄糖酸钙含量测定。
糖酸钙;电位滴定法;饲料添加剂混合型饲料添加剂中液态葡萄糖酸钙含量测定,目前检测依据GB 15571—2010《食品安全国家标准食品添加剂葡萄糖酸钙中葡萄糖酸钙的含量测定方法》,测定中采用滴定方法,滴定的终点判断标准为紫色转变为纯蓝色。
该判断主观差异大。
本研究参考了部分文献[1-3],采用电位滴定法测定葡萄糖酸钙的含量,实验结果表明其方法简便、准确可靠,重现性好,能够有效的控制混合型饲料添加剂中液态葡萄糖酸钙含量。
1材料与方法1.1仪器与试药1.1.1仪器设备全自动电位滴定仪:万通809型,钙指示电极,银氯化银参比电极;MILIPORE 超纯水处理器;METTLER XP205电子天平。
1.1.2试药试剂葡萄糖酸钙标准品含量:99.5%;乙二胺四乙酸二钠标准滴定溶液(0.05058mol/L );氢氧化钠溶液:40g/L ;试验中使用的水为超纯水,试剂均为分析纯。
样品为饲料加工厂提供的混合型饲料添加剂液态葡萄糖酸钙。
1.2方法与结果1.2.1分析步骤1)供试品溶液的制备。
称取样品2g ,精密称定,加水100mL ,使溶解,加15mL 氢氧化钠溶液,用乙二胺四乙酸二钠标准溶液滴定液滴定。
每1mL 的乙二胺四乙酸二钠滴定液相当于22.42mg 的C 12H 22CaO 14·H 2O 。
原子吸收光谱分析法测定补钙剂中钙含量

第 2期
大
学
物
理
实
验
V0 1 . 2 8 No . 2 Ap r . 2 01 5
2 0 1 5年 4月
P HYS I C AL EXP E RI MEN T OF C OL L E GE
文章 编 号 : 1 0 0 7 — 2 9 3 4 ( 2 0 1 5 ) 0 2 - 0 0 0 1 - 0 2
文 献标 志码 : A D OI : 1 0 . 1 4 1 3 9 / j . c n k i . c n 2 2 — 1 2 2 8 . 2 0 1 5 . 0 2 . 0 0 1
服液 中钙 的含量 。该方法 准确便捷 , 为特定溶液样 品中各种 微量元素的检测提供 了一条很好 的途径 。
mi n a t i o n o f v a r i o u s n. a c e e l e me nt s i n s p e c i f i c s o l u t i o n s a mp l e s .
Ke y wo r d s : a t o mi c a b s o r p t i o n s p e c t r o p h o t o me t r y ;g r a p h i t e f u r n a c e ;c a l c i u m g l u c o n a t e o r a l s o l u t i o n;
“ 校零” , 再依次 由稀 到浓 测 定 所 配制 的钙元 素 的 标 准使 用液 、 样 品溶 液 的吸光 度值 。
3 结
论
利 用原 子 吸收光谱 分 析法对 不 同品牌 的葡 萄 糖 酸钙 口服溶 液 进 行 了检测 , 准确 测 定 出 了不 同
测定葡萄糖酸钙钙片中钙含量的方法比较

测定葡萄糖酸钙钙片中钙含量的方法比较贺琼【摘要】详细论述了EDTA滴定法与高锰酸钾间接滴定法测定钙片中钙含量的方法比较,从理论上来说,高锰酸钾法具有更高的准确度.通过对样品的测定结果表明,用EDTA滴定法测得钙含量为8.07%,用高锰酸钾间接滴定法测得钙含量为8.29%.经显著性检验,两种方法间不存在显著性差异,可以用EDTA配位滴定法代替高锰酸钾法进行钙含量的测定.【期刊名称】《广州化工》【年(卷),期】2013(041)009【总页数】3页(P159-160,183)【关键词】钙含量;测定;EDTA配位滴定法;高锰酸钾法;葡萄糖酸钙【作者】贺琼【作者单位】常州工程职业技术学院,江苏常州213164【正文语种】中文【中图分类】TQ462钙与身体健康息息相关,钙除成骨以支撑身体外,还参与人体的代谢活动,它是细胞的主要阳离子,还是人体最活跃的元素之一,因此,补钙越来越被人们所重视。
由于中国人的膳食结构因素,从儿童到老年普遍存在补钙问题,众多厂家抓住这一商机,大力宣传,全力推出补钙药品、保健品,目前国内市场有100 多种补钙剂。
我们有必要了解补钙剂中钙的含量。
根据人体需要选择适合自己的补钙方法。
钙片中钙含量的测定有滴定分析法、分光光度法和离子色谱法等很多种方法[1-7]。
鉴定于目前许多补钙制剂尚未收入国家药典,国家尚未提出补钙制剂中钙含量的统一方法[5]。
对此,采用EDTA 滴定法与高锰酸钾间接滴定法两种方法对钙片中钙含量进行测定。
由于钙片本身是颗粒状的,所以要研碎后才能作为试样,否则很难使钙片中的钙成分离解,影响对钙含量的测定。
用EDTA 滴定法是使指示剂与钙离子生成酒红色络合物,当EDTA滴定至终点时,游离出指示剂,溶液呈现蓝色。
用高锰酸钾间接滴定法是利用在弱酸性溶液中,,过滤洗涤后,用硫酸溶解,CaC2O4+2H+=Ca2++H2C2O4,生成用高锰酸钾标准溶液滴定,以高锰酸钾自身为指示剂,从而测得钙的含量。
葡萄糖酸钙钙含量测定分析报告

分析化学大型实验报告葡萄糖酸钙中钙含量的测定姓名学号学院班级一、实验名称:葡萄糖酸钙中钙含量的测定二、实验摘要本实验主要要求对葡萄糖酸钙中钙含量的测定,即如标定溶液中钙的含量,本实验主要采用EDTA络合滴定法与KMnO4氧化法测定钙离子的百分含量。
三、序言葡萄糖酸钙,分子式为Ca(C6H11O7)2,白色结晶性粉末,无臭无味。
主要用作食品的钙强化剂与营养剂、缓冲剂、固化剂、鳌合剂。
本品为白色结晶性或颗粒性粉末;无臭,无味,易溶于沸水,略溶于冷水,不溶于乙醇或乙醚等有机溶剂。
水溶液显中性。
钙是体含量最大的无机物,为维持人体神经,肌肉,骨骼系统,细胞膜和毛细血管通透性正常功能所必需。
钙离子是多酶促反应的重要激活剂,对多生理过程是必需的,如神经冲动传递,平滑肌和骨骼肌的收缩,肾功能,呼吸和血液凝固等。
因此,钙离子的研究对我们的生活有着重大的意义。
四、实验主题自主设计试验,用两种滴定法进行葡萄糖酸钙中钙含量的测定五、主要仪器试剂1.仪器:分析天平(0.1mg)酸式滴定管(50mL)锥形瓶(250 mL)洗耳球移液管(25mL)容量瓶(250mL)烧杯(100mL、600 mL)表面皿玻璃棒煤气灯棉网2.药品:一、EDTA固体CaCO3优级纯酚酞指示剂葡萄糖酸钙样品钙指试剂蒸馏水NaOH优级纯固体二、HCl (6 mol•L、浓盐酸) KMnO4分析纯NaOH优级纯固体Na2C2O4基准试剂NH3.H2O-NH4Cl缓冲溶液(pH=10)甲基橙指示剂H2SO43mol/L蒸馏水六、实验步骤I、用EDTA测定葡萄糖酸钙中钙的含量1、EDTA标准溶液的配置与标定⑴0.020mol/LEDTA溶液的配制称取4.0g乙二胺四乙酸二钠于500ml烧杯中,加200ml水,温热使其溶解完全,加水稀释至500ml,摇匀。
⑵配制0.020mol/L钙标准溶液准确称取110℃干燥过的CaCO30.50~0.55g,置于250ml锥形瓶中,用少量水润湿,盖上表面皿,慢慢滴加1:1 HCl 5 ml使其溶解,加少量水稀释,定量转移至250ml容量瓶中,用水稀释至刻度,摇匀,计算其准确浓度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
分析化学大型实验报告葡萄糖酸钙中钙含量的测定
姓名
学号
学院班级
一、实验名称:
葡萄糖酸钙中钙含量的测定
二、实验摘要
本实验主要要求对葡萄糖酸钙中钙含量的测定,即如何标定溶液中钙的含量,本实验主要采用EDTA络合滴定法与KMnO4氧化法测定钙离子的百分含量。
三、序言
葡萄糖酸钙,分子式为Ca(C6H11O7)2,白色结晶性粉末,无臭无味。
主要用作食品的钙强化剂与营养剂、缓冲剂、固化剂、鳌合剂。
本品为白色结晶性或颗粒性粉末;无臭,无味,易溶于沸水,略溶于冷水,不溶于乙醇或乙醚等有机溶剂。
水溶液显中性。
钙是体内含量最大的无机物,为维持人体神经,肌肉,骨骼系统,细胞膜和毛细血管通透性正常功能所必需。
钙离子是许多酶促反应的重要激活剂,对许多生理过程是必需的,如神经冲动传递,平滑肌和骨骼肌的收缩,肾功能,呼吸和血液凝固等。
因此,钙离子的研究对我们的生活有着重大的意义。
四、实验主题
自主设计试验,用两种滴定方法进行葡萄糖酸钙中钙含量的测定
五、主要仪器试剂
1.仪器:
分析天平(0.1mg)酸式滴定管(50mL)
锥形瓶(250 mL)洗耳球
移液管(25mL)容量瓶(250mL)
烧杯(100mL、600 mL)表面皿
玻璃棒煤气灯
石棉网
2.药品:
一、EDTA固体 CaCO3优级纯
酚酞指示剂葡萄糖酸钙样品
钙指试剂蒸馏水
NaOH优级纯固体
二、HCl (6 mol•L、浓盐酸) KMnO4分析纯
NaOH优级纯固体 Na2C2O4基准试剂
NH3.H2O-NH4Cl缓冲溶液(pH=10)
甲基橙指示剂 H2SO43mol/L
蒸馏水
六、实验步骤
I、用EDTA测定葡萄糖酸钙中钙的含量
1、EDTA标准溶液的配置与标定
⑴0.020mol/LEDTA溶液的配制
称取4.0g乙二胺四乙酸二钠于500ml烧杯中,加200ml水,温热使其溶解完全,加水稀释至500ml,摇匀。
⑵配制0.020mol/L钙标准溶液
准确称取110℃干燥过的CaCO30.50~0.55g,置于250ml锥形瓶中,用少量水润湿,盖上表面皿,慢慢滴加1:1 HCl 5 ml使其溶解,加少量水稀释,定量转移至250ml容量瓶中,用水稀释至刻度,摇匀,计算其准确浓度。
⑶EDTA溶液浓度的标定
称取NaOH固体4.0g溶于100ml水中,配制成40g/LNaOH溶液。
移取25.00ml钙标准溶液置于250ml锥形瓶中,加5ml40g/LNaOH 溶液及少量钙指示剂,摇匀后,用EDTA溶液滴定至溶液由酒红色恰变为纯蓝色,即为终点。
平行滴定三份。
2、葡萄糖酸钙中钙含量的测定
准确称取质量为2.0g的葡萄糖酸钙样品,置于100ml烧杯中,加入5ml6mol/L HCl,适当加热至完全溶解后冷至室温,定量转移至250ml容量瓶中,用水稀释至刻度,摇匀。
用移液管移取上述溶液25.00ml于锥形瓶中,加入
5ml40g/LNaOH,再加少许钙指示剂,用EDTA标准溶液滴定至溶液由酒红色变为纯蓝色,记取EDTA耗用的体积,平行测定三份。
数据处理:
II、高锰酸钾法测定葡萄糖酸钙中钙的含量
利用葡萄糖酸钙中Ca2+与草酸盐形成难溶的草酸钙沉淀,将沉淀经过滤洗涤分离后溶解,用高锰酸钾法测定草酸根含量,换算出Ca 的含量。
反应如下:
Ca2+ + C2O42- == CaC2O4↓
CaC2O4 + 2H+ == Ca2+ + H2C2O4
5H2C2O4 + 2MnO4- +6H+ ==2Mn2+ + 10CO2↑ + 8H2O
1、高锰酸钾标准溶液的配置与标定
(1)高锰酸钾标准溶液的配置
称取1.6gKMnO4溶于500ml水中,盖上表面皿,加热至沸并保持微沸状态半小时,冷却后于室温下放置。
(2)高锰酸钾标准溶液的标定
准确称取0.13~0.16g基准物质NaC2O4置于250ml锥形瓶中,加40ml水,10ml3mol/LH2SO4,加热至70~80℃,趁热用KMnO4溶液进行滴定。
直至滴定的溶液呈微红色,半分钟内不褪色为终点。
2、葡萄糖酸钙中钙含量的测定
准确称取葡萄糖酸钙粉三份,每份0.10g,分别置于250ml,锥形瓶中,加1:1 HCl 2.5ml溶解,加20ml水,加入5%草酸铵溶液50ml,若出现沉淀,再滴加浓HCl至溶解,然后加热至70~80℃,
加入2~3滴甲基橙,溶液呈红色,逐滴加入10%氨水,不断搅拌直至变黄并有氨味逸出为止。
将溶液在温水浴上加热陈化,过滤,沉淀
经洗涤,直至无Cl-。
然后,将带有沉淀的滤纸竖贴在先前用来进行沉淀的烧杯壁上,用1mol/L50ml硫酸把沉淀由滤纸引入烧杯中,再用洗瓶吹洗1~2次,提出滤纸,放在洁净的表面上。
然后,稀释溶液至体积约为100ml,加热至70~80℃,趁热用高锰酸钾标准溶液滴定至溶液呈浅红色,再把滤纸推入溶液中搅碎、褪色,再滴加至浅红色在30S内不消失为止。
数据处理
七、实验结论
经实验测试所得,所用葡萄糖试剂纯度较高,且通过本次试验,我进一步掌握并训练了各种实验操作技巧,锻炼了自己搜集资料并设计实验方案的能力,试验收获颇丰。
八、参考文献
1、《分析化学实验》第三版高等教育出版社。
