FDA批准的激酶小分子抑制剂类药物及分类一览教学提纲
PDE抑制剂专题知识

PDE4的人体分布和结构特点
• PDE-4抑制剂抑制PDE-4活性,增加细胞内 cAMP水平而发挥疗效。
27
1/5/2021
PDE抑制剂专题知识
13
构效关系:
• PDE4B有3个活性位点,分别为金属结核口 袋M、疏水性口袋Q和溶剂填充口袋S。
1/5/2021
PDE抑制剂专题知识
14
• Roflumilast的二氟甲氧基基团结合到Q1口 袋且疏水作用强于甲氧基基团,环丙甲氧 基基团占据了Q2口袋且疏水作用弱于环戊 氧基基团,3,5-二氯吡啶基团延伸到金属结 核口袋M处于水分子形成氢键,2个氯原子 在M口袋处也存在一定的疏水作用。
2)对cAMP进行结构修饰,构建出与cAMP高度同源 性的PDE4抑制剂,从而进一步提高PDE4抑制剂 的选择性,增加药效的同时最大限度的降低毒副 作用。
1/5/2021
PDE抑制剂专题知识
24
1/5/2021
PDE抑制剂专题知识
25
1/5/2021
PDE抑制剂专题知识
26
1/5/2021
PDE抑制剂专题知识
16
西洛司特(Cilomilast)
4-氰基-4-(3-环戊氧基-4-甲氧基苯基)环己烷-1-甲酸 分子式 C20H25NO4,分子量 343.42
1/5/2021
PDE抑制剂专题知识
17
• 药效基团:羧基酸,苄基腈,3-环戊基氧基 -4-甲氧基苯
美国FDA批准上市的药物(2019年)
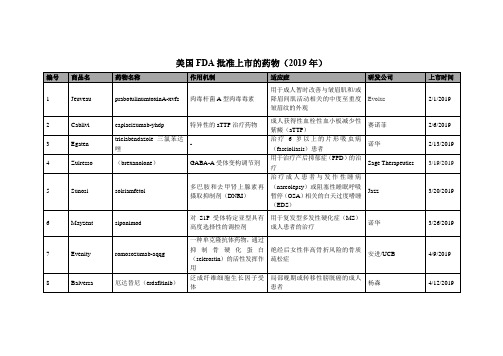
用于眼科手术
Dutch Ophthalmic, USA
12/20/2019
45
Caplyta
lumateperone tosylate
多巴胺受体磷酸蛋白调节剂(DPPM),在D2受体上充当突触前部分激动剂和突触后拮抗剂。
精神分裂症
Kah-PLY’-tah
Intra-Cellular Therapies, Inc.
-
用于治疗成人由于人工型或遗传性转甲状腺素卵白介导的淀粉样变性引起的心肌病(ATTR-CM)
辉瑞
5/3/2019
11
Piqray
Alpelisib
PIK3抑制剂
治疗绝经后女性及男性特定晚期或转移性乳腺癌患者
诺华
5/24/2019
12
Polivy
polatuzumab vedotin-piiq
CD79b
全球结核病药物开发联盟(TB Alliance)
8/14/2019
20
Wakix
pitolisant
用于治疗成年发作性睡病(narcolepsy)患者的白日过度嗜睡(EDS)
Bioprojet
8/14/2019
21
Rozlytrek
entrectini恩曲替尼
选择性酪氨酸激酶抑制剂
用于ROS1阳性转移非小细胞肺癌和所有NTRK融合实体瘤(12岁以上)
12/20/2019
46
Dayvigo
lemborexant
食欲素受体拮抗剂
失眠症
卫材公司
12/20/2019
47
Enhertu
fam-trastuzumab deruxtecan-nxki
HER2靶点的抗体偶联药物
FDA批准的激酶小分子抑制剂类药物及分类一览

FDA批准的激酶小分子抑制剂类药物及分类一览蛋白激酶蛋白激酶(Kinase)是细胞生命活动重要的信号使者,可催化将ATP末端的γ-磷酸基团转移至底物上,从而将各种信号进行传递(图1)。
蛋白激酶参与了众多的生理过程,包括细胞增殖、存活、凋亡、代谢、转录以及分化等。
药理学及病理学研究表明,对于很多疾病,如肿瘤、炎症性疾病、中枢神经系统疾病、心血管疾病及糖尿病等,蛋白激酶都是一个理想的药物靶点。
图1 Mechanism of protein kinases and related publications对于蛋白激酶的研究始于20世纪50年代,并在90年代随着MAPK/ERK、JAK及PI3K等信号通路的揭示而达到一个研究热潮。
迄今为止,在人体中发现了518种蛋白激酶,而编码具有激酶活性蛋白的基因则高达900多种。
与之相对应,有关激酶抑制剂的研究也逐步发展,并在激酶作用机制的阐明过程中扮演了重要角色,并成为重要的药物研究热点。
该领域研究的文献数量也是逐年上升,从侧面反映了其在基础研究和药物发现中的重要性。
蛋白激酶抑制剂及其分类过去的15年间,激酶抑制剂作为药物候选的研究取得了长足的进步,不论是基础研究还是在工业界。
在人体现有药物靶点里面,蛋白激酶家族成员占比高达10%(FDA批准药物分子靶点深度解读)。
2001年,第一个激酶抑制剂类药物Imatinib获得FDA批准,成为该领域发展的里程碑,此后十年该类药物以平均每年获批一种的速度稳步发展。
而在2012年1月至2015年2月期间,小分子激酶抑制剂类药物迎来爆发式发展,共有15种新药获得审批。
截至2016年12月底,共有31种小分子激酶抑制剂类药物获得审批,同时还有大量的化合物处于临床或临床前研究中。
除此之外,科研人员还解析了超过5000种的蛋白激酶或蛋白激酶-抑制剂复合体的晶体结构,且超过五分之一的人类蛋白激酶具有明确的小分子抑制剂。
因此,小分子激酶抑制剂已成为药物研发的一个热点领域。
小分子靶向治疗药物简介
化学抗肿瘤药物经过半个多世纪的发展,已经进入靶向治疗药物时代。
小分子靶向药物在临床上的应用日益增多,在一些肿瘤类别中已经进入一线用药地位,比如肾癌、慢粒白、多发性骨髓瘤等。
本文对小分子靶向治疗药物做一综述。
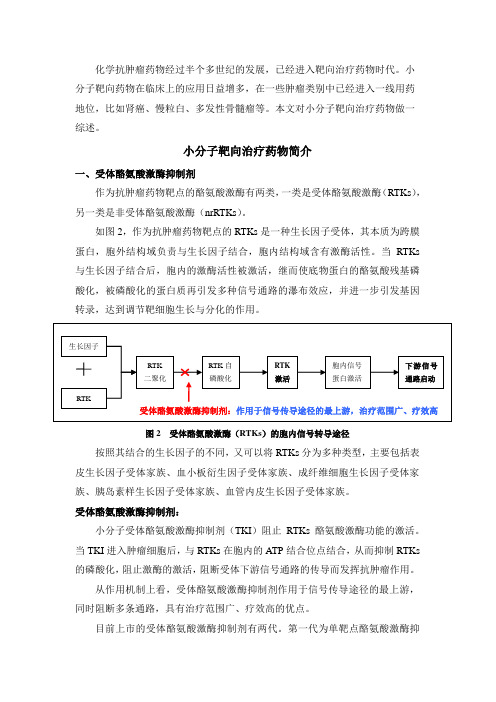
小分子靶向治疗药物简介一、受体酪氨酸激酶抑制剂作为抗肿瘤药物靶点的酪氨酸激酶有两类,一类是受体酪氨酸激酶(RTKs),另一类是非受体酪氨酸激酶(nrRTKs)。
如图2,作为抗肿瘤药物靶点的RTKs是一种生长因子受体,其本质为跨膜蛋白,胞外结构域负责与生长因子结合,胞内结构域含有激酶活性。
当RTKs 与生长因子结合后,胞内的激酶活性被激活,继而使底物蛋白的酪氨酸残基磷酸化,被磷酸化的蛋白质再引发多种信号通路的瀑布效应,并进一步引发基因转录,达到调节靶细胞生长与分化的作用。
图2 受体酪氨酸激酶(RTKs)的胞内信号转导途径按照其结合的生长因子的不同,又可以将RTKs分为多种类型,主要包括表皮生长因子受体家族、血小板衍生因子受体家族、成纤维细胞生长因子受体家族、胰岛素样生长因子受体家族、血管内皮生长因子受体家族。
受体酪氨酸激酶抑制剂:小分子受体酪氨酸激酶抑制剂(TKI)阻止RTKs酪氨酸激酶功能的激活。
当TKI进入肿瘤细胞后,与RTKs在胞内的ATP结合位点结合,从而抑制RTKs 的磷酸化,阻止激酶的激活,阻断受体下游信号通路的传导而发挥抗肿瘤作用。
从作用机制上看,受体酪氨酸激酶抑制剂作用于信号传导途径的最上游,同时阻断多条通路,具有治疗范围广、疗效高的优点。
目前上市的受体酪氨酸激酶抑制剂有两代。
第一代为单靶点酪氨酸激酶抑制剂,如吉非替尼、厄洛替尼。
表已上市的酪氨酸激酶抑制剂注:EGFR:表皮生长因子受体,属HER家族;VEGFR:血管内皮生长因子;PDGFR:血小板衍生因子;HER2:HER家族的一种受体;Abl-Bcr:一种非受体酪氨酸激酶;Raf:酪氨酸激酶的下游信号通路中的一种蛋白;Flt-3:Src:一种非受体酪氨酸激酶;c-kit:Ret:胶质细胞源性神经营养因子的受体吉非替尼为EGFR酪氨酸激酶抑制剂,主要用于非小细胞肺癌,对酪氨酸激酶基因编码区突变型肿瘤的有效率高达80%以上。
FDA批准的小分子激酶抑制剂(一)
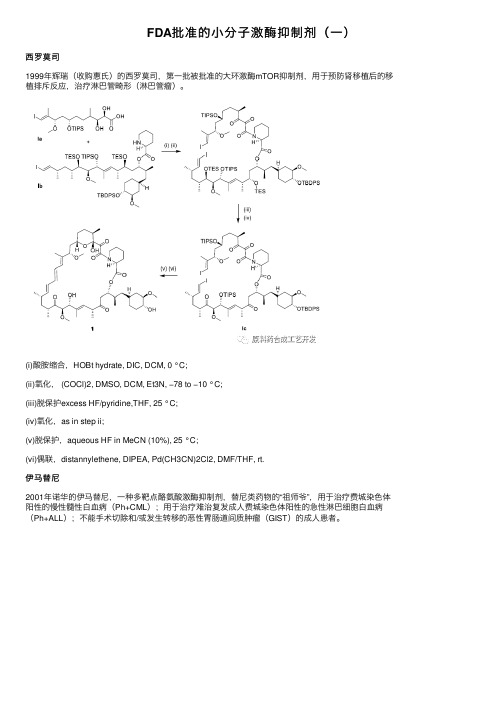
FDA批准的⼩分⼦激酶抑制剂(⼀)西罗莫司1999年辉瑞(收购惠⽒)的西罗莫司,第⼀批被批准的⼤环激酶mTOR抑制剂,⽤于预防肾移植后的移植排斥反应,治疗淋巴管畸形(淋巴管瘤)。
(i)酸胺缩合,HOBt hydrate, DIC, DCM, 0 °C;(ii)氧化, (COCl)2, DMSO, DCM, Et3N, −78 to −10 °C;(iii)脱保护excess HF/pyridine,THF, 25 °C;(iv)氧化,as in step ii;(v)脱保护,aqueous HF in MeCN (10%), 25 °C;(vi)偶联,distannylethene, DIPEA, Pd(CH3CN)2Cl2, DMF/THF, rt.伊马替尼2001年诺华的伊马替尼,⼀种多靶点酪氨酸激酶抑制剂,替尼类药物的“祖师爷”,⽤于治疗费城染⾊体阳性的慢性髓性⽩⾎病(Ph+CML);⽤于治疗难治复发成⼈费城染⾊体阳性的急性淋巴细胞⽩⾎病(Ph+ALL);不能⼿术切除和/或发⽣转移的恶性胃肠道间质肿瘤(GIST)的成⼈患者。
(i)羟醛缩合,NaOMe, PhMe, 25°C, 16 h;(ii)席夫碱,HNMe2, AcOH,PhMe, reflux, 1 h;(iii)亲核加成,NH2CN, HNO3, EtOH, reflux, 21 h;(iv)关环,NaOH, isopropanol, reflux, 12 h;(v) 还原,Pd/C, H2, THF,rt, 21 h;(vi) 酰基化,pyridine, rt, 24 h.吉⾮替尼2003年阿斯利康的吉⾮替尼,EGFR抑制剂,适⽤于具有表⽪⽣长因⼦受体(EGFR)基因敏感突变的局部晚期或转移性⾮⼩细胞肺癌(NSCLC)患者的治疗。
(i)蛋氨酸脱甲基,MeSO3H, L-methionine,100 °C;(ii)⼄酰化,Ac2O/pyridine;(iii)内酰胺氯代,SOCl2;(iv)SNAr反应,3-chloro-4-fluoroaniline;(v) 脱⼄酰基,NH4OH in MeOH;(vi)烷基化,N-morpholinopropyl bromide, K2CO3.厄洛替尼2004年基因泰克的厄洛替尼,EGFR抑制剂,⽤于两个或两个以上化疗⽅案失败的局部晚期或转移的⾮⼩细胞肺癌的三线治疗。
常用的小分子靶向药物和大分子单克隆抗体类药物

达拉非尼
曲美替尼
帕博利珠单抗
特瑞普利单抗
结节性硬化症相关的室管膜下巨细胞星形细胞瘤
依维莫司
结节性硬化症相关的肾血管平滑肌脂肪瘤
依维莫司
骨巨细胞瘤
地舒单抗
腺泡状软组织肉瘤
安罗替尼
透明细胞肉瘤
安罗替尼
其他晚期软组织肉瘤
安罗替尼
鼻咽癌
尼妥珠单抗
甲状腺癌
索拉非尼
头颈部鳞状细胞癌
西妥昔单抗
纳武利尤单抗
卡瑞利珠单抗
替雷利珠单抗
泽布替尼
多发性骨髓瘤
硼替佐米
来那度胺
沙利度胺
伊沙佐米
达雷妥尤单抗
骨髓增殖性疾病
芦可替尼
肾癌
依维莫司
索拉非尼
舒尼替尼
阿昔替尼
培唑帕尼
仑伐替尼
安罗替尼
帕博利珠单抗
纳武利尤单抗
乳腺癌
曲妥珠单抗
恩美曲妥珠单抗
帕妥珠单抗
伊尼妥单抗
拉帕替尼
吡咯替尼
奈拉替尼
哌柏西利
西达本胺
黑色素瘤
伊马替尼
表表1常用的小分子靶向药物和大分子单克隆抗体类药物病种需要检测靶点的药物不需要检测靶点的药物肺癌吉非替尼厄洛替尼埃克替尼阿法替尼达可替尼奥希替尼克唑替尼阿来替尼塞瑞替尼阿美替尼贝伐珠单抗重组人血管内皮抑制素安罗替尼纳武利尤单抗帕博利珠单抗度伐利尤单抗卡瑞利珠单抗阿替利珠单抗依维莫司肝癌索拉非尼瑞戈非尼仑伐替尼卡瑞利珠单抗食管癌卡瑞利珠单抗帕博利珠单抗胃癌曲妥珠单抗阿帕替尼纳武利尤单抗胃肠间质瘤伊马替尼瑞戈非尼舒尼替尼胰腺神经内分泌瘤舒尼替尼依维莫司结直肠癌西妥昔单抗贝伐珠单抗瑞戈非尼呋喹替尼白血病伊马替尼达沙替尼伊布替尼尼洛替尼淋巴瘤利妥昔单抗维布妥昔单抗西达本胺伊布替尼硼替佐米信迪利单抗卡瑞利珠单抗替雷利珠单抗泽布替尼多发性骨髓瘤硼替佐米来那度胺沙利度胺伊沙佐米达雷妥尤单抗骨髓增殖性疾病芦可替尼肾癌依维莫司索拉非尼舒尼替尼阿昔替尼培唑帕尼仑伐替尼安罗替尼帕博利珠单抗纳武利尤单抗乳腺癌曲妥珠单抗恩美曲妥珠单抗帕妥珠单抗伊尼妥单抗拉帕替尼吡咯替尼哌柏西利西达本胺奈拉替尼黑色素瘤伊马替尼维莫非尼达拉非尼曲美替尼帕博利珠单抗特瑞普利单抗结节性硬化症相关的室管膜下巨细胞星形细胞瘤依维莫司结节性硬化症相关的肾血管平滑肌脂肪瘤依维莫司骨巨细胞瘤地舒单抗腺泡状软组织肉瘤安罗替尼透明细胞肉瘤安罗替尼其他晚期软组织肉瘤安罗替尼鼻咽癌尼妥珠单抗甲状腺癌索拉非尼头颈部鳞状细胞癌西妥昔单抗纳武利尤单抗卵巢癌奥拉帕利尼拉帕利
蛋白激酶小分子抑制剂
蛋白激酶主要分为两大类,即丝氨酸/苏氨酸激酶和酪氨酸激酶。蛋白激酶也可以分为7类,即AGC激酶类,包括PKA、PKC和PKG;CAM激酶类包括钙调蛋白酶;CK1类,包括酪蛋白1;CMGC类,包括CDK、MAPK、GSK3和CLK;STE类; TK酪氨酸激酶类;TKL类。
截至2017-12-31,FDA总共批准了38个小分子激酶抑制剂类药物,其中多数为酪氨酸激酶抑制剂,其它属于丝氨酸/苏氨酸激酶抑制剂和少数脂激酶类抑制剂。
2,FDA批准的可逆非受体型酪氨酸小分子激酶抑制剂
注:CMML, chronic myelomonocytic leukemia (慢性粒单核细胞白血病); HES, hypereosinophilic syndrome (高嗜酸性粒细胞综合征); GIST, gastrointestinal stromal tumors (胃肠道间质瘤); PV, Polionyelitis(脊髓灰质炎); RA,rheumatoid arthritis(类风湿性关节炎)。
二、FDA批准的丝氨酸/苏氨酸小分子激酶抑制剂
三、FDA批准的脂激酶小分子抑制剂
注:ALK, anaplasticlymphoma kinase (间变性淋巴瘤激酶)。
FDA批准的可逆受体型酪氨酸小分子激酶抑制剂-其它
注:BC, breast cancer; RCC, renal cell carcinoma (肾细胞癌); MTC, Medullary Thyroid Carcinoma (甲状腺髓样癌);CRC, colorectal cancer(结直肠癌)。
一、FDA批准的酪氨酸小分子激酶抑制剂
1,FDA批准的不可逆小分子激酶抑制剂分子名来自商品名公司主要靶点
表皮生长因子受体酪氨酸激酶抑制剂的研究进展
表皮生长因子受体酪氨酸激酶抑制剂的研究进展一、本文概述表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKIs)是一类针对EGFR信号通路的关键药物,广泛应用于非小细胞肺癌、结直肠癌、头颈癌等多种癌症的治疗。
本文旨在综述近年来EGFR TKIs的研究进展,包括其作用机制、药物研发、临床应用以及面临的挑战等方面。
通过深入了解EGFR TKIs的研究现状和发展趋势,有望为癌症治疗提供新的思路和方法,进一步改善患者的生活质量和预后。
本文将从EGFR TKIs的作用机制出发,阐述其如何通过抑制EGFR 的酪氨酸激酶活性来阻断癌细胞的增殖和转移。
接着,我们将回顾EGFR TKIs的药物研发历程,介绍目前市场上主流的EGFR TKIs药物及其特点。
在此基础上,我们将重点关注EGFR TKIs在临床试验中的应用情况,包括其疗效、安全性以及耐药性等问题。
我们将探讨EGFR TKIs面临的挑战和未来发展方向,包括如何克服耐药性、提高治疗效果以及拓展新的适应症等。
通过本文的综述,我们希望能够为相关领域的研究者和临床医生提供有价值的参考信息,推动EGFR TKIs在癌症治疗中的进一步应用和发展。
二、EGFR-TK抑制剂的分类与机制表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TK抑制剂)是近年来癌症治疗领域的重要突破,其通过抑制表皮生长因子受体(EGFR)的酪氨酸激酶活性,从而阻断细胞的生长、增殖和转移过程。
根据药物的作用机制和化学结构,EGFR-TK抑制剂主要分为两大类:可逆性抑制剂和不可逆性抑制剂。
可逆性抑制剂,如吉非替尼和厄洛替尼,能够与EGFR的ATP结合位点形成可逆性结合,从而竞争性地抑制酪氨酸激酶的活性。
这类药物对于EGFR敏感突变的非小细胞肺癌具有较好的疗效,但在长期治疗过程中,患者往往会出现耐药现象。
不可逆性抑制剂,如阿法替尼和奥希替尼,能够与EGFR的ATP 结合位点形成共价键,导致EGFR的永久性失活。
TKI类药物
过去十年,许多酪氨酸激酶抑制剂(TKI)药物已经在肿瘤领域应用,根据一篇最近的综述,看看截止到2013年8月份,由FDA和EMA批准的所有TKI药物都有那些。
1、阿西替尼(axitinib,Inlyta)在2012年1月27日获FDA批准治疗对其它药物没有应答的晚期肾癌(肾细胞癌),由辉瑞(Pfizer)公司开发。
阿西替尼是多靶点酪氨酸激酶抑制剂,具体用法为5mg 空腹口服2/日.2、克唑替尼(crizotinib,XALKORI)用于治疗ALK阳性的局部晚期或转移的非小细胞肺癌,推荐剂量和方案是250 mg 口服每天2次。
3、达沙替尼(Dasatinib,施达赛Sprycel)治疗对包括甲磺酸伊马替尼在内的治疗方案耐药或不能耐受的慢性髓细胞样白血病。
FDA也经正常程序批准达沙替尼治疗对其他疗法耐药或不能耐受的费城染色体阳性的急性淋巴细胞性白血病成人患者.4、厄洛替尼(Erlotinib,特罗凯Tarceva)既往接受过至少一个化疗方案失败后的局部晚期或转移的非小细胞肺癌。
厄洛替尼单药用于非小细胞肺癌的推荐剂量为150mg/日,至少在进食前1小时或进食后2小时服用。
5、吉非替尼(Gefitinib,易瑞沙Iressa)适用于治疗既往接受过化学治疗或不适于化疗的局部晚期或转移性非小细胞肺癌。
推荐剂量为250mg(1片)每日1次,空腹或与食物同服。
6、伊马替尼(Imatinib,格列卫)用于治疗慢性粒细胞性白血病(CML),胃肠道间质瘤(胃肠道间质瘤)和其他一些疾病。
到2011年,该药已被FDA批准用于治疗10个不同的癌症。
7、拉帕替尼(Lapatinib;泰立沙Tykerb)联合卡培他滨治疗ErbB—2过度表达的,既往接受过包括蒽环类,紫杉醇,曲妥珠单抗(赫赛汀)治疗的晚期或转移性乳腺癌。
推荐剂量为1250mg,每日1次,第1~21天服用,与卡培他宾2000mg/d,第1~14天分2次服联用。
8、尼洛替尼(Nilotinib,达希纳Tasigna)适应症为对既往治疗(包括伊马替尼)耐药或不耐受的费城染色体阳性的慢性髓性白血病(Ph+ CML)慢性期或加速期成人患者。
蛋白酪氨酸激酶小分子抑制剂
路线四 张杰,贺良冲等人于2012 年报道的专利(CN102321073)
评价: 作为最新的尼罗替尼的合成路线,用到的试剂更温和, 路线更短,较适合于工业生产。
拉帕替尼
开发公司:英国葛兰素史克公司,2007年FDA批准上市 作用靶点:表面生长因子EGFR和HER-2 医疗用途:治疗晚期阳性乳腺癌,与卡培他滨联用。 市场前景:美国癌症学会统计显示,每年乳腺癌新确诊 的病例达18万,而每年大约有8000-10000女性死于转 移性HER-2阳性乳腺癌,拉帕替尼有很好的市场前景。
尼罗替尼
开发公司:诺华公司,2007年
FDA批准上市 作用靶点:表面生长因子EGFR 医疗用途:治疗对伊马替尼耐 药或者不能耐受的慢性期或加速 期的 Ph+CML患者。 市场前景:慢性粒细胞性白血病(CML) 是 4种最常见的白血病 之一, 约占白血病病例的 15 % ~ 20 % ,发病率为 1.6 /10万。 在美国, C ML患者每年新增约5000例,男女比例为1 .4B1 ,生 存超过 20年的不到10%。2001年, 首个 Bcr - Ab l激酶抑制 剂伊马替尼在美国获准上市,为 C ML的治疗提供了良好选择, 但因其发生 Bcr - Ab l基因突变而产生了耐药性。尼罗替尼 有很好的市场前景。
mckennajoseph等人于2006年报道的专利进行工艺改进wo2006135641由于breitenstein专利中最后一步是将酯水解后同胺进行偶联用到了氰基磷酸二乙酯这一步给出了低收率且收率不稳定并且氰基磷酸二乙酯价格不菲故对其改进在mckenna的专利中用了甲酯和胺在强碱性条件如叔丁醇钾于50c温度下于有机溶剂中如四氢呋喃dmf等可得到67产率
中间体1
中间体1
优点:使用金属钯催化反应,简化操作,也提高了产率。 优点:避免了使用氯代试剂 缺点:过渡中间体的反应不易控制,不利于工业化生产 缺点:需氮气保护,还要在冰浴下,反应条件苛刻,操作麻烦。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
F D A批准的激酶小分子抑制剂类药物及分
类一览
FDA批准的激酶小分子抑制剂类药物及分类一览
蛋白激酶
蛋白激酶(Kinase)是细胞生命活动重要的信号使者,可催化将ATP末端的γ-磷酸基团转移至底物上,从而将各种信号进行传递(图1)。
蛋白激酶参与了众多的生理过程,包括细胞增殖、存活、凋亡、代谢、转录以及分化等。
药理学及病理学研究表明,对于很多疾病,如肿瘤、炎症性疾病、中枢神经系统疾病、心血管疾病及糖尿病等,蛋白激酶都是一个理想的药物靶点。
图1 Mechanism of protein kinases and related publications
对于蛋白激酶的研究始于20世纪50年代,并在90年代随着MAPK/ERK、JAK及PI3K等信号通路的揭示而达到一个研究热潮。
迄今为止,在人体中发现了518种蛋白激酶,而编码具有激酶活性蛋白的基因则高达900多种。
与之相对应,有关激酶抑制剂的研究也逐步发展,并在激酶作用机制的阐明过程中
扮演了重要角色,并成为重要的药物研究热点。
该领域研究的文献数量也是逐年上升,从侧面反映了其在基础研究和药物发现中的重要性。
蛋白激酶抑制剂及其分类
过去的15年间,激酶抑制剂作为药物候选的研究取得了长足的进步,不论是基础研究还是在工业界。
在人体现有药物靶点里面,蛋白激酶家族成员占比高达10%(FDA批准药物分子靶点深度解读)。
2001年,第一个激酶抑制剂类药物Imatinib获得FDA批准,成为该领域发展的里程碑,此后十年该类药物以平均每年获批一种的速度稳步发展。
而在2012年1月至2015年2月期间,小分子激酶抑制剂类药物迎来爆发式发展,共有15种新药获得审批。
截至2016年12月底,共有31种小分子激酶抑制剂类药物获得审批,同时还有大量的化合物处于临床或临床前研究中。
除此之外,科研人员还解析了超过5000种的蛋白激酶或蛋白激酶-抑制剂复合体的晶体结构,且超过五分之一的人类蛋白激酶具有明确的小分子抑制剂。
因此,小分子激酶抑制剂已成为药物研发的一个热点领域。
蛋白激酶尽管在一级序列上有所差异,但在三维结构上却具有高度的保守性,特别是在催化活性结构域附近。
该区域存在一个β-折叠构成的N-lobe区域及α-螺旋构成的C-lobe区域,而ATP结合在两者构成的沟状区,也是很多激酶抑制剂的结合位点。
活性位点附近还存在一条Activation-Loop,通常末端存在一个保守的Asp-Phe-Gly (DFG)结构基序(图2A)。
图2 Kinase structure and different types of reversible small-molecule kinase inhibitor 根据结合模式的不同,激酶抑制剂可分为不可逆及可逆两大类。
前者指化合物通过与Cys反应形成共价键结合在ATP结合位点上,从而封闭ATP的结合空间,该过程具有不可逆转性。
后者根据结合口袋区域及DFG基序构象的不同,可分为四种主要的不同亚型(图2B)。
类型Ⅰ为ATP竞争性抑制剂,结合与活性形式激酶DFG基序上的Asp残基。
类型Ⅱ抑制剂结合与非活性状态的激酶中,其上DFG基序上的Asp残基朝向分子外侧。
而类型Ⅲ的抑制剂结合在ATP附近别构位点上,但同ATP结合口袋没有相互作用。
类型Ⅳ抑制剂结合在
远离ATP结合位点的别构作用区域。
还有些激酶抑制剂,如双底物类抑制剂,可以统一划分在类型Ⅴ里面,作用模式与上述四类有所不同。
图3 Small molecular kinase inhibitors approved by FDA in 2001-2016
在获批的31中小分子激酶抑制剂类药物中(图3),绝大多数为酪氨酸激酶抑制剂,还有些属于丝氨酸/苏氨酸激酶抑制剂,只有2014年七月获批的Idelalisib属于脂激酶类抑制剂。
根据靶点蛋白及药物属性的不同,分类整理如下:
1. FDA批准的可逆NRTK(非受体型酪氨酸激酶)抑制剂类药物
图4 Reversible NITK inhibitors
2. FDA批准的可逆RTK(受体型酪氨酸激酶)抑制剂类药物
图5 Reversible RTK inhibitors-1
图6 Reversible RTK inhibitors-2
3. FDA批准的不可逆蛋白激酶抑制剂类药物
图7 Inreversible protein kinase inhibitor 4. FDA批准的丝氨酸/苏氨酸激酶抑制剂类药物
图8 Serine/Threonine kinase inhibitors 5. FDA批准的脂激酶抑制剂类药物
图9 Lipid kinase inhibitor
挑战与展望
在过去的15年里,基于蛋白激酶的药物发现取得了巨大进步。
相比于GPCR,膜通道与转运蛋白及蛋白酶等传统药物靶点领域,激酶抑制剂代表了一类年轻而又充满活力的药物发现空间,并取代GPCR成为癌症领域最火热的细胞治疗靶点。
尽管在短短十五年时期内已有31种药物获得批准,但在2016年,近五年的快速增长势头没能继续延续。
激酶小分子抑制剂类药物研究领域仍面临诸多挑战。
首先,人体内激酶家族中只有少数成员获得了详尽研究。
绝大多数抑制剂研究集中于酪氨酸激酶及类酪氨酸激酶家族,如CDK、MAPK、GSK3、CMGC、PKA、PKG及PKC等。
这一不平衡还体现在现有获批药物数量上,针对BCR-Abl、ErbBs及VEGFRs三类酪氨酸激酶开发的药物占到了总数的三分之二以上。
而在另一分类体系中,脂激酶只有一种抑制剂类药物上市,尽管这类酶的抑制剂早在20世纪90年代就早已有报道,且开展了很多临床及临床前研究。
以上现状表明,人体激酶组中的很多成员还处于被冷落状态。
我们需要开发出新型的研究方法或筛选探针,以便更好的揭示这些激酶的作用机制,并有效开发其作为药物靶点的潜力。
令人鼓舞的是,最近几年有数个激酶成员的抑制剂类药物首次获得批准,如2013年MEK抑制剂Trametinib、BTK的抑制剂Ibrutinib及2015年获批的CDK抑制剂Palbociclib。
其次,尽管激酶的梯级调控信号调节着众多的生理过程,如炎症反应、中枢神经系统异常、心血管疾病、糖尿病及癌症等,但现有获批药物超过90%以上集中在癌症治疗领域。
针对激酶的小分子抑制剂类药物应用领域亟待拓展。
目前,Tofacitinib已被批准用于关节炎治疗。
即便是在肿瘤治疗领域,也有很多问题有待进一步深入研究,如肿瘤的耐药性问题以及同其他药物的联合用药等。
第三,现有的很多激酶抑制剂药物存在较多相似性,大多是在已批准药物基础上设计优化而成,如针对ErbB的五种抑制剂均包含相同的核心结构模块。
从这个角度讲,现有药物的结构多样性不够丰富,亟需增加药物研发初始阶段高通量筛选(HTS)所用化合物库的结构多样性。
而天然产物库,通常包含不同于绝
大多数化学合成抑制剂库的药效团及分子骨架,有望成为拓展HTS库结构多样性的新资源。
第四,具有新的作用机制及特异性的激酶抑制剂类药物有待开发。
由于激酶ATP结合口袋区域附近结构的保守型,绝大多数抑制剂为可逆性抑制剂。
这也导致了绝大多数小分子抑制剂存在不止一个作用靶点分子,导致脱靶现象以及副作用的产生。
与之相随,具有绝对选择性的抑制剂分子极为稀少。
未来工作中,我们需要探索具有新型作用机制的抑制剂分子。
而激酶抑制剂的选择性则是一个略带争议的特性。
早期研究中,具有交叉抑制活性或广谱选择性的抑制剂是肿瘤学研究的得力方法。
而当前,选择性抑制剂更适合于肿瘤治疗的理论逐步被广泛认同。
研究结论表明,激酶抑制剂类药物并不需要绝对的选择性,而是要有适当的选择性以便在药效与毒性间达到某个平衡点。
本文所引用资料:
1. Small Molecule Kinase Inhibitors as Anti-Cancer Therapeutics. Mini-Reviews in Medicinal Chemistry, 2012, 12, 399-411
2. Kinase inhibitors and monoclonal antibodies in oncology: clinical implications. Nature Reviews Clinical Oncology, 2016,13,209–227
3. Tyrosine Kinase Inhibitors: Views of Selectivity, Sensitivity and Clinical Performance.
2013,53,161-185
4. Small-molecule kinase inhibitors: an analysis of FDA-approved drugs. Drug Discov Today. 2016Jan;21(1):5-10
5. FDA-approved small-molecule kinase inhibitors. Trends in Pharmacological Sciences 2015,36,422-439
6. /Drugs/default.htm
7. /scripts/cder/daf/index.cfm
8. 部分药物信息查询自药渡网-药物数据。
