醛固酮(ALD)测定试剂盒(化学发光法)产品技术要求新产业
醛固酮(ALD)测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求模板

医疗器械产品技术要求编号:醛固酮(ALD)测定试剂盒(磁微粒化学发光免疫分析法)1.产品型号/规格及其划分说明1.1包装规格:100测试/盒,200测试/盒1.2主要组成成分:校准品和质控品具有批特异性,具体浓度见瓶签。
1.3适用范围本产品用于体外定量测定人血浆中的醛固酮(ALD)的含量。
2性能要求2.1外观试剂盒各组分应齐全、完整,液体无渗漏;磁微粒试剂摇匀后为棕色含固体微粒的均匀悬浊液,无明显凝集;其他液体组分应澄清,无沉淀或絮状物;包装标签应清晰、易识别。
2.2装量各组分装量应不得低于标示体积。
2.3溯源性根据GB/T21415-2008及有关规定,提供试剂盒内校准品的来源、赋值过程以及测量不确定度等内容,溯源至企业一级校准品,一级校准品用纯品质量赋值,与已上市产品比对验证。
2.4线性在[25.0,2000.0]pg/mL线性区间内,相关系数r应不低于0.9900。
2.5空白限应不高于20.0pg/mL。
2.6准确度回收率应在85.0%~115.0%范围内。
2.7重复性在试剂盒线性区间范围内,分别检测高、低两个浓度的质控品(QC2、QC1),检测结果的变异系数(CV,%)应不高于8.0%。
2.8质控品的测定值高、低两个浓度的质控品(QC2、QC1)检测结果均应在质控范围内。
2.9特异性测定浓度均为1000ng/mL的皮质醇、11-脱氧皮质醇、雌二醇和睾酮,其测定结果均应不高于25.0pg/mL。
2.10批间差用三个批号的试剂盒分别检测高、低两个浓度的质控品(QC2、QC1),批间变异系数(CV,%)应不高于15.0%。
2.11稳定性试剂盒在2~8℃保存,有效期为12个月,在有效期结束的前后两个月内进行检测,结果应符合2.1、2.2、2.4、2.5、2.6、2.7、2.8的规定。
从醛固酮(ALD)的分泌与合成探讨硝菔通结方从肾论治便秘的作用机制

从醛固酮(ALD)的分泌与合成探讨硝菔通结方从肾论治便秘的作用机制梁星琛;周永学;闫曙光;张小波【摘要】目的:观察硝菔通结方对功能性便秘大鼠醛固酮(ALD)合成和分泌的影响,从现代医学肾脏调节水液代谢的角度揭示硝菔通结方从肾论治便秘的作用机制.方法:48只成年雄性SD大鼠采用随机数字表法分为空白组(8只)和造模组(40只),造模组灌胃复方地芬诺酯混悬液6周复制便秘模型后随机分为模型组(FC组)、硝菔通结方高、中、低剂量组、阳性药物对照组(苁蓉通便口服液组,简称口服液组).各治疗组给予不同剂量的硝菔通结方,阳性药物对照组给予苁蓉通便口服液(后简称口服液组)灌胃1个月.观察各组大鼠的一般情况以及结肠含水率,ELISA法检测各组大鼠血清中醛固酮(ALD)、肾素(PRA)、血管紧张素Ⅱ(AngⅡ)、血管紧张素转化酶(ACE)的含量,RT-PCR法检测肾脏组织中MRmRNA的水平,Western-Blot法检测结肠组织中AQP3的表达.结果:模型组大鼠粪便量少、质地干硬,结肠含水率明显降低,血清中ALD、PRA、AngⅡ、ACE的含量升高,肾脏组织中MRmRNA表达升高,结肠组织中AQP3的表达明显升高;与模型组比较,各剂量硝菔通结方治疗组以及口服液组大鼠粪便量增加且质地稀软,结肠含水率增高,血清中ALD、PRA、AngⅡ、ACE的含量均降低,肾脏组织中MRmRNA表达降低,结肠组织中AQP3的表达显著降低.结论:肾脏能通过调节ALD合成与分泌而影响肠道的水液代谢,这可能是中医从肾论治便秘的科学内涵之一,硝菔通结方可通过影响ALD合成与分泌调节肠道的水液代谢,从而对功能性便秘发挥治疗作用.%To observe the influnce that Xiao Fu Tong Jie Prescription to treat functional constipation rats from the view of aldosterone's synthesis and secretion.From the view of the kindney adjust water metabolism,we reveal the mechanism of action of nursingfunctional constipation from the kindey.Methods:48 SD rats were randomly divided into blank control group(8 SD rats)and functional constipation model group(40 SD rats).All were given compound diphenoxylate for 6 weeks and then divided into Xiao Fu Tong Jie Prescription high,medium,low dose group and positive drug group (Cong Rong Tong Bian oral liquid).These treatment groups were treated with different dose of Xiao Fu Tong Jie Prescription.Positive drug group was treated with Cong Rong Tong Bian oral liquid.All for one month.Observed the general condition of each group and the water content of the colon.The protein expression of the aldosterone(ALD) 、renin(PRA) 、angiotensin Ⅱ (Ang Ⅱ)、angiotensin-converting enzyme (ACE)by enzyme linked immunosorbent assay (ELISA).The mRNA and protein expression of MR were determined by Real-time PCR.The protein expression of the Western blot were used to detect the expression of AQP3 incolon.Results:Compared with the blank control group,the rats of model group had less feces and texture was hard.The water content of the colon levels were significantly decreased.ALD、PRA、Ang Ⅱ 、ACE content were increased.MR mRNA relative expression levels were increased.Levels of AQP3 relative expression levels were significantly increased;Compared with the model group,the rats of treatment groups had more feces and texture was loose.The water content of the colon levels were significantly increased.ALD 、PRA、Ang Ⅱ 、ACE content were decreased.MR mRNA relative expression levels were decreased.Levels of AQP3 relative expression levels were significantly decreased after giving Xiao Fu Tong JiePrescription and Cong Rong Tong Bian oral liquid.Conclusions:The kidney can affect water metabolism disorder in colon by adjusting ALD's synthesis and secretion.This may be one of the scientific connotation of nursing functional constipation from the kindey;Xiao Fu Tong Jie Prescription can affect water metabolism disorder in colon by adjusting ALD's synthesis and seeretion to nursing functional constipation.【期刊名称】《中国中医基础医学杂志》【年(卷),期】2017(023)003【总页数】5页(P338-341,370)【关键词】硝菔通结方;功能性便秘;ALD;RAAS【作者】梁星琛;周永学;闫曙光;张小波【作者单位】成都中医药大学,成都 610075;陕西中医药大学,陕西咸阳 712046;陕西中医药大学,陕西咸阳 712046;陕西中医药大学,陕西咸阳 712046【正文语种】中文【中图分类】R285.5便秘是以排便次数减少、粪便量减少、粪便干结、排便费力等表现为主的一种复杂症状。
化学发光免疫法检测醛固酮和肾素浓度及对原发性醛固酮增多症诊断价值的评价

化学发光免疫法检测醛固酮和肾素浓度及对原发性醛固酮增多症诊断价值的评价王芳;康金锁;邹玉宝;蒋雄京;丛祥凤;陈曦【期刊名称】《中国循环杂志》【年(卷),期】2016(031)006【摘要】Objective: To evaluate chemiluminescence immunoassay (CLIA) for detecting blood levels of aldosterone and rennin with its diagnostic value of primary aldosteronism (PA) with comparison to radio immunoassay (RIA). Methods: According to American protocols of CLSI, we conducted a veriifcation study between RIA and CLIA for their precision, accuracy, linearity and reference ranges; meanwhile, taking clinical diagnosis as golden standard, examined renin activity or concentration and aldosterone concentration in 20 healthy volunteers and 40 hypertension patients by both RIA and CLIA, compared the ratios of ARR (aldosterone concentration/renin activity) or ADRR (aldosterone concentration/renin concentration) for the speciifcity and sensitivity of PA diagnosis. Results: Within-lot and between-lot accuracies of CLIA for detecting aldosterone levels were below 5% and 10%, the recoveries were 102% and 95% respectively. There was a good linear correlation in the range of aldosterone at (3-74) ng/dl and renin at (0.99-330) µIU/ml. In healthy volunteers, renin level was higher in 2 subjects, while aldosterone level and ADRR ratio were within normal references in all subjects by themanufacturer. In hypertension patients, the sensitivity and speciifcity for aldosterone and rennin detections by CLIA were at 85.7% and 97.0%, by RIA were at 85.7% and 94.0%. Conclusion: CLIA has the superiority of simple performance, repeatable and without radioactive contamination; itis recommended for replacing RIA as necessity.%目的:对化学发光免疫法(CLIA)检测醛固酮和肾素浓度进行方法学评价,并通过和放射免疫法(RIA)比较评价其对原发性醛固酮增多症(原醛)的诊断价值。
碘标记醛固酮放射免疫分析药盒说明书

碘[125I]醛固酮放射免疫分析药盒【药品名称】碘标记醛固酮放射免疫分析药盒【概述】醛固酮是肾上腺皮质球状带合成和分泌的盐皮质类固醇激素,属于21碳类甾体激素,分子量360D。
它是一个非常强的电解质排泄调节因子,其作用是保钠排钾,增加Na+和Cl-的回放,排出K+和H+,维持电解质平衡与体液容量恒定。
从临床的观点看,某些疾病与体内ALD的水平有关,醛固酮含量的测定,应用于原发性醛固酮增多症的诊断与疗效观察,Addison氏病的诊断和肾上腺肿瘤、肾上腺皮质增生与继发性醛固酮增多症的鉴别诊断,以及某些抗高血压药物的临床药理研究,尤其对继发性高血压的诊断有临床价值。
【测定原理】本试剂盒采用放射免疫分析方法测定人血浆中醛固酮(ALD)的含量。
先将校准品(或样品)、标记物和抗体按操作程序依次加入试管中,使标记抗原和抗原与限量抗体发生竞争性结合,待反应平衡后,加入分离剂,离心沉淀,使游离抗原与抗原抗体复合物分离,测量沉淀中放射性强度。
随醛固酮含量增加,放射性强度减少。
【试剂组成和配制方法】1.校准品 7瓶 (冻干品) 每瓶溶于 ml蒸馏水(如不填写,则用1.0ml溶解) 浓度分别为:0,0.0625,0.125,0.25,0.5,1.0,2.0ng/ml,0,0.174,0.347,0.694,1.39,2.78,5.56nmol/L 2.125I—ALD 1瓶(红色溶液) 10ml/瓶(100T),比活度:4.0μCi/μg 3.抗体 1瓶(蓝色溶液) 10ml/瓶(100T) 4.分离试剂 1瓶(悬浮液) 使用前充分摇匀。
5.阻断剂(ANS) 1瓶(溶液) 6.质控血清 2瓶冻干品使用前0.5ml/瓶蒸馏水溶解【样本要求】样品采集:卧位:早晨6—8时起床前,取静脉血,肝素抗凝。
立位:起床后三小时,静脉取血,肝素抗凝。
注意:每1ml血浆中用10μl肝素注射液(12500单位)抗凝;溶血、脂血、黄疸标本不要使用。
磁微粒化学发光法检测醛固酮肾素检测限功能与灵敏度研究

磁微粒化学发光法检测醛固酮肾素检测限功能与灵敏度研究张靖;倪媛媛;张厚亮【期刊名称】《湖北民族学院学报(医学版)》【年(卷),期】2016(033)004【摘要】目的评价磁微粒化学发光法检测肾素、醛固酮的空白限、检出限、功能灵敏度.方法根据(Clinical and Laboratory Standards Institute,CLSI)文件,利用空白样品和系列梯度样品在AutoLumo A2000全自动化学发光系统上检测,来确定配套试剂的空白限、检出限、功能灵敏度.结果醛固酮的空白限为4.93 pg/mL,检出限为13.08 pg/mL,20%变异系数(coefficient of variation,CV)功能灵敏度为10.0 pg/mL.肾素的空白限为0.482 pg/mL,检出限为1.15 pg/mL,20%变异系数(coefficient of variation,CV)功能灵敏度为1.5 pg/mL.结论 AutoLumo A2000全自动化学法测定仪测定醛固酮,肾素的空白限、检出限、功能灵敏度的建立为临床诊断提供了有价值信息.【总页数】3页(P17-19)【作者】张靖;倪媛媛;张厚亮【作者单位】天津医科大学静海临床学院,天津301600;天津医科大学静海临床学院,天津301600;天津医科大学静海临床学院,天津301600【正文语种】中文【中图分类】R586.24【相关文献】1.磁微粒化学发光法的肝纤四项检测限与功能灵敏度研究 [J], 刘玉文;蒋长斌2.基于磁微粒化学发光法的肝纤四项检测限与功能灵敏度研究 [J], 王新灵;李忠信;关学;渠海3.Roche电化学发光免疫法检测NT-proBNP的检测限值和功能灵敏度研究 [J], 索明环;张秀明;温冬梅;王伟佳;李飞;欧阳能良;阚丽娟;严海忠4.化学发光免疫法检测甲胎蛋白的生物检测限和功能灵敏度研究 [J], 郑松柏;张伟铮;张秀明;庄俊华;林莲英;马艳;马骥;王云秀5.化学发光免疫法检测B型利钠肽的检测限值和功能灵敏度研究 [J], 李飞;王伟佳;温冬梅;索明环;欧阳能良;严海忠;阚丽娟;张秀明因版权原因,仅展示原文概要,查看原文内容请购买。
生长激素(GH)测定试剂盒(化学发光法)产品技术要求新产业
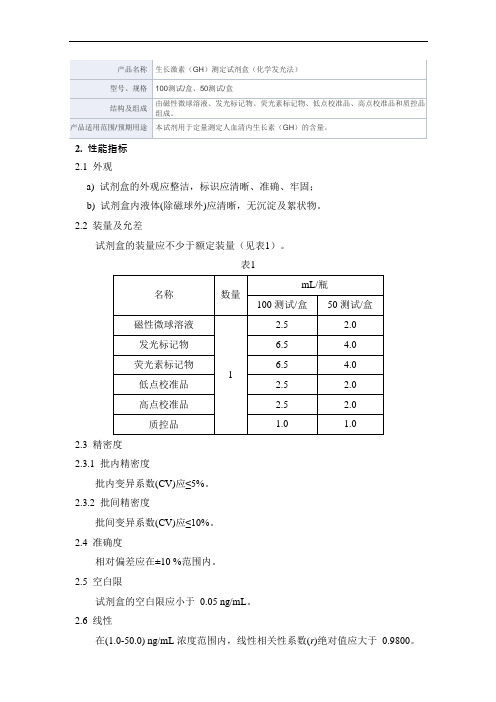
生长激素(GH)测定试剂盒(化学发光法)
型号、规格
100测试/盒、50测试/盒
结构及组成
由磁性微球溶液、发光标记物、荧光素标记物、低点校准品、高点校准品和质控品组成。
产品适用范围/预期用途
本试剂用于定量测定人血清内生长素(GH)的含量。
2.性能指标
2.1外观
a)试剂盒的外观应整洁,标识应清晰、准确、牢固;
2.3.1批内精密度
批内变异系数(CV)应≤5%。
2.3.2批间精密度
批间变异系数(CV)应≤10%。
2.4准确度
相对偏差应在±10 %范围内。
2.5空白限
试剂盒的空白限应小于0.05 ng/mL。
2.6线性
在(1.0-50.0) ng/mL浓度范围内,线性相关性系数(r)绝对值应大于0.9800。
1 /5
b)试剂盒内液体(除磁球外)应清晰,无沉淀及絮状物。
2.2装量及允差
试剂盒的装量应不少于额定装量(见表1)。
表1
名称
数量
mL/瓶
100测试/盒
50测试/盒
磁性微球溶液Байду номын сангаас
1
2.5
2.0
发光标记物
6.5
4.0
荧光素标记物
6.5
4.0
低点校准品
2.5
2.0
高点校准品
2.5
2.0
质控品
1.0
1.0
2.3精密度
孕酮检测试剂盒(化学发光法)审评要点(江苏省药品监督管理局)

孕酮检测试剂盒(化学发光法)审评要点(江苏省药品监督管理局)一、申请表1、主要成分:浓度表述为“>...”过于笼统,应明确浓度;明确抗体属性;明确射频卡的作用。
2、(1)首次注册、适用机型变更及其他涉及机型变化的注册,需提供适用机型的注册证复印件并加盖企业章。
(2)产品规格型号应与实际生产的规格型号完全一致。
(3)全部申报资料随申请表统一修改。
三、综述资料1、根据国家总局公布的2014年第44号文修改。
2、提供生物来源的原材料的出厂检验报告。
四、主要原材料的研究资料1、(1)根据国家总局公布的2014年第44号文修改。
(2)研究过程建议按照以下思路表述:试剂(批号)和质控品及校准品(如用到)、仪器、样本→方案→数据→数据的统计分析过程→结果→判定依据及结论。
2、应提供。
描述产品所采用的技术原理,主要原材料的来源及制备方法,主要生产工艺过程,质控品、校准品的制备方法及溯源(定值)情况。
五、主要生产工艺及反应体系的研究资料1、(1)根据国家总局公布的2014年第44号文。
(2)研究过程建议按照以下思路表述:试剂(批号)和质控品及校准品(如用到)、仪器、样本→方案→数据→数据的统计分析过程→结果→判定依据及结论。
2、应提供。
主要生产工艺包括:工作液的配制、分装和冻干,固相载体的包被和组装,显色/发光系统等的描述及确定依据等,反应体系包括样本采集及处理、样本要求、样本用量、试剂用量、反应条件、校准方法(如有)、质控方法等。
六、分析性能评估资料1、根据国家总局公布的2014年第44号文修改。
补盖骑缝章。
3、该产品是否存在钩状效应的问题?如有,应有相应的研究。
4、应说明不同包装规格是否存在差异。
5、技术要求修改的的内容应重新提供研究资料。
七、阳性判断值或参考区间确定资料1、补盖骑缝章。
2、所用的试剂为“雌二醇检测试剂盒”,是否有误?八、稳定性研究资料1、补盖骑缝章。
2、提供试剂和质控品的检测数据。
3、技术要求修改的内容应重新提供研究资料。
一种血浆中醛固酮检测方法及检测试剂盒[发明专利]
![一种血浆中醛固酮检测方法及检测试剂盒[发明专利]](https://img.taocdn.com/s3/m/fdb9c72dc4da50e2524de518964bcf84b8d52d72.png)
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 201911222656.7(22)申请日 2019.12.03(71)申请人 天津国科医工科技发展有限公司地址 300300 天津市东丽区开发区五经路16号4号楼(72)发明人 李艳 周传贵 周玉松 胡玮 徐振 程文播 (74)专利代理机构 天津滨海科纬知识产权代理有限公司 12211代理人 耿树志(51)Int.Cl.G01N 30/06(2006.01)G01N 30/86(2006.01)G01N 30/88(2006.01)(54)发明名称一种血浆中醛固酮检测方法及检测试剂盒(57)摘要本发明提供了一种血浆中醛固酮检测方法及检测试剂盒,其中,血浆中醛固酮的检测试剂盒,包括校准品和质控品;所述校准品和质控品均为含有醛固酮的牛血清白蛋白。
本发明所述的血浆中醛固酮的检测试剂盒,能够提供校准品、样品前处理所涉及的试剂和质控品,免除实验室检测自配的繁琐步骤和造成的误差,保证检测结果的准确性。
权利要求书2页 说明书7页 附图3页CN 110865137 A 2020.03.06C N 110865137A1.一种血浆中醛固酮的检测试剂盒,其特征在于:包括校准品和质控品;所述校准品和质控品均为含有醛固酮的牛血清白蛋白。
2.根据权利要求1所述的血浆中醛固酮的检测试剂盒,其特征在于:所述校准品为含有梯度浓度醛固酮的牛血清白蛋白;和/或,所述校准品的制备方法为:先用甲醇稀释醛固酮标准品到梯度浓度,然后与牛血清白蛋白混合均匀,得到含有醛固酮的牛血清白蛋白校准品;优选的,校准品中醛固酮的浓度范围为50-10000pg/mL。
3.根据权利要求1所述的血浆中醛固酮的检测试剂盒,其特征在于:所述质控品包括第一质控品、第二质控品和第三质控品,且三者浓度依次升高;优选的,所述第一质控品中醛固酮的含量范围为80-500pg/mL,第二质控品中醛固酮的含量范围为2000-6000pg/mL,第三质控品中醛固酮的含量范围为7000-10000pg/mL。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2.性能指标
2.1外观
a)试剂盒的外观应整洁,标识应清晰、准确、牢固;
b)试剂盒内液体(除磁珠外)应清晰,无沉淀及絮状物。
2.2装量及允差
试剂盒的装量应不少于额定装量(见表1)。
表1
2.3精密度
2.3.1批内精密度
批内变异系数(CV)应≤5%。
2.3.2批间精密度
批间变异系数(CV)应≤10%。
2.4准确度
回收率应在90%~110%范围内。
2.5分析灵敏度
试剂盒的分析灵敏度应小于 5.0 pg/mL。
2.6特异性
试剂盒对DHEA 标准浓度的检测结果应符合以下的要求: 当DHEA 为1000 μg/dL 时,检测结果ALD<100 pg/mL。
2.7线性
在(20-1000)p g/mL 浓度范围内,线性相关性系数(r)绝对值应大于0.9900。
2.8稳定性
试剂盒在规定的储存条件下储存超过有效期后两个月内的外观、批内精密度、准确度、分析灵敏度、特异性、线性应分别符合2.1、2.3.1、2.4、2.5、2.6、2.7 的要求。
2.9生物安全性
试剂盒中成分经检测,HIV 抗体、HCV 抗体和HBsAg 应为阴性。
