小分子靶向治疗药物简介
分子靶向药物概念

分子靶向药物概念近年来,分子靶向药物成为医学领域的热门研究方向,被广泛应用于癌症等疾病的治疗。
分子靶向药物是一类可以直接干预特定分子、基因或信号通路的药物,具有高效、低毒副作用等优势。
本文将介绍分子靶向药物的概念、作用机制以及临床应用情况。
一、分子靶向药物的概念分子靶向药物是指能够靶向特定生物分子(如蛋白质、DNA、RNA 等)进行干预治疗的药物。
与传统化学药物相比,分子靶向药物具有更高的选择性,能够在目标分子上发挥更为显著的作用,减轻对正常细胞的伤害。
它们通常是由小分子化合物、抗体、核酸等构成,通过与特定的分子靶点结合,抑制某种生物过程或促进另一种生物过程的发生。
二、分子靶向药物的作用机制分子靶向药物的作用机制多种多样,根据药物的性质和分子靶点的差异,分子靶向药物可以实现以下几种作用机制:1. 抑制靶点活性:某些分子靶向药物可以与靶点结合,阻断其活性。
例如,基于表皮生长因子受体(EGFR)的靶向药物可以结合EGFR,抑制其信号传导,从而抑制肿瘤细胞的生长和分裂。
2. 诱导细胞凋亡:某些分子靶向药物可以通过与细胞的生存信号通路干扰,诱导肿瘤细胞自身程序性死亡,即细胞凋亡。
这种作用机制能够有效地限制肿瘤细胞的生长和扩散。
3. 阻断血供:一些分子靶向药物可以通过干扰肿瘤的血管生成,阻断其血供,从而导致肿瘤细胞因缺氧而死亡。
这种作用机制被广泛应用于肿瘤治疗中,被称为抗血管生成治疗。
4. 免疫激活:一部分分子靶向药物可以通过激活免疫系统,增强机体对肿瘤的免疫应答。
这些药物可以增加肿瘤细胞被免疫细胞攻击的可能性,提高治疗效果。
三、分子靶向药物的临床应用情况目前,分子靶向药物已经广泛应用于临床治疗中,取得了显著的疗效。
其中,最典型的应用领域就是癌症治疗。
许多分子靶向药物已经成功用于多种癌症的治疗,如乳腺癌、结直肠癌、肺癌等。
这些药物可以针对癌症细胞中的特异性分子靶点,干预其生长和扩散,达到治疗的目的。
此外,分子靶向药物还被应用于其他一些疾病的治疗中,如类风湿性关节炎、糖尿病等。
小分子靶向治疗药物简介
化学抗肿瘤药物经过半个多世纪的发展,已经进入靶向治疗药物时代。
小分子靶向药物在临床上的应用日益增多,在一些肿瘤类别中已经进入一线用药地位,比如肾癌、慢粒白、多发性骨髓瘤等。
本文对小分子靶向治疗药物做一综述。
小分子靶向治疗药物简介一、受体酪氨酸激酶抑制剂作为抗肿瘤药物靶点的酪氨酸激酶有两类,一类是受体酪氨酸激酶(RTKs),另一类是非受体酪氨酸激酶(nrRTKs)。
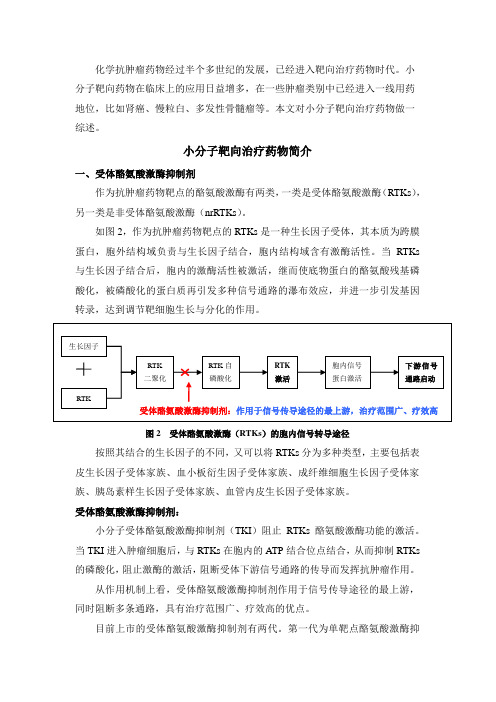
如图2,作为抗肿瘤药物靶点的RTKs是一种生长因子受体,其本质为跨膜蛋白,胞外结构域负责与生长因子结合,胞内结构域含有激酶活性。
当RTKs 与生长因子结合后,胞内的激酶活性被激活,继而使底物蛋白的酪氨酸残基磷酸化,被磷酸化的蛋白质再引发多种信号通路的瀑布效应,并进一步引发基因转录,达到调节靶细胞生长与分化的作用。
图2 受体酪氨酸激酶(RTKs)的胞内信号转导途径按照其结合的生长因子的不同,又可以将RTKs分为多种类型,主要包括表皮生长因子受体家族、血小板衍生因子受体家族、成纤维细胞生长因子受体家族、胰岛素样生长因子受体家族、血管内皮生长因子受体家族。
受体酪氨酸激酶抑制剂:小分子受体酪氨酸激酶抑制剂(TKI)阻止RTKs酪氨酸激酶功能的激活。
当TKI进入肿瘤细胞后,与RTKs在胞内的ATP结合位点结合,从而抑制RTKs 的磷酸化,阻止激酶的激活,阻断受体下游信号通路的传导而发挥抗肿瘤作用。
从作用机制上看,受体酪氨酸激酶抑制剂作用于信号传导途径的最上游,同时阻断多条通路,具有治疗范围广、疗效高的优点。
目前上市的受体酪氨酸激酶抑制剂有两代。
第一代为单靶点酪氨酸激酶抑制剂,如吉非替尼、厄洛替尼。
表已上市的酪氨酸激酶抑制剂注:EGFR:表皮生长因子受体,属HER家族;VEGFR:血管内皮生长因子;PDGFR:血小板衍生因子;HER2:HER家族的一种受体;Abl-Bcr:一种非受体酪氨酸激酶;Raf:酪氨酸激酶的下游信号通路中的一种蛋白;Flt-3:Src:一种非受体酪氨酸激酶;c-kit:Ret:胶质细胞源性神经营养因子的受体吉非替尼为EGFR酪氨酸激酶抑制剂,主要用于非小细胞肺癌,对酪氨酸激酶基因编码区突变型肿瘤的有效率高达80%以上。
药物化学中的小分子靶向药物研究

药物化学中的小分子靶向药物研究药物化学是研究药物的化学性质、结构和制备方法的学科。
在药物研究和开发的过程中,药物化学发挥着关键作用,通过合理设计和合成药物分子,提高药物的疗效和安全性。
其中小分子靶向药物是近年来药物研究的重要方向,其疗效和安全性优于传统的非靶向药物。
一、小分子靶向药物的定义及优势小分子靶向药物是指分子量小于1000的药物,能够特异性地与靶点结合,并发挥治疗作用。
靶点可以是蛋白质、酶、受体等与疾病相关的生物分子。
与传统的非靶向药物相比,小分子靶向药物具有以下优势。
1. 靶向性强:小分子药物可以与特定的靶点结合,发挥更强的治疗作用,并减少对非靶点的副作用。
2. 疗效高:小分子药物可以经过合理设计和优化,增加其在靶点上的亲和力和选择性,从而提高其疗效。
3. 可溶性好:小分子药物的分子量小,通常具有良好的溶解性,更容易经口服或注射等途径给药。
4. 更容易制备:由于小分子药物的分子量小,结构相对较简单,因此其研制和制备常常比生物制剂更加容易和经济。
二、小分子靶向药物的研究方法小分子靶向药物的研究涉及多个学科领域,包括药物化学、生物化学、分子生物学等。
其研究方法主要包括以下几个方面。
1. 靶点的确认和筛选:首先需要确定与疾病相关的靶点,然后利用生物学方法(如酶活性测定、受体结合实验等)进行初步筛选。
2. 分子设计和合成:根据靶点的特性,结合统计学或计算机化学方法,设计和合成一系列具有不同化学结构和生物活性的小分子化合物。
3. 药代动力学和毒理学研究:对候选药物进行药代动力学和毒理学研究,评估其药效和安全性。
4. 临床前研究:进行细胞和动物模型实验,评估小分子药物的疗效和安全性,并确定最佳的给药途径和剂量。
5. 临床试验:进行临床试验,评估小分子药物在临床上的安全性和有效性,寻求最佳的治疗方案。
三、小分子靶向药物的案例目前,小分子靶向药物已经成功地应用于多种疾病的治疗。
以下是几个常见的小分子靶向药物案例。
有机小分子脾靶向

有机小分子脾靶向有机小分子脾靶向是一种用于治疗脾相关疾病的新型药物策略。
脾脏作为人体重要的免疫器官,具有调节免疫功能、清除老化红血球、储存血液等多种功能。
然而,由于脾脏深藏于人体内部,传统的药物很难直接作用于脾脏,导致治疗效果不佳。
因此,有机小分子脾靶向的研究备受关注。
有机小分子脾靶向药物的研发主要通过设计合成具有高亲脾性的药物分子,以实现药物对脾脏的定向输送和作用。
这些药物分子通常具有特定的结构和化学性质,以增强其在体内的脾脏富集能力。
其中,药物的分子大小、电荷、亲脂性等特性都会对药物在体内的分布和靶向作用产生影响。
在有机小分子脾靶向药物的设计中,研究人员通常运用一系列的化学策略。
例如,通过改变分子的架构和空间构型,可以调控药物与脾脏细胞之间的相互作用,从而提高药物的靶向性。
此外,研究人员还可以利用化学修饰方法,在药物分子上引入特定的官能团,以增加药物与脾脏细胞的结合能力。
有机小分子脾靶向药物的研发还面临着许多挑战。
首先,脾脏作为一个复杂的器官,其内部结构和功能多样,不同的疾病可能对药物的靶向性要求不同。
因此,研究人员需要根据具体疾病的特点来设计相应的药物。
其次,由于药物的代谢和排泄过程复杂,药物在体内的稳定性和生物利用度也是研发过程中需要考虑的重要问题。
尽管有机小分子脾靶向药物的研发面临着诸多挑战,但其潜在的临床应用前景依然巨大。
通过有机小分子脾靶向药物的研究和应用,我们有望有效治疗脾相关疾病,提高患者的生活质量。
同时,该领域的不断发展也为其他器官的靶向治疗提供了新的思路和方法。
有机小分子脾靶向药物的研发为治疗脾相关疾病提供了新的方向。
通过运用合适的化学策略和设计原则,研究人员可以开发出具有高靶向性和安全性的药物,为患者带来更好的治疗效果。
随着技术的不断进步,相信有机小分子脾靶向药物将会在未来发挥更大的作用,为人类健康作出更大的贡献。
最热门抗肿瘤靶点及小分子靶向药物全景报告

最热门抗肿瘤靶点及小分子靶向药物全景报告靶向分子治疗(Targeted therapy )是一种以干扰癌变或肿瘤增生所需的特定分子来阻止癌细胞增长的一种药物疗法。
而非一般的干扰所有持续分裂细胞(不稳定细胞)的传统化疗法。
据美国FDA药品评价和研究中心(CDER)公布信息显示,自1997年第一个靶向抗肿瘤小分子获批以来,至2016年已有72个靶向抗肿瘤药物被批准,其中小分子制剂已达到30多个。
抗肿瘤小分子靶向制剂是近15年来脱颖而出的作用机制独特的药物,自从以酪氨酸激酶抑制剂(替尼类)代表的药物格列卫一战成功后,研发管线中的新产品接二连三地进入临床,上市后的品种也取得了优异的销售业绩,销售额每年过千亿。
因为小分子靶向药物的优势和巨大的市场前景,靶向药物受到各类研究机构和药物开发公司的关注。
陶素化合物筛选专家根据已上市的靶向抗癌药物整理了最热门的癌症治疗靶点,助您更便捷的锁定研究方向,获得筛选库,让我们一起来了解这些前沿靶点和小陶的供应情况吧抗癌热门靶点TOP榜F表为小陶根据已上市的靶向抗癌药物整理的最热门的癌症治疗靶点及靶向药。
还有该靶向药物在陶素官网上的货号,以及陶素针对该靶点的供应情况。
靶向药物极大改变了各类疾病的治疗局面,在副作用小、疗效显著,改善患者生存质量的同时,也创造了巨大的市场机会。
陶素生化致力于提供优质,合物库,联系我们获高效,最具研究价值的化取文中热门靶点的产品列表T argetMol 中国陶素生化药物筛选专家电话:<100-821-2233 邮箱:lnfo@tsttocInQmcom▽ Click to Follow Us回TargetMol回□。
贝福替尼 分子量

贝福替尼分子量贝福替尼(Befitinib)是一种小分子靶向药物,其分子量约为328.33克/摩尔。
这种药物主要用于治疗非小细胞肺癌,能够通过抑制肿瘤细胞的生长和扩散来达到治疗的效果。
贝福替尼属于酪氨酸激酶抑制剂,通过作用于肿瘤细胞上的表皮生长因子受体(EGFR)来抑制肿瘤细胞的增殖。
EGFR是一种重要的信号转导分子,参与调控细胞的生长、分化和增殖等生命活动。
在某些肿瘤细胞中,EGFR异常活跃,导致肿瘤细胞无限增殖,形成肿瘤。
贝福替尼能够选择性地结合于EGFR的ATP结合口袋,阻断ATP与酶结合,从而抑制EGFR的活性,减少信号传导,抑制肿瘤细胞的增殖和转移。
贝福替尼的分子量决定了其在体内的代谢和药效。
由于其较小的分子量,贝福替尼可以很好地穿透细胞膜进入细胞内部,达到对靶点的作用。
一旦进入细胞内,贝福替尼能够与EGFR结合,抑制其活性,从而抑制肿瘤细胞的生长和扩散。
同时,贝福替尼在体内的代谢和排泄也受到其分子量的影响,较小的分子量使得贝福替尼更容易被肝脏代谢和排泄,减少了药物在体内的残留时间,降低了毒副作用的发生。
贝福替尼作为一种靶向药物,在治疗非小细胞肺癌方面取得了一定的成效。
临床研究表明,贝福替尼可以延长患者的生存期和提高生存质量,减少肿瘤的复发和转移。
然而,贝福替尼也存在一些副作用,如皮疹、腹泻、高血压等,需要在临床应用中加以注意和处理。
总的来说,贝福替尼作为一种小分子靶向药物,具有较小的分子量,能够有效地抑制肿瘤细胞的生长和扩散,是治疗非小细胞肺癌的有效药物之一。
在临床应用过程中,医生需要根据患者的具体情况和病情选择合适的剂量和疗程,并注意监测患者的药物反应和副作用,以确保治疗的有效性和安全性。
希望随着科学技术的不断发展,贝福替尼这类靶向药物能够为更多肿瘤患者带来更好的治疗效果,为人类健康作出更大的贡献。
什么是小分子靶向药物?
什么是小分子靶向药物?展开全文生物大分子药物(包括多肽、蛋白质、抗体、聚糖与核酸等)多用于治疗肿瘤、艾滋病、心脑血管病、肝炎等重大疾病。
小分子靶向药物:通常是信号传导抑制剂,它能够特异性地阻断肿瘤生长、增殖过程中所必需的信号传导通路,从而达到治疗的目的。
小分子药物具有使用广泛、理论成熟等优势。
常用药物,小分子药物的数量占总量的98%。
截至2016年7月,FDA一共批准了43个抗肿瘤小分子靶向药物,其中有2个是不用于肿瘤治疗的替尼类药物,分别是治疗类风湿关节炎的托法替尼和治疗骨髓纤维化的鲁索替尼。
这45个小分子靶向药物中,治疗肺癌和白血病的最多,各有8个,其次是肾癌,有7个。
目前,小分子化学药物仍然是当前药物设计的主要方向。
治疗肿瘤的小分子靶向药物多为口服药,方便,对正常细胞损伤小,具有特异性,也是抗肿瘤药研发的热点。
下面整理了最新小分子靶向药物,以及详细的分析介绍。
肺癌。
用于治疗肺癌的小分子靶向药物有8种,见下表。
肺癌的治疗靶点主要有两类,一类是表皮生长因子受体(EGFR),以吉非替尼、厄洛替尼为代表;另一类是间变性淋巴瘤激酶(ALK),主要是克唑替尼、色瑞替尼等。
目前在我国上市的品种有原研进口的吉非替尼、厄罗替尼、克唑替尼,及我国自主研发的埃克替尼。
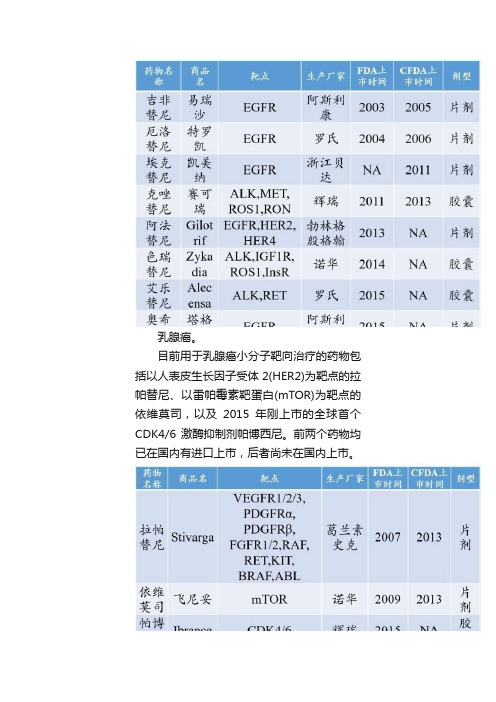
乳腺癌。
目前用于乳腺癌小分子靶向治疗的药物包括以人表皮生长因子受体2(HER2)为靶点的拉帕替尼、以雷帕霉素靶蛋白(mTOR)为靶点的依维莫司,以及2015年刚上市的全球首个CDK4/6激酶抑制剂帕博西尼。
前两个药物均已在国内有进口上市,后者尚未在国内上市。
胃癌&胃肠道间质瘤。
胃癌靶向治疗起步较晚,小分子靶向药物较少,治疗靶点目前主要集中在VEGFR。
伊马替尼除了是白血病的一线用药,也可以治疗胃肠道间质瘤;舒尼替尼和瑞戈非尼属于多靶点药物。
值得一提的是,阿帕替尼是中国自主研发的一种小分子 VEGF 受体抑制剂。
除了瑞戈非尼,其他三个小分子靶向药在中国均有上市;伊马替尼国内仿制药有正大天晴、江苏豪森、石药欧意三家。
新型药物——小分子抑制剂

新型药物——小分子抑制剂小分子抑制剂是一种新型的药物,这种药物的特点是分子很小,可以轻易地渗透到细胞内,对某些疾病的治疗效果是非常明显的。
这篇文章将为您介绍小分子抑制剂的原理、应用和未来发展。
原理小分子抑制剂是一种靶向治疗。
它的原理是针对某些分子的作用机制,通过降低它们的活性来达到治疗的效果。
这些分子可以是酶、代谢物、受体甚至是DNA。
药物通过与这些分子结合,改变它们的结构或者活性,从而影响它们在细胞内的功能。
例如,丙戊酸抑制剂是一种针对缺乏激素的疾病的药物。
这种药物能够抑制一个叫做丙戊酸合成酶的酶的活性,从而减少丙戊酸的合成,达到治疗的效果。
又比如,一些肿瘤抑制剂能够通过与癌细胞的DNA结合,阻止癌细胞的分裂和增殖,从而起到治疗的效果。
应用范围小分子抑制剂的应用范围很广泛,它可以用来治疗许多疾病。
目前,针对癌症的小分子抑制剂最为发达。
根据当前临床试验,小分子抑制剂已经能够用来治疗许多类型的癌症,包括前列腺癌、卵巢癌、肺癌等。
同样,小分子抑制剂也可以用来治疗心血管疾病、炎症性疾病等其他非肿瘤性疾病。
值得注意的是,小分子抑制剂的应用范围和作用机制千差万别。
因此,在治疗之前,医生需要根据病情和药物特性来选择合适的药物。
未来发展小分子抑制剂是一种很有前景的药物。
尽管它已经在医学上发挥了很大的作用,但是小分子抑制剂还有很大的发展空间。
下面简单介绍一下它的未来发展方向:一、针对特定基因的治疗;二、开发具有多种作用的小分子抑制剂;三、研究小分子抑制剂和其他药物的组合治疗效果;四、通过纳米技术,将小分子抑制剂送达到目标细胞的更深层次等。
当然,这些方向目前仍然在不断完善和研究之中,需要更多的科学家和医生的共同努力。
小结小分子抑制剂是一种很有潜力的药物,它的应用范围广泛,并且有着很好的治疗效果。
尽管目前已经有不少的小分子抑制剂面市,但我们相信,未来它们的发展一定会更加迅速和广泛。
对于我们日常生活的健康,它们也一定会起到越来越重要的作用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学抗肿瘤药物经过半个多世纪的发展,已经进入靶向治疗药物时代。
小分子靶向药物在临床上的应用日益增多,在一些肿瘤类别中已经进入一线用药地位,比如肾癌、慢粒白、多发性骨髓瘤等。
本文对小分子靶向治疗药物做一综述。
小分子靶向治疗药物简介一、受体酪氨酸激酶抑制剂作为抗肿瘤药物靶点的酪氨酸激酶有两类,一类是受体酪氨酸激酶(RTKs),另一类是非受体酪氨酸激酶(nrRTKs)。
如图2,作为抗肿瘤药物靶点的RTKs是一种生长因子受体,其本质为跨膜蛋白,胞外结构域负责与生长因子结合,胞内结构域含有激酶活性。
当RTKs 与生长因子结合后,胞内的激酶活性被激活,继而使底物蛋白的酪氨酸残基磷酸化,被磷酸化的蛋白质再引发多种信号通路的瀑布效应,并进一步引发基因转录,达到调节靶细胞生长与分化的作用。
图2 受体酪氨酸激酶(RTKs)的胞内信号转导途径按照其结合的生长因子的不同,又可以将RTKs分为多种类型,主要包括表皮生长因子受体家族、血小板衍生因子受体家族、成纤维细胞生长因子受体家族、胰岛素样生长因子受体家族、血管内皮生长因子受体家族。
受体酪氨酸激酶抑制剂:小分子受体酪氨酸激酶抑制剂(TKI)阻止RTKs酪氨酸激酶功能的激活。
当TKI进入肿瘤细胞后,与RTKs在胞内的ATP结合位点结合,从而抑制RTKs 的磷酸化,阻止激酶的激活,阻断受体下游信号通路的传导而发挥抗肿瘤作用。
从作用机制上看,受体酪氨酸激酶抑制剂作用于信号传导途径的最上游,同时阻断多条通路,具有治疗范围广、疗效高的优点。
目前上市的受体酪氨酸激酶抑制剂有两代。
第一代为单靶点酪氨酸激酶抑制剂,如吉非替尼、厄洛替尼。
表已上市的酪氨酸激酶抑制剂注:EGFR:表皮生长因子受体,属HER家族;VEGFR:血管内皮生长因子;PDGFR:血小板衍生因子;HER2:HER家族的一种受体;Abl-Bcr:一种非受体酪氨酸激酶;Raf:酪氨酸激酶的下游信号通路中的一种蛋白;Flt-3:Src:一种非受体酪氨酸激酶;c-kit:Ret:胶质细胞源性神经营养因子的受体吉非替尼为EGFR酪氨酸激酶抑制剂,主要用于非小细胞肺癌,对酪氨酸激酶基因编码区突变型肿瘤的有效率高达80%以上。
厄洛替尼为EGFR酪氨酸激酶抑制剂,该药对非小细胞肺癌复治患者的有效率为10%左右。
酪氨酸激酶的研发仍然面临着一些很关键的问题,一是耐药性的出现,二是肿瘤通常有一条以上的激酶通路被激活,信号通路存在交叉和代偿。
因此,研究人员开发出第二代酪氨酸激酶抑制剂,包括:凡德他尼、达沙替尼、舒尼替尼、拉帕替尼、达沙替尼和尼洛替尼,它们对伊马替尼耐药的白血病有一定的治疗效果。
二、非受体酪氨酸激酶抑制剂和RTKs不同,nrRTKs不与配体结合,但是当其他受体与配体结合后,nrRTKs将被激活,后者再激活下游的信号转导途径,诱导类似RTKs的反应。
nrRTKs 能够促进细胞增殖,抑制细胞凋亡,从而促进肿瘤发生和发展。
与细胞生存和增殖相关的nrPTK有Src家族,如Src、Abl、Lck等,以及其他酪氨酸激酶,如JAK、FAK和Ack等。
图3 非受体酪氨酸激酶(nrRTKs)的胞内信号转导途径首个上市的小分子酪氨酸激酶抑制剂——伊马替尼,为Abl-Bcr蛋白激酶抑制剂,主要用于慢性粒细胞白血病。
其他多靶点受体酪氨酸激酶抑制剂也可以作用于由非受体酪氨酸蛋白激酶介导的信号转导通路,如达沙替尼除作用于PDGFR外,也作用于Bcr-Abl和Src。
尼洛替尼除作用于PDGFR外,也作用于Bcr-Abl(参表)。
三、Ras-Raf-MEK-MAPK信号通路阻滞剂如图2、3所示,酪氨酸激酶的激活将引发下游信号通路的启动。
其中Ras/MAPK通路是研究最多的一种,除此之外还有PI3K等通路。
Ras/MAPK通路是调控细胞增殖和细胞生存过程的信号通路,可以由EGF、PDGF和IGF-1等多种细胞外生长因子激活。
受体酪氨酸激酶激活后,将依次激活Ras、Raf、MEK和MAPKs,活化的MAPKs进入细胞核,通过磷酸化作用激活转录因子,从而干扰细胞周期和细胞转化过程。
MAPKs还能诱导蛋白及基质降解,促进细胞迁移,维持肿瘤生长。
图4 Ras-Raf-MEK-MAPK信号通路法尼酰基转移酶抑制剂Ras蛋白必须经过“法尼基转移酶”法尼基化后才能成长为成熟蛋白,参与Ras-Raf-MEK-MAPK信号通路,调控细胞的增殖和恶性转化。
故,抑制“法尼基转移酶”可以抑制Ras蛋白的法尼基化,阻断癌细胞的增殖。
目前上市的法尼酰基转移酶抑制剂只有arglabin,其为一种从多花蒿植物中提取的倍半萜烯内酯,已在萨哈特斯坦和前苏联上市,目前正准备在美国等其他国家上市。
处于Ⅲ期临床的法尼酰基转移酶抑制剂有tipifarnib ,处于Ⅱ期临床的有lonafarnib。
Arglabin tipifarniblonafarnibRaf激酶抑制剂目前上市的Raf抑制剂只有索拉非尼。
索拉非尼是一种多靶点激酶抑制剂,可以同时抑制VEGFR-2,3,PDGFR,Raf和Flt-3。
MEK抑制剂MEK抑制剂目前没有上市,trametinib处于Ⅲ期临床阶段。
p38 MAPK抑制剂没有上市四、mTOR激酶抑制剂mTOR是一种丝/苏氨酸激酶,在调节细胞的生长和增殖过程中起重要作用。
mTOR直接或间接调节翻译其实、肌动蛋白构建、t-RNA的合成、核蛋白体的形成及其他许多关键细胞的功能维持,包括蛋白质降解和转录、抑制mTOR是通过阻止细胞从G1期到S期。
mTOR激酶抑制剂尚未在中国上市用于抗肿瘤。
西罗莫司在中国上市用于治疗排异反应,国内有5家企业生产,其用于治疗非小细胞肺癌处于临床2期试验。
依维莫司最早于2004年在德国上市,2009年在美国上市,尚未在中国上市。
、其他信号传导途径阻断剂五、组蛋白脱乙酰基酶抑制剂(HDACIs)除基因序列外,还有一些因素也参与决定基因的表达与否,并可稳定遗传给子代细胞。
这些因素称为“表观遗传密码”,包括DNA的后天性修饰(如甲基化修饰)和组蛋白的各种修饰(如乙酰化修饰)等。
核心组蛋白尾部发生的翻译后修饰可以影响组蛋白与DNA的亲和性,而改变染色质的状态,也可以影响转录因子与DNA序列的结合。
肿瘤细胞主要表现为低乙酰化状态,组蛋白去乙酰化酶活性异常,组蛋白过度去乙酰化,从而引起抑癌基因表达抑制、癌基因激活或过度表达。
组蛋白脱乙酰基酶抑制剂(HDACIs)抑制组蛋白的去乙酰化,增强抑癌基因的表达和抑制癌基因的表达。
与传统抗肿瘤药物相比,HDACIs有两个治疗优势:①可以直接作用于基因的异常表达这一关键环节,从而抑制和纠正肿瘤细胞的增殖过度、逃逸凋亡、分化能力下降,这将有别于传统抗肿瘤药物仅针对细胞增殖过度单一表型,对因基因表达异常所致的其他表型作用较弱的缺点。
②可以针对患者化疗中常见的耐药问题,HDACIs不仅可以增加抗肿瘤药物种类的选择性,还可以与不同作用机制的药物联合应用,有利于避免耐药的发生,提高患者的生产率。
组蛋白脱乙酰基酶抑制剂用于抗癌大多处于临床前研究,仅romidepsin和伏立诺他两个品种上市。
另外,有14个化合物进入2期临床:ACY-1215、resminostat、DAC-60、AR-42、chidamide、SB-939、panobinostat、abexinostat、vorinostat、belinostat、entinostat、mocetinostat、givinostat、romidepsin。
Romidepsin于2009年在美国上市,用于治疗T细胞淋巴瘤,其他适应症,如乳腺癌、非霍奇金淋巴瘤、骨髓瘤、卵巢癌、胰腺癌、前列腺癌和肾癌,处于Ⅱ期临床研究。
我国尚无Romidepsin的注册申报信息。
伏立诺他于年在上市,用于治疗。
尚未在我国上市,目前有家申报。
Romidepsin和伏立诺他的具体申报信息见附录,专利信息见附录……五、泛素-蛋白酶体抑制剂肿瘤是一类渐进性细胞周期调控机制破坏的疾病。
细胞周期的正常运行依赖于正负调控机制的平衡,细胞周期蛋白依赖性激酶(CDK)是细胞周期运行的动力,它的活性受细胞周期蛋白(cyclin)和细胞周期蛋白依赖性激酶抑制剂(CDKI)的调控。
当cyclin与CDK结合时,细胞周期开始运行,而CDKI是细胞周期的负调控机制,对细胞周期运行起抑制作用。
故上述调控因子的消失和出现的平衡维持着正常的细胞周期。
在肿瘤细胞中,正调控机制往往被上调,而负调控机制被下调。
可以理解为CDKI被过多的降解了,故细胞不断的分裂生长。
在细胞内,细胞周期调控蛋白的降解工作由“泛素——蛋白酶体”负责。
如下图示,当蛋白质有待降解时,它首先被泛素标记,被泛素标记的蛋白再被26S蛋白酶体识别并予以降解,泛素被释放出来再次参与循环。
硼替佐米可逆性地抑制26S蛋白酶体的糜蛋白酶样活性,防止靶蛋白的分解,调整细胞周期正负调控机制之间的关系,引起细胞凋亡。
硼替佐米于2003年在美国上市,用于治疗①多发性骨髓瘤和②外套细胞淋巴瘤。
2005年进口到我国。
六、血管生成抑制剂血管生成是实体肿瘤细胞的生长和转移的必要条件,血管生成能够为肿瘤细胞提供更多的营养物质和氧气,阻止肿瘤血管网的形成能够使肿瘤变小,并阻止肿瘤的转移。
尽管抗血管治疗在预防肿瘤复发、预防转移形成中具有重要作用,但该疗法只能延缓肿瘤的生长,难以彻底消灭肿瘤细胞,对体积较大的肿瘤治疗效果并不乐观。
此外,该疗法在临床试验中仍存在一定的问题:(1)有形成血栓、出血、生殖功能障碍、伤口愈合延迟等多种毒副作用;(2)最佳用药时间和剂量的确定;(3)动物实验中疗效显著,但在临床试验中效果不佳。
如何解决这些问题已经成为当前抗血管生成药物研究工作的重点,有待于进一步探讨研究。
小分子靶向药物临床使用现状:从抗肿瘤用药指南来看,传统细胞毒类药物仍然为主流用药,小分子靶向治疗药物主要集中在肾癌、多发性骨髓瘤及血液瘤,在乳腺癌、非小细胞肺癌、胃癌中也有应用,内分泌治疗主要集中在乳腺癌、卵巢癌、子宫肿瘤、前列腺癌。
2011年NCCN推荐的一线抗肿瘤药物盐酸吉非替尼O O厄洛替尼Trametinib西罗莫司sirolimus(雷帕霉素rapamycin)依维莫司everolimus别名:依维菌素Romidepsin伏立诺他vorinostat帕比诺他PanobinostatAbexinostatBelinostatEntinostatHN NHNNNH2NOMocetinostatGivinostat硼替佐米Bortezomib。
