肿瘤小分子靶向药物分类
小分子靶向治疗药物简介
化学抗肿瘤药物经过半个多世纪的发展,已经进入靶向治疗药物时代。
小分子靶向药物在临床上的应用日益增多,在一些肿瘤类别中已经进入一线用药地位,比如肾癌、慢粒白、多发性骨髓瘤等。
本文对小分子靶向治疗药物做一综述。
小分子靶向治疗药物简介一、受体酪氨酸激酶抑制剂作为抗肿瘤药物靶点的酪氨酸激酶有两类,一类是受体酪氨酸激酶(RTKs),另一类是非受体酪氨酸激酶(nrRTKs)。
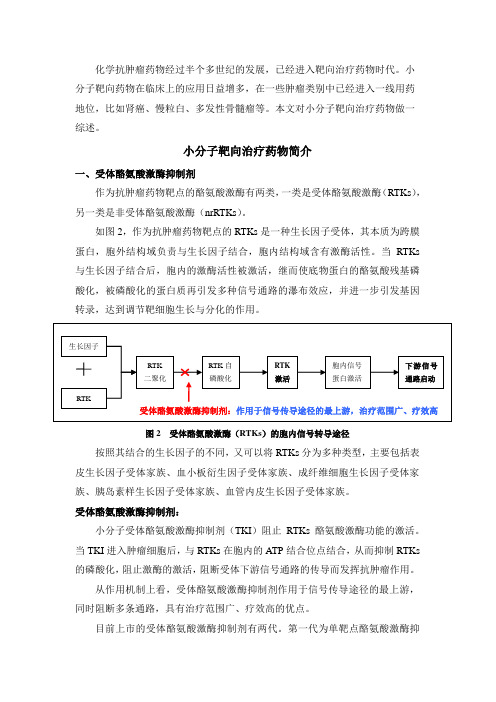
如图2,作为抗肿瘤药物靶点的RTKs是一种生长因子受体,其本质为跨膜蛋白,胞外结构域负责与生长因子结合,胞内结构域含有激酶活性。
当RTKs 与生长因子结合后,胞内的激酶活性被激活,继而使底物蛋白的酪氨酸残基磷酸化,被磷酸化的蛋白质再引发多种信号通路的瀑布效应,并进一步引发基因转录,达到调节靶细胞生长与分化的作用。
图2 受体酪氨酸激酶(RTKs)的胞内信号转导途径按照其结合的生长因子的不同,又可以将RTKs分为多种类型,主要包括表皮生长因子受体家族、血小板衍生因子受体家族、成纤维细胞生长因子受体家族、胰岛素样生长因子受体家族、血管内皮生长因子受体家族。
受体酪氨酸激酶抑制剂:小分子受体酪氨酸激酶抑制剂(TKI)阻止RTKs酪氨酸激酶功能的激活。
当TKI进入肿瘤细胞后,与RTKs在胞内的ATP结合位点结合,从而抑制RTKs 的磷酸化,阻止激酶的激活,阻断受体下游信号通路的传导而发挥抗肿瘤作用。
从作用机制上看,受体酪氨酸激酶抑制剂作用于信号传导途径的最上游,同时阻断多条通路,具有治疗范围广、疗效高的优点。
目前上市的受体酪氨酸激酶抑制剂有两代。
第一代为单靶点酪氨酸激酶抑制剂,如吉非替尼、厄洛替尼。
表已上市的酪氨酸激酶抑制剂注:EGFR:表皮生长因子受体,属HER家族;VEGFR:血管内皮生长因子;PDGFR:血小板衍生因子;HER2:HER家族的一种受体;Abl-Bcr:一种非受体酪氨酸激酶;Raf:酪氨酸激酶的下游信号通路中的一种蛋白;Flt-3:Src:一种非受体酪氨酸激酶;c-kit:Ret:胶质细胞源性神经营养因子的受体吉非替尼为EGFR酪氨酸激酶抑制剂,主要用于非小细胞肺癌,对酪氨酸激酶基因编码区突变型肿瘤的有效率高达80%以上。
靶向药物的分类和作用机理

靶向药物的分类和作用机理
一、概念:所谓靶向药物,就是以参与肿瘤发生发展过程的重要分子作为靶点,通过抑制或阻断该靶点,而发挥治疗作用的药物。
二、机理:靶点通常是与肿瘤细胞的增殖、抗凋亡、迁移和转移、以及血管生成等相关的分子。
在众多的靶点中,与肿瘤细胞增殖密切相关的驱动基因,往往是最好的靶点,比如表皮生长因子受体抑制剂,用于治疗EGFR基因突变的肺腺癌患者,获得了比传统细胞毒性药物治疗更好的疗效,且毒性反应轻微。
与传统化疗药物相比,靶向药物具有特异性、个体化、疗效高和对正常组织损伤小的特点。
三、分类:靶向药物按照分子结构和作用机制,可以分为两大类:单克隆抗体类和小分子化合物类。
单克隆抗体属于生物大分子,无法穿透细胞膜,主要通过与细胞外或胞膜上的抗原结合发挥作用。
抗体类包括裸抗体和修饰抗体。
裸抗体抑制肿瘤细胞增殖的主要机制包括:抗体依赖的细胞毒性作用、补体依赖的细胞毒性作用以及通过受体——配体的相互作用诱导细胞凋亡等。
修饰抗体可通过特异性的抗原抗体反应,将偶联上的放射性核素、毒素、药
物、酶等带至肿瘤局部或肿瘤细胞内,起到杀伤肿瘤细胞的作用。
肿瘤靶向治疗经典药物

肿瘤靶向治疗经典药物
EEGFR(表皮生长因子)抑制剂:
(1)单克隆抗体:Erbitux(爱必妥。
西妥昔单抗,IMC-C225)
(2)作用于TPK系统的小分子靶向药物:
①IreSSa(gefitinib,ZD1839)(易瑞沙,吉非替尼片)可抑制EGFR酪氨酸激酶;是肺癌生物靶点治疗中较为成熟的药物,公认适用于复发、晚期NSCLC二线、三线治疗;IrSSSa治疗临床观察:女性,腺癌,年龄>68岁,不吸烟者疗效较好;
②TarCeVa(erlotinib,0SI-774)(特罗凯,盐酸厄洛替尼片)酪氨酸酶抑制剂。
认为主要对细支气管肺泡癌最有活力,而且在不吸烟中有较好RR;
2、其他酪氨酸激酶抑制剂:
①GIiVeC(格列卫)针对BCR-ABL基因靶目标治疗慢性粒细胞白血病,针对C-Kit基因靶目标从而治疗GlST(胃肠道间质瘤)。
通过与ATP竞争性结合酪氨酸激酶催化部位的核甘酸结合位点,使得激酶不能发挥催化活性,底物的酪氨酸残基不能被磷酸化,使其不能与下游的效应分子进一步作用,导致细胞增殖受抑,诱导细胞凋亡。
②SOrafenib(多激酶抑制剂)索拉非尼
③SUtent(多个受体TK抑制剂)舒尼替尼
3、其他单克隆抗体:
①HerCePtin:赫赛汀,抗HER-2受体单抗;
②Mabthera(美罗华,rituximab利妥昔单抗)抗CD20受体单抗。
4、血管生长抑制剂:AVaStin(贝伐单抗制抗VEGF单抗。
沙利度胺(反应停)。
肿瘤分子靶向药物分类及作用机制

· 526ห้องสมุดไป่ตู้·
专题笔谈
中国实用外科杂志 2010 年 7 月 第 30 卷 第 7 期
肿瘤靶向药物治疗
文章编号:1005-2208(2010)07-0526-04
肿瘤分子靶向药物分类及作用机制
王雅杰,王 宁
【摘要】 分子靶向治疗与传统化疗的作用机制和副反应不 同,是针对肿瘤特殊的分子靶点而起到个体化治疗的作 用,对正常组织的毒副反应轻微。10 年来,由于靶向治疗 独特的作用机制,使肿瘤的治疗模式有了根本性的改变。 单克隆抗体和小分子化合物是最重要的两类靶向治疗药 物,其作用主要是对酪氨酸受体激酶(RTKs)和非受体激 酶、抗血管生成、细胞外基质蛋白酶等方面的抑制。 【关键词】 肿瘤;分子靶向治疗 中图分类号:R6 文献标志码:A
past 10 years. The two main types of targeted therapies are
monoclonal antibodies and small molecule inhibitors that they
would inhibit receptor tyrosine kinases (RTKs), nonreceptor
常用的小分子靶向药物和大分子单克隆抗体类药物

达拉非尼
曲美替尼
帕博利珠单抗
特瑞普利单抗
结节性硬化症相关的室管膜下巨细胞星形细胞瘤
依维莫司
结节性硬化症相关的肾血管平滑肌脂肪瘤
依维莫司
骨巨细胞瘤
地舒单抗
腺泡状软组织肉瘤
安罗替尼
透明细胞肉瘤
安罗替尼
其他晚期软组织肉瘤
安罗替尼
鼻咽癌
尼妥珠单抗
甲状腺癌
索拉非尼
头颈部鳞状细胞癌
西妥昔单抗
纳武利尤单抗
卡瑞利珠单抗
替雷利珠单抗
泽布替尼
多发性骨髓瘤
硼替佐米
来那度胺
沙利度胺
伊沙佐米
达雷妥尤单抗
骨髓增殖性疾病
芦可替尼
肾癌
依维莫司
索拉非尼
舒尼替尼
阿昔替尼
培唑帕尼
仑伐替尼
安罗替尼
帕博利珠单抗
纳武利尤单抗
乳腺癌
曲妥珠单抗
恩美曲妥珠单抗
帕妥珠单抗
伊尼妥单抗
拉帕替尼
吡咯替尼
奈拉替尼
哌柏西利
西达本胺
黑色素瘤
伊马替尼
表表1常用的小分子靶向药物和大分子单克隆抗体类药物病种需要检测靶点的药物不需要检测靶点的药物肺癌吉非替尼厄洛替尼埃克替尼阿法替尼达可替尼奥希替尼克唑替尼阿来替尼塞瑞替尼阿美替尼贝伐珠单抗重组人血管内皮抑制素安罗替尼纳武利尤单抗帕博利珠单抗度伐利尤单抗卡瑞利珠单抗阿替利珠单抗依维莫司肝癌索拉非尼瑞戈非尼仑伐替尼卡瑞利珠单抗食管癌卡瑞利珠单抗帕博利珠单抗胃癌曲妥珠单抗阿帕替尼纳武利尤单抗胃肠间质瘤伊马替尼瑞戈非尼舒尼替尼胰腺神经内分泌瘤舒尼替尼依维莫司结直肠癌西妥昔单抗贝伐珠单抗瑞戈非尼呋喹替尼白血病伊马替尼达沙替尼伊布替尼尼洛替尼淋巴瘤利妥昔单抗维布妥昔单抗西达本胺伊布替尼硼替佐米信迪利单抗卡瑞利珠单抗替雷利珠单抗泽布替尼多发性骨髓瘤硼替佐米来那度胺沙利度胺伊沙佐米达雷妥尤单抗骨髓增殖性疾病芦可替尼肾癌依维莫司索拉非尼舒尼替尼阿昔替尼培唑帕尼仑伐替尼安罗替尼帕博利珠单抗纳武利尤单抗乳腺癌曲妥珠单抗恩美曲妥珠单抗帕妥珠单抗伊尼妥单抗拉帕替尼吡咯替尼哌柏西利西达本胺奈拉替尼黑色素瘤伊马替尼维莫非尼达拉非尼曲美替尼帕博利珠单抗特瑞普利单抗结节性硬化症相关的室管膜下巨细胞星形细胞瘤依维莫司结节性硬化症相关的肾血管平滑肌脂肪瘤依维莫司骨巨细胞瘤地舒单抗腺泡状软组织肉瘤安罗替尼透明细胞肉瘤安罗替尼其他晚期软组织肉瘤安罗替尼鼻咽癌尼妥珠单抗甲状腺癌索拉非尼头颈部鳞状细胞癌西妥昔单抗纳武利尤单抗卵巢癌奥拉帕利尼拉帕利
抗肿瘤靶向药物的分类_张百红

1230.[19] CostaBM,SmithJS,ChenY,etal.ReversingHOXA9oncogeneactivationbyPI3Kinhibition:Epigeneticmechanismandprognos ticsignificanceinhumanglioblastoma[J].CancerRes,2010,70(2):453-462.[20] VerhaakRG,HoadleyKA,PurdomE,etal.Integratedgenomicanalysisidentifiesclinicallyrelevantsubtypesofglioblastomachar acterizedbyabnormalitiesinPDGFRA,IDH1,EGFR,andNF1[J].CancerCell,2010,17(1):98-110.[21] PojoM,GoncalvesCS,Xavier-MagalhaesA,etal.AtranscriptomicsignaturemediatedbyHOXA9promoteshumanglioblastomainitiation,aggressivenessandresistancetotemozolomide[J].On cotarget,2015,6(10):7657-7674.[22] OtaT,KlausenC,ClaraSalamancaM,etal.ExpressionandfunctionofHOXAgenesinnormalandneoplasticovarianepithelialcells[J].Differentiation,2009,77(2):162-171.[23] KoSY,BarengoN,LadanyiA,etal.HOXA9promotesovariancancergrowthbystimulatingcancer-associatedfibroblasts[J].JClinicalInvestigation,2012,122(10):3603-3617.[24] KoSY,NaoraH.HOXA9promoteshomotypicandheterotypiccellinteractionsthatfacilitateovariancancerdisseminationviaitsin ductionofP-cadherin[J].MolCancer,2014,13:170.[25] WrangleJ,MachidaEO,DanilovaL,etal.Functionalidentificationofcancer-specificmethylationofCDO1,HOXA9,andTAC1forthediagnosisoflungcancer[J].ClinCancerRes,2014,20(7):1856-1864.[26] HwangJ,LeeBB,KimY,etal.HOXA9inhibitsmigrationoflungcancercellsanditshypermethylationisassociatedwithrecurrenceinnon-smallcelllungcancer[J].MolecularCarcinogenesis,2015,54(S1):E72-E80.[27] ReynoldsPA,SigaroudiniaM,ZardoG,etal.Tumorsuppressorp16INK4Aregulatespolycomb-mediatedDNAhypermethylationinhumanmammaryepithelialcells[J].JBiolChem,2006,281(34):24790-24802.[28] ParkSY,KwonHJ,LeeHE,etal.PromoterCpGislandhypermethylationduringbreastcancerprogression[J].VirchowsArch,2011,458(1):73-84.[29] SunM,SongCX,HuangH,etal.HMGA2/TET1/HOXA9signalingpathwayregulatesbreastcancergrowthandmetastasis[J].ProceedingsoftheNationalAcademyofSciences,2013,110(24):9920-9925.[30] LvJ,CaoXF,JiL,etal.Associationofbeta-catenin,Wnt1,Smad4,Hoxa9,andBmi-1withtheprognosisofesophagealsquamouscellcarcinoma[J].MedOncol,2012,29(1):151-160.[31] SunX,LiuB,JiW,etal.TheroleofHOXA9inhumanlaryngealsquamouscellcarcinoma[J].OncologyResearchFeaturingPre clinicalandClinicalCancerTherapeutics,2012,20(10):467-472.[32] KimY,YoonH,KimJS,etal.HOXA9,ISL1andALDH1A3methylationpatternsasprognosticmarkersfornonmuscleinvasivebladdercancer:Array-basedDNAmethylationandexpressionprofiling[J].InternationalJCancer,2013,133(5):1135-1142.[33] KuoC,LinC,ShihY,etal.FrequentmethylationofHOXA9geneintumortissuesandplasmasamplesfromhumanhepatocellularcarcinomas[J].ClinicalChemistryandLaboratoryMedicine(CCLM),2014,52(8):1235-1245.(编校:张西敏)抗肿瘤靶向药物的分类张百红1,岳红云2AnewclassificationfortargetedanticanceragentsZhangBaihong1,YueHongyun21DepartmentofOncology;2DepartmentofOphthalmology,LanzhouGeneralHospital,LanzhouMilitaryAreaCommand,PLA,GansuLanzhou730050,China.【Abstract】Theclassificationoftargetedanticanceragentsiselusive.Accordingtotherapeutictargets,weproposeanewclassificationfortheseagentstoevaluatethem:Moleculartargetedagents,vasculartargetedagents,immunomodu latoryagentsandcellulartargetedagents.Thisclassificationfortargetedagentsaccountingforoptimaltargetsandpre cisionmechanisms,couldprovideeffectivetoolsforclinicians.【Keywords】neoplasms,targetedanticancertherapies,targetedagents,classificationModernOncology2017,25(02):0299-0303【收稿日期】 2016-06-07【修回日期】 2016-07-11【基金项目】 甘肃省自然科学基金项目(编号:1308RJZA181)【作者单位】 1兰州军区兰州总医院肿瘤科;2眼科,甘肃 兰州 730050【作者简介】 张百红(1970-),男,河南陕县人,副主任医师,副教授,主要从事消化道肿瘤的基础和临床研究。
肿瘤的分子靶向治疗方法
肿瘤分子靶向治疗的治疗方法分类
小分子靶向药物:通过抑制肿瘤细胞 生长和增殖,达到治疗目的
单克隆抗体:通过特异性识别肿瘤细 胞表面抗原,达到治疗目的
基因治疗:通过基因编辑技术,改变 肿瘤细胞基因表达,达到治疗目的
免疫治疗:通过激活或增强免疫系统, 达到治疗目的
细胞治疗:通过细胞移植或细胞工程, 达到治疗目的
肿瘤分子靶向治疗的临床应用
肿瘤分子靶向治疗在肺癌中的应用
肺癌是常见的恶性肿瘤之一,分子靶向治疗在肺癌中的应用越来越广泛。 常见的分子靶向治疗药物包括EGFR抑制剂、ALK抑制剂等。 靶向治疗可以针对特定的基因突变进行治疗,提高治疗效果,减少副作用。 靶向治疗在肺癌中的应用还需要进一步研究和探索,以找到更有效的治疗方法。
肿瘤分子靶向治疗在结直肠癌中的应用
结直肠癌的分子靶向治疗: 针对特定基因突变的靶向 药物
靶向药物的选择:根据基 因突变类型选择合适的靶 向药物
治疗效果:靶向药物在结 直肠癌治疗中的疗效和副 作用
联合治疗:靶向药物与其 他治疗方法的联合应用
患者预后:靶向治疗对结 直肠癌患者预后的影响
肿瘤分子靶向治疗在其他癌症中的应用
来经济压力。
缺乏有效的生物标志物: 目前缺乏有效的生物标志 物来预测靶向药物的疗效, 导致治疗效果难以预测。
肿瘤分子靶向治疗的研究方向与展望
研究方向:寻找新 的肿瘤分子靶点,
提高治疗效果
展望:开发新型 免疫治疗方法,
提高治疗效果
展望:开发新型靶 向药物,提高治疗
效果
研究方向:研究 肿瘤耐药机制,
提高治疗效果
THANK YOU
汇报人:XX
添加 标题
乳腺癌:HER2靶向治疗
分子靶向药物分子量大小分类作用机制临床运用
福建医科大学基础临床——恶性肿瘤靶向分子治疗3,分子靶向治疗药物按分子量大小可分为哪两类,以抗EGFR为例说明两类药物的作用机制,临床运用等方面的差别第一种答案:3.1 EGFR的单克隆抗体(mAbs)直接作用于EGFR的细胞外配体结合区,阻滞配体与EGFR 的结合,抑制生长因子激活细胞有丝分裂信号的下传,抑制肿瘤细胞增殖。
这类抗体主要有:西妥昔单抗(Cetuximab,Erbitux IMC C225嵌和型单抗)[8]、曲妥珠单抗(Trastuzumab)[9]、ABX EGFR(人源化单抗)[10]和EMD72000(人化的单克隆抗体)等。
3.2 EGFR的小分子抑制物这些小分子可逆的与ATP竞争结合EGFR胞内区激酶催化位点,抑制信号的下传达到抗肿瘤作用。
此类已经进行临床研究的小分子化合物有:ZD1839(易瑞沙)[11]、OSI774(它赛瓦)[12]、CI1033(PD183805)、PKI166等。
第二种答案:随着针对实体肿瘤治疗的分子靶点研究的深入,目前已经可以通过多种途径抑制这些靶点:一种是利用单克隆抗体等主要作用于胞外途径的大分子物质(相对分子质量为150000)与靶点结合,阻断胞外信号分子与靶点的结合;另一种是利用小分子抑制物(相对分子质量通常为500)直接进入细胞内封闭受体,干扰细胞内信号的传递。
目前用于EGFR靶向性治疗肿瘤的药物主要分为两类: EGFR单克隆抗体和小分子化合物酪氨酸激酶拮抗剂。
酪氨酸激酶拮抗剂主要为小分子喹啉类化合物,能够竞争性抑制ATP与EGFR胞内酪氨酸激酶结构域的结合,进而影响酪氨酸残基磷酸化,抑制EGFR下游的信号转导。
酪氨酸激酶拮抗剂的抗EGFR单克隆抗体治疗肿瘤进展临床疗效有很大的个体差异,使治疗剂量的确立存在困难。
EGFR单克隆抗体是与内源性配体竞争结合EGFR,通过抑制酪氨酸激酶的激活、促进EGFR内化等作用产生抗肿瘤效应。
目前已有3种抗EGFR单克隆抗体上市,与其他化疗药相比,这些抗体作用特异性强,副作用小,在临床上取得了较好的疗效。
常见的靶向治疗药物
⒋ Bcr-Abl酪氨酸激酶抑制剂:
甲磺酸伊马替尼〔Imatinib,mesylate,STI571> : 商品名:格列卫〔美国称Gleevec,欧洲称Glivec 生产商:瑞士诺华〔Novartis
是一种2-苯胺嘧啶的衍生物,是与ATP相关的选择性 Bcr-Abl酪氨酸激酶选择性抑制剂,能够与Abl激酶上的 ATP结合位点相互作用,从而阻止下游蛋白的磷酸化,用于 治疗慢性粒细胞白血病〔CML,单药有效率98%.
主要分子靶向药物的分类
1. 小分子表皮生长因子受体〔EGFR酪氨酸激酶抑制剂:吉非替尼 〔Gefitinib、埃罗替尼〔Erlotinib等.
2. 抗EGFR的单抗:西妥昔单抗〔Cetuximab、帕尼单抗〔Panitumumab、 Matuzumab<EMD 72000>.
3. 抗Her-2的单抗:曲妥珠单抗〔Trastuzumab. 4. Bcr-Abl酪氨酸激酶抑制剂:伊马替尼〔Imatinib、尼洛替尼〔Nilotinib、
⒍ 抗CD20的单抗:
利妥昔单抗Rituximab>商品名:美罗华〔Mabthera 生产商:瑞士豪夫迈·罗氏〔F.Hoffmann-La Roche
1997年11月26日上市,是第1个应用于临床肿瘤的靶向治疗药物.
由小鼠可变区和人恒定区结合的单抗.与CD20抗原特异性结合,诱导 抗体依赖性细胞介导的细胞毒作用〔ADCC和补体介导的溶细胞作用杀伤 靶细胞,从而抑制B细胞增殖,诱导B细胞凋亡,提高肿瘤细胞对化疗的敏 感性.
1、表皮生长因子受体〔EGFR 小分子酪氨酸激酶抑制剂
吉非替尼〔Gefitinib,ZD 1839 商品名:易瑞沙〔Irressa 生产商:英国阿斯利康〔AstraZeneca
靶向药物的分类
靶向药物的分类小分子药物靶向药物小分子药物通常是信号传导抑制剂,它能够特异性地阻断肿瘤生长、增殖过程中所必需的信号传导通路,从而达到治疗的目的。
例如诺华制药生产的用于治疗慢性粒细胞白血病和肠胃基质瘤的格列卫Gleevec,通用名Imitinib、以EGFR表皮生长因子受体为靶点的用于治疗非小细胞肺癌NSCLC的阿斯利康生产的易瑞沙Iressa,通用名Gefitinib和德国默克的特罗凯tarceva,通用名Erlotinib均属此类,并已进入临床应用。
美国千年制药公司生产的Velcade通用名bortezomib是细胞凋亡诱导剂,也属于小分子药物。
单克隆抗体例如用于治疗HER2基因阳性过量表达的乳腺癌的赫塞汀Herceptin,通用名Trastuzumab、以EGFR为靶点的结肠癌和非小细胞肺癌治疗药物爱必妥Erbitux,通用名Cetuximab等。
这类药物是通过抗原抗体的特异性结合来识别肿瘤细胞的。
从通用名的后缀上来看,单克隆抗体类靶向药物以“-mib”为后缀,而酪氨酸激酶类靶向药物以“-nib”为后缀。
除上述列举的已经进入临床使用的靶向药物外,另外还有多种靶向药物正在开发中。
靶向药物的使用靶向药物一般单独使用或和化疗药物配合使用。
对于已经经过充分临床验证的靶向药物,在临床上可用作一线、二线、三线治疗,而对于新的靶向药物,尽管已有资料表明其有效性,但还未经过充分的临床验证,一般用于二线、三线治疗即常规化疗无效后的治疗。
靶向药物的使用,应该在医生的指导下科学用药。
当临床上已经显示靶向药物已经没有明显效果时例如连续用药一年后,说明癌细胞已经产生了耐药性,这时应停止使用靶向药物或更换治疗方案。
靶向药物的价格仍高于常规化疗药物,这在一定程度上限制了靶向药物的推广。
但相信随着科技的进步,其价格会降低,种类会增加,靶向药物将会成为一类能够带来更好疗效、更少痛苦的癌症治疗药物。
靶向药物的机理根据靶向机理的不同,药物靶向可分为被动靶向、主动靶向、物理靶向等几类:1、被动靶向被动靶向制剂是指利用特定组织、器官的生理结构特点,使药物在体内能够产生自然的分布差异,从而实现靶向效应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
肿瘤小分子靶向药物分类
肿瘤小分子靶向药物分类
如今肿瘤的治疗手段多元化,其中靶向治疗为较新兴的治疗方式,由于毒副作用较小,疗效较突出,使得靶向治疗的成本也相对高昂。
分子靶向药物是在分子生物学、分子遗传学理论基础上出现的新药, 因其精确的靶向治疗作用,相对于传统化疗药物有很多优势, 形成了一门治疗肿瘤的新领域,为肿瘤的治疗提供了一种不良反应较小的方法。
近20 年来,随着医学科学的发展,大量以肿瘤细胞水平表达为靶点的新的抗肿瘤药物不断问世,并逐渐走向临床, 主要包括细胞信号转导分子抑制剂、新生血管抑制剂、靶向端粒酶抑制剂以及针对肿瘤耐药的逆转剂。
攻击肿瘤的靶点有多方面, 目前研究较成熟的主要有肿瘤细胞表面的靶点(抗原或抗体), 如细胞膜分化相关抗原(CD13,CD20,CD22,CD33,CD52,CD117 等),细胞信号转导分子如表皮生长因子(EGF及其受体(EGFR和血管内皮生长因子(VEGF及其受体上的酪氨酸激酶,以及法尼基转移酶,基质金属蛋白酶等。
分子靶向药物目前尚无统一的分类方法。
根据作用靶点不同,可分为以下
4 类。
•蛋白激酶细胞的分化信号传导因子中, 含有大量的蛋白激酶家族。
在细胞信号传导过程中, 蛋白酪氨酸激酶十分重要, 它可催化ATP 上的磷酸基转移到许多重要蛋白质酪氨酸残基上使其磷酸化, 导致传导支路的活化, 影响细胞生长、增殖和分化,
而许多肿瘤细胞中酪氨酸激酶活性异常升高。
超过50% 的癌基因及其产物具有蛋白酪氨酸激酶活性, 它们的异常表达将导致肿瘤的发生。
此外, 该酶的异常表达还与肿瘤转移、肿瘤新生血管生成、肿瘤对化疗耐药有关。
研究能阻断或修饰由信号传导失常引起疾病的选择性蛋白激酶抑制剂, 被认为是有希望的药物开发途径。
目前, 已经发现了一些蛋白激酶抑制剂和针对不同蛋白激酶ATP结合位点的小分子治疗剂,并已
进入临床研究,如酪氨酸激酶抑制剂吉非替尼、厄洛替尼等及法尼基转移酶抑制剂安卓健等。
•肿瘤血管生成因子正负调控子的平衡控制着肿瘤血管的生成,由此促进肿瘤的生长和转移,开发血管生成抑制剂是肿瘤研究最为活跃的领域之一。
临床试验中的血管生成抑制剂有以下4 类。
①调节基质反应,抑制基底膜降解的药物:Marimastat、BMS-275291等。
基质蛋白酶(MMP )是一种蛋白水解酶,可使细胞外基质降解,它在肿瘤浸润、转移和血管形成过程中发挥关键作用。
基质蛋白酶抑制剂(MMPI)可以通过抑制金属蛋白酶起到抗肿瘤生长与转移的作用。
BMS-275291 是一种MMPI, 它与化疗联合用于晚期非小细胞肺癌的治
疗,目前已进入U /川期临床试验;Col-3是MMP-2 和MMP-9 抑制剂(I / U 期临床);AE941 是MMP-2、MMP-9 和MMP-12 抑制剂,它可以封闭VEGF和它受体的结合汕期临床试验治疗多发性骨髓瘤,川期临床试验用于肾癌和非小细胞肺癌的治疗。
②直接抑制内皮细胞的药物:沙立度胺(Thalidomide)、烟曲霉素衍生物
(TNP470)恩度(Endostatin)等。
TNP 470 是第一个进入临床试验的抑血管药物, 它对内皮细胞增殖和新生血管形成都具有强烈抑制作用,它与吉西他滨或顺铂联合使用,川期临床用于宫颈癌、胃癌、前列腺癌、乳腺癌和肺癌等实体瘤治疗显示出了明显的抗肿瘤活性。
内源性血管生成抑制因子:血管抑素(an giostati n)和内皮抑素(en dostat in) 都对老鼠肿瘤新生血管生成有强烈抑制作用, 且没有发现耐药现象, 联合使用这两种抑制因子可以彻底根除小鼠体内的移植瘤,但临床有待进一步验证。
目前两药均已在美国进行临床试验。
③抑制内皮细胞特异性整合素的药物:Vitaxin/ a V B 3人源化单克隆抗体、
EMD121974/ a V B 3小分子拮抗剂。
肿瘤细胞的粘附性在肿瘤侵袭和转移中起着极为重要的作用。
粘附分子如整合素可以促进肿瘤转移, 另外它还可启动某些细胞逃逸机制抑制细胞凋亡。
因此抑制了粘附分子/整合素的信号传导就可起到抗肿瘤作用。
Vitaxin 是一种抗a V B 3 的单克隆抗体,I / U期临床试验用于治疗晚期直肠癌;EMD121974是一个抗a V B 3的小分子,进入了川期临床试验,也有很好的疗效。
④抑制血管生长因子活化的药物:VEGF单克隆抗体等。
近几年抗肿瘤血管药研究进展非常迅速, 全世界大约有75 种抗血管药物
进入了临床试验阶段,大多数处于I期或U期临床试验阶段,但至少有12种已进入或已完成了川期临床试验。
已发现特异性调控表皮特异受体酪氨酸激酶的配体蛋白是一类前血管生
成因子,如VEGF/ VEGF系统,被认为是肿瘤药物很好的作用靶点。
VEGFs是一类蛋白,为高度特异的血管内皮细胞有丝分裂原,通过与受体结合激
活后发挥作用。
VEGF可促进内皮细胞的有丝分裂、延长细胞的存活期,提高基质降解过程中所需酶的表达,增加血管的通透性等。
VEGF对体积超过2mm 的实体瘤的快速生长发挥作用。
VEGFR是一类重要的酪氨酸激酶,许多研究表明,其信号转导途径失调在肿瘤的发生、生长和转移中有重要作用。
VEGFR主要有VEGFR-1( Flt-1)、VEGFR-2( KDR /Flt-1)和VEGFR-3( Flt-4),均属酪氨酸激酶受体。
VEGF通过与两种跨内皮细胞膜受体结合发挥生物学功能。
•DNA 拓扑异构酶
真核细胞的DNA拓扑异构酶在DNA的复制、转录、重组以及在形成正确的染色体结
构、染色体分离、浓缩中发挥重要作用。
拓扑异
构酶抑制剂已经成为抗肿瘤药物研究开发最重要的靶点之一。
•其他
DNA复制是肿瘤细胞增殖的关键。
抑制DNA引物酶,使引物的合成受阻,
DNA 复制受到抑制,肿瘤细胞不能增殖,从而达到抗肿瘤的目的。
因此,
DNA引物酶是抗肿瘤药物研究的一个理想靶点。
细胞周期调控、凋亡、分化等大量的生物过程都依赖于不同蛋白的调控表达和降解, 其中许多反应物下调作用是通过泛素依赖性水解毁坏完成的。
已发现在整个泛素化过程中的许多水平可被调控, 寻找靶向该途径中不同因子的药物有很好的前景。
在肿瘤
治疗中, 泛素-蛋白酶途径抑制剂可作为一种新型的抗肿瘤药物。
组蛋白的乙酰化是基因表达的主要调节因子, 它通过改变转录因子与
DNA的接近性以激活基因表达。
组蛋白去乙酰化酶(histo ne deacetylase, HDA基因表达的抑制作用为肿瘤治疗提供了新的靶标。
HDA抑制剂能引起
细胞周期阻断和凋亡基因的激活, 该作用可用于肿瘤的治疗。
