湖南大学_有机化学及实验-第十一章教学课件
高考化学一轮复习第十一章有机化学基础第一讲认识有机化合物课件

1.含有羟基的物质只有醇或酚。( ) 2.官能团相同的物质一定是同一类物质。( ) 3.含有醛基的有机物一定属于醛类。( )
4. 、—COOH的名称分别为苯、酸基。( ) 5.醛基的结构简式为“—COH”。( ) 6.含有苯环的有机物属于芳香烃。( ) 7.同分异构体可以是同一类物质,也可以是不同类 物质。( )
1.有机物的分类
(1)根据元素组成分类。
有机化合物烃烃:的烷衍烃生、物烯:烃卤、代炔烃烃、、醇苯、及酚其、同醛系、物羧等酸、酯等 (2)根据碳骨架分类。
链状化合物(如CH3CH2CH3)
有机物环状化合物脂环化合物 如
芳香化合物如
(链脂状肪烃烃)炔烷 烯烃烃 烃(( (如如 如CCCHHH≡42) ==C=HC)H2)
(2)有机化合物结构的表示方法。
结构式
结构简式 键线式
CH3CH===CH2
CH3CH2OH
(3)有机物的同分异构现象。
同分异构 化合物具有相同的分子式,但结构不 现象 同,因而产生性质上的差异的现象
同分异 具有同分异构现象的化合物互为同分异 构体 构体 碳链骨架不同,如
类 碳链 CH3—CH2—CH2—CH3和 型 异构
有机物 类别
官能团 名称
官能团 结构
典型代表物 (结构简式)
烯烃 炔烃
碳碳双键 碳碳三键
CH2===CH2 —C≡C— CH≡CH
续上表
卤代烃 卤素原子 醇 醇羟基 酚 酚羟基
—X —OH —OH
CH3CH2Cl CH3CH2OH
醚
醚键
CH3CH2OCH2CH3
醛
醛基
CH3CHO、HCHO
续上表
8.丙烷的一氯代物和正丁烷的一氯代物数目相 同。( )
高三化学总复习课件第十一章有机化学基础(选修5)11-36

【解析】 芥子醇分子中含有三种含氧官能团,分别为醚 键、酚羟基和醇羟基,A错误;苯和乙烯都是平面结构,通 过单键的旋转,可以使所有碳原子处于同一平面上,B错误 ;由于酚类与溴水的取代反应通常发生在酚羟基的邻、对位 上,但芥子醇分子中这些位置均被其他基团占据,故只有碳 碳双键能与溴水发生反应,C错误;芥子醇分子结构中含有 碳碳双键、醇羟基、酚羟基,故能发生加成、取代和氧化反 应,D正确。
【解析】 与—OH相连的C原子的邻位C原子上有H原子,能 发生消去反应,故A错误;二甘醇中含有—CH2—OH结构,被 氧化生成醛,故B错误;分子中含有羟基,可与钠反应生成氢 气,故C正确;含—OH,能发生取代反应,故D错误。
【答案】 C
5.(2018·四川成都期末)己烯雌酚是一种激素类药物,结 构如图,下列有关叙述中不正确的是( )
【解析】 苯酚的酸性太弱,不能使酸碱指示剂变色,故A 错误;溴、三溴苯酚均易溶于苯,不能除杂,故B错误;苯 酚钠不溶于苯,易溶于水,可加入NaOH溶液,通过分液的 方法除去苯中少量苯酚,故C正确;浓溴水与苯酚反应生成 白色沉淀,可用于苯酚检验,而不能用稀溴水检验溶液中的 苯酚,故D错误。
【答案】 C
(1) 其 中 属 于 脂 肪 醇 的 有 ________ , 属 于 芳 香 醇 的 有 ________,属于酚类的有________。
(2)其中物质的水溶液显酸性的有________。 (3)其中互为同分异构体的有________。 (4)列举出⑤所能发生反应的类型________(任写三种)。 【答案】 (1)①② ③⑤ ④⑤ (2)④⑤ (3)③④ (4)取代(酯化)、氧化、消去、加成反应
【答案】 A
考点2 醛基的检验 4.(2018·茂名模拟)糖尿病是由于人体内胰岛素分泌紊乱 而导致的代谢紊乱综合征,以高血糖为主要标志。长期摄入 高热量的食品和缺乏运动都易导致糖尿病。血糖是指血液中 的葡萄糖(C6H12O6)。下列有关说法中不正确的是( )
高考化学一轮复习第11章有机化学基础第35讲认识有机化合物课件新人教版

第35讲 认识有机化合物
1. 能根据有机化合物的元素含量、相对分子质量确定有机化合 物的分子式。 2. 了解常见有机化合物的结构;了解有机物分子中的官能团,能 正确表示它们的结构。 3.了解确定有机化合物结构的化学方法和某些物理方法(如质谱、 红外线光谱、核磁共振氢谱等)。 4. 了解有机化合物存在同分异构现象,能判断简单有机化合物的 同分异构体(不包括手性异构体)。 5. 能够正确命名简单的有机化合物。
返回
题号 1 2 3 4
解析: (1)有机物中碳的质量分数是 64.86%,氢的质量分数是 13.51%, 则氧的质量分数为 1-64.86%-13.51% =21.63%,n(C)∶n(H)∶n(O) =(64.86%÷12)∶(13.51%÷1)∶(21.63%÷16)=4∶10∶1,所以该有机 物的实验式为 C4H10O。 (2)该有机物的相对分子质量为 37×2=74,则其相对分子质量为 74。 该有机物的实验式的相对分子质量也为 74,则实验式即为分子式。 答案: (1)C4H10O (2)74 C4H10O
答案: CH4 C2H6 C3H8 CH4O C2H6O C3H8O 等。
返回
题号 1
23
3.如何确定分子式 C4H6O2 的不饱和度?若其中含有一个 ,试推测分子中还可能含有什么官能团?
返回
题号 1 2 3 4
题组一 分子结构与波谱分析 1.下列化合物在核磁共振氢谱中能出现两组峰,且其峰面积之比为
—CH3、
,其中—CH3、—OH、
的不饱和度为 0,
—COOH 的不饱和度为 1,则侧链的总不饱和度为 1。
所以,侧链的三个参数:不饱和度为 1、碳原子数为 5、氧原子数为 3。
有机化学实验课件ppt

将待分离的物质加到装有固定相的色谱柱顶端,通过洗脱剂的洗脱作用使各组分 在柱内分离的色谱方法。
CHAPTER 03
有机化学实验实践操作
烷烃的性质与合成
烷烃的物理性质
烷烃的熔点、沸点、溶解 度等。
烷烃的化学性质
烷烃的稳定性、氧化反应 、卤化反应等。
烷烃的合成
烷烃可以通过烃类的热裂 解、催化裂解等方法合成 。
结晶与重结晶
结晶
通过冷却或蒸发使溶液达到饱和状态,析出固体晶体的过程 。
重结晶
将晶体溶解在溶剂中,通过加热蒸发溶剂或加入其他溶剂使 溶液再次达到饱和状态,再析出晶体的过程。
薄层色谱与柱色谱
薄层色谱
将固定相涂布在玻璃板或塑料板上,形成薄层,然后将待分离的物质点在薄层的 一端,通过展开剂的移动使各组分在薄层上分离的色谱方法。
烯烃的性质与合成
1 2
烯烃的物理性质
烯烃的熔点、沸点、溶解度等。
烯烃的化学性质
烯烃的双键加成反应、氧化反应、聚合反应等。
3
烯烃的合成
烯烃可以通过烃类的热裂解、催化裂解等方法合 成。
芳香烃的性质与合成
芳香烃的物理性质
芳香烃的熔点、沸点、溶解度等。
芳香烃的化学性质
芳香烃的取代反应、加成反应等。
芳香烃的合成
实验操作规范
遵循正确的操作顺序和规 范,确保实验结果的准确实验台,并 按照规定处理废弃物。
有机化学实验常用仪器
蒸馏装置
用于分离和提纯有机化 合物,包括蒸馏烧瓶、
冷凝器、接收器等。
分液漏斗
用于分离两种不混溶的 液体,如水和有机溶剂
。
滴定管
用于测量溶液的浓度和 体积。
数据整理
湖南大学有机化学-课后例题习题-第十一章
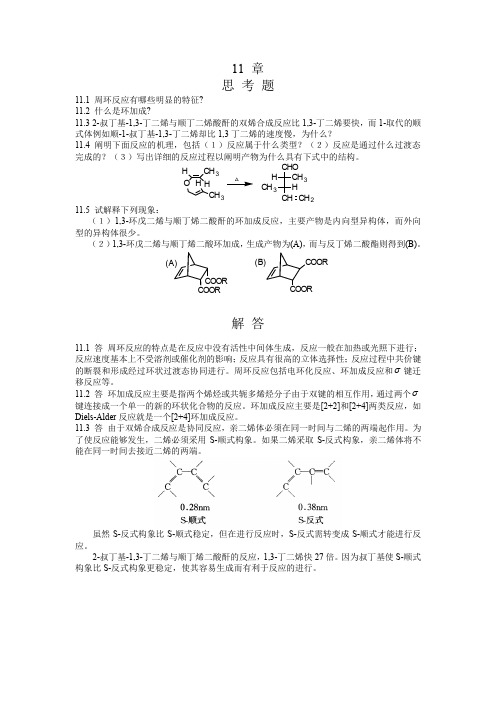
11 章 思 考 题11.1 周环反应有哪些明显的特征? 11.2 什么是环加成?11.3 2-叔丁基-1,3-丁二烯与顺丁二烯酸酐的双烯合成反应比1,3-丁二烯要快,而1-取代的顺式体例如顺-1-叔丁基-1,3-丁二烯却比1,3丁二烯的速度慢,为什么?11.4 阐明下面反应的机理,包括(1)反应属于什么类型?(2)反应是通过什么过渡态完成的?(3)写出详细的反应过程以阐明产物为什么具有下式中的结构。
H O HCH 3CH 3HH CHO CH 3CH CH 3HCH 2 △11.5 试解释下列现象:(1)1,3-环戊二烯与顺丁烯二酸酐的环加成反应,主要产物是内向型异构体,而外向型的异构体很少。
(2)1,3-环戊二烯与顺丁烯二酸环加成,生成产物为(A),而与反丁烯二酸酯则得到(B)。
解 答11.1 答 周环反应的特点是在反应中没有活性中间体生成,反应一般在加热或光照下进行;反应速度基本上不受溶剂或催化剂的影响;反应具有很高的立体选择性;反应过程中共价键的断裂和形成经过环状过渡态协同进行。
周环反应包括电环化反应、环加成反应和σ键迁移反应等。
11.2 答 环加成反应主要是指两个烯烃或共轭多烯烃分子由于双键的相互作用,通过两个σ键连接成一个单一的新的环状化合物的反应。
环加成反应主要是[2+2]和[2+4]两类反应,如Diels-Alder 反应就是一个[2+4]环加成反应。
11.3 答 由于双烯合成反应是协同反应,亲二烯体必须在同一时间与二烯的两端起作用。
为了使反应能够发生,二烯必须采用S-顺式构象。
如果二烯采取S-反式构象,亲二烯体将不能在同一时间去接近二烯的两端。
虽然S-反式构象比S-顺式稳定,但在进行反应时,S-反式需转变成S-顺式才能进行反应。
2-叔丁基-1,3-丁二烯与顺丁烯二酸酐的反应,1,3-丁二烯快27倍。
因为叔丁基使S-顺式构象比S-反式构象更稳定,使其容易生成而有利于反应的进行。
有机化学ppt课件完整版

有机化学ppt课件完整版目录•绪论•有机化合物的结构与性质•烃类化合物•烃的衍生物•有机合成与反应机理•生物活性有机化合物绪论碳氢化合物研究碳氢化合物(烃)的结构、性质、合成和反应机理。
碳氢化合物的衍生物研究烃的衍生物,如醇、醛、酮、羧酸、酯等有机化合物的结构、性质、合成和反应机理。
生命体系中的有机化合物研究生物体内的氨基酸、蛋白质、核酸、多糖等生命物质的结构、性质和功能。
经典时期19世纪初到20世纪初,以经验规律为指导,通过大量的实验总结出了许多有机化学的基本概念和原理。
萌芽时期从远古时期到18世纪,人们开始使用天然有机物,如木材、植物、动物等。
现代时期20世纪至今,以量子力学和统计力学为基础,发展出了现代有机化学的理论和方法,如分子轨道理论、价键理论、反应机理理论等。
环境领域有机化学在环境保护方面发挥着重要作用,如研究大气污染物、水体污染物的来源和治理方法等。
同时,有机化学也致力于开发环保材料和清洁能源。
材料领域合成纤维、塑料、橡胶等高分子材料广泛应用于服装、家居用品、交通工具等领域。
医药领域合成药物如抗生素、抗癌药物等对于治疗疾病具有重要意义。
同时,天然药物中提取的有效成分也是有机化学的研究对象。
农业领域合成农药和化肥对于提高农作物产量具有重要作用。
此外,生物农药和生物肥料的研发也需要有机化学的支持。
有机化学与生产生活的关系有机化合物的结构与性质碳原子通过四个共价键与其他原子或基团相连,形成复杂的有机分子结构。
碳原子的四价性键的极性空间构型碳原子与其他原子形成的共价键具有不同的极性,影响有机物的物理和化学性质。
有机化合物分子中的原子或基团在空间的排列方式不同,导致同分异构现象的产生。
030201有机化合物的结构特点03同分异构体的性质差异由于结构上的差异,同分异构体在物理性质、化学性质以及生物活性等方面表现出明显的不同。
01构造异构分子式相同但连接方式不同,如正丁烷和异丁烷。
02立体异构分子式相同、连接方式也相同,但空间构型不同,如顺反异构、对映异构等。
大学科目《有机化学》各章节课件

3
芳香烃的性质
具有较高的熔点和沸点,难溶于水,易溶于有机 溶剂;具有共轭体系和电子离域效应,容易发生 亲电取代反应。
芳香烃的命名与分类
芳香烃的命名
01
以苯环为母体,根据取代基的不同进行命名,如甲苯、二甲苯
医药化学
研发新药、合成药物中间体等, 用于治疗疾病和保障人类健康。
农业化学
合成农药、肥料等,提高农作物 产量和品质,保障粮食安全。
环境科学
研究有机污染物的来源、迁移转 化和治理方法,保护生态环境。
02 烷烃
烷烃的结构与性质
结构特点
化学性质
碳原子之间以单键相连,形成链状或 环状结构;每个碳原子上的剩余价键 均与氢原子相连。
卤代烃的反应与合成
反应类型
卤代烃的反应类型丰富多样,主要包括亲 核取代反应、消除反应、还原反应以及与 金属有机化合物的反应等。这些反应在有 机合成中具有重要的应用价值,可用于构 建碳碳键、引入或转化官能团等。
VS
合成方法
卤代烃的合成方法主要有两种:一种是通 过烃类的直接卤化反应得到相应的卤代烃; 另一种是通过烯烃或炔烃与卤化氢的加成 反应得到卤代烷。此外,还可利用醇与氢 卤酸的取代反应制备卤代烃。在实际合成 中,需根据目标产物的结构和性质选择合 适的合成路线和反应条件。
03 烯烃
烯烃的结构与性质
01
烯烃的通式与结构特点
烯烃是一类含有碳碳双键的烃类化合物,通式为CnH2n。其结构特点
包括碳碳双键的存在以及与之相连的四个原子共平面。
02 03
烯烃的物理性质
烯烃的物理性质与其分子量和双键位置有关。一般来说,随着分子量的 增加,烯烃的沸点、熔点和密度逐渐升高。双键位置对物理性质也有影 响,如顺式异构体的沸点通常高于反式异构体。
高考化学一轮复习 第11章 有机化学基础(选修)第1讲 认识有机化合物课件 新人教版

第一讲 认识有机化合物
[考纲要求] 1.了解常见有机化合物的结构,了解常见有机化合物中的官能团, 能正确表示简单有机化合物的结构。 2.了解有机化合物存在同分异构现象,能判断并正确书写简单有机 化合物的同分异构体的结构简式(不包括立体异构体)。 3.能根据有机化合物的命名规则命名简单的有机化合物。 4.能根据有机化合物的元素含量、相对分子质量确定有机化合物的 分子式。 5.了解测定有机化合物结构的化学方法和某些物理方法。
解析 只含有一个甲基的同分异构体有:CH3CH2CH2CHCl2、
、
答案 C
,4种同分异构体。
4.下列有关有机物同分异构体说法中不正确的是( ) A.分子式为C4H8的同分异构体共有(不考虑立体异构)5种 B.立方烷(C8H8)的六氯取代物有3种 C.分子式为C5H10O2的同分异构体中属于酯的有8种
考点一 有机化合物的分类
知识梳理
1.按组成元素分类 有机化合物可分为烃和烃的衍生物。 2.按碳的骨架分类
3.按官能团分类 (1)官能团:决定化合物特殊性质的原子或原子团。 (2)有机物的主要类别、官能团和典型代表物:
思考辨析
判断正误,正确的划“√”,错误的划“×” (1)官能团相同的物质一定是同一类物质( × ) (2)含有羟基的物质只有醇或酚( × ) (3)含有醛基的有机物一定属于醛类( × )
(4)
、—COOH的名称分别为笨、酸基( × )
(5)醛基的结构简式为“—COH”( × )
(6)含有苯环的有机物属于芳香烃( × )
(7)CO2、CO、NaHCO3中都含有碳元素,它们都属于有机物( × )
题组训练
1.(2015·厦门一模)有机化合物有不同的分类方法,下列说法正确 的是( )
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
十一章 生物有机化合物一 基本要求掌握:糖、氨基酸、蛋白质、核酸的基本结构与性质 熟悉:糖、氨基酸、蛋白质基本性质与生理功能的关系 了解:蛋白质、核酸的结构与性质及功能11.1 碳水化合物碳水化合物(即糖类),按其能否水解和水解的产物情况可分为以下三类:(1) (1) 单 糖:不能水解的多羟基醛或多羟基酮。
例如葡萄糖、果糖和核糖。
(2) (2) 低聚糖: 水解后能生成2~10个分子单糖的化合物。
其中最重要的是二糖,例如蔗糖、麦芽糖、纤维二糖等。
(3) (3) 多 糖:水解后生成10个以上单糖分子的化合物。
例如淀粉、纤维素等。
11.1.1 单 糖11.1.1.1 单糖的结构通过对单糖化学性质的研究得知单糖既有开链式结构,又有环状结构。
1、开链式结构化学事实得知葡萄糖的开链式结构为:CH 2OHCH CH OHOHCH OHCH OHCHO用类似的化学方法证明果糖的开链式结构为五羟基-2-己酮。
CH 2OH CH CH OH OH CH OH C O CH 2OH在书写单糖的开链式结构时,一般将碳链竖写,羰基位于上端,碳链的编号从靠近羰基的一端开始。
单糖的开链式结构常用Fischer 投影式或更简单的式子表示。
右旋葡萄糖的结构可用Fischer 投影式或更简单的式子表示如下:或H CHO *OH *H HO *OH H *OHHCH 2OH CHO *OH*HO*OH *OHCH 2OHCHO****CH 2OH 或2、 2、 构型和标记法在碳水化合物中存在立体异构体,为了确定其构型一般采用D 、L 相对标记法和R 、S 绝对标记法。
D-(+)-甘油醛D-(+)-葡萄糖D-(-)-果糖L-(-)-甘油醛L-(-)-葡萄糖L-(+)-阿拉伯糖3、环状结构D-葡萄糖的两种正位异构体分别为α-D-(+)-葡萄糖和β-D-(+)-葡萄糖。
在溶液中环状结构与开链结构之间存在动态平衡。
HCHOOHHO HH OHH OHCH2OH6α-D-(+)-葡萄糖β-D-(+)-葡萄糖-葡萄糖在溶液中有α-和β-两种半缩醛结构,所以D-葡萄糖与甲醇生成两种苷,它们是α-D-(+)-甲基葡萄糖苷和β-D-(+)-甲基葡萄糖苷。
33α-D-(+)-甲基葡萄糖苷β-D-(+)-甲基葡萄糖苷CH 2OHOO14α-D-(+)-葡萄糖β-D-(+)-葡萄糖糖的这种环状结构称为哈沃史(Howorth)式。
有时不需要指出糖的正位异构体,就把异头碳上羟基写在环平面上,且异头碳原子上的H 也可以省去:或单糖分子中的半缩醛环并不都是六员环,也有的是五员环。
例如D-(-)-果糖:β-D-(-)-呋喃果糖CH 2OH 2OH 2OHD-(-)-果糖4、 4、 构象糖的哈沃史式能清楚地表示出环上各原子和原子团之间相互关系,但吡喃环上的原子并不在同一平面内,而是类似于环己烷,具有椅式构象,例如β-D-葡萄糖的两种椅式构象为:β-D-甘露糖β-D-阿洛糖β-D-半乳糖D-果糖也有变旋光现象。
在水溶液中果糖主要为吡喃型环状结构(分为α-型和β-型)。
而果糖苷主要以呋喃型环状结构(分为α-型和β-型)形式存在。
X-射线分析表明,呋喃型糖中五员环在同一平面上;吡喃型糖中六员环主要为椅式构象。
10.1.1.2 10.1.1.2 单糖的反应单糖是多羟基醛酮,含有羰基和羟基,能发生这些官能团的特性反应,如还原反应、氧化反应、加成反应、成醚反应、成酯反应等。
单糖还含有相邻的醇羟基结构,故还能发生邻二醇的特性反应,如被高碘酸氧化。
1、还原反应单糖用还原剂或催化加氢将羰基还原为羟基生成糖醇(即多元醇)。
例如,D-葡萄糖还原生成D-葡萄糖醇(又叫D-山梨醇),L-古洛糖还原也生成D-山梨醇:H CHO OH HO H H OH HOH CH 2OH [H]H CH 2OH OH HO H H OH HOH CH 2OH H CH 2OH OH H H OH HOH CHO [H]HO CHO H HO H H OH HOH CH 2OH即:D-葡萄糖D-山梨醇L-古洛糖D-甘露糖还原为D-甘露醇,D-果糖的羰基在2位,故还原产生新的手性中心,生成非对映异构体D-甘露醇和D-山梨醇:HO CHO H HO H H OH HOH CH 2OH HO CH 2OHH HO H H OH HOH CH 2OH CH 2OH COHO H H OH HOH CH 2OH H CH 2OHOH HO H H OH HOH CH 2OH D-甘露糖D-山梨醇D-果糖[H][H][H]D-甘露醇2、 2、 氧化反应单糖被不同的氧化剂氧化生成氧化程度不同的产物。
醛糖或酮糖与弱氧化剂Tollens 试剂和Fehling 试剂均发生反应,与Tollens 试剂作用都产生银镜,与Fehling 试剂一起加热时生成氧化亚铜的砖红色沉淀。
Cu 2+醛糖或酮糖氧化产物Cu 2O +Tollens 试剂和Fehling 试剂都是碱性溶液。
醛糖含有醛基,能被弱氧化剂氧化;酮糖都是α-碳上有羟基的酮,在碱性溶液中,存在开链式醛糖与开链式酮糖通过烯二醇而进行互变异构的平衡。
例如:CHO CHOH HO H H OH HOH CH 2OH CHOH CH H OH HOH CH 2OH CH 2OH CHO H H OH HOH CH 2OH OH O 醛糖烯二醇酮糖因此,酮糖也能被弱氧化剂(Tollens 试剂和Fehling 试剂)氧化。
许多糖在生物体内的代谢都包括有烯醇化反应。
酮糖在同样氧化条件下不反应。
因此,可用溴水作为试剂区别醛糖和酮糖。
β-D-葡萄糖苷用臭氧氧化生成葡萄糖酸酯,α-异构体活性较低,不易被臭氧氧化。
硝酸是强氧化剂,能使醛糖氧化为糖二酸。
例如:HCHOOHHO HH OHH OHCH2OHHCOOHOHHO HH OHH OHCOOHHNO3D-葡萄糖D-葡萄糖二酸内酯D-葡萄糖二酸有旋光性。
将醛糖氧化为糖二酸,然后测其旋光性,这些性质可用于推测糖的构型。
糖二酸也容易生成γ-内酯和δ-内酯。
D-果糖用硝酸氧化时,发生碳链的断裂,生成D-阿拉伯糖二酸及其它小分子氧化产物。
CH2OHCHO HH OHH OHCH2OHOCO2HHO HH OHH OHCO2H+CO2HH OHH OHCO2H3+......生物体内由酶催化进行醛糖的氧化反应,醛基不受影响,而末端-CH2OH氧化为羧基,生成糖醛酸。
这是一个重要的生化反应。
生成的糖醛酸衍生物可由尿液从动物体内排出,起到排毒作用。
高碘酸氧化糖类时,邻二醇结构的碳链处及羰基与羰基α-碳链处均发生断裂得到醛及酸:2+2IO4HCHO2HCOOH+反应常是定量的,断裂一个碳-碳键消耗一摩尔IO4-,产生一摩尔IO3-。
用银盐溶液滴定反应生成的IO3-,可以知道反应中C-C键断裂的数目。
例如氧化D-葡萄糖时,消耗5摩尔高碘酸,生成5摩尔甲酸和1摩尔甲醛,表明葡萄糖中有5个C-C键,共6个碳原子,且这6个碳原子或为羰基碳,或与羟基相连。
CHOCHO HH OHH OHCH2OHOHH+5IO4HCHO5HCOOH+糖苷中也存在邻二醇结构,故也可被高碘酸氧化。
例如:D-甲基吡喃葡萄糖苷氧化时消耗2摩尔高碘酸,生成1摩尔甲酸和1摩尔二醛,从后者的结构可以得知糖苷分子中成环情况及三个相邻羟基的存在。
3+2IO4HCOOH+HCOOHOCH3HCH2OHH3、成脎反应H CHO *OH **HO H *H OH HOHCH 2OHD-(+)-葡萄糖652NNHC 6H 5**HO H *H OH HOHCH 2OHNNHC 6H 5HOCHO *H **HO H *H OH HOHCH 2OH652D-(+)-葡萄糖脎D-(+)-甘露糖26523-C 6H 5NH 2CH 2OH C R265H 2NNHC 6H 52CH C RNNHC 6H 5NNHC 6H 5NNHC 6H 5CHO C R NNHC 6H CH 2OH C RO4、醚化和酯化反应CHOHOHO HOHOH 2C OH32232CHOCH 3OCH 3O CH 3OCH 3OH 2COCH 3D-葡萄糖D-五甲基葡萄糖D-葡萄糖与乙酸酐发生酯化反应生成D-五乙酸葡萄糖酯(又叫D-五乙酰基葡萄糖)。
(CH 3CO)2O CHOOCCH 3OCH 2OOCCH 3CH 3COOCH 3COO CH 3COOCHOH OHO HOHOH 2C OH D-葡萄糖D-五乙酸葡萄酯糖糖的磷酸酯在生物体内有重要作用。
它们是许多代谢过程的中间体。
例如,在肝糖的生物合成和生物降解过程中,都含有α-D-1-磷酸葡萄糖酯和D-6-磷酸葡萄糖酯。
OHO HOHOH 2C OHOPO 3H 2CHOH OHO HOH 2COHOPO 3H 2α-D-1-磷酸葡萄糖酯D-6-磷酸葡萄糖酯核酸在生物体内起着极其重要的作用,β-D-核糖和β-D-2-脱氧核糖的磷酸酯是核酸的组成部分。
O HOH 2CHH OH H OHOHH O HOH 2CHH OH H HOHH β-D-核糖β-D -2 -脱氧核糖β-D-核糖和β-D-2-脱氧核糖为呋喃型环状结构,3-和5-位上的羟基与磷酸形成酯,同时1-位上的羟基与嘧啶或嘌呤缩合后形成核酸的基本单位──核苷酸(见11.3.1)。
5、 5、 差向异构化(epimerization)差向异构化作用就是在差向异构体之间进行的一种直接可逆的转化过程。
在碱性条件 下,醛糖通过烯醇式转化为差向异构体,同时发生醛糖与酮糖间的相互转化。
HCHO ROHCH C HOCHORH CH 2OH CROOH OH例如:在8×10-3mol·L -1氢氧化钠溶液中,35℃下D-葡萄糖反应4昼夜后生成D-果糖(28%),D-甘露糖(3%)和D-葡萄糖的混合物。
D-葡萄糖与D-甘露糖的差向异构化也可通过下列反应实现。
H CHO OH HO H H OH HOH CH 2OHH CO 2H OH HO H H OH HOH CH 2OHHO CO 2H H HO H H OH HOH CH 2OHHOCHOH HO H H OH HOH CH 2OHHOC H HO H HHOH CH 2OHOOBr 2吡啶分离Na/Hg2△ 1)2)醛糖还可以通过下列反应转化为酮糖。
2653OCHO CHOH RCH C R NNHC 6H 5NNHC 6H 5C CRO OHCH 2OH C R O醛糖邻酮醛糖糖脎酮糖6、 6、 醛糖的递升和递降CHO HO H H OH HOH CH OH HOCN H H HOH HOH CH 2OHHOCOOH H HO H H HOH CH 2OHHOCHO H HO H HOH HOH CH 2OHH CN OH H H OH HOH CH 2OHHCOOH OH HO H H OH HOH CH 2OHHCHO OH H HOH HOHCH 2OH PH=3~52PH=3~5Na-Hg,H 2O D-(+)-甘露糖D-(+)-葡萄糖醛糖递降一般有两种方法。
