浙江高考化学有机化学推断(经典题型)(含答案)
高考化学《有机合成推断》真题练习含答案
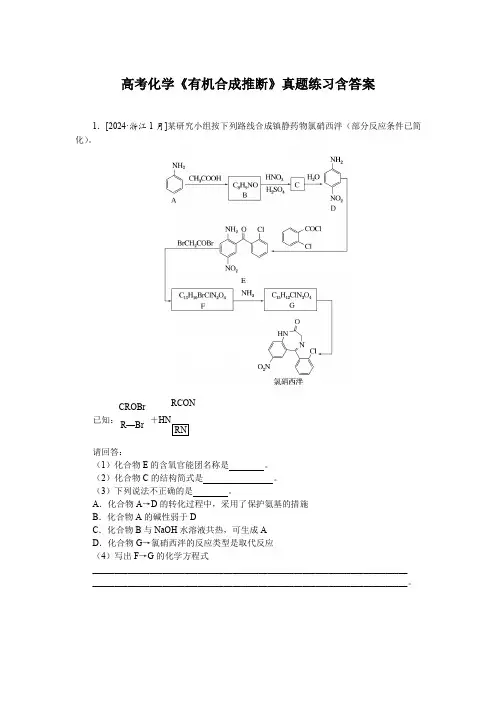
高考化学《有机合成推断》真题练习含答案1.[2024·浙江1月]某研究小组按下列路线合成镇静药物氯硝西泮(部分反应条件已简化)。
已知:CROBrR—Br +HNRCON RN 请回答:(1)化合物E 的含氧官能团名称是 。
(2)化合物C 的结构简式是 。
(3)下列说法不正确的是 。
A .化合物A →D 的转化过程中,采用了保护氨基的措施B .化合物A 的碱性弱于DC .化合物B 与NaOH 水溶液共热,可生成AD .化合物G →氯硝西泮的反应类型是取代反应(4)写出F →G的化学方程式________________________________________________________________________ ________________________________________________________________________。
(5)聚乳酸()是一种可降解高聚物,可通过化合物开环聚合得到。
设计以乙炔为原料合成X的路线(用流程图表示,无机试剂任选)。
(6)写出同时符合下列条件的化合物B的同分异构体的结构简式。
①是苯的二取代物;②1HNMR谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,无碳氧单键。
答案:(1)硝基、羰基(2)(3)BD(4)(5)(6)解析:A与乙酸发生取代反应生成B,则B的结构简式为;B发生硝化反应生成C,结合D的结构简式可知C为;E发生取代反应生成F,根据F和G的分子式以及氯硝西泮的结构简式,结合题给已知条件可知,F的结构简式为,G的结构简式为。
(3)A→B的过程中,氨基被转化为酰胺基,硝化反应后再水解出氨基,属于氨基的保护,A项正确;硝基为吸电子基团,使化合物中负电荷向硝基偏移,导致氨基中的N原子结合质子的能力减弱,所以碱性:A>D,B项错误;B的结构简式为,在氢氧化钠溶液、加热的条件下,酰胺基发生水解反应,可转化为化合物A,C项正确;G的结构简式为,G中氨基与酮羰基发生脱水缩合反应,生成了氯硝西泮,不属于取代反应,D项错误。
历年浙江高考化学真题(有机合成与推断)
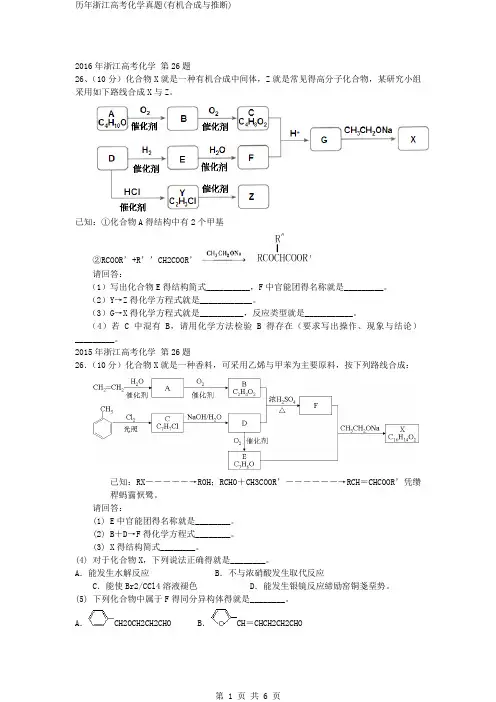
2016年浙江高考化学第26题26、(10分)化合物X就是一种有机合成中间体,Z就是常见得高分子化合物,某研究小组采用如下路线合成X与Z。
已知:①化合物A得结构中有2个甲基②RCOOR’+R’’CH2COOR’请回答:(1)写出化合物E得结构简式__________,F中官能团得名称就是_________。
(2)Y→Z得化学方程式就是____________。
(3)G→X得化学方程式就是__________,反应类型就是___________。
(4)若C中混有B,请用化学方法检验B得存在(要求写出操作、现象与结论)_________。
2015年浙江高考化学第26题26.(10分)化合物X就是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:已知:RX―――――→ROH;RCHO+CH3COOR’――――――→RCH=CHCOOR’凭缵稈蚂靄恹鹭。
请回答:(1) E中官能团得名称就是________。
(2) B+D→F得化学方程式________。
(3) X得结构简式________。
(4) 对于化合物X,下列说法正确得就是________。
A.能发生水解反应B.不与浓硝酸发生取代反应C.能使Br2/CCl4溶液褪色D.能发生银镜反应締励窑铜戔堊势。
(5) 下列化合物中属于F得同分异构体得就是________。
A.CH2OCH2CH2CHO B.CH=CHCH2CH2CHOC.CH2=CHCH=CHCH=CHCH=CHCOOHD.COOCH2CH2CH3氩頜镉攏軸懍剂。
2014年浙江高考化学第29题29.(15分)某兴趣小组以苯与乙烯为主要原料,采用以下路线合成药物普鲁卡因:已知:;。
请回答下列问题:(1)对于普鲁卡因,下列说法正确得就是________。
A.可与浓盐酸形成盐B.不与氢气发生加成反应C.可发生水解反应D.能形成内盐(2)写出化合物B得结构简式____________________。
2020年浙江省高考化学(选考)一轮复习有机推断基础能力过关(包含答案)
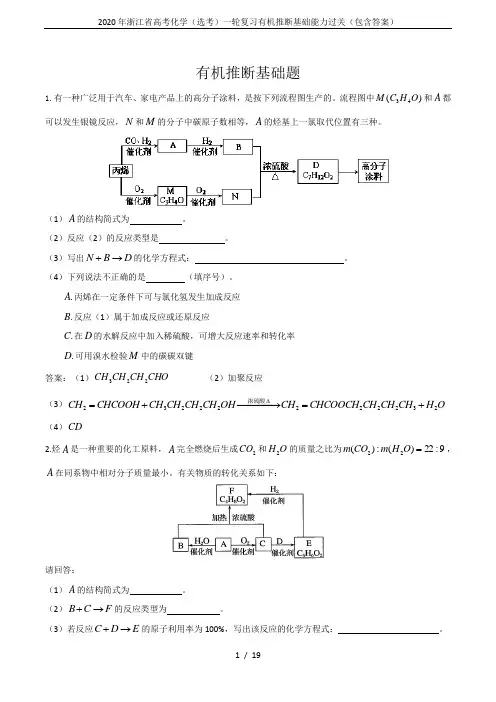
有机推断基础题 1.有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程图生产的。
流程图中)(43O H C M 和A 都可以发生银镜反应,N 和M 的分子中碳原子数相等,A 的烃基上一氯取代位置有三种。
(1)A 的结构简式为 。
(2)反应(2)的反应类型是 。
(3)写出D B N →+的化学方程式: 。
(4)下列说法不正确的是 (填序号)。
.A 丙烯在一定条件下可与氯化氢发生加成反应.B 反应(1)属于加成反应或还原反应.C 在D 的水解反应中加入稀硫酸,可增大反应速率和转化率.D 可用溴水检验M 中的碳碳双键答案:(1)CHO CH CH CH 223 (2)加聚反应(3)O H CH CH CH CHCOOCH CH OH CH CH CH CH CHCOOH CH 23222222232+=−−−→−+=∆浓硫酸(4)CD2.烃A 是一种重要的化工原料,A 完全燃烧后生成2CO 和O H 2的质量之比为9:22)(:)(22=O H m CO m ,A 在同系物中相对分子质量最小。
有关物质的转化关系如下:请回答:(1)A 的结构简式为 。
(2)F C B →+的反应类型为 。
(3)若反应E D C →+的原子利用率为100%,写出该反应的化学方程式: 。
(4)下列说法不正确的是 。
.A 有机物E 和F 互为同系物.B 绿豆大小的钠投入到B 中,钠块浮在液面上,熔化成小球,并四处游动.C 有机物E 能使溴的四氯化碳溶液褪色,其原因是发生加成反应.D 为制备干燥的F ,可在分离出F 后,选用碱石灰作干燥剂答案:(1)22CH CH = (2)酯化反应(或取代反应)(3)233CH COOCH CH CH CH COOH CH =→≡+ (4)ABD3.烃A 与等物质的量的O H 2反应生成B ,B 的一种同系物(比B 少一个碳原子)的溶液可以浸制动物标本。
M 是有芳香气味、不易溶于水的油状液体。
第27题有机推断-2023年7月浙江省普通高中学业水平考试化学分题(原卷版)
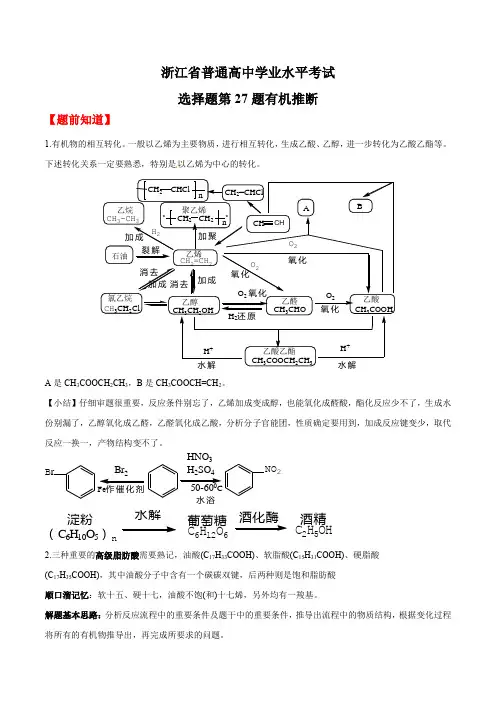
浙江省普通高中学业水平考试 选择题第27题有机推断【题前知道】1.有机物的相互转化。
一般以乙烯为主要物质,进行相互转化,生成乙酸、乙醇,进一步转化为乙酸乙酯等。
下述转化关系一定要熟悉,特别是以乙烯为中心的转化。
A 是CH 3COOCH 2CH 3,B 是CH 3COOCH=CH 2。
【小结】仔细审题很重要,反应条件别忘了,乙烯加成变成醇,也能氧化成醛酸,酯化反应少不了,生成水份别漏了,乙醇氧化成乙醛,乙醛氧化成乙酸,分析分子官能团,性质确定要用到,加成反应键变少,取代反应一换一,产物结构变不了。
2.三种重要的高级脂肪酸需要熟记,油酸(C 17H 33COOH)、软脂酸(C 15H 31COOH)、硬脂酸 (C 17H 35COOH),其中油酸分子中含有一个碳碳双键,后两种则是饱和脂肪酸 顺口溜记忆:软十五、硬十七,油酸不饱(和)十七烯,另外均有一羧基。
解题基本思路:分析反应流程中的重要条件及题干中的重要条件,推导出流程中的物质结构,根据变化过程将所有的有机物推导出,再完成所要求的问题。
NO 2B rHNO 3H SO 水浴Br 淀粉(C 6H 10O 5)n水解葡萄糖C 6H 12O 6酒精C 2H 5OH【真题回顾】1.(2022年7月浙江学考)土豆丝放入水中浸泡,水变浑浊并产生白色沉淀,其主要成分是有机物A,A 遇碘会变蓝。
以A为原料获得有机物E的转化关系如下图,已知E是有香味的无色油状液体。
请回答:(1)有机物A的名称是_______。
(2)有机物B的分子式是_______。
(3)有机物C与D反应生成E的化学方程式是_______。
(4)下列说法正确的是_______。
A. 仅用Na2CO3溶液无法鉴别有机物C、D和EB. 有机物A的分子式为C6H10O5C. 有机物B能发生银镜反应D. 工业上可以利用乙烯与水的加成反应制取有机物C2.(2021年7月浙江学考)烃A的相对分子质量为28,B是一种高分子化合物。
有机推断浙江高考真题含答案

CH 3CH -COOHOCH 2CH 2OCH 3C H 3 OCH-O —CHNO 2有机推断浙江高考真题1. (2009浙江高考)[14分]苄佐卡因是一种医用麻醉药品,学名对氨基苯甲酸乙酯,它以对硝基甲苯为主 要起始原料经下列反应制得:CH 3COO CH 2CH 3B r^~| Fe/H浓硫酸/ △ C 还原i (D )NO 2NH 2请回答下列问题:(1) 写出A 、B 、C 的结构简式:A ______________ ,B ______________ ,C _____________ 。
(2) 用1H 核磁共振谱可以证明化合物 C 中有 种氢处于不同的化学环境。
(3) 写出同时符合下列要求的化合物 C 的所有同分异构体的结构简式(E 、F 、G 除外)① 为1,4-二取代苯,其中苯环上的一个取代基是硝基;②分子中含有注:E 、F 、G 结构如下:化合物H 经聚合反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域。
请写出该聚合反应的化学方程式 _________________________________________________ 答案.[14分] COOH COO CH 2CH 3 (1) A :「i ; B : CH 3CH 2-OH ; C :| I NO 2NO 2(2) 4;OO 2N ?》CH 2O-CCH 3 OO 2N 彳 \ O-CCH 2CH 3 O O 2N Q 》CH 2C~OCH 3(E) 、 (F) 、(G) (4) E 、F 、G 中有一化合物经酸性水解,其中的一种产物能与O—C- O —结构的基团。
FeCl 3溶液发生显色反应,写出该水解反应的化学方程式 _____________(5)苄佐卡因(D)的水解反应如下: OH 2N 《C-OCH 2CH 3H 2O/OHH ++ C 2H 5OH(D)(3)NO 2NO 2NO 20 + 0(4) O 2N -「》-O —CCH 2CH 3 + 出0 — O 2N Y 〉0H + CH 3CH 2-C-OH ; 0催化剂0 I(5)n H 2NC-OHNH C 上 + n H 202 (2010浙江高考)(14分)•最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物在研究其性能的过程中,发现结构片段X 对化合物A 的性能重要作用。
浙江选考高考化学二轮复习专题训练高分子化合物有机合成推断

高分子化合物有机合成推断一、选择题1.〔2021·浙江桐乡高级中学〕由CH3CH3→CH3CH2Cl→CH2=CH2→CH3CH2OH转化过程中,经过反响类型是〔〕A.取代→加成→氧化B.加成→取代→消去C.取代→消去→加成D.取代→消去→水解解析CH3CH3可与氯气在光照下发生取代反响生成CH3CH2Cl;CH3CH2Cl在氢氧化钠醇溶液加热条件下发生消去生成CH2===CH2;CH2===CH2可与水发生加成反响生成CH3CH2OH。
答案C2.〔2021·金华艾青中学〕酸性强弱:羧酸>碳酸>酚,以下含溴化合物中溴原子,在适当条件下都能被羟基〔—OH〕取代〔均可称之为水解反响〕,所得产物能跟NaHCO3溶液反响是〔〕解析酸性强弱:羧酸>碳酸>酚,所以能与碳酸氢钠反响官能团只能是—COOH,A.该物质水解后生成醇—OH,生成物中没有—COOH,所以不能与碳酸氢钠反响,故A错误;B.该物质水解后生成—COOH,所以有羧基,能与碳酸氢钠反响,故B正确;C.该物质水解生成酚—OH,不能与碳酸氢钠反响,故C错误;D.该物质水解生成酚—OH,不能与碳酸氢钠反响,故D错误;答案B3.〔2021·浙江瑞安质检〕有机物X是一种广谱杀菌剂,作为香料、麻醉剂、食品添加剂,曾广泛应用于医药与工业。
该有机物具有以下性质:①与FeCl3溶液作用发生显色反响;②能发生加成反响;③能与溴水发生反响。
依据以上信息,一定可以得出结论是〔〕A.有机物X是一种芳香烃B.有机物X可能不含双键构造C.有机物X可以与碳酸氢钠溶液反响D.有机物X一定含有碳碳双键或碳碳叁键解析由信息①与FeCl3溶液作用发生显色反响;②能发生加成反响;③能与溴水发生反响可知,该物质一定含酚—OH与苯环,可能含双键或三键,A.该物质一定含O元素,不属于芳香烃,故A错误;B.由上述分析可知,X中可能不含双键构造,故B正确;C.酚—OH 不能与碳酸氢钠溶液反响,故C错误;D.X中可能含有碳碳双键或碳碳叁键,故D错误。
浙江省金华市新新高考化学经典推断题含解析
浙江省金华市新新高考化学经典推断题有答案含解析1.从薄荷油中得到一种烃A(C10H16),叫ɑ—非兰烃,与A相关反应如下:已知:(1)H的分子式为________________。
(2)B所含官能团的名称为_________________。
(3)含两个—COOCH3基团的C的同分异构体共有_________种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体结构简式为_______________________。
(4)B→D,D→E的反应类型分别为___________、_______________。
(5)G为含六元环的化合物,写出其结构简式:_____________________。
(6)F在一定条件下发生聚合反应可得到一种高级吸水性树脂,该树脂名称为______________。
(7)写出E→F的化学方程式:______________________________________________。
(8)A的结构简式为_____________,A与等物质的量的Br2进行加成反应的产物共有______种(不考虑立体异构)。
2.某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:已知:煅烧时,Cu2Te 发生的反应为Cu2Te+2O22CuO+TeO2。
(1)煅烧时,Cr2O3发生反应的化学方程式为______。
(2)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有_____(填化学式)。
(3)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:通过冷却结晶能析出大量K2Cr2O7的原因是_____。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50 g 配成250 mL 溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。
高考化学有机推断题,含答案
高考化(Hua)学有机推断题,含答案一、有机推(Tui)断题题型分析1、出(Chu)题的一般形式是推导有机物的结(Jie)构,写同分异构体、化学方程式、反应(Ying)类型及判断物质的性质。
2、经常围绕乙烯、苯及其同系物、乙醇等这些常见物质为中心的转化和性质来考察。
【经典习题】请观察下列化合物A —H 的转换反应的关系图(图中副产物均未写出),请填写:(1)写出反应类型:反应① ;反应⑦ 。
(2)写出结构简式:B ;H 。
(3)写出化学方程式:反应③ ;反应⑥ 。
解析:本题的突破口有这样几点:一是E 到G 连续两步氧化,根据直线型转化关系,E 为醇;二是反应条件的特征,A 能在强碱的水溶液和醇溶液中都发生反应,A 为卤代烃;再由A 到D 的一系列变化中碳的个数并未发生变化,所以A 应是含有苯环且侧链上含2个碳原子的卤代烃,再综合分析可得出结果。
二、有机推断题的解题思路解有机推断题,主要是确定官能团的种类和数目,从而得出是什么物质。
首先必须全面地掌握有机物的性质以及有机物间相互转化的网络,在熟练掌握基础知识的前提下,要把握以下三个推断的关键:1、审清题意 (分析题意、弄清题目的来龙去脉,掌握意图)2、用足信息 (准确获取信息,并迁移应用)3、积极思考 (判断合理,综合推断)①浓NaOH 醇溶液△BA CDEFGH (化学式为C H O )C 6H 5-C 2H 5②Br 2 CCl 4③浓NaOH 醇溶液△④足量H 2 催化剂⑤稀NaOH 溶液△⑥ O 2 Cu △⑦ O 2 催化剂⑧乙二醇 浓硫酸△根据以上的思维判断,从中抓住问题的突破(Po)口,即(Ji)抓住特征(Zheng)条件(特殊性质或(Huo)特征反应 。
但有机物的特征条件并非都有,因此(Ci)还应抓住题给的关系条件和类别条件。
关系条件能告诉有机物间的联系,类别条件可给出物质的范围和类别。
关系条件和类别条件不但为解题缩小了推断的物质范围,形成了解题的知识结构,而且几个关系条件和类别条件的组合就相当于特征条件。
浙江省台州市新新高考化学精选推断题汇总含解析
浙江省台州市新新高考化学精选推断题汇总有答案含解析1.Q、W、X、Y、Z 是位于不同主族的五种短周期元素,其原子序数依次增大。
①W 的氢化物与W 最高价氧化物对应水化物反应生成化合物甲。
②X、Y、Z 的最高价氧化物对应水化物之间两两反应均可生成盐和水。
③常温下,Q 的最高价气态氧化物与化合物X2O2发生反应生成盐乙。
请回答下列各题:(1)甲的水溶液呈酸性,用离子方程式表示其原因____________________________________________________________________________。
(2)③中反应的化学方程式为____________________________________________________________________________________________ ____。
(3)已知:ZO3n-+M2++H+→Z-+M4+ + H2O(M 为金属元素,方程式未配平)由上述信息可推测Z 在周期表中位置为____________________________________________________________________________________________ ____。
(4)Y 形成的难溶半导体材料CuYO2可溶于稀硝酸,同时生成NO。
写出此反应的离子方秳式_____________________________。
2.2一氧代环戊羧酸乙酯(K)是常见医药中间体,聚酯G是常见高分子材料,它们的合成路线如下图所示:已知:①气态链烃A在标准状况下的密度为1.875g·L-1;(1)B的名称为__________;E的结构简式为__________。
(2)下列有关K的说法正确的是__________。
A.易溶于水,难溶于CCl4B.分子中五元环上碳原子均处于同一平面C.能发生水解反应加成反应D.1molK完全燃烧消耗9.5molO2(3)⑥的反应类型为__________;⑦的化学方程式为__________(4)与F官能团的种类和数目完全相同的同分异构体有__________种(不含立体结构),其中核磁共振氢谱为4组峰,且峰面积之比为1:2:3:4的是__________(写结构简式)。
高考化学:有机推断题(含答案)
有机推断题1、(1)芳香醛(如糠醛)在碱作用下,可以发生如下反应:(2)不饱和碳碳键上连有羟基不稳定。
(3)化合物A~F之间的转化关系如下图所示。
其中,化合物A含有醛基,E与F是同分异构体,F能与金属钠反应放出氢气。
A生成F的过程中,A中醛基以外的基团没有任何变化。
据上述信息,回答下列问题:(1)写出A生成B和C的反应式:(2)写出C和D生成E的反应式:(3)F结构简式是:(4)A生成B和C的反应是(),C和D生成E的反应是()A、氧化反应B、加成反应C、消除反应D、酯化反应E、还原反应(5)F不可以发生的反应有()A、氧化反应B、加成反应C、消除反应D、酯化反应E、还原反应2、已知实验室常用无水醋酸钠粉末和碱石灰共热制取CH4气体,该反应发生的原理可简单表示如下:试从上述信息得出必要的启示回答下列小题:(1)实验室制取甲烷的装置还能制取哪些气体:。
(2)试写出固体与碱石灰共热所发生的主要化学反应方程式:(3)X、Y、Z、W分别是酸、碱、盐中的一种,A、B、C、D、E、F均为常见气体,A、B分子中含有相同数目的电子,b、e中均含有氧元素,各步反应生成的水均略去,反应条件未注明,试回答:①写出下列物质的化学式:X Y②写出物质B和b的电子式:B b③反应Ⅰ的化学方程式。
④反应Ⅱ的离子方程式。
⑤在上述各步反应中,有两种物质既做氧化剂又做还原剂,它们是:,。
3、(R、R`、R``是各种烃基)如上式烯烃的氧化反应,双键被高锰酸钾酸性溶液氧化而断裂,在断键两端的碳原子都被氧化成为羧基或酮羰基。
由氧化所得的产物,可以推测反应物烯烃的结构。
今有A、B、C三个含有双键的化合物,它们被上述溶液氧化:1molA (分子式C8H16),氧化得到2mol酮D 。
1molB(分子式C8H14),氧化得到2mol酮E和1mol二元羧酸。
1molC(分子式C8H14),氧化只得到一种产物,它是一种没有支链的二元羧酸。
请据此推断B、C、D、E 的结构简式。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2013年浙江高考化学——有机化学推断(经典题型)31.(本题共14分)5—氨基酮戊酸盐是一种抗肿瘤药,其合成路线如下:已知:(1)已知A 分子结构中有一个环,A 不能使溴水褪色,且核磁共振氢谱图上只有一个峰,则A 的结构简式为 。
(2)5—氨基酮戊酸盐中含氧官能团的名称是 ,C→D 的反应类型为 。
(3)G 是B 的一种同分异构体,能与NaHCO 3溶液反应,能发生银镜反应,1molG 与足量金属Na 反应能生成1molH 2,且G 分子中不含甲基,写出一种符合上述条件的G 的结构简式 。
(4)写出D→E 的反应方程式 。
(5)已知,请结合题中所给信息,写出由CH 3CH 2COOH 、为原料合成单体..的合成路线流程图(无机试剂任选)。
合成路线流程图示例如下:。
32.( 16 分)丙烯是重要的化工原料,以丙烯为原料合成有机玻璃和油墨材料DAP-A 树脂的流程如下:试回答下列问题:(1)写出下列物质可能的结构简式:B________________ ___,F____________ ____________。
KMnO 4浓H 2SO 4NaOH/H 2O∆HCl① Cl 2/光B C C 3H 5ClO 2∆Cu/D AF :C 8H 10 GH一定条件 ③(DAP-A 树脂) CH =CH-COOHEn462)CH 3OH有机玻璃H +②条件一定 nCOOCH 2-CH=CH 2COOCH 2CH-CH 2(2)写出反应类型:反应②_______________;反应③____________________________。
(3)1 mol DAP-A树脂在一定条件下与H2发生加成反应,最多消耗H2_______________mol。
(4)写出反应①的化学方程式:_______________ _________。
(5)写出G在一定条件下与乙二醇发生反应生成一种高分子化合物的化学方程式为__ ____。
(6)E的同分异构体中,属于酯类且没有顺反异构的链状有机物有(写结构简式):33.(15分)仔细体会下列有机合成过程中碳骨架的构建及官能团的引入和转化,完成下题:已知两个醛分子在NaOH溶液作用下可以发生加成反应,生成一种羟基醛:肉桂醛F(分子式为C9H8O)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:已知:反应⑤为羟醛缩合反应。
请回答:(1)肉桂醛F的结构简式为:。
E中含氧官能团的名称为。
(2)反应①~⑥中符合原子经济性的是。
(3)写出下列转化的化学方程式:②,③。
写出有关反应的类型:②⑥。
(4)符合下列要求的E物质的同分异构体有种(苯环上有两个取代基,其中有一个甲基在对位且属于酯类)。
34.(18分)已知:① CH3CH=CHCH2CH3CH3COOH+CH3CH2COOH② R-CH=CH2R-CH2-CH2-Br香豆素的核心结构是芳香内酯A,A经下列步骤转变为水杨酸。
请回答下列问题:(1)下列有关A、B、C的叙述中不正确的是a.C中核磁共振氢谱共有8种峰b.A、B、C均可发生加聚反应c.1mol A最多能和5mol氢气发生加成反应d.B能与浓溴水发生取代反应(2)B 分子中有2个含氧官能团,分别为 和 (填官能团名称),B→C的反应类型为 。
(3)在上述转化过程中,反应步骤B→C 的目的是 。
(4)化合物D 有多种同分异构体,其中一类同分异构体是苯的对二取代物,且水解后生成的产物之一能发生银镜反应。
请写出其中一种的结构简式: 。
(5)写出合成高分子化合物E 的化学反应方程式: 。
(6)写出以为原料制备的合成路线流程图(无机试剂任用),并注明反应条件。
合成路线流程图示例如下:CH 3CH 2OHC H 2CH 2C H 2CH 2Br Br Br 2浓硫酸35.(14分)化合物A(C 8H 8O 3)为无色液体,难溶于水,有特殊香味,从A 出发,可发生图示的一系列反应,图中的化合物A 苯环上取代时可生成两种一取代物,化合物D 能使FeCl 3溶液显紫色,G 能进行银镜反应。
E 和H 常温下为气体。
试回答:(1) 写出下列化合物的结构简式:A : ;B : ;G : (2)C 中的官能团名称为(3)反应类型:( I ) ;(Ⅱ) 。
(4) 写出D→H 的化学方程式: 。
36.(12分)化合物A(C 8H 8O 3)为无色液体,难溶于水,有特殊香味,从A 出发,可发生图示的一系列反应,图中的化合物A 苯环上取代时可生成两种一取代物,化合物D 能使FeCl 3溶液显紫色,G 能进行银镜反应。
E 和H 常温下为气体。
试回答:(1)写出下列化合物的结构简式:A : ;B : ;G : (2)反应类型:(I ) ;(Ⅱ) 。
(3) 写出D→H 的化学方程式: 。
(4) L 是D 的同分异构体,L 具备下列条件。
① L 能与使FeCl 3溶液显紫色 ② 能进行银镜反应A (C 8H 8ONaOH 水反应(Ⅰ)B+ C 氧E氧FHDHNaHCO 3G浓硫反应(Ⅱ)③其中一种水解产物的核磁共振氢谱表明有四组峰写出L与氢氧化钠溶液的化学方程式:。
37.(14分)某相对分子质量为26的烃A,是一种重要的有机化工原料,以A为原料在不同的反应条件下可以转化为烃B、烃C。
B、C的核磁共振谱显示都只有一种氢,B分子中碳碳键的键长有两种。
以C为原料通过下列方案可以制备具有光谱高效食品防腐作用的有机物M,M分子的球棍模型如图所示。
⑴B能使溴的四氯化碳溶液褪色,则B的结构简式为,B与等物质的量Br2作用时可能有种产物。
⑵C→D的反应类型为,M的分子式为。
⑶写出E→F的化学方程式。
⑷G中的含氧官能团的名称是,写出由G反应生成高分子的化学反应方程式:。
⑸M的同分异构体有多种,写出四种满足以下条件的同分异构体的结构简式:①能发生银镜反应②含有苯环且苯环上一氯取代物有两种③遇FeCl3溶液不显紫色④1mol该有机物与足量的钠反应生成1mol氢气(一个碳原子上同时连接两个-OH的结构不稳定)、、38.(14分)按以下步骤可从合成(部分试剂和反应条件已去).请回答下列问题:(1)B、F的结构简式为:B F。
(2)反应①~⑦中属于消去反应的是(填代号)。
(3)根据反应写出在同样条件下,Br发生加成反应的化学方程式:CH2=CH—CH=CH2与等物质的量2。
(4)写出第④步的化学方程式(有机物写结构简式,注明反应条件).。
(5)A—G这七种有机物分子中含有手性碳原子的是(填序号)。
(6)核磁共振谱是测定有机物分子结构最有用的工具之一。
在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。
例如:乙醛的结构式为:H CHHCOH,其PMR谱中有2个信号峰,其强度之比为3∶1。
则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1∶1∶2的是。
A.B.C.D.39.(10分)是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:(1)A与银氨溶液反应有银镜生成,则A的结构简式是。
(2)B→C的反应类型是。
(3)E的结构简式是。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:。
(5)下列关于G的说法正确的是。
a.能与溴单质反应b.能与金属钠反应c.1molG最多能和3mol氢气反应d.分子式是C9H6O340.(16分)聚合物NM、的合成路线如下:(1)在合成M 的反应路线中:①生成A 的反应类型是 。
②由B 生成OH CH CH CH CH HO ——2222的化学方程式是 。
③聚合物M 的结构简式是 。
(2)F 的结构简式是 。
(3)①D 的名称是 。
②写出生成E 的化学方程式 。
(4)在合成N 的反应路线中:①H 的分子式是107H C ,写出H G 的化学方程式 。
②下列说法正确的是 。
a. 乙烯与H 互为同系物b. H 的同分异构体中存在芳香烃c. N 分子中可能存在碳碳双键d. H→N 的反应原子利用率是100%41.(15分)用煤化工产品C 8H 10合成高分子材料I 的路线如下:R-CH=C-CHOR'已知:(1)B 、C 、D 都能发生银镜反应,且苯环上的一卤代物有两种。
H 含有三个六元环。
(2)RCHO +R'CH 2CHO −−−→−∆/NaOH 稀 + H 2O根据题意完成下列填空:(1)A 的名称是 ; D 中含有官能团的名称 。
(2)D→E 的反应类型是 ;(3)C 和H 的结构简式分别为 、 。
(4)E→F 的化学方程式是 。
(5)G→I 的化学方程式是 。
(6)符合下列条件的G 的同分异构体有 种,写出其中任意一种的结构简式 A 、能发生银镜反应和水解反应,且1mol 该同分异构体能消耗2mol 的NaOH B 、含有苯环,但不能与FeCl 3显色。
C 、不含甲基42.(15分)2011年5月24日,台湾地区有关方面向国家质检总局通报,发现台湾“昱伸香料有限公司”制售的食品添加剂“起云剂”,主要化学成分是含苯环的酯类物质,在台湾此化学物质被确认为第四类毒性化学物质,为非食用物质,不得用于食品生产加工。
现有含苯环的酯类物质A 、B ,两者互为同分异构体,B 的结构简式为;A 经①、②两步反应得C 、D 和E ,B 经①、②两步反应得E 、F 和H ,上述反应过程、产物性质及相互关系如图所示。
(1)B 可以发生的反应类型有(填序号) ①加成反应 ②酯化反应 ③消去反应 ④取代反应 ⑤聚合反应 B 的核磁共振氢谱中会出现_______个峰。
(2)F 与H 在浓硫酸作用下加热时发生反应的方程式为 (3)E 的结构简式为 ,其中含有的官能团的名称是 (4)A 有两种可能的结构,其对应的结构简式为 ,(5)B 、C 、D 、F 、G 化合物中互为同系物的是 。
I 的一种同分异构体满足:①能与碳酸氢钠反应产生二氧化碳气体,②1mol 该物质与足量金属钠反应产生1mol 氢气。
则该同分异构的名称为 。
43.(15分)乙基香草醛()是食品添加剂的增香原料。
(1)写出乙基香草醛分子中两种含氧官能团的名称 。
(2)与乙基香草醛互为同分异构体,能与NaHCO 3溶液反应放出气体,且苯环上只有一个侧链(不含R -O -R’及R -O -COOH 结构)的有 种。
(3)A 是上述同分异构体中的一种,可发生以下变化:H 2SO 4CrO 3COOHKMnO 4/H +①( C 9H 10O 3)A( C 9H 9O 2)Br②( C 9H 8O 3)能发生银镜反应BH+C已知:i. RCH 2OHCrO 3 /H 2SO 4RCHO ;ii. 与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性KMnO 4溶液氧化为羧基。
