芳烃的卤取代反应PPT课件
第六章 卤代芳烃

本文由恶魔之始贡献 ppt文档可能在WAP端浏览体验不佳。
建议您优先选择TXT,或下载源文件到本机查看。
第三节 定义: 定义: 卤代芳烃 芳烃分子中的一个或几个氢原子被卤原子取代后的化合物称为 卤代芳烃。
卤代芳烃。
分类: 分类: 1.侧链取代的卤代芳烃 1.侧链取代的卤代芳烃 Br 2.芳环上取代的卤代芳烃 2.芳环上取代的卤代芳烃 CH2Cl CH2CH2Cl 一、卤代芳烃的命名 二、卤代芳烃的制法 三、卤代芳烃的物理性质 四、卤代芳烃的化学性质 1.苯环位置对卤原子活泼性的影响 苯环位置对卤原子活泼性的影响 2.芳环上的亲核取代反应 2.芳环上的亲核取代反应 3.芳环上的亲核反应机理 3.芳环上的亲核反应机理 4.与金属作用 . 5. 芳环上的亲电取代反应 一、卤代芳烃的命名 1.卤原子直接与芳环相边连时,以芳烃为母体, 1.卤原子直接与芳环相边连时,以芳烃为母体,卤原子作为取代基 卤原子直接与芳环相边连时 CH3 C2H5 4-氯甲苯 (对氯甲苯) 对氯甲苯) Cl Br Cl 2-氯-4-溴乙苯 2.卤原子与侧链相连时,通常以脂肪烃为母体 卤原子与侧链相连时, 卤原子与侧链相连时 αβ CH=CHBr CHCH2CH2Cl CH3 β-溴代苯乙烯 3-苯基-1-氯丁烷 苯基- 二、卤代芳烃的制法 1.直接卤化法 1.直接卤化法 芳环的直接卤化与芳烃侧链的直接卤化的机理是不同 的。
芳环的直接卤化是通过亲电取代反应,而芳烃侧链 进行的。
的直接卤化是按自由基机理进行的。
由于芳烃侧链的α原子比较活泼,取代反应多发生 由于芳烃侧链的α原子比较活泼, 在α位。
CH3 Cl 2 hv CH2Cl Br2 CH2CH3 CHCH3 Br hv 一般Cl 的活性高于Br 而选择性要小于Br 一般Cl2的活性高于Br2,而选择性要小于Br2。
因此乙苯的溴化得到一种产物; 因此乙苯的溴化得到一种产物;而氯化得到的是 氯代的混合物。
卤代烃及亲核取代反应PPT课件

叔丁基溴SN1水解反应的反应进程势能曲线
第42页,共95页。
单分子亲核取代反应(SN1)特点
在亲核取代反应中,在决速步骤中发生共价键变化 的只有一种分子,把这种反应称为单分子反应历程
A.反应分二步进行
(SN1)
B.反应速度只与反应物浓度有关;
C.反应有碳正离子产生。
可以得到“构型保持”和“构型转化”两种产物(卤代烃中 卤素所连的碳为手性碳,经SN1反应后,得到的产物基本上 是外消旋化的)。有重排产物(SN1 反应的标志).
第35页,共95页。
8.5 饱和碳原子上的亲核取代反应机理
X + Nu-
Nu + X
CH3Br + OH―→ROH + Br―
底物的浓度
υ = κ [CH3Br][OH―]
(CH3)3CBr + OH― → (CH3)3COH + Br―
υ = κ [(CH3)3CBr] 反应的级数
碱的浓度
第36页,共95页。
(CH2O)n HCl
NaCN CH2Cl
CH2CN
CH2CN
H+ ,H2O
CH2COOH
第24页,共95页。
3.与醇钠作用 ( Nu=RO-)
RX + RONa
ROR' + NaX
Williamson醚合成法; RX——伯卤烷。
ONa
O
+
Br
第25页,共95页。
4.与氨作用 ( Nu=NH3)
过渡态
CH3
CH3
........OH
CH3
过渡 态
CH3
CH3
+ + Br
芳香烃ppt课件

+ HNO3
+ 2HNO3
浓硫酸 60℃
—NO2 + H2O
硝基苯
浓硫酸
100~110℃
间二硝基苯
NO +2H2O N2 O2
玻璃 管
实验步骤:①先将1.5mL浓硝酸注入 大试管中,再慢慢注入2mL浓硫酸,并 及时摇匀和冷却. ②向冷却后的酸中逐滴加入1mL苯, 充分振荡,混和均匀. ③将混合物控制在50-60℃的条件下 约10min,实验装置如左图.
CH3
C. CH3 CH2 CH CH3
D.
CH3
—CH2—CH3
练习2
CH3
COOH
KMnO4(H+)
COOH CH3
C| H3
CH3 |
CH3—CH2—
—C—CH3 | CH3
KMnO4/H+
HOOC |
HOOC—
CH3 | —C—CH3 | CH3
2、加成反应
+ H2
催化剂 △
3、取代反应
制鞋、皮革、箱包、家具、喷漆、油漆等工作
引起急性中毒或慢性中毒,诱发白血病
致癌物质
稠环 萘——过去卫生球的主要成分 芳烃 秸秆、树叶等不完全燃烧形成的烟雾中
香烟的烟雾中
()
B
A.C6H5Br和C6H6 B.C6H5NO2和H2O
C.C6H6和CCl4
D.C6H14和C6H6
第二单元 芳香烃
芳香烃的来源与应用
练习
1.下列有机物属于芳香族化合物的是__①_②__③__④_⑥______
2.下列有机物属于芳香烃的是___②__③__④__⑥____
①
—OH
芳烃的卤取代反应ppt课件

[45] (97%)
Cl
实际上是三氟甲磺酰次氯酸酐CF3SO2OCl 参与反应
学习交流PPT
18
缺电子芳核的卤取代实例2
B r B r2/H 2SO 4/SO 3
[48a]
130℃ , 7.5h N
(86% ) N
1.用发烟硫酸氧化生成的溴化氢成溴。 2.如果用AlCl3催化,氮原子与AlCl3络合,进一步降低了 芳核的电子云,使反应难易进行。
• 采用强的碘化剂(ICl,RCOOI,CF3COOI)来 增强碘正离子的浓度。
学习交流PPT
10
芳核的碘取代实例1 和2
C H 3O C H 3O
C H 2O H
C H 3O
I2/H g(O A c)2
CH 2Cl2/r.t.,3h C H 3O
O C H 3
C H 2O H[50]
(76% )
[53]
(97% ) I
oxidization
学习交流PPT
13
芳核上选择性卤取代的方法之一 ——改变溶剂和温度
HO 1mol Br2/CS2
OH
0~5℃
非极性溶剂
[42a] (80%~84% ) Br
缚酸剂
Br 2mol Br2/Tol t--BuNH2/-70℃
OH Br
[42b]
(87%)
倘若在碱性水溶液中卤化,得到的是2,4,6-三卤代苯酚
Cl OBz
(50%) (41%)
Cl
Cl
OBz
(40%) (74%) (37%)
硫酰氯,刺激性液体,学习高交流活PPT性的卤化剂,溶于乙醚
15
芳核上选择性卤取代的方法之三 ——NBS+DMF
《烃的卤代物》PPT课件

石Байду номын сангаас醚
C4H9X + 2 Li
C4H9Li + LiX
HX
R-CH-CH-CH-CH-R KOH- 醇 R-CH=CH-CH=CH-R + 2NaX + 2H2O
HXXH
Hβ
X + 2NaOH
乙醇
X
+ 2NaX + 2H2O
Hβ '
24
2021/4/26
青岛理工大学
24
有 机化学 2
1)消除反应的活性: 3°RX > 2°RX > 1°RX
马氏规则:烯烃和 酸(HX)加成时,X 加到含氢较少的双
3-氯-4-溴己烷
6
2021/4/26
青岛理工大学
6
有 机化学 2
1)含卤素最长碳链为主链,卤原子及其它支链作取代基,从
取代基较小的一端开始编号,取代基按“顺序规则”较优在后
面列出:
H3C CH2 CH2 CH CH2 CH3
CH2Cl
2-乙基-1—氯戊烷
2)以烯烃为母体,含双键最长碳链为主链,双键位次最小编
于制取引入OH比引入卤素困难的醇。
15
2021/4/26
青岛理工大学
15
有 机化学 2
2.与氰化钠反应
醇 RCH2X + NaCN
RCH2CN + NaX 腈
1°反应后分子中增加了一个碳原子,是有机合成中增长碳链 的方法之一。
2°CN可进一步转化为–COOH,-CONH2等基团。
3.与氨反应
R-X + NH3(过量)
KOH 乙醇
H3C CH C CH3 CH3
化学竞赛PPT-第八章 芳烃-第8章_3
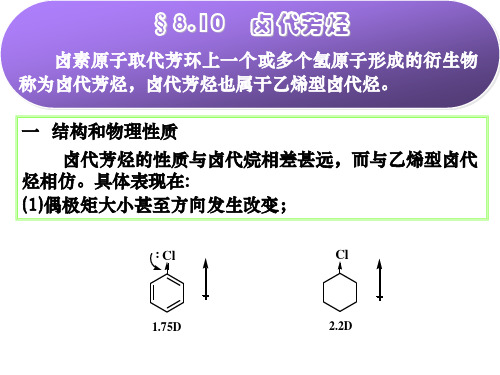
Z
Z
Z
Z
X
X
由于Z与叁键碳原子的相对位置不同,亲核试剂进攻叁 键碳原子,将分别得到两种碳负离子中间体,相对比例取 决于取代基的性质——加成的方向主要依赖于Z的诱导效应, 亲核试剂与苯炔生成的碳负离子越稳定则越容易生成。
值得指出的是,此处只需要考虑取代基的诱导效应, 因为在苯炔与亲核试剂加成后生成的苯基碳负离子中,负
电荷处于sp2杂化轨道中,该轨道与苯环共平面,不可能 与取代基的孤对电子发生p-π共轭。p-π共轭效应不影响苯
基碳负离子的稳定性。
sp2杂化轨道
:
OCH3 -I
所以,像甲氧基、氨基等带有孤对电子的取代基,只 需考虑其电负性比碳原子的大,具有吸电子诱导效应即可。
:
邻位取代卤代苯
Z X
Z
Z
NH2
(I)
Cl
溴苯和氯苯都能与金属锂反应得到苯基锂。
Cl
Li
+ 2 Li Et2O
+ LiCl
练习:
1.
Cl
CH 3
Mg(过量)
干 Et2O
Br
DCl
Cl
CH 3 D
CH 3
CH 2CN
2.
Cl 2 hv CN
Br I
Br I
§8.11 休克尔规则和非苯系芳烃
一 休克尔规则
一百多年前凯库勒就预见到,除苯外,可能存在其他 具有芳香性的环状共轭多烯烃。自然而然,与苯相邻的两 个类似物——环丁二烯和环辛四烯就成了研究的目标。但 结果证明,环丁二烯和环辛四烯具有烯烃的典型性质(譬 如容易发生亲电加成反应),而没有芳烃的特征性质—— 芳香性。为了解决这个问题化学家们作了许多努力,但用 共价键理论没有很好的解决。
《芳烃的取代反应》课件

⑴分速度因数(factors of partial rate)
分速度因数 (f) =
6 y
×
kk取苯代底物×z位产物的百分比)
校正因素
分速率
k取代底物:取代苯的反应总速率;
Z:
所在取代位置的产物的百分数;
y:
z位置的数目;
k苯: 苯的反应速率。
取代苯的亲电反应总速率除以苯的反应速率,然 后与某位置的产率相乘,再乘上校正因素(反应位置 的相对数目——分速度因数
3%
fo
(6) (2)
(23) × (1)
× (0.63)
43.5
fm
(6) (2)
(23) × (1)
×
(0.03)
2.1
fp
(6) (1)
(23) × (1)
× (0.34)
46.9
由计算知:f0 ,fp ,fm均大于1,所以,甲基是致活基。 且在甲基苯的取代反应中,邻,对位的活性﹥﹥间位。
所以,f是定量表示某一位置的取代速率(与未取代苯相 同反应速率的比较)
一取代苯有5个位置可取代:2个邻位,2个间位,一个对位。
fo=
kPhZ/2 kPhH/6
×
o
异构体 100
fm=
kPhZ/2 × kPhH/6
m
异构体 100
fp=
kPhZ/1 kPhH/6
×
p 异构体
100
➢fo fm fp分别是邻间对位 上的分速率因数;
➢kphH、kphZ分别是苯和取 代苯的反应速率常数
CH3
C6H5CH2Br GaCl3
CH3
CH2C6H5
+
CH3
+
有机化学第七章 芳烃 131页PPT

苯甲醛 benzaldehyde
COOH
苯甲酸 benzoic acid
S O 3H
苯磺酸 benzenesulfonic acid
29
有两种以上取代基时,选择母体的顺序为:
—OR,—R,—NH2,—OH,—COR,—CHO, —CN,—CONH2,—COCl,—COOR,—SO3H, —COOH,正离子等。
+
-
1
2
3
4
5
经典结构式1和2占的分量较大,3、4、5都是键长和键 角变形较大的脂环烃,在共振杂化体中占的分量较小。
因此苯只有一个邻位二元取代物,且不易发生加成反应。
20
关于共振论应用的几点说明:
共振论在有机化学上有重要的作用,能解释并预测一些 有机化合物的基本的化学性质; 共振论是一种理论,共振式是理论上存在的,无法测得; 共振论引入了一些人为规定,对某些化学现象尚不能给 出满意的解释。 共振论实际上是用有机化学中的通用语言,即两个或几 个经典结构式,来翻译量子化学的计算结果。 共振式中的经典结构式实际上是不存在的。
CH3
CH3
CH3
CH3
CH3 CH3
1,2-二甲苯 邻二甲苯
1,3-二甲苯 间二甲苯
1,4-二甲苯 对二甲苯
1,2-dimethylbenzene o-xylene
1,3-dimethylbenzene 1,4-dimethylbenzene
m-xylene
p-xylene
25
在外文名称中,IUPAC允许甲苯、(邻、间、对)二甲苯、 1,3,5-三甲苯、异丙苯、苯乙烯等的俗名继续使用。
1911年 Willstatter 合成了环 辛四烯,但它没有芳香性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Cl
Cl
OBz
(40%) (74%) (37%)
硫酰氯,刺激性液体,高. 活性的卤化剂,溶于乙醚 15
芳核上选择性卤取代的方法之三 ——NBS+DMF
H2N
H2N
NBS/DM F
[44]
r. t. ,24h
(93% )
Br
NBS可避免生成HBr, HBr本身有催化作用,使
DMF为极性非质子溶剂
• 在芳环的碘取代过程中为什么加入氧化剂 和碱性缓冲物质?
• 对于缺电子的芳杂环和富电子的芳杂环的
卤取代有什么差异?
.
20
下次课程预习
• 醛和酮的-卤取代反应(重点)
• 烯醇和烯胺衍生物的卤化反应(次重点)
• 羧酸衍生物的-卤取代反应(有兴趣自 学)
oxidization
.
13
芳核上选择性卤取代的方法之一
——改变溶剂和温度
非极性溶剂
HO 1mol Br2/CS2
OH
0~5℃
[42a] (80%~84% )
Br
缚酸剂
Br 2mol Br2/Tol t--BuNH2/-70℃
OH Br
[42b]
(87%)
倘若在碱性水溶液中卤化,得到的是2,4,6-三卤代苯酚
.
14
芳核上选择性卤取代的方法之二
——改变卤素的浓度
CO2Me
Me
OH
CO2Me
Me
OH
CO2Me
Me
OH
+
OBz
(62)
1molCl2/NaOAc/AcOH/r. t.
2molCl2/NaOAc/AcOH/r. t.
4molCl2/NaOAc/AcOH/r. t. SO2Cl2/Et2O/0℃
Cl OBz
3.倘若吡啶环上有供电基团,反应就容易的多。
Br Br2/AcOH
20~ 50℃
N
NH2
.
[48b]
(62%~ 67% )
N NH2
19
芳烃的卤取代
-复习需思考的问题
• 芳烃卤取代的反应机理是什么?如果需要 催化剂,最常用的催化剂有哪些?
• 芳烃的氯取代和溴取代,常用的卤取代试 剂是什么?
• 如何通过改变条件实现芳环卤取代的区域 选择性?举例说明
Br CH3
NBS
CH3CN OCH3
CH3 OCH3
C O N (C H 3)2
H B r/t-B uO O H
OCH3
H O A c/H 2O
.
C O N (C H 3)2 Br
OCH3
9
芳核的碘取代
• 单独的碘取代效果不好,因碘化氢具有还原性; • 除去碘化氢的方法:
– 加入氧化剂(硝酸、过氧化氢、过碘酸或醋酸汞) – 加入碱(氨水、碳酸钠或碳酸氢钠)中和 – 加入氧化汞或氧化镁与HI形成难溶于水的碘化物
I CF3COOI
.
[51]
(77%)
11
I
芳核的碘取代实例3
NH2
ICl/AcOH I
100oC, 2h
NH2 I
NO2
NO2
ICl:无机盐,溶于乙醇、乙醚、四氯化碳和冰醋酸 。
.
12
芳核的碘取代实例4
H O
H O N aI/t-B uO C l
C H 3C N ,0℃
[53]
(97% ) I
OH
定位规律:与一般芳烃亲电 取代相同
▲次卤酸(酯) ▲次卤酸酐(Cl2O) . ▲酰基次溴酸酐(CF3COOB2 r)
芳烃的卤取代反应-主要的影响素
• 催化剂: FeCl3,AlCl3,ZnCl2,TiCL4,SnCl4, 缺电子芳烃的卤取代尤其需要。
• 溶剂:极性溶剂为多,常用稀醋酸和稀盐 酸(反应激烈)、氯仿或二氯甲烷(反应 温和)。非极性溶剂中反应速度慢,可提 高选择性。
.
4
氯取代实例1
Cl2/FeCl3 Cl
.
5
氯取代实例2
N N
N C S
C H C l3 ,reflu x
C l
N N
.
6
芳核的溴取代
• 溴化条件: – 铁粉或三氯化铝催化下,溴为溴化剂; – 碘催化下,溴为溴化剂; – NBS为溴化剂 – 溴化氢+过氧化物:HBr+t-BuOOH(叔丁基过 氧化氢) – HOBr – CH3COOBr, CF3COOBr
.
7
芳核的溴取代实例1-3
A r H + B r 2 + I 2
A r B r+ H + I 2 B r
C H 3 B r2/I2(F e)
- 5~ 0℃
C H 3
B r
CH3
Br2/Fe
C H 3 [40]
( 94% ~ 97% ) C H 3
CH3 Br
NO2
.
NO2
8
芳核的溴取代实例5和6
得NBS上的溴更易离去 1.NBS+DMF同样适用苯酚和高级芳烃的卤化。
.
16
2. 苯胺若在水溶液中用卤素卤化会得到三卤代苯胺。
改善缺电子芳核的卤取代方法
• 采用催化剂 • 采用活性强的卤化剂
.
17
缺电子芳核的卤取代实例1
O2N
O2N Cl2O/(CF3SO2)2O
POCl3/0℃
[45] (97%)
• 温度:一般为室温到低温范围,缺电子芳 烃需要高温。低温反应速度慢,但能提高 选择性。
• 芳烃上取代基的影响:吸电子(存在卤化
困难的问题)和释电子(存在多卤取代的
问题)
.
3
芳核的氯取代
• 氯取代条件: – 在三氯化铝或三氯化铁的催化下与氯气 反应生成氯代苯,但也会得到二氯代苯, 分离困难,工业上制备氯代苯为用。see – NCS为常用的试剂,温和的氯化剂,选 择性好。 see – HOCl, Cl2O, H2+OCl(酸性条件下HOCl中 氢氧根负离子被氢离子结合)
Cl
实际上是三氟甲磺酰次氯酸酐CF3SO2OCl 参与反应
.
18
缺电子芳核的卤取代实例2
B r B r2/H 2SO 4/SO 3
[48a]
130℃ , 7.5h N
(86% ) N
1.用发烟硫酸氧化生成的溴化氢成溴。 2.如果用AlCl3催化,氮原子与AlCl3络合,进一步降低了 芳核的电子云,使反应难易进行。
• 采用强的碘化剂(ICl,RCOOI,CF3COOI) 来增强碘正离子的浓度。
.
10
芳核的碘取代实例1 和2
C H 3O C H 3O
C H 2O H
C H 3O
I2/H g(O A c)2
CH 2Cl2/r.t.,3h C H 3O
O C H 3
C H 2O H[50]
(76% )
I O C H 3
芳烃的卤取代反应
• 反应机理 • 主要的影响因素 • 氯取代 • 溴取代 • 碘取代 • 两大问题:选择性和卤取代的强化
.
1
芳烃的卤取代反应-反应机理
XX
or X-L
H
X
_H X
Àý£º X X
MXn
X
X N COR CR
(61)
络合物中间体
卤化剂:
▲卤素(有时用Lewis酸催化)
▲卤代酰胺(如NBS)
