上海市静安区名校化学高考流程题大全100题word含答案
上海市静安区达标名校2020年高考一月化学模拟试卷含解析

上海市静安区达标名校2020年高考一月化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.根据下列实验操作和现象所得到的结论正确的是选项实验现象结论A 向苯酚浊液中加入Na2CO3溶液溶液变澄清酸性:苯酚>碳酸B向20%蔗糖溶液中加入少量稀硫酸,加热;再加入银氨溶液并水浴加热未出现银镜蔗糖未水解C向2支盛有2mL相同浓度银氨溶液的试管中,分别加入2滴相同浓度的NaCl和NaI溶液一支无明显现象,另一支产生黄色沉淀相同条件下,AgI比AgCl的溶解度小DC2H5OH与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液KMnO4溶液褪色乙烯能被KMnO4氧化A.A B.B C.C D.D2.下列有关物质的性质与用途具有对应关系的是()A.Al2O3的熔点很高,可用作耐火材料B.NH3具有还原性,可用作制冷剂C.SO2具有氧化性,可用于纸浆的漂白D.钠钾合金的密度小,可用作快中子反应堆的热交换剂3.如图表示某个化学反应过程的能量变化。
该图表明()A.催化剂可以改变该反应的热效应B.该反应是个放热反应C.反应物总能量低于生成物D.化学反应遵循质量守恒定律4.在标准状况下,ALNH3溶于B mL水中,得到密度为ρg/cm3的RL氨水,则此氨水的物质的量浓度是()A.A22.4Rmol/L B.1000ρAA+22.4Bmol/LC.A22.4mol/L D.1000ρ17A+22.4Bmol/L5.某溶液X含有K+、Mg2+、Fe3+、Al3+、Fe2+、Cl-、CO32-、OH-、SiO32-、NO3-、SO42-中的几种,已知该溶液中各离子物质的量浓度均为0.2mol·L-1(不考虑水的电离及离子的水解)。
为确定该溶液中含有的离子,现进行了如下的操作:下列说法正确的是A.无色气体可能是NO和CO2的混合物B.原溶液可能存在Fe3+C.溶液X中所含离子种类共有4种D.另取l00mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为2.4g6.成语、古诗词、谚语等都是我国传统文化的瑰宝。
上海市静安区达标名校2018年高考四月化学模拟试卷含解析

上海市静安区达标名校2018年高考四月化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.下列有关化学用语表示正确的是()A.中子数比质子数多1的磷原子:B.Al3+的结构示意图:C.次氯酸钠的电子式:D.2-丁烯的结构简式:CH2=CH-CH=CH22.下列实验操作正确的是A.用长预漏斗分离油和水的混合物B.配制0.5mol/LFe(NO3)2溶液时将固态Fe(NO3)2溶于稀硝酸中加水稀释至指定体积C.将含氯化氢的氯气通过碳酸氢钠溶液,可收集到纯氯气D.用湿布熄灭实验台上酒精着火3.实现化学能转变为电能的装置是()A.干电池B.电解水C.太阳能热水器D.水力发电4.向3mol·L-1盐酸中加入打磨后的镁条,一段时间后生成灰白色固体X,并测得反应后溶液pH升高。
为确认固体X的成分,过滤洗涤后进行实验:①向固体X中加入足量硝酸,固体溶解,得到无色溶液,将其分成两等份;②向其中一份无色溶液中加入足量AgNO3溶液,得到白色沉淀a;③向另一份无色溶液中加入足量NaOH溶液,得到白色沉淀b。
下列分析不正确...的是()A.溶液pH升高的主要原因:Mg + 2H+ === Mg2+ + H2↑B.生成沉淀a的离子方程式:Ag+ + Cl-=== AgCl↓C.沉淀b是Mg(OH)2D.若a、b的物质的量关系为n(a):n(b)= 1:3,则可推知固体X的化学式为Mg3(OH)6Cl5.含有酚类物质的废水来源广泛,危害较大。
含酚废水不经处理排入水体,会危害水生生物的繁殖和生存;饮用水含酚,会影响人体健康。
某科研结构研究出一种高效光催化剂BMO(Bi2MoO6),可用于光催化降解丁基酚,原理如图所示。
下列说法错误的是()A.光催化剂BMO可降低丁基酚氧化反应的ΔHB.在丁基酚氧化过程中BMO表现出强还原性C.苯环上连有一OH和一C4H9的同分异构体共有12种(不考虑立体异构)D.反应中BMO参与反应过程且可以循环利用6.设N A为阿伏加德罗常数的值,下列说法正确的是A.1L 0.1mol/L的NaHS溶液中HS-和S2-离子数之和为0.1N AB.2.0 g H218O与D2O的混合物中所含中子数为N AC.1 mol Na2O2固体中含离子总数为4N AD.3 mol Fe在足量的水蒸气中完全反应转移9N A个电子7.下列各选项有机物同分异构体的数目,与分子式为ClC4H7O2,且能与碳酸氢钠反应生成气体的有机物数目相同的是(不含立体异构)()A.分子式为C5H10的烯烃B.分子式为C4H8O2的酯C.的一溴代物D.立方烷()的二氯代物8.锂—铜空气燃料电池(如图)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是A.整个反应过程中,氧化剂为O2B.放电时,正极的电极反应式为:Cu2O+H2O+2e-=2Cu+2OH-C.放电时,当电路中通过0.1 mol电子的电量时,有0.1 mol Li+透过固体电解质向Cu极移动,有标准状况下1.12 L氧气参与反应D.通空气时,铜被腐蚀,表面产生Cu2O9.下列有关溶液的说法中,正确的是A.(NH4)2SO4溶液浓缩时温度过高可能导致生成NH4HSO4B.相同温度下,强酸溶液的导电能力一定大于弱酸溶液C.通电时,溶液中溶质粒子分别向两极移动D.蒸干Na2CO3溶液最终得到NaOH10.下列实验合理的是()A.证明非金属性Cl>C>SiB.制备少量氧气C.除去Cl2中的HClD.吸收氨气,并防止倒吸A.A B.B C.C D.D11.利用如图装置探究铁在海水中的电化学防护,下列说法不正确的是A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀B.若X为锌棒,开关K置于M处,铁电极的反应:Fe−2e−=Fe2+C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀D.若X为碳棒,开关K置于N处,铁电极的反应:2H++2e−=H2↑12.下列离子方程式不正确...的是A.足量SO2通入NaClO溶液中:SO2+H2O+ClO-=SO42-+Cl-+2H+B.在稀氨水中通入过量CO2:NH3·H2O+CO2=NH4++HCO3-C.用浓H2SO4溶解FeS固体:FeS+2H+=Fe2++H2S↑D.氢氧化钡溶液与等物质的量的稀H2SO4混合:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O13.2016年,我国科研团队开创了以煤为原料合成气态烯烃的新途径。
2022届上海市静安区高考化学经典100流程题word含答案

2022届上海市静安区高考化学经典100流程题word含答案一、实验题1.氢氧化镁广泛用作阻燃剂和填充剂。
以白云石(化学式:MgCO3•CaCO3)为原料制备氢氧化镁的工艺流程如下:(1)根据流程图,白云石“轻烧”分解的化学方程式是。
(2)“研磨”的目的是。
(3)加入氨水时反应的化学方程式为;检验Mg(OH)2沉淀是否洗涤干净的方法是。
(4)本流程中可以循环利用的物质是。
(5)传统工艺是将白云石高温分解为氧化镁和氧化钙后提取,而该工艺采用轻烧白云石的方法,其优点是。
2.(13分)某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
请回答下列问题:(1)硬质试管中发生反应的化学方程式为____________________________ 。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分一定有,可能有,若溶液未变红色则说明硬质试管中固体物质的成分是。
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。
若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出上述白色沉淀变成红褐色的化学方程式:(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有性。
由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是,并且配制含Fe2+的盐溶液时应加入少量。
3.工业以浓缩海水为原料提取溴的部分过程如下:某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):(1)实验开始时,A装置中不通热空气,先通入a气体的目的是(用离子方程式表示)_________。
上海市名校化学高考精选流程题100题汇总word含答案
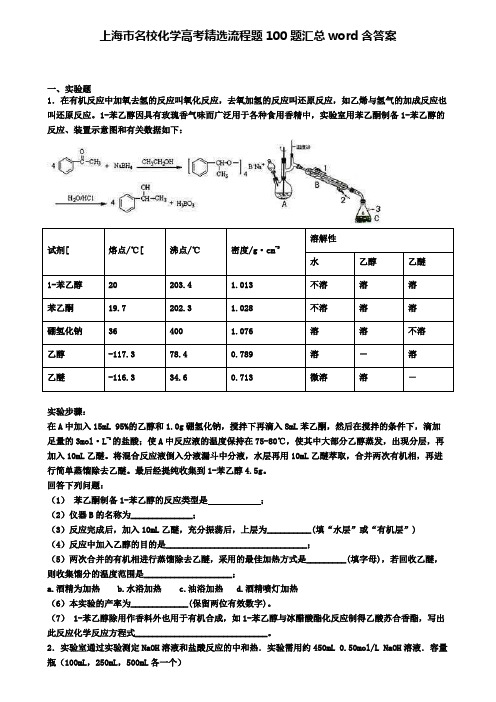
上海市名校化学高考精选流程题100题汇总word含答案一、实验题1.在有机反应中加氧去氢的反应叫氧化反应,去氧加氢的反应叫还原反应,如乙烯与氢气的加成反应也叫还原反应。
1-苯乙醇因具有玫瑰香气味而广泛用于各种食用香精中,实验室用苯乙酮制备1-苯乙醇的反应、装置示意图和有关数据如下:实验步骤:在A中加入15mL 95%的乙醇和1.0g硼氢化钠,搅拌下再滴入8mL苯乙酮,然后在搅拌的条件下,滴加足量的3mol·L-1的盐酸;使A中反应液的温度保持在75-80℃,使其中大部分乙醇蒸发,出现分层,再加入10mL乙醚。
将混合反应液倒入分液漏斗中分液,水层再用10mL乙醚萃取,合并两次有机相,再进行简单蒸馏除去乙醚。
最后经提纯收集到1-苯乙醇4.5g。
回答下列问题:(1)苯乙酮制备1-苯乙醇的反应类型是;(2)仪器B的名称为______________;(3)反应完成后,加入10mL乙醚,充分振荡后,上层为__________(填“水层”或“有机层”)(4)反应中加入乙醇的目的是________________________________;(5)两次合并的有机相进行蒸馏除去乙醚,采用的最佳加热方式是_________(填字母),若回收乙醚,则收集馏分的温度范围是____________________;a.酒精为加热b.水浴加热c.油浴加热d.酒精喷灯加热(6)本实验的产率为_____________(保留两位有效数字)。
(7) 1-苯乙醇除用作香料外也用于有机合成,如1-苯乙醇与冰醋酸酯化反应制得乙酸苏合香酯,写出此反应化学反应方程式______________________________。
2.实验室通过实验测定NaOH溶液和盐酸反应的中和热.实验需用约450mL 0.50mol/L NaOH溶液.容量瓶(100mL,250mL,500mL各一个)(1)配制0.50 mol/L NaOH溶液:将NaOH固体放在_________________(填实验用品或仪器的名称),用托盘天平___g NaOH固体.在使用容量瓶前必须进行的操作是_____.(2)下列操作会使所配溶液的浓度偏高的是(填序号)______________.A.烧杯、玻璃棒没有洗涤B.转移时有溶液溅出容量瓶外C.定容时,将容量瓶上、下颠倒摇匀后发现液面低于刻度线再加水D.容量瓶用蒸馏水洗涤后再用相同溶质的溶液润洗E.定容时俯视容量瓶刻度线.(3)将50mL 0.50mol/L盐酸与60mL 0.50mol/L NaOH溶液在图所示的装置中进行中和反应.从实验装置上看,图中尚缺少的一种玻璃仪器是________________________.(4)一定量的稀盐酸和过量的NaOH溶液反应,当生成1mol H2O时放出的热量为57.3 kJ,则该反应的热化学方程式为___________________________________.已知:① HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+H2O(l);△H=-a kJ·mol-1② HCl(aq)+NaOH(s)=NaCl(aq)+H2O(l);△H=-b kJ·mol-1③ HNO3(aq)+KOH(aq)=NaNO3(aq)+H2O(l);△H=-c kJ·mol-1则a、b、c三者的大小关系为_________(填字母).A.a>b>c B.b>c>a C.a=b=c D.无法比较3.废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列方法回收钴、锂。
上海市静安区达标名校2020年高考二月仿真备考化学试题含解析

上海市静安区达标名校2020年高考二月仿真备考化学试题一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.下列操作一定会使结果偏低的是()A.配制一定物质的量浓度的溶液时,用胶头滴管将超过刻度线的溶液吸出B.测定胆矾晶体中的结晶水含量,加热后,未进行恒重操作C.酸碱滴定实验,滴加最后一滴标准液,溶液颜色突变,未等待半分钟D.测定气体摩尔体积时,气体体积未减去注入酸的体积2.下列说法不正确的是()A.用容量瓶配制溶液时,先用蒸馏水洗涤,再用待装液润洗B.用蒸馏法可由含有Fe3+的自来水获取较纯净的水C.焰色反应后用稀盐酸洗涤铂丝并在火焰上灼烧至无色,再进行其它物质的测试D.金属镁着火可用沙子覆盖3.草酸是二元中强酸,草酸氢钠溶液显酸性。
常温下,向10mL 0.01mol·L-1NaHC2O4溶液中滴加0.01mol·L-1NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是()A.V[NaOH(aq)]=0时,c(H+)=1×10-2mol·L-1B.V[NaOH(aq)]<10mL时,不可能存在c(Na+)=2c(C2O42-)+c(HC2O4-)C.V[NaOH(aq)]=10mL时,c(H+)=1×10-7mol·L-1D.V[NaOH(aq)]>10mL时,c(Na+)>c(C2O42-)>c(HC2O4-)4.Y是合成香料、医药、农药及染料的重要中间体,可由X在一定条件下合成:下列说法错误的是()A.Y的分子式为C10H8O3B.由X制取Y过程中可得到乙醇C.一定条件下,Y能发生加聚反应D.等物质的量的X、Y分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为3:25.化学与生活、人类生产、社会可持续发展密切相关,下列叙述正确的是A.塑料、有机玻璃、光导纤维、碳纤维都是新型有机高分子材料B.磁性氧化铁可用于制备红色颜料和油漆C.用明矾溶液可清除铜镜表面的铜锈,是因为溶液中的A13+离子能与铜锈反应D.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗,该过程涉及胶体性质的应用6.在下列各用途中,利用了物质的氧化性的是A.用食盐腌制食物B.用漂粉精消毒游泳池中的水C.用汽油洗涤衣物上的油污D.用盐酸除去铁钉表面的铁锈7.下列叙述正确的是A.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同B.原电池中发生的反应达平衡时,该电池仍有电流产生C.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中D.反应4Fe(s)+3O2(g)=2Fe2O3(s)常温下可自发进行,该反应为吸热反应8.下表中各组物质之间不能通过一步反应实现如图转化的是甲乙丙A CH2=CH2CH3CH2Cl CH3CH2OHB NH3NO HNO3C AlCl3Al(OH)3Al2O3D Cl2HCl CuCl2A.A B.B C.C D.D9.下列表示对应化学反应的离子方程式正确的是A.碳酸钙溶于稀醋酸:CaCO3+2H+=Ca2++H2O+CO2↑B.铜与稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2OC.向NH4HCO3溶液中滴加过量Ba(OH)2溶液:HCO3-+OH-+Ba2+=H2O+BaCO3↓D.用银氨溶液检验乙醛中的醛基:CH3CHO+[Ag(NH3)2]++2OH-CH3COO-+NH4++NH3+ Ag↓+H2O 10.室温下,0.1mol下列物质分别与1L0.1mol/LNaOH溶液反应,所得溶液pH最小的是A.SO3B.NO2C.Al2O3D.SO211.不能用NaOH溶液除去括号中杂质的是A.Mg(Al2O3)B.MgCl2(AlCl3)C.Fe(Al)D.Fe2O3(Al2O3)12.2,3 −二甲基丁烷中“二”表示的含义是A.取代基的数目B.取代基的种类C.主链碳的数目D.主链碳的位置13.设N A为阿伏加德罗常数的值,下列说法正确的是()A.pH=1的硫酸溶液1L,溶液中含SO42-的数目等于0.1N AB.真空密闭容器中充入0.1molH2和0.1molI2充分反应后,容器内分子总数为0.2N AC.10mL0.1mol⋅L-1的FeCl3与20mL0.1mol⋅L-1KI溶液反应,转移电子数为0.001N AD.60gSiO2晶体中Si-O键数目为2N A14.下列化合物中,属于酸性氧化物的是()A.Na2O2B.SO3C.NaHCO3D.CH2O15.一定条件下,CO2分子晶体可转化为具有类似SiO2结构的原子晶体.从理论上分析,下列说法正确的是()A.该转化过程是物理变化B.1molCO2原子晶体中含2mol C﹣O键C.CO2原子晶体的熔点高于SiO2D.CO2的原子晶体和分子晶体互为同分异构体二、实验题(本题包括1个小题,共10分)16.利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。
上海市静安区名校化学高考实验题大全100题word含答案
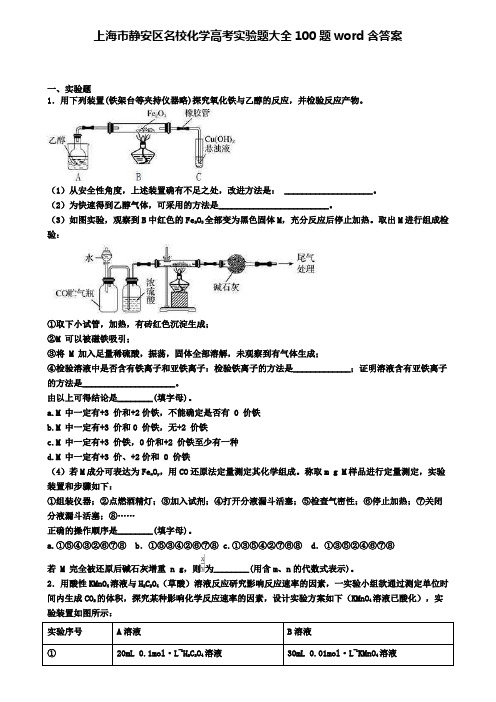
上海市静安区名校化学高考实验题大全100题word含答案一、实验题1.用下列装置(铁架台等夹持仪器略)探究氧化铁与乙醇的反应,并检验反应产物。
(1)从安全性角度,上述装置确有不足之处,改进方法是: ____________________。
(2)为快速得到乙醇气体,可采用的方法是_________________________。
(3)如图实验,观察到B中红色的Fe2O3全部变为黑色固体M,充分反应后停止加热。
取出M进行组成检验:①取下小试管,加热,有砖红色沉淀生成;②M 可以被磁铁吸引;③将 M 加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成;④检验溶液中是否含有铁离子和亚铁离子:检验铁离子的方法是_____________;证明溶液含有亚铁离子的方法是_____________________。
由以上可得结论是________(填字母)。
a.M 中一定有+3 价和+2价铁,不能确定是否有 0 价铁b.M 中一定有+3 价和0 价铁,无+2 价铁c.M 中一定有+3 价铁,0价和+2 价铁至少有一种d.M 中一定有+3 价、+2价和 0 价铁(4)若M成分可表达为Fe x O y,用CO还原法定量测定其化学组成。
称取m g M样品进行定量测定,实验装置和步骤如下:①组装仪器;②点燃酒精灯;③加入试剂;④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧……正确的操作顺序是________(填字母)。
a.①⑤④③②⑥⑦⑧ b.①⑤③④②⑥⑦⑧ c.①③⑤④②⑦⑥⑧ d.①③⑤②④⑥⑦⑧若 M 完全被还原后碱石灰增重 n g,则为________(用含m、n的代数式表示)。
2.用酸性KMnO4溶液与H2C2O4(草酸)溶液反应研究影响反应速率的因素,一实验小组欲通过测定单位时间内生成CO2的体积,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图所示:(1)写出该反应的离子方程式__________________________________________。
上海市静安区达标名校2019年高考二月化学模拟试卷含解析
上海市静安区达标名校2019年高考二月化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.下列说法正确的是A.氢氧燃料电池放电时化学能全部转化为电能B.反应4Fe(s)+3O 2(g)2Fe2O3(s)常温下可自发进行,该反应为吸热反应C.3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023D.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快2.短周期元素W、X、Y和Z的原子序数依次增大.元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍.下列说法错误的是()A.元素W、X的氯化物中,各原子均满足8电子的稳定结构B.元素X与氢形成的原子比为1:1的化合物有很多种C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成D.元素Z可与元素X形成共价化合物XZ23.某同学探究温度对溶液pH值影响,加热一组试液并测量pH后得到如下数据(溶液浓度均为0.1mol/L):温度(℃)10 20 30 40纯水7.30 7.10 6.95 6.74NaOH溶液13.50 13.11 12.87 12.50CH3COOH溶液 2.90 2.89 2.87 2.85CH3COONa溶液9.19 9.00 8.76 8.62下列说法正确的是A.随温度升高,纯水中的k w逐渐减小B.随温度升高,NaOH溶液pH变化主要受水电离平衡变化影响C.随温度升高,CH3COOH的电离促进了水的电离D.随温度升高,CH3COONa溶液的pH减小,说明水解程度减小,c(CH3COO-)增大4.一种从植物中提取的天然化合物,可用于制作“香水”,其结构简式为,下列有关该化合物的说法错误的是A.分子式为C12H18O2B.分子中至少有6个碳原子共平面C.该化合物能使酸性高锰酸钾溶液褪色D.一定条件下,1 mol该化合物最多可与3 mol H2加成5.某有机物结构简式如图,下列对该物质的叙述中正确的是A.该有机物易溶于苯及水B.该有机物苯环上的一氯代物共有4种C.该有机物可以与溴的四氯化碳溶液发生加成反应使之褪色D.1mol该有机物最多可与1mol NaOH发生反应6.下列物质属于碱的是A.CH3OH B.Cu2(OH)2CO3C.NH3·H2O D.Na2CO37.R是合成某高分子材料的单体,其结构简式如图所示。
上海高考化学试题及答案
上海高考化学试题及答案一、选择题(每题3分,共30分)1. 下列物质中,属于混合物的是A. 蒸馏水B. 液态氧C. 空气D. 氯化钠2. 根据化学方程式2H2 + O2 → 2H2O,下列说法正确的是A. 氢气和氧气反应生成水B. 氢气和氧气的体积比为1:1C. 氢气和氧气的质量比为2:1D. 氢气和氧气的摩尔比为2:13. 元素周期表中,下列元素属于主族元素的是A. 氦(He)B. 氧(O)C. 铁(Fe)D. 铀(U)4. 下列物质中,属于电解质的是A. 蔗糖B. 酒精C. 氯化钠D. 二氧化碳5. 根据质量守恒定律,下列化学反应中,生成物的质量总和等于反应物的质量总和的是A. 碳在氧气中燃烧B. 镁在二氧化碳中燃烧C. 氢气在氯气中燃烧D. 铁在氧气中燃烧6. 下列物质中,属于非金属单质的是A. 铁(Fe)B. 硫(S)C. 铜(Cu)D. 氩(Ar)7. 根据酸碱中和反应的化学方程式,下列说法正确的是A. 酸和碱反应生成盐和水B. 酸和碱反应生成氧化物和水C. 酸和碱反应生成盐和氧化物D. 酸和碱反应生成盐和氢气8. 下列物质中,属于有机化合物的是A. 二氧化碳(CO2)B. 甲烷(CH4)C. 氯化钠(NaCl)D. 水(H2O)9. 根据化学方程式,下列化学反应中,属于氧化还原反应的是A. CO2 + H2O → H2CO3B. 2H2 + O2 → 2H2OC. NaCl + AgNO3 → AgCl + NaNO3D. 2NaOH + H2SO4 → Na2SO4 + 2H2O10. 下列物质中,属于碱的是A. 硫酸(H2SO4)B. 氢氧化钠(NaOH)C. 硝酸(HNO3)D. 氯化铵(NH4Cl)二、填空题(每题5分,共20分)11. 根据化学方程式,写出下列化学反应的生成物:2H2O → 2H2↑ + O2↑生成物为:氢气和氧气。
12. 写出下列元素的化学符号:钠(Na)、氯(Cl)、钙(Ca)、铁(Fe)。
2019-2020学年上海市静安区市级名校新高考化学模拟试卷含解析
2019-2020学年上海市静安区市级名校新高考化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.按照物质的组成分类,SO2属于()A.单质B.酸性氧化物C.碱性氧化物D.混合物【答案】B【解析】【分析】A、SO2由两种元素组成,不符合单质的概念;B、能与碱反应生成盐和水的氧化物叫做酸性氧化物;C、SO2是能与碱反应只生成盐和水的氧化物,属于酸性氧化物;D、SO2属于纯净物。
【详解】A、SO2由两种元素组成,不属于单质,故A错误;B、能与碱反应生成盐和水的氧化物叫做酸性氧化物;SO2是能与碱反应只生成盐和水的氧化物,属于酸性氧化物,故B正确;C、SO2是能与碱反应只生成盐和水的氧化物,属于酸性氧化物,故C错误;D、SO2属于纯净物,不属于混合物,故D错误;故选:B。
2.设N A为阿伏加德罗常数的值。
关于常温下pH=10的Na2CO3~NaHCO3缓冲溶液,下列说法错误的是A.每升溶液中的OH﹣数目为0.0001N AB.c(H+)+c(Na+)=c(OH﹣)+c(HCO3﹣)+2c(CO32﹣)C.当溶液中Na+数目为0.3N A时,n(H2CO3)+n(HCO3﹣)+n(CO32﹣)=0.3molD.若溶液中混入少量碱,溶液中-32-3c(HCO)c(CO)变小,可保持溶液的pH值相对稳定【答案】C【解析】【分析】A、pH=10的溶液中,氢氧根浓度为10-4mol/L;B、根据溶液的电荷守恒来分析;C、在Na2CO3中,钠离子和碳原子的个数之比为2:1,而在NaHCO3中,钠离子和碳原子的个数之比为1:1;D、根据2-3CO的水解平衡常数来分析。
【详解】A 、常温下,pH =10的溶液中,氢氧根浓度为10-4mol/L ,故1L 溶液中氢氧根的个数为0.0001N A ,故A 不符合题意;B 、溶液显电中性,根据溶液的电荷守恒可知c(H +)+c(Na +)=c(OH ﹣)+c(-3HCO )+2c(2-3CO ),故B 不符合题意; C 、在Na 2CO 3中,钠离子和碳原子的个数之比为2:1,而在NaHCO 3中,钠离子和碳原子的个数之比为1:1,故此溶液中的当溶液中Na +数目为0.3N A 时,n(H 2CO 3)+n(-3HCO )+n(2-3CO )<0.3mol ,故C 符合题意; D 、2-3CO 的水解平衡常数()()()--3h 2-3HCO OH =CO c c K c g ,故当加入少量的碱后,溶液中的c(OH -)变大,而K h 不变,故溶液中()()-32-3HCO CO c c 变小,c(OH -)将会适当减小,溶液的pH 基本保持不变,故D 不符合题意;故选:C 。
上海市静安区达标名校2020年高考三月化学模拟试卷含解析
上海市静安区达标名校2020年高考三月化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.下列离子方程式正确的是A.Cl2通入水中:Cl2+H2O = 2H++Cl-+ClO-B.双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2OC.用铜做电极电解CuSO4溶液:2Cu2++2H2O2Cu+O2↑+4H+D.Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O2.在给定条件下,下列选项所示的物质间转化均能实现的是()A.Cu2S(s)Cu(s)CuCl2(s)B.SiO2(s)H2SiO3(s)Na2SiO3(aq)C.Fe(s)Fe2O3(s)Fe2(SO4)3(aq)D.NaCl(aq)Na2CO3(s)NaOH(aq)3.下列不符合安全规范的是()A.金属钠着火时使用泡沫灭火器灭火B.NH3泄露时向空中喷洒水雾C.含Cl2的尾气用碱溶液处理后再排放D.面粉生产车间应严禁烟火4.有机物X、Y的转化如下:下列说法不正确的是A.X能加聚反应B.Y分子苯环上的二氯代物有5种C.与Y互为同分异构体D.X、Y分子的所有原子可能共平面5.A、B、C、X为中学化学常见物质,A、B、C含有相同元素甲,可以发生如下转化(水参与的反应,水未标出)。
下列说法不正确...的是A.若A、B、C的焰色反应呈黄色、水溶液均呈碱性,则X可以是CO2B.若C为红棕色气体,则A一定为空气中含量最高的气体C.若B为FeCl3,则X一定是FeD.A可以是碳单质,也可以是O26.25 ℃时,向NaHCO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。
下列叙述错误的是A.25 ℃时,H2CO3的一级电离K a1(H2CO3)=1.0×10-6.4B.M点溶液中:c(H+)+ c(H2CO3)=c(Cl-) +2c(C O32-) +c(OH-)O+H2O H2CO3+OH-的K h=1.0×10-7.6C.25 ℃时,HC-3D.图中a=2.67.下列各组离子能在指定溶液中,大量共存的是()①无色溶液中:K+,Cu2+,Na+,MnO4-,SO42-②使pH=11的溶液中:CO32-,Na+,AlO2-,NO3-③加入Al能放出H2的溶液中:Cl-,HCO3-,NO3-,NH4+④加入Mg能放出H2的溶液中:NH4+,Cl-,K+,SO42-⑤使石蕊变红的溶液中:Fe3+,MnO4-,NO3-,Na+,SO42-⑥酸性溶液中:Fe2+,Al3+,NO3-,I-,Cl-A.①②⑤B.①③⑥C.②④⑤D.①②④8.下列各组离子在溶液中可以大量共存,且加入或通入试剂X后,发生反应的离子方程式也正确的是A.A B.B C.C D.D9.用下列装置进行实验能达到相应实验目的的是A.装置配制100 mL某浓度NaNO3溶液B.分离溴苯和水混合物C.验证质量守恒定律D.可以实现防止铁钉生锈10.下列属于原子晶体的化合物是()A.干冰B.晶体硅C.金刚石D.碳化硅11.某溶液只含有K+、Fe2+、Cl-、Mg2+、I-、CO32-、SO42-中的几种,限用以下试剂检验:盐酸、硫酸、硝酸银溶液、硝酸钡溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
上海市静安区名校化学高考流程题大全100题word含答案一、实验题1.某化学兴趣小组用铝土矿(主要成分为A12 O3,还含有SiO2及铁的氧化物)提取氧化铝做冶炼铝的原料,提取的操作过程如下:(1)实验室中制取CO2时,为了使反应随开随用、随关随停,应选用下图中的装置______________(填字母代号)。
(2)在过滤操作中,除烧杯、玻璃棒外,还需用到的玻璃仪器有_________________;洗涤沉淀的操作是________________________(3)实验室制备氢氧化铝的方案有多种。
现提供铝屑、氢氧化钠溶液、稀硫酸三种药品,若制备等量的氢氧化铝,请你从药品用量最少的角度出发,设计出最佳实验方案(方案不必给出),写出此方案中发生反应的离子方程式:________、______________、_____________________;此方案中所用药品的物质的量之比是:n(Al):n(H2SO4):n(NaOH=______。
(4)兴趣小组欲对铝土矿中铁元素的价态进行探究:取少量固体,加入过量稀硝酸,加热溶解;取少许溶液滴加KSCN溶液后出现红色。
由此得出,铁元素的价态为+3的结论。
请指出该结论是否合理并说明理由。
__________________________________2.已知:ICl的熔点为13.9℃,沸点为97.4℃,易水解,且能发生反应:ICl(l) + Cl2(g) ==ICl3(l)。
(图中夹持装置略去)(1)装置A中发生反应的化学方程式是。
(2)装置B的作用是。
不能用装置F代替装置E,理由。
(3)所制得的ICl中溶有少量ICl3杂质,提纯的方法是 (填标号)。
A.过滤 B.蒸发结晶 C.蒸馏 D.分液(4)用ICl的冰醋酸溶液测定某油脂的不饱和度。
进行如下两个实验,实验过程中有关反应为:①②ICl+KI=I2+KCl ③I2+2Na2S2O3=2NaI+Na2S4O6实验1:将5.00g该油脂样品溶于四氯化碳后形成100mL溶液,从中取出十分之一,加入20mL某ICl的冰醋酸溶液(过量),充分反应后,加入足量KI溶液,生成的碘单质用a mol/L的Na2S2O3标准溶液滴定。
经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1mL。
实验2(空白实验):不加油脂样品,其它操作步骤、所用试剂及用量与实验1完全相同,测得消耗的Na2S2O3溶液的平均体积为V2mL。
①滴定过程中可用作指示剂。
②滴定过程中需要不断振荡,否则会导致V1 (填“偏大”或“偏小)。
③5.00g该油脂样品所消耗的ICl的物质的量为 mol。
由此数据经换算即可求得该油脂的不饱和度。
3.已知二氧化硅、二氧化硫和二氧化碳都是酸性氧化物,化学性质具有一定的相似性,镁和钠的化学性质也具有一定的相似性。
用如上图所示装置进行镁和二氧化硫的实验,其中A是制备二氧化硫的发生装置。
(1)选择制取二氧化硫的合适试剂________(填序号)。
①10%的硫酸溶液②80%硫酸溶液③亚硫酸钠固体④亚硫酸钙固体(2)写出装置B中发生反应的化学方程式: ______________________。
(3)你认为该装置的不足之处是_______________________________(任写2条)。
4.制取氯化铁粉末,已知氯化铁粉末很容易吸水生成结晶化合物FeCl3+6H2O===FeCl3·6H2O。
(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):①接_______________________________________________________(2)烧瓶A发生的反应中,氧化剂是________(填物质名称),B中反应的化学方程式是___________________。
(3)容器D的作用是_____________________________________________,容器E的作用是__________________________________________________。
(4)A、B中的酒精灯应先点燃________处(填“A”或“B”)的酒精灯,理由是___________________。
(5)这套实验装置是否完整?________(填“是”或“否”),若不完整,还须补充________装置(若第一问填“是”,则此问不需要作答)。
5.按以下装置图进行实验,填写有关现象及化学方程式。
(1)A中现象是____________________,(2)B中浓硫酸的作用是_______________(3)C中发生反应的化学方程式为______________,(4)D中现象是_______________;反应的离子方程式是__________________________,E中收集的气体是____________。
6.实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)①A为氯气发生装置。
A中反应方程式是________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。
_______③C中得到紫色固体和溶液。
C中Cl2发生的反应有3Cl 2+2Fe(OH)3+10KOH2K2FeO4+6KCl+8H2O,另外还有________________。
(2)探究K2FeO4的性质①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。
为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:Ⅰ.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。
用KOH溶液洗涤的目的是________________。
②根据K2FeO4的制备实验得出:氧化性Cl2________(填“>”或“<”),而方案Ⅱ实验表明,Cl2和的氧化性强弱关系相反,原因是________________。
③资料表明,酸性溶液中的氧化性>,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性>。
若能,请说明理由;若不能,进一步设计实验方案。
理由或方案:________________。
7.硝基苯是是医药和染料的中间体,还可做有机溶剂。
反应如下:组装如右上图反应装置。
有关数据列表如右下表:制备硝基苯流程如下:(1)步骤①配制混酸:取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混和酸,操作是:在烧杯中先加入________,再,并不断搅拌、冷却;把配好的混和酸加入恒压漏斗中;最后在三颈烧瓶中加入18 mL苯。
(2)在室温下向三颈瓶中的苯逐滴加入混酸,边滴边搅拌,混和均匀、加热。
实验装置中长玻璃管最好用________代替(填仪器名称);上图中的加热方式称为;反应温度控制在50~60 ℃的原因是。
硝基苯的提纯步骤为:(3)步骤⑤表明混合物中有苯和硝基苯的操作和现象是。
(4)验证步骤⑥中液体已洗净的操作和现象是:取最后一次洗涤液,;为了得到更纯净的硝基苯,还须先向液体中加入无水CaCl2除去水,然后(填操作名称)。
(5)设计实验证明中:“粗产品中2”中含二硝基苯。
(6)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示)反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为。
8.某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置。
A中所用试剂,从下列固体物质中选取:①NH4HCO3、②NH4Cl、③Ca(OH)2、④NaOH。
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯,铂丝继续保持红热,F处铜片逐渐溶解。
(1)实验室制取A中气体时若只用一种试剂,该试剂是_________________(填代表备选试剂的序号);此时A中主要的玻璃仪器有__________________________________(填名称)。
(2)下面关于A中所用试剂的说法正确的是___________________。
A.施用该物质会大大提高粮食产量而对环境无影响B.向该物质的溶液中加入足量氢氧化钡溶液发生反应的离子方程式为:NH4++ OH–= NH3•H2OC.可通过加热方法区别该试剂和(NH4)2SO4D.工业上用NH3等合成该物质的过程可称为氮的固定(3)装置C中发生催化氧化反应的化学方程式为_________________________,装置E发生反应的化学方程式为_________________________________________________。
(4)假设A、B中的药品充足,则装置F中可以观察到的现象有_____________________________________________________________________________________________。
(5)指导老师从安全与环保角度考虑,指出该装置有两处明显的缺陷,请你提出修改建议:___________________________________________________________________________________________ ______________________________________________________。
9.为测定某Na2SO3样品(含少量Na2SO4杂质)的纯度,实验室按以下步骤进行;①称取ag样品,置于烧杯中;②加入适量蒸馏水,使样品溶解,然后配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液;然后,可采用下列两种方法进行测定:请根据上述实验,回答:(1)上图所示仪器中,本实验步骤①②③中必须用的的仪器是E和______(填字母);(2)在方法一④中加入过量稀盐酸的目的是________________________________;(3)在方法一测定得到Na2SO3样品的纯度是_______________(列出算式,可不化简);(4)在方法二中,是否需要加入指示剂_______(填“是”或“否”),请简述理由________;(5)在方法二中达到滴定终点读取数据时,俯视液面,则测定结果________________________(填“偏高”、“偏低”、“无影响”)。
