第七章习题分子结构
高中化学必修2第7章第2节 烃 有机高分子材料 练习新解析版)

第七章有机化合物第二节乙烯与有机高分子材料第2课时烃有机高分子材料1.既能用来鉴别乙烯和乙烷,又能用来除去乙烷中混有的乙烯的方法是()A.通入足量溴水中B.在空气中燃烧C.通入酸性高锰酸钾溶液中D.在一定条件下通入氢气【答案】A【解析】乙烯能与Br2发生加成反应而使溴水褪色,而乙烷不能,用溴水除去乙烯的同时又不产生新的气体杂质,A项正确;二者都能燃烧,故不能通过燃烧的方法达到除去乙烯的目的,B项错误;乙烯能使酸性高锰酸钾溶液褪色,乙烷不能,但乙烯被酸性高锰酸钾溶液氧化成CO2,产生新的气体杂质,不能作为除去乙烷中乙烯的方法,C项错误;在一定条件下通入氢气,虽可将乙烯转变为乙烷,但通入氢气的量不易控制,很难得到纯净的乙烷,D项错误。
2.下列烃分子中所有原子均在同一平面内的是()A.甲烷B.苯C.丙烯(CH2==CH—CH3)D.正戊烷【答案】B【解析】甲烷是正四面体形分子,所有原子不可能都在同一平面上,A项错误;苯是平面形分子,所有原子处于同一平面,B项正确;丙烯(CH3—CH==CH2)中含有甲基,甲基碳上所连的原子不可能在同一平面内,C项错误;正戊烷中含有甲基,甲基具有甲烷的结构特点,因此所有原子不可能处于同一平面,D 项错误。
3.将溴水分别与四氯化碳、己烷、己烯、酒精四种试剂混合,充分振荡后静置,下列现象与所加试剂不相吻合的是()【答案】D【解析】四氯化碳与溴水混合,四氯化碳将溴从溴水中萃取出来,得到溴的四氯化碳溶液,该溶液呈橙色,由于四氯化碳密度大于水,在下层,水层的颜色变浅,呈淡黄色,A正确;己烷和溴水混合,己烷将溴从溴水中萃取出来,得到溴的己烷溶液,该溶液呈橙色,己烷密度小于水,在上层,水层的颜色变浅,呈淡黄色,B正确;己烯和溴水混合发生加成反应,溴水褪色并分层,分层后水在上层,生成的二溴己烷在下层,C正确;溴水和酒精混合,不分层,D错误。
4.下列叙述中正确的是()A.丙烷分子中的3个碳原子处在同一直线上B.甲苯()分子中的7个碳原子处在同一平面上C.乙烷分子中的碳原子和氢原子都处在同一平面上D.丙烯(CH2==CHCH3)分子中的3个碳原子处在同一直线上【答案】B【解析】甲烷分子是正四面体结构,丙烷可看作是2个甲基取代甲烷分子中的2个氢原子形成的,所以丙烷分子中的3个碳原子不可能处在同一直线上,而是锯齿形,A错误;甲苯分子中甲基的碳原子取代苯分子中氢原子的位置而在苯分子的平面上,B正确;甲烷分子是正四面体结构,乙烷可看作是一个甲基取代甲烷分子的氢原子形成的,所以乙烷分子中的碳原子和氢原子不可能都处在同一平面上,C错误;丙烯(CH2==CHCH3)可看作是乙烯分子中的一个氢原子被甲基取代形成的,乙烯分子是平面结构,键角是120°,所以丙烯分子中的3个碳原子不可能在同一直线上,D错误。
第七章-芳烃-习题-答案
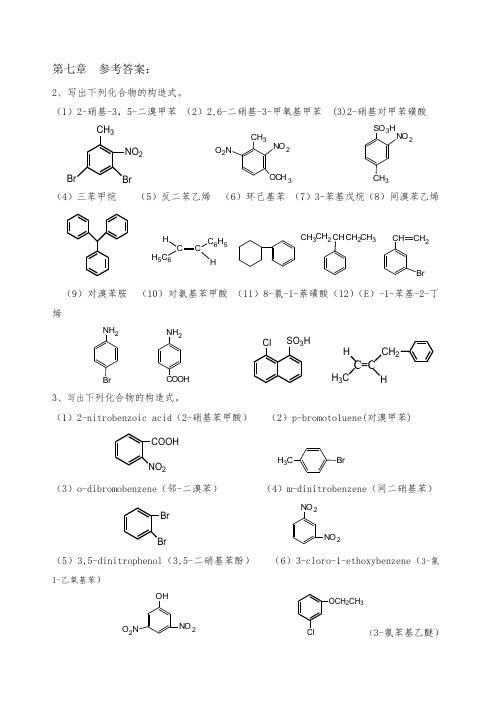
第七章 参考答案:2、写出下列化合物的构造式。
(1)2-硝基-3,5-二溴甲苯 (2)2,6-二硝基-3-甲氧基甲苯 (3)2-硝基对甲苯磺酸CH 3NO 2BrBrCH 3NO 2O 2NOC H 3SO 3HNO 23(4)三苯甲烷 (5)反二苯乙烯 (6)环己基苯 (7)3-苯基戊烷(8)间溴苯乙烯CCC 6H 5H 5C 6HH CH 3CH 2CHCH 2CH 3CHCH 2Br(9)对溴苯胺 (10)对氨基苯甲酸 (11)8-氯-1-萘磺酸(12)(E )-1-苯基-2-丁烯NH 2BrNH 2SO 3HClC=CHHH 3CCH 23、写出下列化合物的构造式。
(1)2-nitrobenzoic acid (2-硝基苯甲酸) (2)p-bromotoluene(对溴甲苯)COOH NO 2CH 3Br(3)o-dibromobenzene (邻-二溴苯) (4)m-dinitrobenzene (间二硝基苯)BrBrNO 2NO 2(5)3,5-dinitrophenol (3,5-二硝基苯酚) (6)3-cloro-1-ethoxybenzene (3-氯1-乙氧基苯)OHNO 2O 2NOCH 2CH 3(3-氯苯基乙醚)(7)2-methyl-3-phenyl-1-butanol (2-甲基-3-苯基1-丁醇)CH 3CHCHCH 2OHCH 3(8)p-chlorobenzenesulfonic acid (对氯苯磺酸)(9)benzyl bromide (苄基溴)SO 3HClCH 2Br(11)o-xyene (邻二甲苯)(12)tert-butylbenzene (叔丁基苯)(13)p-cresol (对甲苯酚)CH 3CH 3C(CH 3)3CH 3OH (14)3-phenylcyclohexanol (3-苯环己醇)(15)2-phenyl-2-butene (16)naphthalene(萘)HO5、写出下列反应的反应物构造式。
分子结构4 PPT课件

第七章 化学键与分子结构
二、氢键的形成
如 HF分子之间的氢键,F - H ····F - H 又如水分子之间的氢键
氢键的形成有两个条件: 有与电负性大且半径小的原子 ( F,O, N ) 相连的H ; 在附近有电负性大,半径 小的原子 ( F,O,N ) 。
第四节 分子间作用力和氢键
5、为什么常温下Cl2是气体,Br2是液体,I2是固体?
第四节 分子间作用力和氢键
F-H···F E/kJ ·mol-1 28.0
O-H···O 18.8
N-H···N 5.4
第四节 分子间作用力和氢键
第七章 化学键与分子结构 氢键有分子间氢键和分子内氢键
H OO
N O
分子间氢键
OH
N
O
O
分子内氢键
第四节 分子间作用力和氢键
第七章 化学键与分子结构
四、氢键对化合物性质的影响 1、对分子熔沸点的影响
取向力 诱导力 色散力
第四节 分子间作用力和氢键
第七章 化学键与分子结构
一、取向力
两个永久偶极间存在的同极相斥、异极相吸的定向作用
+
+_ +_
+_
_
分子离得较远
取向
取向力只存在于极性分子之间。
第四节 分子间作用力和氢键
第七章 化学键与分子结构
二、诱导力
由于诱导偶极-永久偶极之间相互作用所产生的。
第四节 分子间作用力和氢键
第七章 化学键与分子结构 3、永久偶极------极性分子本身所固有的
极性分子放入电场中
第四节 分子间作用力和氢键
第七章 化学键与分子结构
7-4-2 分子间作用力
人教版化学必修第二册同步练习第7章 第4节 第3课时基本营养物质 (原卷版+解析版)

第七章第4节基本营养物质(原卷版)基础达标一、选择题(每小题只有一个选项符合题意)1.昆虫信息素是昆虫之间传递信号的化学物质。
人工合成信息素可用于诱捕害虫、测报虫情等。
一种信息素的分子结构简式如图所示,关于该化合物说法不正确的是()A.属于烷烃B.可发生水解反应C.可发生加聚反应D.具有一定的挥发性2.下列有机物按碳的骨架进行分类,其中与其他三种有机物属于不同类别的是()3.科学家在-100 ℃的低温下合成了一种烃X,此分子的结构如图所示(图中的连线表示化学键)。
下列说法不正确的是()A.X在常温下不能稳定存在B.X的性质与烯烃类似,容易发生加成反应C.X不能使酸性KMnO4溶液褪色D.充分燃烧等质量的X和甲烷,X消耗氧气比甲烷少4.下列物质中,碳碳间成键方式与其他不同的是()A.C2H6B.苯C.D.聚乙烯5.“化学是五颜六色的”是指在化学实验中有着丰富多彩的颜色变化。
下列有关反应获得的颜色不正确的是()①红②橙③黄④绿⑤青⑥蓝⑦紫A.乙烯气体通入酸性高锰酸钾溶液中:⑦B.淀粉遇碘:⑥C.蛋白质遇浓硝酸:③D.热的氧化铜遇酒精:①6.下表为某有机物与各种试剂的反应现象,则这种有机物可能是()二、非选择题7.100多年前,“化学守护神”德国化学家李比希发现了一种至今仍在临床使用的催眠药(化合物Ⅳ)。
由源自石油的基本化工原料Ⅰ合成化合物Ⅳ的一种途径为(1)由化合物Ⅰ合成化合物Ⅱ的反应类型为。
(2)下列关于化合物Ⅰ和化合物Ⅱ的说法正确的有(填字母)。
A.化合物Ⅰ可以作为植物生长调节剂B.化合物I能发生加聚反应,不能使酸性KMnO4溶液褪色C.化合物Ⅱ能发生酯化反应D.化合物Ⅱ不能与金属Na反应(3)由化合物Ⅲ合成化合物Ⅳ的反应的原子利用率为100%,则除化合物Ⅲ外,另一种反应物是。
(4)化合物Ⅰ含有的官能团是碳碳双键(填名称),化合物Ⅱ与Ⅳ都含有的官能团是(填名称),化合物Ⅳ的分子式为。
8.石油是工业的血液,与我们的生产、生活息息相关,乙烯的产量通常用来衡量一个国家的石油化工水平。
高中化学必修二第七章《有机化合物》经典习题

一、选择题1.下列有关化学用语使用正确的是( )A .干冰的电子式:B.S 的原子结构示意图:C .氧化钠的电子式:D.原子核内有18个中子的氯原子:3517Cl 2.乙烯的结构简式是A.C2H4B.CH2=CH2C.CH2CH2D .3.化学在切断传播途径,防控新冠肺炎疫情的过程中发挥了重要作用。
下列说法正确的是A.新冠病毒的外壳蛋白质是小分子B.医用酒精通过氧化灭活病毒C.医用口罩可以水洗重复使用D.抗病毒疫苗冷藏存放避免蛋白质受热变性4.下列反应中,属于取代反应的是()A.乙烯与溴反应制1,2-二溴乙烷B.苯与浓硝酸、浓硫酸混合共热制取硝基苯C.乙烯使酸性高锰酸钾溶液褪色D.在一定条件下苯与氢气反应制取环己烷5.“人造肉”一般分为两种,一种是被称为植物肉的“人造肉”,主要以大豆等植物蛋白制成。
另一种是用动物干细胞制造的“人造肉”,从活的鸡鸭鱼牛羊猪身上采集干细胞,然后在实验室培养。
下列说法不正确的是()A.肉的主要成分是蛋白质,而蛋白质是生命的基础B.蛋白质水溶液加入饱和Na2SO4溶液,有沉淀析出C.人造肉在一定程度上能减少动物的屠杀D.人体自身能合成的氨基酸称为必需氨基酸6.根据下列实验操作和现象所得出的结论正确的是选项实验操作和现象实验结论A 向淀粉溶液中加入稀硫酸,水浴加热一段时间后,加入NaOH溶液至溶液呈碱性,再加入新制Cu(OH)2悬浊液,加热煮沸,有砖红色沉淀产生淀粉已水解完全B 卤代烃Y与氢氧化钠溶液共热后,滴加AgNO3溶液,观察,无淡黄色沉淀产生说明卤代烃不是溴代烃C 向浑浊的苯酚试液中滴加饱和Na2CO3溶液,试液变澄清且无气体产生说明苯酚的酸性强于碳酸D 向蛋白质溶液中滴加饱和Na2SO4溶液,有固体析出,过滤,向固体中加足量蒸馏水,固体溶解蛋白质的盐析过程是可逆的A.A B.B C.C D.D7.下列食物属于酸性食物的是A.柠檬B.苹果C.生菜D.火腿肠8.下列物质既能使酸性高锰酸钾溶液又能使溴水(发生化学反应)褪色的是A.乙烯B.乙烷C.乙醇D.苯9.下列有机物中不属于...烃类物质的是()A.乙烷B.乙烯C.乙酸D.苯10.下列实验中观察不到..颜色变化的是A.葡萄糖与新制的氢氧化铜悬浊液共热B.向氯化钠溶液中滴加硝酸银溶液C.氯气通入紫色石蕊试液D.二氧化碳通入稀氢氧化钠溶液二、填空题11.将一根下端绕成螺旋状的铜丝烧至表面由红变黑,迅速插入盛有乙醇的试管中,铜丝表面又由黑变红,反复多次,闻到有别于乙醇气味的特殊气味。
有机化学课后习题答案7第七章答案
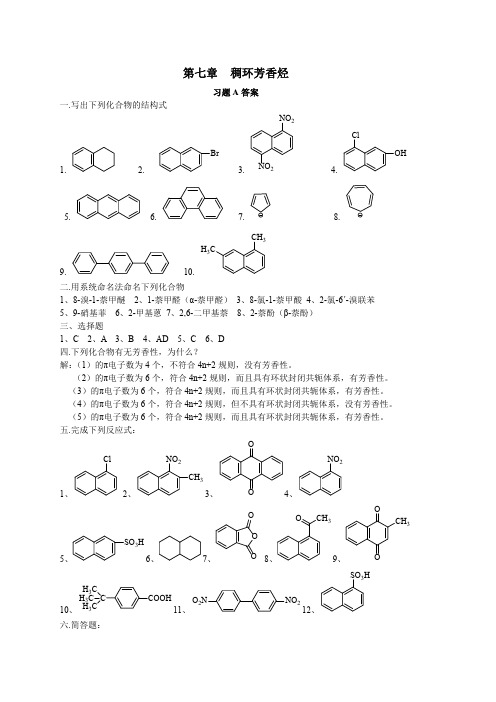
4.
V2O5, O2
一. 命名或写出结构式
1.
2. C2H5
NO2
Br2 Fe
NO2 Br
O
O
O
O
浓H2SO4
AlCl3 O
COOH
O
习题 B 答案
CH3 3.
OH 4.
SO3H
H3C
5.
6.
7. 2-乙基-9,10-蒽醌 8. 2-环丙基萘
9. 1,4-二甲基萘 10. 邻苯二甲酸酐
二.用休克尔规则判断下列化合物是否有芳香性
CHO
CHO
CH3 NBS
O2, V2O5 400-500℃
CH2MgBr 无水乙醚
CH2Br Mg 无水乙醚
CH2MgBr
O
O AlCl3
O
O Zn-Hg HCl
HOOC
H2SO4 HOOC
H3O+
H2/Ni HO CH2
H2SO4 HO CH2
O CH2
5.
O
O
Zn-Hg
浓H2SO4
O AlCl3
第七章 稠环芳香烃
一.写出下列化合物的结构式
习题 A 答案
NO2
Cl
Br
OH
1.
2.
3. NO2
4.
5.
6.
7.
8.
CH3 H3C
9.
10.
二.用系统命名法命名下列化合物 1、8-溴-1-萘甲醚 2、1-萘甲醛(α-萘甲醛) 3、8-氯-1-萘甲酸 4、2-氯-6ˊ-溴联苯 5、9-硝基菲 6、2-甲基蒽 7、2,6-二甲基萘 8、2-萘酚(β-萘酚) 三、选择题 1、C 2、A 3、B 4、AD 5、C 6、D 四.下列化合物有无芳香性,为什么? 解:(1)的π电子数为 4 个,不符合 4n+2 规则,没有芳香性。
07第7章_芳烃

+
R
C X
注意:
每类反应的特点; 比较苯、甲苯和硝基苯的反应活性; 反应机理。
总目录
1. 硝化反应
注意1:反应 温度、试剂浓 度的差别!
注意2: 引入取代基的位置!
总目录
两个取代基定位作用一致
两个取代基定位作用不一 致,致活基团起主导作用
总目录
思考
(1)浓硫酸起什么作用? (2) 从反应条件(试剂浓度、反应温度),看几种 单环芳烃的硝化活性。
6个Csp2— Csp2键 6个C—H键
Csp2杂化(垂直的p 轨道未画出)
总目录
(2)6个p 轨道平行重叠形成大π键
碳原子的p轨道
苯分子的大π 键
总目录
苯环所有键示意图
总目录
2. 分子轨道理论解释
(1)苯的骨架结构(同上) (2)6个p 原子轨道线性组合成6个分子轨道:
反键轨道 原子轨道 成键轨道
第四节 苯环的亲电取代定 位效应 一、定位效应 二、定位效应的解释 三、定位效应的应用 第五节 多环芳烃 一、联苯 二、稠环芳烃 第六节 非苯系芳烃 一、芳香性的几个特征 二、休克尔规则 三、非苯芳烃 四、大环芳烃 第七节 富勒烯与C60
ห้องสมุดไป่ตู้
总目录
脂肪烃
aliphatics
烃
芳香烃
aromatic hydrocarbons
+
总目录
(2)反应机理—— 亲电加成-消除反应历程
σ 络合物 (该中间体亲电取代都经历) 亲电加成 消除
说明σ 配合物的生成决速步骤
总目录
σ 配合物: 碳原子杂化态从sp2转化为sp3,大π
键被破坏,4个π电子离域于环上5 个碳原子上,使苯环呈正电荷。
《有机化学》(第四版)第七章卤代烃(习题答案)

第七章卤代烃相转移催化反应邻基效应思考题P235 习题用普通命名法命名下列各化合物,并指出它们属于伯、仲、叔卤代烷中的哪一种。
(1) (CH3)3CCH2Cl (2) CH3CH2CHFCH3 (3) CH2=CHCH2Br解:(1) 新戊基氯 (伯卤代烷) (2) 仲丁基氟(仲卤代烷) (3) 烯丙基氯(伯卤代烷)习题用系统命名法命名下列各化合物,或写出结构式。
(1)CH3CHCHCH2CHCH3CH3CH3Cl2,3-二甲基-5-氯己烷 (2)CH3CHCH2C CHCH33Cl2-甲基-3,3,5-三氯己烷(3) BrCH2CH2CHCH2CH2CH3C2H53-乙基 -1-溴己烷 (4) CH3CH2CHCH2CH3CH2Cl3-氯甲基戊烷(5) Cl1-环戊基-2-氯乙烷或 氯乙基环戊烷 (6)CH3Cl1-甲基-1-氯环己烷(7) CH3CH3CH2Cl1,1-二甲基-2-氯甲基环戊烷 (8)Cl1-氯双环[2.2.1]庚烷(9)CH 3CH CH 2CH 2BrCH 3异戊基溴 (10)CH 3CH 2CH 2CH 3H Br(R)-2-溴戊烷P236 习题 命名下列各化合物:(1) Cl 2CHCH=CH 23,3-二氯-1-丙烯(2) CH 3CHCH=CHCH 3Cl4-氯-2-戊烯(3)CH 3Br1-甲基-4-溴-2-环戊烯(4)BrCl 1-氯-4-溴苯(5)CH=CHCH 2CH 2Br 1-苯-4-溴-1-丁烯(6)CH 2CH=CH 2ClBr2-氯-4-溴烯丙基苯3-(2-氯-4-溴苯基)-1-丙烯P236 习题 写出下列各化合物的构造式或结构式:(1)4-溴-1-丁烯-3-炔CH 2=CH C CBr(2) 反-1,2-二氯-1,2-二苯乙烯C=C ClPhPh(3)对氯叔丁苯ClC(CH 3)3(4) -溴 代乙苯CHCH 3P239 习题 试预测下列各对化合物哪一个沸点较高。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章习题
1。 指出下列离子分边属于何种电子构型:
Ti4+, Be2+, Cr3+, Fe2+, Ag+, Cu2+, Zn2+, Sn4+, Pb2+, Tl+, S2—, Br
—
2。 已知KI的晶格能(U)为-631.9 kJ·mol—1,钾的升华热[S(K)]为90。0 kJ·mol—1,钾
的电离能(I)为418.9 kJ·mol—1,碘的升华热[S(I)]为62。4kJ·mol-1,碘的解离能(D)为151
kJ·mol—1,碘的电子亲核能(E)为—310。5 kJ·mol-1,求碘化钾的生成热(△fH)
3. 根据价键理论画出下列分子的电子结构式(可用一根短线表示一对公用电子)
BCl3, PH3, CS2, HCN, OF2, H2O2, N2H4, AsCl3, SeF6
4. 试用杂化轨道理论说明BF3是平面三角形,而NF3是三角锥形.
5. 指出下列化合物的中心原子可能采取的杂化类型,并预测其分子的几何构型。
BBr3, SiH4, PH3, SeF
6
6. 将下列分子按照键角从大到小排列:
BF3, BeCl2, SiH4, H2S, PH3, SF6
7。 用价层电子对互斥理论预言下列分子和离子的几何构型.
CS2, NO2—, ClO2-, I3—, NO3-, BrF3, PCl4+, BrF—, PF5, BrF5, [AlF6]
3—
8。 根据分子轨道理论比较N2和N2+键能的大小。
9. 根据分子轨道理论判断O2+, O2, O2-, O22-的键级和单电子数.
10. 用分子轨道理论解释:
(1)氢分子离子H2+可以存在。
(2)Be2为顺磁性物质。
(3)N2分子不存在。
11. 试问下列分子中哪些是极性的?那些是非极性的?为什么?
CH4, CHCl3, BCl3, NCl3, H2S, CS2
12. 试比较下列各对分子偶极矩的大小:
(1) CO2和CS2 (2) CCl4和CH4 (3)PH3和NH3
(4)BF3和NF3 (5)H2O和H2S
13. 将下列化合物按熔点从高到低的顺序排列:
NaF,NaCl,NaBr,NaI,SiF4,SiCl4,SiBr4,SiI4
14。 试用离子极化观点解释:
(1)KCl熔点高于GeCl4
(2)ZnCl2熔点低于CaCl2
(3)FeCl3熔点低于FeCl
2
15. 下列说法是否正确?为什么?
(1)分子中的化学键为极性键,则分子也为极性分子。
(2)Mn2O7中Mn(Ⅶ)正电荷高,半径小,所以该化合物的熔点比MnO高。
(3)色散力仅存在与非极性分子间.
(4)3电子π键比2电子π键的键能大。
16. 指出下列各对分子间存在的分子间作用力的类型(取向力、诱导力、色散力和氢键):
(1)苯和CCl4 (2)甲醇和H2O
(3)CO2和H2O 4)HBr和HI
17。 下列化合物中哪些自身能够形成氢键?
C2H6, H2O2, C2H5OH, CH3CHO, H3BO3, H2SO4, (CH3)2O
18。 比较两种化合物熔沸点高低,并说明原因。
(1)乙醇(C2H5OH)和二甲醚(CH3OCH3)组成相同,但前者的沸点为78.5℃,而后者的沸点
为-23℃,为什么?
(2)OHCHO和 OHCHO 组成也相同,但前者的熔点为_,后者的熔点为_,
这又是为什么?
19。 比较下列各组中两种物质的熔点高低,并简单说明原因.
(1)NH3和PH3 (2)PH3和SbH3 (3)Br2和ICl
(4)MgO和NaO (5)SiO2和SO2 (6)SnCl2和SnCl4
20。填充下表
物质 晶格上质点 质点间作用力 晶体类型 熔点高低
MgO
SiO2
Br2
NH3
Cu
21.由N2和H2每生成1molNH3,放热46.02kJ,而生成1molNH2-NH2却吸热96.26kJ。又知
H-H键能为436kJ·mol-1, N=N键能为945kJ·mol-1。求:
(1)N-H键的键能:
(2)N-N单键的键能。
