芳香性和芳香族化合物取代反应
第7章芳香族化合物

三、苯及其同系物的化学性质 ———芳香烃的特征反应 ***1 ***1、亲电取代反应 ———芳香烃的特征反应 (1)卤化反应 Cl
+ Cl2 FeCl3 + HCl
机理: 机理: Cl Cl + FeCl3
+
H Cl
Cl
Cl+
Cl FeCl3
H Cl
(FeCl4 + Cl+)
+
Cl
+
+ FeCl4CH3 +Cl2 FeCl3
+ FeCl3 + HCl
CH3 Cl
取 代 反 应
离 子 型 游 离 基
CH3 + Cl +2HCl
CH3 hv +Cl2
CH 2Cl
+
HCl
δ+
δ−
+
H E
+
H
+ E+
慢
E
快 σ配合物 (碳正离子)
hv Cl . + Cl .
CH2 .
E + H+
亲电试剂
链引发 自 由 基 取 代
Cl2
CH3
α 8 β7 β6 5 α 10 γ 4 α γ 9 α 1 2β 3β
CH3
2-甲基蒽
γ 9 8 γ 10 6 1α 2β 6 β 5 α 4 α 3 β 3 2
1
α β 7
5 4
7 8 9
10
芘
致癌烃
j i h g f e d c k l mn a b
二苯并[ 二苯并[a,h]蒽 h]蒽 1,2,5,6二苯并蒽 1,2,5,6二苯并蒽
第二章 10芳香性
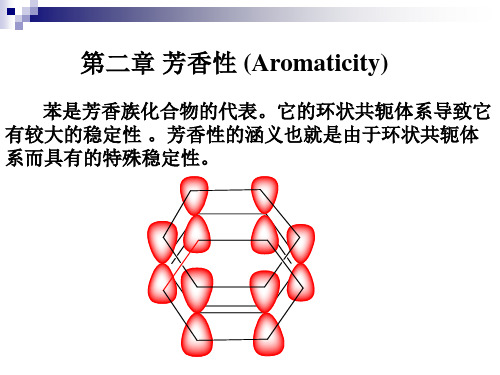
H 即 H H
H
环丙烯
H
环丙烯正离子
H
环丙烯正离子中的碳—碳键长都是0.140nm,因此它的电子 不是固定在其两个碳原子之间而是离域的,正电荷不是集中 于某一原于上,而是分布在由三个碳原于组成的共轭体系 中 三原子二电子π 体系。
环丙烯正离的正电荷离域
+
环丙烯正离子本身和它的某些取代的衍生物已被合成, 例如:
C6H5 C6H5 BF4ˉ C6H5 Cl Cl AlCl4ˉ
Cl
事实上,三丙基环丙烯正离于是最稳定的正碳离子之 一,甚至在水溶液中它还是稳定的。三叔丁基环丙烯正离 子也是很稳定的。此外,环丙烯酮也是稳定的化合物。
O
环丙烯酮
O-
环丙烯负离子的情况与相应的正离子就不同了
环丙烯负离子的四电子体系不符合Hückel规则,因而 它没有芳香性。
O O
卓酚酮是卓酮的羟基游衍生物。
或写作
OH O
O O H
2.6 八元环的π体系
虽然环辛四烯没有芳香性,但在环辛四烯分子中除去两个电子 的双正离子和增加两个电子的双负离子都是存在的,并都有一定程 度的芳香性。前者相当于六电子体系,后者相当于十电子体系,都 符合4n+2规则,前者n=1,后者n=2。它们的分子轨道和基态时 的电子排布如下图所示: 环辛四烯双负离子的存在需要有两个负电荷置于同一环上,这只 能用芳香性来解释。
2.3 四元环的π体系
环丁二烯π电子不符合4n+2规则,它没有芳香性。
按照Hückel规则,如果在环丁二烯分子中减去两个电 子,则将成为二电子体系,也就可以具有芳香性。同预测 的情况一致,下列化合物已被合成,并可代表具有芳香性 的二电子体系。
R R
有机化学基础知识点芳香性与芳香烃的性质

有机化学基础知识点芳香性与芳香烃的性质有机化学基础知识点——芳香性与芳香烃的性质有机化学是研究有机物质及其反应机理的一门学科,其中芳香性与芳香烃是其中重要的知识点之一。
本文将着重介绍芳香性以及芳香烃的性质,帮助读者更好地理解有机化学中的这一概念。
一、芳香性的定义与特点芳香性是指具有特殊结构和性质的有机化合物所表现出的香味和稳定的π电子结构。
根据芳香性的定义,芳香性化合物需要满足以下几个条件:1. 分子结构中含有一个或多个芳环(由6个共轭π电子组成的环状结构);2. 芳环中每个原子都以杂化sp2形式存在,磁性势能相对稳定;3. 芳环中的每个杂化的p轨道上都有一个未被配对的π电子。
值得注意的是,非芳香性化合物虽然可能具有香味,但其分子结构不符合芳香性的定义。
二、芳香烃的分类与性质芳香烃是一类基础的有机化合物,其分子中至少含有一个芳环。
根据芳香烃分子中芳环的个数及其它官能团,芳香烃可以分为以下几类:1. 单核芳香烃:只含有一个芳环的芳香烃。
例如,苯(C6H6)是最简单的芳香烃,其分子结构中含有一个六元环。
2. 多核芳香烃:含有两个或多个连接在一起的芳环的芳香烃。
最常见的多核芳香烃是萘(C10H8),它由一个苯环和一个呈共轭连结的五元环组成。
3. 取代芳香烃:分子中的芳环上存在取代基的芳香烃。
通过对芳环中的氢原子进行取代,可以获得各种不同性质和用途的化合物。
芳香烃的一些重要性质包括:1. 稳定性:芳香烃具有相对较高的稳定性,这是因为芳香烃分子中的共轭π电子系统能够稳定结构和分子。
2. 可溶性:大多数芳香烃在非极性溶剂中具有较好的溶解性,但在水中溶解度较低。
3. 反应性:芳香烃在化学反应中常常表现出亲电取代反应、脱氢反应等特性。
三、应用与实际意义芳香烃是有机化学中重要的化合物类别之一,其应用领域非常广泛。
以下是一些芳香烃的应用和实际意义:1. 燃料:芳香烃类化合物广泛应用于燃料行业,用作汽车燃料和燃气等能源。
8-芳烃,芳核亲电取代

缓慢进行,控制体系的温度。硝化和卤化都是不可逆的反应。
上页
下页
返回
Mechanism for the Nitration of Benzene
上页
下页
返回
3. 磺化反应
苯与98%的浓硫酸在75-80℃时发生反应,苯环上的氢原子被磺酸基取
代生成苯磺酸,在有机化合物的分子中引入磺酸基团的反应称为磺化反应。
+ 浓 H2SO 4 80℃
SO3H
+ H2O
SO3H
H2SO 4, SO 3 30~50℃
SO3H
反应可逆,生成的水 H2SO 4 变稀,磺化速度 使 变慢,水解速度加快,故 常用发烟硫酸进行磺化, 以减少可逆反应的发生。
若在较高温度下,继续反应,则生成间苯二磺酸。
SO3H H2SO4/SO3 200~250℃ SO3H 间苯二磺酸
CH3
(二)、命名(Nomenclature)
1、芳烃(仅含有C、H两种元素)
(1)、烷基取代苯(侧链为烷基, 以苯为母体)
A、单取代芳烃 ——通常称为某烷基苯,“基”字一般省略。
上页
下页
返回
CH3
CH2CH3
CH(CH3)2
C(CH3)3
甲(基)苯
乙(基)苯
异丙(基)苯
叔丁(基)苯
B、二取代芳烃 (多取代苯) 由于取代基在苯环上的相对位置不同,可以有三种不同 的异构体,两个取代基的相对位置可以用阿拉伯数字表示, 也可以用词头“邻(ortho,简写o-)、间(meta,简写m) 、对(para,简写p- )”来表示。
第八章、芳烃( Aromatics)
2单环芳烃 的同分异 构及命名
1苯的结构
第5章 芳香性

桥基共扼体系化合物E、F也可以使分子变成平面分子,
因此这些分子都具有芳香性。
H H O
Ac N
D
E
F
② [14]-轮烯
[14]-轮烯有明显的反磁环流,而且具有键长交替现象。 它有两种较稳定的处于平衡中的构型异构体A和B 。[14]轮烯的内腔要比[10]-轮烯大,故环内氢的干扰相对较小, [14]-轮烯的3,6,10和13位碳有点偏离平面。
环体系不在一个平面里。而表现出非芳香
性。
① [10]-轮烯
即环癸五烯,具有三种异构体。A和C度不稳定,B碳原
子按类似萘的骨架排列,它的角张力最小,但是两个环内氢 原子的非键斥力严重地阻碍了环的稳定性。 [10]-轮烯不显
芳香性。
H
H
A
B
C
全顺式
反-顺-反-顺-顺五烯
顺-顺-顺-顺-反
[10]-轮烯不显芳香性,有人用架桥基取代这两个环 内氢(图D)能使分子变成平面分子体系。以杂原子为架
休克尔的分子轨道理论揭示了结构和芳香性
的关系。HMO法计算可以得出环状共扼多烯分子
轨道的能量。根据Pauli不相容原理和能量最低原理。
基态分子的 电子优先占据成键分子轨道并把这些
轨道全都填满时,分子就是稳定的。
3
6
+ 1 .4 1 + 1 .4 1 +2
则。因为它可以存在着下列偶极形式而呈现芳香 性,使体系稳定。
O
或
O
2.五元环
① 环戊二烯 环戊二烯的酸性所得到的环戊二烯负离子具有芳香性, 它符合4n+2规则,6个π电子均匀地分布在环上五个原子 所在的分子子轨道中。
H
高四5章 芳烃芳香性

CH2Cl 苯氯甲烷 氯苄
•
C6H5- 苯基(Ph-) ;
C6H5CH2- 苄基 ;
Ar- 芳基(芳环上去掉一个氢后,所剩下的原子团);
5.2 苯的结构
5.2 苯的结构
仪器测得: 苯分子中12个原子共平面。所有的C-C键长为0.140nm,所 有的C-H键长为0.108nm,键角∠CCH及∠CCC均为120º 。
(Å ð)
(Å ð)
OCH3
x
CH3
(Å ð)
此外,温度和催化剂等对异构体的比例也有一定的影响。
5.5 苯环上取代反应的定位规则 5.5.3 二取代苯的定位规则
当苯环上已有二个取代基时,第三个基团进入苯环位置主要
(2) 硝化
+ HNO3
浓H2SO4
50-60 C
。
NO2 + H O 2
硝基苯
若苯环上已有取代基:
NO2 + 发烟HNO3
发烟H 2SO 4 90 C
NO2 。 NO2
间二基苯 93%
(苯环钝化)
CH3 + HNO3
H2SO 4 30 C
CH3 。 NO2 +
邻硝基甲苯 58%
CH3
(苯环活化)
NO2
② 1600、1500、1580、1450cm-1处苯环呼吸振动;
③ 900~650cm-1处(指纹区)一系列γC-H面外弯曲振动可 提供苯环上的取代信息。
例:邻二甲苯、间二甲苯、对二甲苯的IR谱图。
单环芳烃的NMR谱图特征:
δ苯氢≈7.25 例:甲苯、异丙苯的NMR谱图。
第五章
芳烃
芳香性
5.4 单环芳烃的化学性质
有机化学学习笔记:第九章芳香烃

CH3 CH3
1,3-二甲苯 (m-二甲苯)
C2H5
CH 3 CHCH 3
C H
3
1,4-二甲苯 (p-二甲苯)
乙苯
异 丙 苯
B. 以苯作为取代基的命名
CHO
C H = C H 2
C H 3 C H C O O H 2 C H C = C H 3
苯 甲 醛
苯 乙 烯
苯 乙 酸
1 苯 基 2 甲 基 丙 烯
A l C l 3 C H C H C H C H 3 2 2 2
C H C H C H 2 3 C H C H C H C H 2 2 2 3 CH3 主产物 C H C H C H 2 3 C H 3
重 排
次 产 物
CH2CH2CH2CH3
A l C l 3 + F C H C H C H C l 222
各种取代基在苯环上时作为母体的优先顺序
O O O C O O HS O HC O R C N H C XC N 3 2 O O C H C R O HN H O RRXN O 2 2
O 作 为 母 体 时 称 为 “醛 ” 对 羟 基 苯 甲 醛 对 甲 酰 基 苯 甲 酸 C H 为 取 代 基 时 称 为 “甲 酰 基 ” C H O 作 C H O
O H C O O H
N O
2
对 硝 基 氯 苯
C l
O H
C H
3
C H
3
对 -氯 甲 苯
C l
N H
2
对 甲 基 苯 胺
N H
2
对 氨 基 苯 酚
C. 稠环芳烃的命名
8 7 6 5 4 1 2 3 7 6 5 1 0 4 8 9 1 2 3
第6章 芳香烃及亲电取代反应(有机化学)

180℃
+ H2SO4
SO3H
+
H3 O
+ H2SO4
磺化产物与水共热的可逆,可用于有机合成的苯环的定位。
CH3 + H2SO4
CH3
HNO3 H2SO4
O2N
CH3
NO2
H2O
O2N
CH3 NO2
SO3H
SO3H
6.4.4 付-克反应
法国有机化学家付瑞德(C.Friedel)和美国化学家克拉夫茨 (J .M .Crafts)两人共同发现的,叫做付瑞德-克拉夫茨烷基 化反应,简称付-克烷基化反应。付-克反应分为两类: 付-克烷基化反应,即在苯环上引入烷基 付-克酰基化反应,即在苯环上引入酰基。 两种反应都是在Lewis酸(常用无水三氯化铝)作用下进行的。 付-克反应也是可逆的。
第6章 芳香烃及亲电取代反应
本章内容 6.1 芳烃的分类及单环的同分异构和命名 6.2 苯的结构 6.3 单环芳烃的物理性质 6.4 苯环上的亲电取代反应 6.5 亲电取代反应的定位规律和反应活性 6.6 芳烃侧链的反应 6.7 多环芳烃 6.8 芳香性
芳香族碳氢化合物简称芳香烃或芳烃
苯的六碳环结构
CH2Cl + H2O
[H2C OH] Cl
[H2C OH]Cl
MeO MeO
H2CO, HCl, ZnCl2
MeO
MeO
CH2Cl
E+
6.5 亲电取代反应的定位规律
1.定位规律 2.定位规律的理论说明 3.二元取代物的定位规律 4.合成中的应用
6.5.1 定位规律
第一类:邻对位活化定位基
这类基团连在苯环上,后进入苯环的取代基主要进入 它们的邻、对位,且亲电取代反应比苯更容易进行。
