试论环状化合物“芳香性”的判断方法
芳香性的判断
苯既具有平面的离域体系,电子数也符合4n+2规则; 萘、蒽、菲等也满足休克尔规则,因此都具有芳香性。
专题一
芳香性与休克尔规则
二、非苯型芳香烃
一些不含苯环的环烯,因符合休克尔规则,故也具有 芳香性,此类烃叫做非苯芳香烃。
(一)轮烯
[10]轮烯
[14]轮烯 [18]轮烯
专题一
芳香性与休克尔规则
二、非苯型芳香烃
专题一
芳香性与休克尔规则
三、休克尔规则的修正
1954年伯朗特(Platt)提出了周边修正法,认为可以 忽略中间的桥键而直接计算外围的电子数,对Hückel规则 进行了完善和补充。
两个前提:
使尽量多的双键处在外周上; 处在外周内外的双键写成其共振的正负电荷形式;
专题一
芳香性与休克尔规则
三、休克尔规则的修正
(二)芳香离子
环丙烯 正离子
环戊二烯 负离子
环庚三烯 正离子
专题一
芳香性与休克尔规则
二、非苯型芳香烃
(三)稠合环系
薁(蓝烃),为青蓝色片状物,符合休克尔规则具有芳香性
薁能发生典型的亲电取Βιβλιοθήκη 反应,取代基主要进入1位专题一
芳香性与休克尔规则
判断下列是否芳香性?
16个电子
12个电子
8个电子
都具有芳香性!
专题一
芳香性与休克尔规则
芳香性与休克尔规则
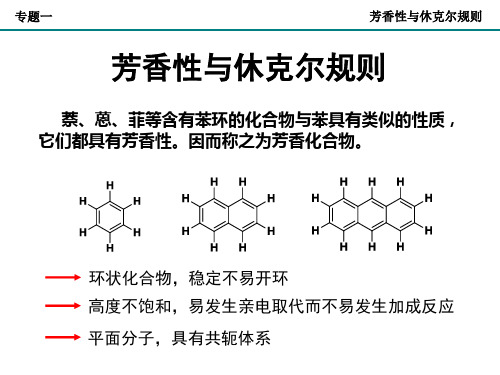
萘、蒽、菲等含有苯环的化合物与苯具有类似的性质, 它们都具有芳香性。因而称之为芳香化合物。
环状化合物,稳定不易开环 高度不饱和,易发生亲电取代而不易发生加成反应
平面分子,具有共轭体系
专题一
芳香性与休克尔规则
一、休克尔规则
成环原子处于同一平面,形成一个闭合的环状π电子 离域体系,且π电子数为4n+2(n = 0,1,2…)时,化合物 具有芳香性。
芳香性判断技巧

芳香性判断技巧-标准化文件发布号:(9556-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII一,芳香性判据——Hückel规则Hückel规则:一个单环化合物只要具有平面离域体系,它的π 电子数为4n+2(n=0,1,3,…整数),就有芳香性(当 n>7 时,有例外).对能看懂这篇文章的人说:苯有有芳香性,那就是废话了.非苯芳烃:凡符合Hückel规则,不含苯环的具有芳香性的烃类化合物,非苯芳烃包括一些环多烯和芳香离子等.二,一些非苯芳烃1.环多烯烃:(通式CnHn )又称作轮烯(也有人把n≥10 的环多烯烃称为轮烯).环丁烯,苯,环辛四烯和环十八碳九烯分别称[4]轮烯,[6]轮烯,[8]轮烯和[18]轮烯.它们是否具有芳香性,可按Hückel规则判断,首先看环上的碳原子是否均处于一个平面内,其次看π 电子数是否符合 4n+2.[18]轮烯环上碳原子基本上在一个平面内,π 电子数为 4n+2(n=4),因此具有芳香性.又如[10]轮烯,π 电子数符合 4n+2(n=2),但由于环内两个氢原子的空间位阻,使环上碳原子不能在一个平面内,故无芳香性.2,芳香离子:某些烃无芳香性,但转变成离子后,则有可能显示芳香性.如环戊二烯无芳香性,但形成负离子后,不仅组成环的 5 个碳原子在同一个平面上,且有 6 个π 电子(n=1),故有芳香性.与此相似,环辛四烯的两价负离子也具有芳香性.因为形成负离子后,原来的碳环由盆形转变成了平面正八边形,且有 10 个π 电子(n=2),故有芳香性.环戊二烯负离子其它某些离子也具有芳香性,例如,环丙烯正离子(Ⅰ),环丁二烯两价正离子(Ⅱ)和两价负离子(Ⅲ),环庚三烯正离子(Ⅳ).因为它们都具有平面结构,且π 电子数分别位 2,2,6,6,符合 4n+2(n 分别位0,0,1,1).具有芳香性的离子也属于非苯芳烃.3,稠环体系:与苯相似,萘,蒽,菲等稠环芳烃,由于它们的成环碳原子都在同一个平面上,且π 电子数分别为 10 和 14,符合 Hückel 规则,具有芳香性.虽然萘,蒽,菲是稠环芳烃,但构成环的碳原子都处在最外层的环上,可看成是单环共轭多烯,故可用 Hückel 规则来判断其芳香性.与萘,蒽,等稠环芳烃相似,对于非苯系的稠环化合物,如果考虑其成环原子的外围π 电子,也可用 Hückel 规则判断其芳香性.例如,薁(蓝烃)是由一个五元环和一个七元环稠合而成的,其成环原子的外围π 电子有 10 个,相当于[10]轮烯,符合 Hückel 规则(n=2),也具有芳香性.三.π 电子数的计算也许你在做题目的时候对于π 电子数的计算弄糊涂了,比如:觉得怎么同是N原子怎么有时候要把它的孤对电子算进去,有时候又不要呢.我以前就是这样的,现在基本知道判断芳香性了,只是有点经验,有些具体原理我还是不懂.下面是我的一些心得体会,若有错误还请留言指正.下面用的例子中的杂原子是N,其他原子类推.吡咯的N的孤对电子要算进去,在家两双键上的4个电子,共有6电子,有芳香性.吡啶中N原子上连有双键,N上孤对电子不能算进去,三双键共轭,共有6个π电子,有芳香性.两个N都与双键相连,孤对电子也都不算,还是6个π电子有一个N与双键相连,有一个没有.按以上的思路,与双键相连的N上的孤对电子不算进去,而右边的N原子上的孤对电子要算进去,结果也是6个π电子这种结构的也具有芳香性,看起来这个七元环没有达到共轭结构,我的也是经验,两双键中间隔了一个碳正离子,你就把这个碳正离子去掉再来计算π电子数,也是6个.注意:若隔的是碳负离子就不能这样了,一定要是碳正离子才可以这样算.这个和上面那个有点相似,但隔的是碳负离子,一个碳负离子算2个电子,图中有2个碳负离子,还有3个双键,有10个π电子.图中左边,一双键连接两个环,可以写出它的共振体,当然尽量往有芳香性的写,而且芳香性的环稳定,贡献大.这样下面的五元环有6π电子,上面的三元环有2π电子.都有芳香性.因为三键中两π键互相垂直,孤只有一个能与其他双键共轭,。
复杂多环化合物芳香性的简单判定方法_袁履冰

1 2 3 4
考
文
献
袁履冰 . 物理有机化学导论 . 大连 : 大连理工大学出版社 , 1989 王文清 . 芳香性和非苯芳香性化合物 . 北京 : 高等教育出版社 , 1985 张彩云 . 大学化学 , 1995( 2) : 20 谷杨 , 袁履冰 . 大学化学 , 2002, 17( 3) : 53
以形成离域的
用这种方法检验 (
法检验芳香性的存在 , 例如(
断如( ) 这样的化合物时 , 其方法就有一定的偏差 , 因为它们周边的 规则 , 可是事实却证明( ) 具有芳香性。 例如 : ( 50 ) 中间的双键并没有参与到离域的共轭
可以这样理解周边修正法 , 只有在一定的条件下 , 它才可以正确地判断化合物的芳香性。 电子中去, 如果忽略双键, 则只是化合物的 构型有所改变, 周边仍然是离域共轭的 电子体系 , 并符合 4 n + 2 规则。这里 , 中间的双键只
因此, 可以得出结论 , 当稠环的中间双键不对体系的离域共轭
电子系有影响时, 即其只
为保持整个化合物的平面结构时, 这样的双键才可以被忽略 , 这时才可以正确地应用周边修正 法。 2. 2 双键修正法 这是 H ckel 理论的另一修正方法, 这种修正法就是忽略某些双键在芳环体系中的影响 , 即可以忽略其中间的双键 , 直接考虑其芳香性问题。 这种方法的实际应用并不如周边修正法的应用那样广泛 , 但是同样可以应用其解决复杂 稠环芳烃的芳香性判定问题。 例如化合物 ( ) , 既无法应用周边修正法来说明其是否具有芳香性, 其 电子数目也不符 合 4 n + 2 规则, 但此化合物却具有芳香性。用什么方法能作为其芳香性的判据呢? 这里可以 使用双键修正法。
52
芳香性的判断

芳香性的判断
• 1931年德国化学家休克尔(Hückel)从分子轨道理论 的角度,对环状多烯烃(亦称轮烯)的芳香性提出了如 下规则,即Hückel规则。
14e
同芳香性
• 同芳香性是指共平面,π电子数为4n+2,共面的 原子均为sp2或sp杂化的轮烯上带有不与轮烯共 平面的取代基或桥。如:
H
R
10e 14e
反同芳香性
• 反同芳香性是指共平面,π电子数为4n,共面的 原子均为sp2或sp杂化的轮烯上带有不与轮烯共 平面的取代基或桥。如:
4e
8e
同芳结构的物质得到或失去电子成为4n体系是很 难的,因为要生成更不稳定的反同芳结构。
10e
6e
6e
14e
O
O
2e
6eΒιβλιοθήκη OO6e10e
6e
2e
• ②轮烯内部通过单键相连,且单键碳与轮 烯共用,单键忽略后,下列物质萘、蒽、 菲均有芳香性。
8e
10e
12e
14e
12e
14e
• ③轮烯外部通过单键相连,且单键碳与轮 烯共用,单键忽略后,分别计算单键所连 的轮烯的芳香性,下列物质均有芳香性。
• 其要点是:化合物是轮烯,共平面, • 它的π电子数为4n+2 (n为0,1,2,3…,n整数), • 共面的原子均为sp2或sp杂化。
1954年伯朗特(Platt)提出了周边修正法,认为可 以忽略中间的桥键而直接计算外围的电子数,对 Hückel规则进行了完善和补充。
Hückel理论的修正
芳香性判定

(个人感悟详细版)芳香性:环状闭合共轭体系,π电子高度离域,具有离域能,体系能量低,较稳定.在化学性质上表现为易进行亲电取代反应,不易进行加成反应和氧化反应,这种物理,化学性质称为芳香性. 一,芳香性判据——Hückel规则Hückel规则:一个单环化合物只要具有平面离域体系,它的π 电子数为4n+2(n=0,1,3,…整数),就有芳香性(当n>7 时,有例外).对能看懂这篇文章的人说:苯有有芳香性,那就是废话了.非苯芳烃:凡符合Hückel规则,不含苯环的具有芳香性的烃类化合物,非苯芳烃包括一些环多烯和芳香离子等.二,一些非苯芳烃1.环多烯烃:(通式CnHn )又称作轮烯(也有人把n≥10 的环多烯烃称为轮烯).环丁烯,苯,环辛四烯和环十八碳九烯分别称[4]轮烯,[6]轮烯,[8]轮烯和[18]轮烯.它们是否具有芳香性,可按Hückel规则判断,首先看环上的碳原子是否均处于一个平面内,其次看π 电子数是否符合4n+2.[18]轮烯环上碳原子基本上在一个平面内,π 电子数为4n+2(n=4),因此具有芳香性.又如[10]轮烯,π 电子数符合4n+2(n=2),但由于环内两个氢原子的空间位阻,使环上碳原子不能在一个平面内,故无芳香性.2,芳香离子:某些烃无芳香性,但转变成离子后,则有可能显示芳香性.如环戊二烯无芳香性,但形成负离子后,不仅组成环的 5 个碳原子在同一个平面上,且有 6 个π 电子(n=1),故有芳香性.与此相似,环辛四烯的两价负离子也具有芳香性.因为形成负离子后,原来的碳环由盆形转变成了平面正八边形,且有10 个π 电子(n=2),故有芳香性.环戊二烯负离子其它某些离子也具有芳香性,例如,环丙烯正离子(Ⅰ),环丁二烯两价正离子(Ⅱ)和两价负离子(Ⅲ),环庚三烯正离子(Ⅳ).因为它们都具有平面结构,且π 电子数分别位2,2,6,6,符合4n+2(n 分别位0,0,1,1).具有芳香性的离子也属于非苯芳烃.3,稠环体系:与苯相似,萘,蒽,菲等稠环芳烃,由于它们的成环碳原子都在同一个平面上,且π 电子数分别为10 和14,符合Hückel 规则,具有芳香性.虽然萘,蒽,菲是稠环芳烃,但构成环的碳原子都处在最外层的环上,可看成是单环共轭多烯,故可用Hückel 规则来判断其芳香性.与萘,蒽,等稠环芳烃相似,对于非苯系的稠环化合物,如果考虑其成环原子的外围π 电子,也可用Hückel 规则判断其芳香性.例如,薁(蓝烃)是由一个五元环和一个七元环稠合而成的,其成环原子的外围π 电子有10 个,相当于[10]轮烯,符合Hückel 规则(n=2),也具有芳香性.三.π 电子数的计算也许你在做题目的时候对于π 电子数的计算弄糊涂了,比如:觉得怎么同是N原子怎么有时候要把它的孤对电子算进去,有时候又不要呢.我以前就是这样的,现在基本知道判断芳香性了,只是有点经验,有些具体原理我还是不懂.下面是我的一些心得体会,若有错误还请留言指正.下面用的例子中的杂原子是N,其他原子类推.吡咯的N的孤对电子要算进去,在家两双键上的4个电子,共有6电子,有芳香性.(成环的四个碳原子和一个杂原子都是sp2杂化,所以你看的图中 N还要再连接一个H. N总共5个电子,连接了三个达到八电子饱和故其还有一对电子对未画出,所以是两个双键4个再加N的一对孤电子对2个总共六个)吡啶中N原子上连有双键,N上孤对电子不能算进去,三双键共轭,共有6个π电子,有芳香性.(貌似是一个原子提供一个π电子既然已经双键提供过一次就只算一次跟三键有点类似)两个N都与双键相连,孤对电子也都不算,还是6个π电子(跟刚才上面解释差不多相当于3个双键)有一个N与双键相连,有一个没有.按以上的思路,与双键相连的N上的孤对电子不算进去,而右边的N原子上的孤对电子要算进去,结果也是6个π电子(上面三个题的组合即没有双键的N提供电子对有双键的按提供一个所以是两个双键加一个电子对的2个π电子共六个)这种结构的也具有芳香性,看起来这个七元环没有达到共轭结构,我的也是经验,两双键中间隔了一个碳正离子,你就把这个碳正离子去掉再来计算π电子数,也是6个.注意:若隔的是碳负离子就不能这样了,一定要是碳正离子才可以这样算.(遇到这种没双键的但是有正负电子的我一般是先数双键然后数几个折角即连接处然后是正的话减去减去正的个数是负的话加上负的个数理论依据是正电荷的话使其sp杂化而负电荷的话使其sp2杂化)这个和上面那个有点相似,但隔的是碳负离子,一个碳负离子算2个电子,图中有2个碳负离子,还有3个双键,有10个π电子.(理由同上)图中左边,一双键连接两个环,可以写出它的共振体,当然尽量往有芳香性的写,而且芳香性的环稳定,贡献大.这样下面的五元环有6π电子,上面的三元环有2π电子.都有芳香性.(遇到这种先拆开难理解的双键然后再分成若干小原子团)因为三键中两π键互相垂直,孤只有一个能与其他双键共轭,(貌似是无机的知识三键算一个双键)。
芳香性判断

芳香性:环状闭合共轭体系,π电子高度离域,具有离域能,体系能量低,较稳定.在化学性质上表现为易进行亲电取代反应,不易进行加成反应和氧化反应,这种物理,化学性质称为芳香性. 一,芳香性判据——Hückel规则Hückel规则:一个单环化合物只要具有平面离域体系,它的π电子数为4n+2(n=0,1,3,…整数),就有芳香性(当 n>7 时,有例外).对能看懂这篇文章的人说:苯有有芳香性,那就是废话了.非苯芳烃:凡符合Hückel规则,不含苯环的具有芳香性的烃类化合物,非苯芳烃包括一些环多烯和芳香离子等.二,一些非苯芳烃1.环多烯烃:(通式CnHn )又称作轮烯(也有人把 n≥10 的环多烯烃称为轮烯).环丁烯,苯,环辛四烯和环十八碳九烯分别称[4]轮烯,[6]轮烯,[8]轮烯和[18]轮烯.它们是否具有芳香性,可按Hückel规则判断,首先看环上的碳原子是否均处于一个平面内,其次看π电子数是否符合 4n+2.[18]轮烯环上碳原子基本上在一个平面内,π电子数为 4n+2(n=4),因此具有芳香性.又如[10]轮烯,π电子数符合 4n+2(n=2),但由于环内两个氢原子的空间位阻,使环上碳原子不能在一个平面内,故无芳香性.2,芳香离子:某些烃无芳香性,但转变成离子后,则有可能显示芳香性.如环戊二烯无芳香性,但形成负离子后,不仅组成环的 5 个碳原子在同一个平面上,且有 6 个π电子(n=1),故有芳香性.与此相似,环辛四烯的两价负离子也具有芳香性.因为形成负离子后,原来的碳环由盆形转变成了平面正八边形,且有 10 个π电子(n=2),故有芳香性.环戊二烯负离子其它某些离子也具有芳香性,例如,环丙烯正离子(Ⅰ),环丁二烯两价正离子(Ⅱ)和两价负离子(Ⅲ),环庚三烯正离子(Ⅳ).因为它们都具有平面结构,且π电子数分别位 2,2,6,6,符合4n+2(n 分别位0,0,1,1).具有芳香性的离子也属于非苯芳烃.3,稠环体系:与苯相似,萘,蒽,菲等稠环芳烃,由于它们的成环碳原子都在同一个平面上,且π电子数分别为 10 和 14,符合 Hückel 规则,具有芳香性.虽然萘,蒽,菲是稠环芳烃,但构成环的碳原子都处在最外层的环上,可看成是单环共轭多烯,故可用 Hückel 规则来判断其芳香性.与萘,蒽,等稠环芳烃相似,对于非苯系的稠环化合物,如果考虑其成环原子的外围π电子,也可用 Hückel 规则判断其芳香性.例如,薁(蓝烃)是由一个五元环和一个七元环稠合而成的,其成环原子的外围π电子有 10 个,相当于[10]轮烯,符合 Hückel 规则(n=2),也具有芳香性.三.π电子数的计算也许你在做题目的时候对于π电子数的计算弄糊涂了,比如:觉得怎么同是N原子怎么有时候要把它的孤对电子算进去,有时候又不要呢.我以前就是这样的,现在基本知道判断芳香性了,只是有点经验,有些具体原理我还是不懂.下面是我的一些心得体会,若有错误还请留言指正.下面用的例子中的杂原子是N,其他原子类推.吡咯的N的孤对电子要算进去,在家两双键上的4个电子,共有6电子,有芳香性.吡啶中N原子上连有双键,N上孤对电子不能算进去,三双键共轭,共有6个π电子,有芳香性. 两个N都与双键相连,孤对电子也都不算,还是6个π电子有一个N与双键相连,有一个没有.按以上的思路,与双键相连的N上的孤对电子不算进去,而右边的N原子上的孤对电子要算进去,结果也是6个π电子这种结构的也具有芳香性,看起来这个七元环没有达到共轭结构,我的也是经验,两双键中间隔了一个碳正离子,你就把这个碳正离子去掉再来计算π电子数,也是6个.注意:若隔的是碳负离子就不能这样了,一定要是碳正离子才可以这样算.这个和上面那个有点相似,但隔的是碳负离子,一个碳负离子算2个电子,图中有2个碳负离子,还有3个双键,有10个π电子.图中左边,一双键连接两个环,可以写出它的共振体,当然尽量往有芳香性的写,而且芳香性的环稳定,贡献大.这样下面的五元环有6π电子,上面的三元环有2π电子.都有芳香性.因为三键中两π键互相垂直,孤只有一个能与其他双键共轭,http://206.108.48.51/forumdisplay.php?fid=63。
芳香性判断依据
有机化学期中论文学校院系:西北大学化工学院班级:化学工程与工艺学号:2009115065姓名:崔尧论碳环化合物的芳香性的判断摘要本文介绍碳环化合物的芳香性,非芳香性,反芳香性,同芳香性及反同芳香性简单判断的方法及在有机化学中的应用。
一芳香性,非芳香性,反芳香性,同芳香性及反同芳香性的判断芳烃一般具有苯环结构,它们是环状闭合共轭体系,π电子高度离域,体系能量低,较稳定。
在化学性质上表现为易进行亲电取代反应,不易进行加成和氧化反应,即具有不同程度的芳香性。
是不是具有芳香性的化合物一定具有苯环?1931年德国化学家休克尔(Hückel)从分子轨道理论的角度,对环状多烯烃(亦称轮烯)的芳香性提出了如下规则,即Hückel 规则。
其要点是:化合物是轮烯,共平面,它的π电子数为4n+2(n为0,1,2,3…,n 整数),共面的原子均为sp2或sp杂化。
1954年伯朗特(Platt)提出了周边修正法,认为可以忽略中间的桥键而直接计算外围的电子数,对Hückel规则进行了完善和补充。
但仍有一些不足之处[1]。
本文根据教学实践,提出了简单判断碳环化合物的芳香性、非芳香性、反芳香性、同芳香性及反同芳香性的方法及在有机化学中的应用[2]。
(1)芳香性一些稠环烃也可将之看成轮烯,画经典结构式时,应使尽量多的双键处在轮烯上,处在轮烯内外的双键写成其共振的正负电荷形式,将出现在轮烯内外的单键忽略后,再用Hückel -Platt规则判断。
(1)双键碳处在不与轮烯共用的内部,计算电子时,只计算轮烯上的电子,内部的不记。
下面的化合物A和D周边分别有双键6个和5个,如此时判断他们的芳香性就会造成错误。
而它们的B和E式分别有双键7个和6个,将内部的双键写成其共振的正负电荷形式C 和F后,将出现在轮烯内外的单键忽略后,用Hückel-Platt规则判断得A为芳香性物质,而D不是芳香性物质。
芳香性判断——精选推荐
芳香性判断13144233周楠乳品2班摘要 :探讨了几类环状化合物“芳香性”的判断方法 ,阐述了解决这类问题的基本思路.关键词:环状化合物 ;芳香性 ;判断方法。
正文:关于“芳香性”的早期定义是考虑动力学稳定性 ,即化合物的取代反应比加成反应更容易发生. 后来定义则依靠化学的稳定性 ,以共振能的大小来量度. 最近的定义提供用光谱及核磁的标准 ,磁有向性在平面π电子体系中能受感应 ,并可用质子磁共振 (Pmr)光谱中位移到较低的场来检定或借反磁性的灵敏度上升的测定 ,π电子流也产生电子光谱 ,和简单的共轭烯类所显示的光谱有重大的不同.关于“芳香性”的另一种物理标准 ,为整个芳香体系具有相同键长和共平面的特性 ,这种分析需要 X光结晶学、微波光谱或电子衍射技术。
一.关于芳香性概念芳香性是化学中使用频率最高且最重要的概念之一。
“芳香性”研究真正始于1825年,因为当年Michael Faraday 成功分离出具有特殊芳香气味的苯。
此后人们把具有类似气味的化合物统称为芳香化合物。
最初芳香性内涵特指像苯及其衍生物之类的有机分子的化学反应性质的总称,认为芳香分子,如苯、萘、蒽,是平面环状的、共轭的、含有4n+2个π电子,并且具有容易进行亲电取代反应,但不易发生加成、氧化等特殊的化学性质。
然而环丁二烯和环辛四烯化学性质活泼,分别具有4、8个π电子,则具有反芳香性。
容易看出,早期芳香性定义实际上是一个特别强调化学反应性能的“化学定义”。
随着研究的深入,当前芳香化合物已经先后扩展到杂原子分子、有机金属、全金属化合物。
在范畴上,已经成功地实现了从有机物到无机物、由非金属化合物到全金属化合物的过渡;在几何结构上,也从最初的二维平面分子延展到准平面分子,甚至三维封闭式笼状分子;类型上,由早期单纯的π型芳香性扩展到σ芳香性甚至δ芳香性。
二.常见芳香性判据及讨论芳香性的判据和定义是密切相关的。
所谓判据就是判断是否具有芳香性的依据或标准。
多环化合物的芳香性
多环化合物的芳香性摘要介绍了简单判断多环化合物的芳香性、非芳香性、反芳香性、同芳香性及反同芳香性的方法及其在有机化学中的应用。
关键词多环化合物芳香性反芳香性同芳香性1芳香性、非芳香性、反芳香性、同芳香性及反同芳香性的判断芳烃一般具有苯环结构,它们是环状闭合共轭体系,π电子高度离域,体系能量低,较稳定。
在化学性质上表现为易进行亲电取代反应,不易进行加成和氧化反应,即具有不同程度的芳香性。
是不是具有芳香性的化合物一定具有苯环?1931年德国化学家休克尔(Hückel)从分子轨道理论的角度,对环状多烯烃(亦称轮烯)的芳香性提出了如下规则,即Hückel规则。
其要点是:化合物是轮烯,共平面,它的π电子数为4n+2(n为0,1,2,3…,n整数),共面的原子均为sp2或sp杂化。
1954年伯朗特(Platt)提出了周边修正法,认为可以忽略中间的桥键而直接计算外围的电子数,对Hückel规则进行了完善和补充。
(1)芳香性(轮烯,共平面,π电子数为4n+2,共面的原子均为sp2或sp 杂化),一些稠环烃也可将之看成轮烯。
画经典结构式时,应使尽量多的双键处在轮烯上,处在轮烯内外的双键写成其共振的正负电荷形式,将出现在轮烯内外的单键忽略后,再用Hückel-Platt规则判断。
下面的化合物A和D周边分别有双键6个和5个,此时直接判断他们的芳香性就会造成错误。
所以首先应将他们改写成尽量多的双键处在轮烯上的B和E 式,B和E分别有双键7个和6个,将内部的双键写成其共振的正负电荷形式C 和F后,将出现在轮烯内外的单键忽略,用Hückel-Platt规则判断得A,G为芳香性物质,D不是芳香性物质。
①双键与轮烯直接相连,计算电子数时,将双键写成其共振的电荷结构,负电荷按2个电子计,正电荷按0计,内部不计。
如下面物质均有芳香性。
②轮烯内部通过单键相连,且单键碳与轮烯共用,单键忽略后,下列物质萘、蒽、菲均有芳香性。
芳香性判断技巧
芳香性判断技巧The final revision was on November 23, 2020一,芳香性判据——Hückel规则Hückel规则:一个单环化合物只要具有平面离域体系,它的π 电子数为4n+2(n=0,1,3,…整数),就有芳香性(当 n>7 时,有例外).对能看懂这篇文章的人说:苯有有芳香性,那就是废话了.非苯芳烃:凡符合Hückel规则,不含苯环的具有芳香性的烃类化合物,非苯芳烃包括一些环多烯和芳香离子等.二,一些非苯芳烃1.环多烯烃:(通式CnHn?)又称作轮烯(也有人把n≥10 的环多烯烃称为轮烯).环丁烯,苯,环辛四烯和环十八碳九烯分别称[4]轮烯,[6]轮烯,[8]轮烯和[18]轮烯.它们是否具有芳香性,可按Hückel规则判断,首先看环上的碳原子是否均处于一个平面内,其次看π 电子数是否符合 4n+2.[18]轮烯环上碳原子基本上在一个平面内,π 电子数为 4n+2(n=4),因此具有芳香性.又如[10]轮烯,π 电子数符合 4n+2(n=2),但由于环内两个氢原子的空间位阻,使环上碳原子不能在一个平面内,故无芳香性.2,芳香离子:某些烃无芳香性,但转变成离子后,则有可能显示芳香性.如环戊二烯无芳香性,但形成负离子后,不仅组成环的 5 个碳原子在同一个平面上,且有 6 个π 电子(n=1),故有芳香性.与此相似,环辛四烯的两价负离子也具有芳香性.因为形成负离子后,原来的碳环由盆形转变成了平面正八边形,且有 10 个π 电子(n=2),故有芳香性.环戊二烯负离子其它某些离子也具有芳香性,例如,环丙烯正离子(Ⅰ),环丁二烯两价正离子(Ⅱ)和两价负离子(Ⅲ),环庚三烯正离子(Ⅳ).因为它们都具有平面结构,且π 电子数分别位 2,2,6,6,符合4n+2(n 分别位0,0,1,1).具有芳香性的离子也属于非苯芳烃.3,稠环体系:与苯相似,萘,蒽,菲等稠环芳烃,由于它们的成环碳原子都在同一个平面上,且π 电子数分别为 10 和 14,符合 Hückel 规则,具有芳香性.虽然萘,蒽,菲是稠环芳烃,但构成环的碳原子都处在最外层的环上,可看成是单环共轭多烯,故可用 Hückel 规则来判断其芳香性.与萘,蒽,等稠环芳烃相似,对于非苯系的稠环化合物,如果考虑其成环原子的外围π 电子,也可用 Hückel 规则判断其芳香性.例如,薁(蓝烃)是由一个五元环和一个七元环稠合而成的,其成环原子的外围π 电子有 10 个,相当于[10]轮烯,符合 Hückel 规则(n=2),也具有芳香性.三.π 电子数的计算也许你在做题目的时候对于π 电子数的计算弄糊涂了,比如:觉得怎么同是N原子怎么有时候要把它的孤对电子算进去,有时候又不要呢.我以前就是这样的,现在基本知道判断芳香性了,只是有点经验,有些具体原理我还是不懂.下面是我的一些心得体会,若有错误还请留言指正.下面用的例子中的杂原子是N,其他原子类推.吡咯的N的孤对电子要算进去,在家两双键上的4个电子,共有6电子,有芳香性.吡啶中N原子上连有双键,N上孤对电子不能算进去,三双键共轭,共有6个π电子,有芳香性.两个N都与双键相连,孤对电子也都不算,还是6个π电子有一个N与双键相连,有一个没有.按以上的思路,与双键相连的N上的孤对电子不算进去,而右边的N原子上的孤对电子要算进去,结果也是6个π电子这种结构的也具有芳香性,看起来这个七元环没有达到共轭结构,我的也是经验,两双键中间隔了一个碳正离子,你就把这个碳正离子去掉再来计算π电子数,也是6个.注意:若隔的是碳负离子就不能这样了,一定要是碳正离子才可以这样算.这个和上面那个有点相似,但隔的是碳负离子,一个碳负离子算2个电子,图中有2个碳负离子,还有3个双键,有10个π电子.图中左边,一双键连接两个环,可以写出它的共振体,当然尽量往有芳香性的写,而且芳香性的环稳定,贡献大.这样下面的五元环有6π电子,上面的三元环有2π电子.都有芳香性.因为三键中两π键互相垂直,孤只有一个能与其他双键共轭,。
