有机化学基本概念
有机化学大一知识点归纳

有机化学大一知识点归纳一、有机化学的基本概念与性质有机化学是研究碳和氢以及它们的衍生物的化学性质和反应机理的科学。
它的研究对象包括有机化合物的结构、性质以及它们之间的相互作用。
1.1 碳的特殊性质碳具有四个价电子,可形成稳定的共价键,并能与其他原子进行多种多样的化学键合。
1.2 有机化合物的特点有机化合物通常具有较低的沸点、溶解度、比熔点和密度。
他们大部分是不导电的,但某些有机物能导电。
1.3 有机反应的特点有机反应具有多种多样的反应类型,包括加成、消除、取代、重排等。
它们往往需要催化剂或特定温度条件下进行。
二、有机化合物的结构与命名2.1 有机化合物的结构有机化合物的结构由碳骨架和官能团组成。
碳骨架是由碳原子通过共价键连接而成的丰富多样的结构,官能团则是在碳骨架上的特定原子或原子团。
2.2 命名有机化合物的常用规则有机化合物的命名一般遵循一定的命名规则,包括根据碳原子数目命名烷烃、根据官能团命名醇、醛、酮等。
三、有机化合物的主要类别与性质3.1 烷烃烷烃是只含有碳碳单键的有机化合物,分为饱和烷烃和不饱和烷烃。
它们具有较低的反应活性,很难发生化学反应。
3.2 烯烃烯烃含有碳碳双键,分为乙烯和非乙烯烯烃。
烯烃具有较高的反应活性,可参与加成、消除等反应。
3.3 芳香化合物芳香化合物是具有特殊的芳香环结构的化合物,如苯环。
它们具有较稳定的结构和独特的化学性质。
3.4 醇醇是含有氢氧基的有机化合物,按照羰基的位置,可分为一元醇、二元醇等。
醇具有较高的极性和良好的溶解性。
3.5 醛和酮醛和酮均含有羰基,区别在于羰基所连接的碳原子数目。
它们具有较高的活性,可发生亲核加成等反应。
四、有机反应机制4.1 加成反应加成反应是指有机化合物中双键(如烯烃)先经过破裂,形成两个相互连接的新键。
4.2 消除反应消除反应是指有机化合物中某些官能团(如卤素)与相邻原子或原子团之间的键断裂,形成烯烃或炔烃。
4.3 取代反应取代反应是指有机化合物中某些原子或原子团被其他原子或原子团取代的反应。
有机化学基本概念汇总

分子组成相同结构不同的物质互称 5、同分异构体: 为同分异构体。 [思考讨论] (1)物质产生同分异构体的原因有哪些?
(2)C8H16主链上有5个碳原子的烷烃的同分异构 体有多少种? (3)C4H10O的醇有多少种? (4)练习: C11H16 的苯的同系物中, 只含有一个 支链, 且支链上含有两个“—CH3”的结构有四种, 写出其结构简式.
再
见
C.羧酸 D.醇钠
3、官能团: 决定有机物化学性质的原子或原子团。
[思考讨论]
(1)有机物有哪些重要的官能团?决定了这 些有机物分别具有哪些性质?
(2 )某有机物的结构简式如右图。则此有机 物可发生的反应 类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解⑥氧化⑦中和 。 A. ①②③⑤⑥ C. ①②③④⑤⑥ B. ②③④⑤⑥ D. ①②③④⑤⑥⑦
结构相似,在分子组成上相差一个或若 4、同系物: 干个“CH2”原子团的物质互称为同系物. [思考讨论] ( 1 )同系物与同分异构体、同素异形体、同位素的 区别。 (2)下列各组物质属于同位素的是 同素异形体的是 ;属于同系物的是 属于同分异构体的是 。 ;属于 ;
① O 2和O 3 ②3517Cl和3717Cl ③氕、氘、氚 ④金刚石和石墨 ⑤ CH3CH3和CH3CH2CH2CH3 ⑥新戊烷和异戊烷
①—NO2与NO2
②—OH与OH-
③—CH3与CH3+、CH3(2)分别写出丁基的几种结构简式
2、有机结构表达式
(1)电子式
(2)结构式
(3)结构简式
[思考讨论]
( 1 )、某有机物是某单炔烃经过加成反应得 到的,请写出此炔烃的可能结构简式。
2 、某期刊物封面上有如下一个分子的球棍模型 图,图中“棍”代表单键或双键或叁健。不同颜色 A ) 的球代表不同元素的原子,该模型图可代表一种( A.卤代羧酸 B.酯
有机化学知识的基本概念第一节有机化合物的组成和结构
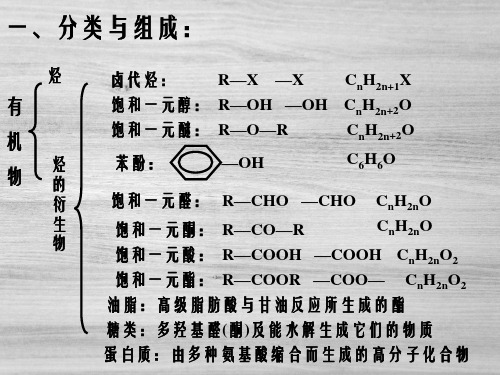
强极性键:如C—O、O—H、C—X等键,一般性质活泼, 较易断裂而发生化学反应。
三、结构与性质的关系:
1、结构与物理性质: (1)熔、沸点:分子量越大;分子中支链越少;分子极
性越大的熔沸点越高。 (2)、溶—解C性H:O只等有官分能子团中的含低有级—化O合H物、可—溶N于H2水、。—其CO余O的H
反应基团:C=C、C=O、C≡C、苯环上的键等
C=O + H—H → H—C—O—H (加氢)
C=C + H—CN → H—C—C—CN (加氢氰酸)
C=C + H—X → H—C—C—X (加卤化氢) C=C + H—OH → H—C—C—OH (加水)
加成反应的规律
. 1mol双键需1molH2 ; 1mol叁键需2molH2 .加成反应发生后,碳链结构不变,一般碳原子数目不 变,但加氢氰酸(HCN)后,碳原子数增加一个。
单体分子中一般应含有至少两个可以发
缩
生缩合反应的官能团
聚 特 反应通常发生在官能团上
反 点 高分子链中一般要通过氧、氮等原子相
·能发生银镜反应的物质有:醛、甲酸、甲酸酯、甲酸盐
有机物燃烧的规律: ⑴ N→有N机2、物X燃→烧H时X,各元素的最终产物:C→CO2、H→H2O、 ⑵烃和烃的含氧衍生物完全燃烧后,产物均为CO2和H2O ⑶烃的含氧衍生物燃烧的耗氧量可转化为烃燃烧的耗氧量
⑷1molC消耗1molO2,4molH消耗1molO2 ⑸ Cn符H2合nO通z的式有C机nH物2nO完z全的燃有烧机,物其完产全物燃C烧O规2和律H:2O(符g)合的通体式积相等。 ⑹100℃以上,有机物完全燃烧前后气体体积不变化的规律。
碳的化合物与有机化学基本概念

碳的化合物与有机化学基本概念碳是地球上自然界中丰富的元素之一,也是生命存在的基础。
由于碳原子独特的化学性质,与其他元素相比,碳具有更大的成键能力和多样的化学反应,因此形成了广泛的化合物。
本文将介绍碳的化合物以及有机化学的基本概念。
一、碳的化合物1. 定义碳的化合物是指由碳与其他元素(如氢、氧、氮等)共同组成的化合物。
碳作为生物体中的主要组成部分,碳的化合物在自然界中广泛存在,包括有机物和无机物。
2. 组成碳的化合物由碳原子与其他元素原子的成键形成。
碳原子具有四个价电子,可以与其他原子形成共价键。
根据碳原子与其他元素的成键数目和类型的不同,碳的化合物可以分为单原子碳化合物、多原子碳化合物和大分子有机化合物。
3. 分类根据碳原子的排列方式和化学性质,碳的化合物可分为饱和碳化合物和不饱和碳化合物。
饱和碳化合物是指碳原子之间单键成键的化合物,其分子中的碳原子与氢原子的比例为2:1,常见的饱和碳化合物有甲烷、乙烷等。
不饱和碳化合物是指碳原子之间存在双键或者三键成键的化合物,不饱和碳化合物包括烯烃、炔烃等。
不饱和碳化合物与饱和碳化合物相比,化学性质更为活泼。
二、有机化学基本概念1. 有机化合物有机化合物是由碳原子与氢原子以及其他元素原子构成的化合物,是有机化学研究的对象。
有机化学是研究有机化合物合成、结构、性质和反应的科学。
2. 碳的价态与键型碳原子的价电子数为四,常见的碳的键型有单键、双键和三键。
碳的价态取决于与其成键的其他原子个数。
3. 功能团功能团是指有机化合物中具有特定化学性质和反应的基团,是有机化合物命名和分类的重要依据。
常见的功能团包括羟基、羰基、氨基、羧基等。
4. 同分异构体由于碳原子的成键能力以及碳原子与其他原子成键的灵活性,导致有机化合物存在多种结构和形式。
具有相同分子式但结构不同的有机化合物称为同分异构体,它们具有不同的化学性质和反应。
5. 有机反应有机化合物的特点之一是能够进行多种多样的化学反应。
有机化学的基本概念
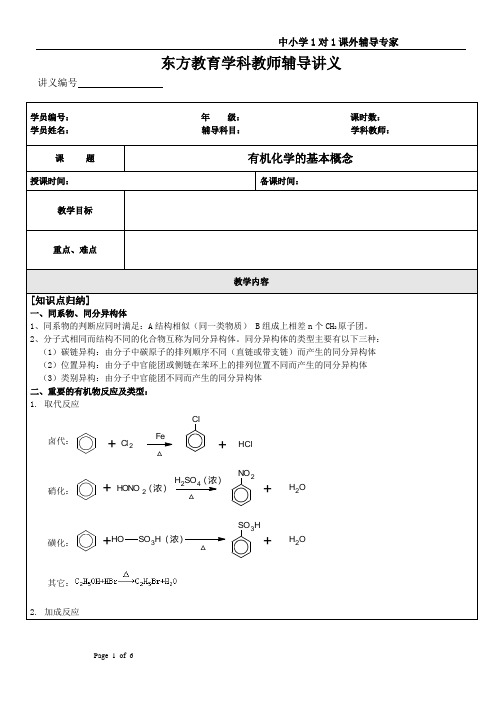
东方教育学科教师辅导讲义讲义编号学员编号:年级:课时数:学员姓名:辅导科目:学科教师:课题有机化学的基本概念授课时间:备课时间:教学目标重点、难点教学内容[知识点归纳]一、同系物、同分异构体1、同系物的判断应同时满足:A结构相似(同一类物质) B组成上相差n个CH2原子团。
2、分子式相同而结构不同的化合物互称为同分异构体。
同分异构体的类型主要有以下三种:(1)碳链异构:由分子中碳原子的排列顺序不同(直链或带支链)而产生的同分异构体(2)位置异构:由分子中官能团或侧链在苯环上的排列位置不同而产生的同分异构体(3)类别异构:由分子中官能团不同而产生的同分异构体二、重要的有机物反应及类型:1.取代反应卤代:+Cl2Fe△C l+C lH硝化:H2SO4(浓)△NO2+H2O +HONO2(浓)磺化:△SO3H+H2O+O H SO3H(浓)其它:2.加成反应CH 3CHC H 2+C lH CH 3HC C H 3C H 3+H 2Ni△3CH 3COH+H 2C H 3CH 2O HNi△3. 氧化反应CH 3+O3CO HOOH 2+2KMnO44. 还原反应:+H5. 消去反应6. 酯化反应(取代反应)CH 3COO H+C 2H 5OHCH 3COC 2H 5O+OH 2浓H2SO 4△7. 水解反应nC 6H 12O 6酸或酶△(C 6H 10O 5)n+nH 2O8. 聚合反应加聚:CH 2CHCHC H 2+CH 2CH一定条件下H 2CCH CHCH 2CH 2CH 2n n缩聚:COOHCOOH+nHOCH2CH 2OH2nH 2OCOOOCH 2CH 2O+一定条件下9. 中和反应O H+NaOHO Na+OH 2三、有机物物理性质:1、能溶于水:低碳的醇、醛、酸、钠盐,如乙(醇、醛、酸)乙二醇、丙三醇、苯酚钠2、难溶于水的:烃,卤代烃,酯类,硝基化合物比水轻:烃(汽油、苯及其同系物、己烷、己烯)酯(如乙酸乙酯)、油脂 比水重:硝基苯,溴苯CCl4,(二)溴乙烷、液态苯 酚 3、微溶于水:苯酚、苯甲酸4、苯酚溶解的特殊性:常温微溶,65℃以上任意溶5.常温下为气体的有机物:烃(C<4)甲醛6、有毒物质:涂料油漆中的苯、硝基苯,假酒中的甲醇,居室装修产生的甲醛气体[例题讲解]1、丁香油酚的结构简式是 ,该物质不应有的化学性质是( ) ①可以燃烧;②可以跟溴加成;③可以使酸性KMnO 4溶液褪色;④可以跟NaHCO 3溶液反应;⑤可以跟NaOH 溶液反应;⑥可以在碱性条件下水解A 、①③B 、③⑥C 、④⑤D 、④⑥2、白藜芦醇HO - -CH =CH - 广泛存在于食物(例如桑葚、花生、尤其是葡萄)中,它可能具有抗癌性。
高中化学中有机化学的知识点总结8篇

高中化学中有机化学的知识点总结8篇第1篇示例:高中化学中有机化学是高中化学课程中的重要部分,主要研究有机物的结构、性质、合成方法和反应机理等内容。
有机化学知识是高中化学学习的难点,掌握有机化学知识对于高中化学学习和日常生活都有重要意义。
下面就是有机化学的一些重要知识点总结:1. 有机物的定义有机化学研究的是含有碳元素的化合物,碳元素是有机物的主要组成元素,因此有机物也被称为碳化合物。
有机物包括烃类、醇类、醛酮类、羧酸类等多种化合物。
2. 有机化合物的分类有机化合物主要分为脂肪烃、环烷烃、环烯烃、芳香烃、醇、醚、醛、酮、羧酸、酯等多种类别,每种类别都有其独特的特性和反应规律。
3. 有机物的结构有机物的结构包括分子式、结构式、键式和构象式等不同表示方法,通过这些表示方法可以清晰地描述有机物的分子结构和化学键构型。
4. 有机物的性质有机物具有多样性和复杂性的性质,包括物理性质(如沸点、熔点、密度等)和化学性质(如稳定性、溶解性、反应性等)。
5. 有机合成方法有机化学是有机合成的基础,有机合成方法包括加成反应、取代反应、消除反应、重排反应等多种方法,通过这些方法可以合成各种有机化合物。
6. 有机反应机理有机反应机理是研究有机反应过程中的原子或基团之间的结合和断裂规律,包括亲核取代、亲电取代、自由基取代等不同类型的有机反应机理。
7. 有机化学在生活中的应用有机化学在生活中有广泛的应用,例如食品添加剂、药物、化妆品、材料合成等领域都离不开有机化学知识。
第2篇示例:高中化学中有机化学的知识点总结有机化学是化学的一个重要分支,研究有机物的结构、性质、合成和反应规律。
在高中化学课程中,有机化学是一个重要的部分,学生需要掌握一定的有机化学知识。
下面我们来总结一下高中化学中有机化学的知识点。
1. 有机物的结构有机物是由碳和氢组成的化合物,其中碳是主要元素。
有机物的结构可以分为链状结构、环状结构和支链结构。
根据碳原子之间的连接方式不同,有机物可以是直链烷烃、环烷烃、烯烃、炔烃、芳香烃等不同类型。
烃复习09.2
同系物的性质: 3、随碳原子个数增加H%有规律的变化 ①烷烃随碳原子数的增加H%减少,燃烧等质量的烷烃 耗氧量减少,生成水减少,生成CO2增多。烷烃C%最大值 =85.7%。 ②烯烃随碳原子数的增加H%不变,燃烧等质量烯烃耗 氧量相等,生成水相等,生成CO2相等。烯烃C%=85.7%。 ③炔烃随碳原子数的增加H%增大,燃烧等质量的炔烃 耗氧量增大,生成水增多,生成CO2减少。炔烃中H的百 分含量最大H%=14.3%。 7、同分异构体
例1.写出醋酸的最简式_______________;分子式________; C2H4O2 CH2O
HO .. H .. . .∶O∶H . . H-C-C-O-H .. 电子式 H∶C∶C∶∶O∶ _____________________________;结构式____________; H H 结构简式____________________;球棍模型_____________。 CH3COOH
5、表示有机物组成和结构的方法
最简式(实验式)---表示有机物组成原子的最简整数比 分子式---表示有机物分子组成的式子(是最简式的整数倍)
电子式---用元素符号和原子最外层电子表示分子结构的式子 结构式—由简化电子式而来,用短线表示共用电子对。表示 分子内原子间的连接顺序和方式(C-C、C=C、 = C 、C=O C 能团不能省去 键线式—省去结构简式中的碳原子和氢原子,以线示键表示有机 物结构的式子。CH2=CHCH=CH2键线式结构:= - = 比例模型、球棍模型、立体结构示意图和结构式的区别。 结构式只表示分子内原子间的连接顺序和方式,不表示分子 的空间构型,而比例模型、球棍模型、立体结构示意图既表示 结构式的含义,又表示分子的空间构型。
化合物分子式相同, 结构不同的现象叫同分异构现象。 分子式相同,结构不同的化合物互称同分异构体。
高中化学有机化学ppt课件
03有机物主要由碳、氢元素组成,还可能含有氧、氮、硫、磷等元素;无机物则可能包含各种元素。
组成元素有机物分子结构复杂,具有同分异构现象;无机物分子结构相对简单。
结构特点有机物大多具有可燃性、难溶于水、反应速率较慢等性质;无机物性质各异,有些具有与有机物相似的性质。
性质特征有机物与无机物区别古代人们对天然动植物和矿物的利用,如木材、药材、染料等。
萌芽时期18世纪末至19世纪初,贝采利乌斯等化学家提出有机化学概念,并合成尿素等有机化合物。
创立时期19世纪中后期,合成染料、香料、药物等有机化合物的出现,推动了有机化学的快速发展。
发展时期20世纪以来,随着物理和化学方法的不断进步,有机化学在合成、结构、反应机理等方面取得了巨大成就。
现代时期有机化学发展简史有机化合物分类及命名分类根据碳骨架形状,有机化合物可分为链状化合物和环状化合物;根据官能团类型,可分为烃类、醇类、醛类、酮类、羧酸类等。
命名有机化合物的命名遵循一定的规则和原则,包括选取主链、编号原则、官能团优先顺序等。
常见的命名法有普通命名法、系统命名法和衍生命名法等。
01结构特点碳原子间以单键相连,其余价键被氢原子饱和。
02物理性质随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
03化学性质相对稳定,主要发生取代反应,如卤代反应。
含有一个或多个碳碳双键。
结构特点物理性质化学性质随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
较为活泼,可发生加成反应、氧化反应、聚合反应等。
030201含有一个或多个碳碳三键。
结构特点随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
物理性质非常活泼,可发生加成反应、氧化反应、聚合反应等。
化学性质1 2 3含有苯环或其他芳香环结构。
结构特点具有特殊芳香味,沸点、熔点较高,密度较大。
物理性质相对稳定,可发生取代反应、加成反应等。
化学性质芳香烃结构和性质卤代烃结构和性质卤代烃的分子结构由烃基和卤素原子组成,卤素原子与烃基通过共价键连接。
有机化学基本概念复习
甲烷 乙烯
乙炔 苯
正四面体
平面 三角 直线型
平面正 六边形
基本概念——原子共平面问题 • 复杂分子实际上是由这几个基本结构单元 按一定的组合方式构成的,在基本结构单 元之间结合的时候,注意单键是可以旋转 的,而双键和三键不能旋转,另外注意问 题的条件是“所有碳原子”还是“所有原 子”、是“一定”还是“可能”共平面。
基本概念——同分异构体
• 书写 –顺序: 碳链异构→位置异构→官能团异构 即判类别、定碳链、移官位、氢饱和 –方法: 主链由长到短, 支链由整到散, 位置由心到边 排列由邻到间
基本概念——同分异构体
• 判断 –等效转换法 若CxHy中的n卤代物与m卤代物的同分异构体的 数目相等,则m+n=y –等效氢原子法(等效氢原种类=一卤代物种类) ①同一碳原子上的氢原子是等效的 ②同一碳原子所连甲基上的氢原子是等效的 ③处于中心对称位置上的氢原子是等效的
有机化学基本概念点:碳原子有四个价电子,和碳原子或其 他的原子形四个共价键;可能为单、双或三键, 可能成链或成环;相同的分子式可能存在多种结 构 ——有机物种类繁多的原因
基本概念比较——基、根、官能团
基 特性 电中性,不能 单独稳定存在 根 官能团 显电性,能独 决定有机物 立存在 的化学性质
知识规律——燃烧规律
燃烧耗氧规律
等n的烃(CxHy)完全燃烧,耗氧量取决于(X+Y/4) 的值,此值越大,耗氧越多 等m的烃(CxHy)完全燃烧时,耗氧量取决于含氢量, 将烃(CxHy)转化为CHy/x的形式,y/x值越大,含氢 越多,耗氧越多 等质量烃耗氧量比较:烷烃>烯烃>炔烃。 等物质的量的有机物CxHyOz完全燃烧时,耗氧量取 决于(X+Y/4—Z/2)的值,此值越大,耗氧越多 分子组成中相差若干个“CO2”或“H2O”的物质,其 耗氧量相等。如等物质的量的C2H4与C2H5OH完全燃烧 时耗氧量相同
有机化学基础知识点总复习
有机化学基础知识点总复习一、协议关键信息1、有机化学的基本概念有机化合物的定义与特点:____________________________官能团的概念与常见官能团:____________________________同系物、同分异构体的定义与判断:____________________________2、烃类化合物烷烃的结构、性质与命名:____________________________烯烃的结构、性质与加成反应:____________________________炔烃的结构、性质与化学性质:____________________________芳香烃的结构、性质与苯的同系物:____________________________3、烃的衍生物卤代烃的性质与卤代烃的取代反应:____________________________醇的结构、性质与醇的氧化反应:____________________________酚的结构、性质与酚的酸性:____________________________醛的结构、性质与醛的氧化还原反应:____________________________羧酸的结构、性质与羧酸的酯化反应:____________________________酯的结构、性质与酯的水解反应:____________________________4、有机化学反应类型取代反应的特点与常见实例:____________________________加成反应的特点与常见实例:____________________________消去反应的条件与常见实例:____________________________氧化反应与还原反应的判断与常见反应:____________________________聚合反应的分类与常见聚合反应:____________________________5、有机化合物的合成合成路线的设计原则:____________________________官能团的引入与转化方法:____________________________有机合成中的保护与去保护策略:____________________________6、有机化合物的结构鉴定红外光谱、核磁共振氢谱的原理与应用:____________________________有机化合物结构推断的方法与思路:____________________________二、协议内容11 有机化学的基本概念111 有机化合物是指含碳的化合物,但一些简单的含碳化合物如一氧化碳、二氧化碳、碳酸盐等通常被归类为无机化合物。
