硝酸和苯的硝化反应
苯环硝化反应的条件

苯环硝化反应的条件苯环硝化反应是有机化学中一种重要的反应,它是通过在苯环上引入硝基基团来合成硝基苯化合物的方法。
本文将介绍苯环硝化反应的条件及其原理。
1. 反应条件苯环硝化反应的条件包括温度、反应物浓度、酸性条件和反应时间等。
(1) 温度苯环硝化反应一般在室温下进行,通常在0-10摄氏度之间。
过高的温度会导致反应速率过快,产生副反应,降低产率。
(2) 反应物浓度苯环硝化反应中,硝化剂浓度对反应速率和产率有一定影响。
一般来说,硝化剂浓度越高,反应速率越快,但同时也容易产生副反应。
因此,合适的硝化剂浓度是保证反应高效进行的关键。
(3) 酸性条件苯环硝化反应需要在酸性条件下进行,常用的酸包括浓硫酸、浓硝酸和混酸等。
酸性条件有助于促进硝基离子的形成和与苯环的反应。
(4) 反应时间苯环硝化反应的反应时间一般较短,一般在数小时至数十小时之间。
过长或过短的反应时间都会影响反应的产率,因此需要根据具体情况进行控制。
2. 反应原理苯环硝化反应是通过硝酸或硝酸盐与苯环发生亲电取代反应而实现的。
反应机理主要分为两步:亲电取代和亲核取代。
(1) 亲电取代亲电取代是苯环硝化反应的第一步,它是由硝酸或硝酸盐作为亲电试剂,与苯环中的亲电子基团发生反应。
在酸性条件下,硝酸或硝酸盐可以释放出硝基离子,硝基离子与苯环中的亲电子基团发生亲电取代反应,生成硝基苯化合物中间体。
(2) 亲核取代亲核取代是苯环硝化反应的第二步,它是由硝基苯化合物中间体与亲核试剂发生反应。
在酸性条件下,硝基苯化合物中间体可以被亲核试剂如水分子或其他亲核试剂攻击,发生亲核取代反应,生成相应的硝基苯化合物。
总结:苯环硝化反应是一种重要的有机合成反应,通过引入硝基基团在苯环上合成硝基苯化合物。
反应条件包括温度、反应物浓度、酸性条件和反应时间等。
反应的原理主要包括亲电取代和亲核取代两个步骤。
通过合理控制反应条件和理解反应机理,可以高效地合成硝基苯化合物。
甲苯发生硝化反应的化学方程式

甲苯发生硝化反应的化学方程式甲苯(C6H5CH3)是一种有机化合物,可以通过硝化反应合成对硝基甲苯(C6H4(CH3)NO2),反应方程式如下:C6H5CH3 + HNO3 + H2SO4 → C6H4(CH3)NO2 + H2O这个方程式描述了甲苯与硝酸和硫酸反应生成对硝基甲苯和水。
下面将对这个反应进行解释。
甲苯发生硝化反应是一种烷基芳香化合物的重要反应。
硝化反应是一种在有机化学中常见的反应类型,用于引入硝基(NO2)基团到有机分子中。
在甲苯的硝化反应中,硝酸(HNO3)和硫酸(H2SO4)充当反应的试剂。
在反应中,首先将硝酸和硫酸混合形成硝酸硫酸混合酸。
这种混合酸是一种强酸,具有强酸性。
硝酸是一种强氧化剂,而硫酸则起到催化剂的作用。
甲苯溶解在硝酸硫酸混合酸中,其中的甲苯分子与硝酸发生反应。
硝酸中的硝根离子(NO3-)攻击甲苯分子上的氢原子,形成甲苯的正离子和硝酸根负离子。
这个过程被称为亲核取代反应。
C6H5CH3 + NO3- → C6H5CH2+ + HNO3甲苯的正离子与硝酸根负离子结合,形成对硝基甲苯的中间产物。
这个中间产物是不稳定的,很容易发生分解反应。
C6H5CH2+ → C6H4(CH3)NO2 + H+在分解反应中,甲苯的正离子失去一个氢离子,形成对硝基甲苯和一个质子(H+)。
质子会与水结合形成H3O+,而对硝基甲苯则稳定存在。
反应中产生的水可以通过分离出来,得到对硝基甲苯。
这个反应过程中,硝酸起到氧化剂的作用,将甲苯中的氢原子氧化为正离子。
硫酸则起到催化剂的作用,加速反应速率。
整个反应过程是一个复杂的离子反应,涉及到正离子和负离子的互相结合和分离。
甲苯的硝化反应是一种重要的有机合成反应,对于制备对硝基甲苯等化合物具有重要意义。
对硝基甲苯是一种重要的化工原料,广泛应用于染料、医药、农药等领域。
硝化反应的研究和应用对于有机化学领域具有重要的意义。
苯

(2)化学方程式
+ Br2
FeBr3
— Br + HBr
溴苯
注意:
①、溴水不与苯发生反应,必须是纯溴、催化
剂(Fe或FeBr3)
②、只发生单取代反应 ③、溴苯是不溶于水,密度比水大的无色,油
状液体,能溶解溴,溴苯溶解了溴时呈褐色
苯的化学性质
2、取代反应
(2)与硝酸发生取代反应(硝化反应) + HO—NO2 注意:
浓硫酸 △
— NO2 + H2O 硝基苯
①. 硝基苯是无色有苦杏仁味的油状液体,不溶 于水,密度比水大,有毒。 ②. 混合时,要将浓硫酸缓缓注入浓硝酸中,并不 断振荡。 ③. 条件: 50-60oC 水浴加热(受热均匀、温度容易控制) ④. 浓H2SO4的作用 : 催化剂 脱水剂
(3)磺化反应
苯磺酸溶于水
⒉能说明苯分子中碳碳键不是单双键相间交替 的事实是 ①苯不能使KMnO4溶液褪色;②苯环 中碳碳键的键长均相等;③邻二氯苯只有一种; ④在一定条件下苯与H2发生加成反应生成环己烷。 (B ) A. ①②③④ B.①②③ C. ②③④ D.①②④ ⒊下列各组物质中可以用分液漏斗分离的( C ) A. 酒精与碘 B. 溴与四氯化碳 C. 硝基苯与水 D. 苯与溴苯
磺酸基是硫原子和苯环直接相连的
浓硫酸的作用 吸水剂和磺化剂
苯的化学性质
3、加成反应 + 3 H2
Ni
△
环己烷
学以致用
1、下列各烃中,完全燃烧时生成的CO2和 H2O的物质的量之比是2 :1的是( D ) A、乙烷 B、乙烯 C、异丁烷 D、苯
2、下列反应属于取代反应的是( AD) A、光照下甲烷与氯气的反应 B、乙烯通入溴水中 C、要Ni作催化剂的条件下,苯与氢气反应 D、苯与液溴混合后撒入铁粉
甲苯的硝化反应式及实验数据如下所示实验情况说明(i)甲苯比苯.

邻位进攻:
Cl + NO2 H
(xix)
Cl
+
NO2
H
Cl
+
NO2
H
(xx)
(xxi)
特 别 不稳定
Cl + NO2 H
(xxii) 比 较 稳定
Cl
+
NO2
-
+
H
H
Cl NO2
对位进攻:
Cl
+H NO2
3.甲苯的硝化
甲苯的硝化反应式及实验数据如下所示:
CH3
+ (浓) HNO3+ (浓)
30℃ H2SO4
CH3 NO2
+
CH3
+
NO2
58%
38%
CH3
NO2 4%
实验情况说明:(i)甲苯比苯容易硝化,(ii)甲苯硝化时,主 要得到邻位和对位产物。
甲苯比苯易硝化的原因是:甲苯具有微弱的给 电子超共轭效应,这种超共轭效应使苯环上的电子 云密度有所增加,这一方面使硝基正离子更容易进 攻苯环,同时也使反应过程中产生的中间体碳正离 子的电荷得到分散而稳定。所以甲苯比苯更易硝化。 但甲基的给电子能力是很弱的,因此它对苯环的活 泼性影响较弱。
4.氯苯的硝化
• 甲苯的硝化反应式及实验数据如下所示:
Cl
+ (浓) + HNO3 (浓) H2SO4
1:1.5
Cl
Cl
Cl
NO2
+
+
NO2 70%
30%
NO2 极微 量
• 实验情况说明:(i)氯苯比苯难以硝化,(ii)氯苯硝化时,
溴苯硝化反应方程式

溴苯硝化反应方程式
1、溴苯硝化反应方程式:C6H6(苯)+3H2==C6H12(环己烷)条件:Ni;加热。
2、苯的取代反应
(1)卤代:C6H6(苯)+Br2(液溴)==C6H5Br(溴苯)+HBr条件:铁或三价铁离子做催化剂。
(2)硝化:苯与浓硫酸浓硝酸水浴加热55—60度C6H6+HNO3(浓)==C6H5NO2(硝基苯)+H2O。
(3)磺化:苯与浓硫酸水浴70—80度。
C6H6+H2SO4==C6H5SO3H (苯磺酸)+H2O。
苯与溴的反应方程式为C6H6+Br2→C6H5Br+HBr,条件是在Fe或FeBr3催化作用下,该化学反应为取代反应,一个溴原子取代了苯环中的一个氢原子,生成溴苯和溴化氢。
硝化是苯环上的亲电取代反应,苯环上电子云密度越高反应活性越强,也就是说苯环上带给电子基时反应活性增加,且给电子能力越强,活化得越厉得越厉害;苯环上带拉电子基时,反应活性下降,拉电子基的拉电子能力越强,钝化得越厉得越厉害。
羟基(—OH)是强给电子基,所以苯酚活性最高,卤素是弱拉电子基,硝基是强拉电子基,二者均使苯环活性下降,但硝基更显著。
注意,苯酚容易被氧化,最后得到的硝化产物收率并不高(硝酸有氧化性),但仅从反应活性看,苯酚肯定是最强的。
苯的化学反应

详细描述
苯的催化加氢反应通常在高温和高压下进行 ,常用的催化剂有铂、钯、镍等。在反应过 程中,苯的六个碳碳双键被氢气还原,生成 环己烷或其他饱和烃类化合物。这种反应广 泛应用于工业上生产环己烷、甲己酮、甲己
醇等有机化合物。
化学还原反应
要点一
总结词
通过使用还原剂,苯能够被还原成环己烯或其他烯烃。
要点二
氧化生成苯甲酸
总结词
苯在氧气的作用下,可以氧化生成苯甲 酸。
VS
详细描述
苯在常温下与氧气反应,可以生成一种叫 做苯甲酸的物质。苯甲酸是一种白色粉末 ,具有酸性,可以与碱反应生成盐。这种 反应通常需要在催化剂的作用下进行,而 且需要一定的温度和压力。
氧化生成苯醌
总结词
苯在特定条件下可以氧化生成苯醌。
详细描述
在某些特定的条件下,例如高温或高压,苯 可以与氧气反应生成苯醌。苯醌是一种具有 特殊化学性质的化合物,它可以与其他化合 物发生反应,生成许多有用的物质,例如染 料、农药和医药等。这种反应通常需要在特 定的反应条件下进行,而且需要使用催化剂。
04
苯的还原反应
催化加氢反应
总结词
在催化剂的作用下,苯与氢气发生反应,生 成环己烷或其他烷烃。
硝化反应
总结词
苯与硝酸在一定条件下发生取代反应 ,生成硝基苯。
详细描述
苯与混酸(浓硫酸和硝酸的混合物)在 50-60℃下反应,生成硝基苯。硝基取 代的位置主要在苯环上,生成邻位、对 位或间位的取代产物。
磺化反应
总结词
苯与浓硫酸发生取代反应,生成苯磺酸或苯磺化物。
详细描述
苯与浓硫酸在加热条件下反应,生成苯磺酸;与浓硫酸和亚硫酸钠作用,生成 苯磺化物。磺酸基取代的位置主要在苯环上,生成邻位、对位或间位的取代产 物。
硝化反应硝基进入苯环的位置

硝化反应硝基进入苯环的位置
硝化反应是一种重要的有机合成方法,可用于将硝基基团引入苯环中的不同位置。
苯环上的氢原子可以被硝酸和硫酸混合酸性条件下的硝酸银催化剂氧化硝化,产生硝基苯衍生物。
硝化反应的位置选择性取决于苯环上氢原子的活性和立体位阻。
苯环上的活性基团,例如甲基、甲氧基等,会导致反应发生在这些基团附近的位置。
这是因为这些基团会增加苯环上氢原子的活性,使其更容易被硝酸硫酸混合酸氧化硝化。
然而,若苯环上存在较大的位阻基团,例如叔丁基、叔戊基等,硝化反应则更倾向于发生在位阻较小的位置上。
这是因为位阻基团会限制其他位点上的反应性,使处于位阻较小位置的氢原子更容易被硝酸硫酸混合酸氧化硝化。
此外,苯环上的立体位阻也会影响硝化反应的位置选择性。
苯环上存在轴手性或平面手性基团时,硝化反应通常会发生在具有较小位阻的位置上,以克服立体位阻的影响。
总的来说,硝化反应硝基进入苯环的位置受到苯环上氢原子的活性、位阻基团的影响,以及立体位阻的影响。
这些因素的综合作用会导致硝化反应在苯环的不同位置上发生,从而得到不同位置的硝基苯衍生物。
硝化反应主要危险及控制措施
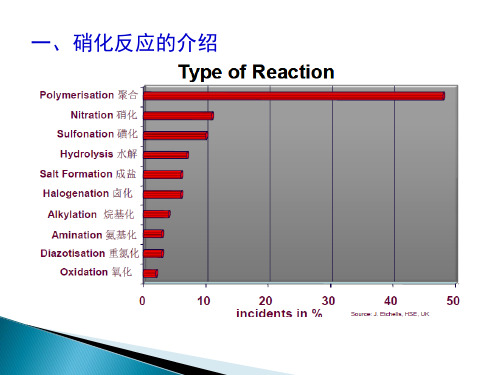
三、硝化过程的危害因素及预防对策(续)
1、硝化过程的危害因素 (4)有机物的意外氧化,易发生燃烧爆炸。
硝化釜内意外掉进棉纱、破布、橡胶手套及机器润滑油等有 机物与混酸中的硝酸发生强烈的氧化反应,放出大量氮氧化物气 体,并引起温度迅速升高,进而可能引起硝化混合物从设备中喷 出而引起爆炸事故。
三、硝化过程的危害因素及预防对策(续)
• 硝化釜为微负压(由负压塔产生),可吸收有害气体,防止外泄。 • 硝化釜装有泄压装置(爆破片)。
三、硝化过程的危害因素及预防对策(续)
4、硝化设备危害的预防对策 (1)设备设计、材质选择要合理,特别对耐腐蚀要求。
(2)硝化釜搪玻璃涂层的完整性必须定期检查 。
(3)电器仪表要防爆,设备、管道要有防静电措施并定期进行 防静电检测。 (4)仪表控制报警联锁要定期检查并试运行。 (5)泄压、防有害气体外泄装置要经常巡查确保有效。
三、硝化过程的危害因素及预防对策
1、硝化过程的危害因素 (1)硝化生产中反应热量大,温度不易控制。
硝化反应一般在较低温度下便会发生,易于放热,反应不易 控制。(其中苯硝化过程中,引入一个硝基,可释放出152.2~ 153KJ/mol的热量。)所以硝化需要在降温条件下进行。在硝化 反应中,倘若稍有疏忽,如中途搅拌停止、搅拌桨脱落、冷却效 果不好、加料速度过快、投料比例不当、反应温度失控等原因, 都可能使反应温度猛增、混酸氧化能力加强,并有多硝基物生成, 容易引起着火和爆炸事故。
三、硝化过程的危害因素及预防对策(续)
1、硝化过程的危害因素 (3)硝化易产生副反应和过反应,二硝和多硝化合物具有易爆 特性。
硝化反应具有深度氧化占优势的链锁反应和平行反应的特点, 同时还伴有水解等副反应,直接影响到生产的安全。硝化过程中 最危险的是有机物质的氧化,氧化反应出现时放出大量氧化氮气 体的褐色蒸气,以及混合物的温度迅速升高而引起硝化混合物从 设备中喷出,发生爆炸事故。芳香族的硝化反应常发生生成硝基 酚的氧化副反应,硝基酚及其盐类性质不稳定,极易燃烧、爆炸。 特别是多硝基化合物和硝酸酯,受热、摩擦、撞击或接触着火源, 极易发生着火或爆炸。
