三氟甲基和氨基定位效应
三氟甲氧基定位效应 -回复

三氟甲氧基定位效应-回复三氟甲氧基定位效应(trifluoromethoxy directing effect)是有机合成中一个重要的现象,指的是在特定反应条件下,三氟甲氧基(CF3O-)取代基能够选择性地导向反应的特定位置。
本文将详细介绍三氟甲氧基定位效应的原理、应用以及相关的研究进展。
一、三氟甲氧基定位效应的原理及机制三氟甲氧基定位效应的出现,是由于三氟甲氧基具有一定的电子吸引性和立体效应。
首先,三氟甲氧基中的氧原子能够通过其电负性,对反应中的亲电位点(通常指芳香环上的邻位或间位)进行强烈的电子云吸引,从而使反应发生在该位置。
其次,由于三氟甲氧基比较大,其取代基会产生一定的立体效应,导致反应发生在邻位或间位。
二、三氟甲氧基定位效应的应用1. 亲电取代反应中的应用:三氟甲氧基作为取代基,可以在亲电取代反应中导向目标化合物的特定位置。
例如,三氟甲氧基可以选择性地引发苯环的卤代反应,使卤素取代在三氟甲氧基的邻位或间位发生,从而得到具有特定取代基的化合物。
2. 符合勃氏碱原理的应用:根据勃林斯基碱(Bodriusky bases)原理,三氟甲氧基的取代位点能够通过亲核试剂进行二次取代反应。
这种应用常见于羧酸酯合成和糖化学合成中。
3. 催化剂的应用:三氟甲氧基定位效应也可以作为催化剂的设计和应用的基础。
例如,在过渡金属催化的反应中,引入三氟甲氧基取代基能够改变反应的立体选择性和产物的生成途径。
三、三氟甲氧基定位效应的研究进展随着有机合成领域的不断发展,对于三氟甲氧基定位效应的研究也越来越深入。
近年来,研究者们通过理论计算、实验验证以及新型试剂的开发,进一步揭示了三氟甲氧基定位效应的机制和应用。
1. 新型试剂的开发:研究者们不断设计和合成新型的三氟甲氧基试剂,以进一步扩展其在有机合成中的应用。
例如,引入手性三氟甲氧基试剂可以实现手性分子的选择性合成。
2. 机理研究:通过理论计算和实验验证,研究者们揭示了三氟甲氧基定位效应的机理细节。
三氟甲氧基 定位基

三氟甲氧基定位基三氟甲氧基是一种有机化合物中的化学基团,化学式为CF3O-,由一个碳原子与三个氟原子和一个氧原子组成。
该化学基团常常用作有机合成中的定位基,可以引入到目标分子中的特定位置上,从而改变其物理化学性质或增加其活性。
下面将从三氟甲氧基的合成方法、反应性质以及在有机合成中的应用等方面进行介绍,以简体中文写出。
三氟甲氧基的合成方法有多种,其中一种常见的方法是利用三氟甲醇和碱反应得到。
三氟甲醇是从铁三氟甲烷铁、三氟甲烷和碱的反应中获得的,简称TFM法。
铁三氟甲烷铁是一种常见的三氟甲基化试剂,可与异氰酸酯或叔丁基氰酸酯反应得到三氟甲基叔丁氧基化合物,再通过水解反应脱除叔丁氧基基团,得到三氟甲氧基化合物。
三氟甲氧基具有一定的反应性质,可以参与多种有机反应。
例如,三氟甲氧基可被氢化钠处理成甲醇,可以被碱处理生成碱式盐,还可以与酸反应生成对应的酯。
此外,三氟甲氧基还可以与叔醇反应生成叔醚,与硅烷反应生成三氟甲基硅烷等。
在有机合成中,三氟甲氧基常用作定位基,用于引入三氟甲氧基化合物中的特定位置上。
这是因为三氟甲氧基具有较强的电子吸引性,可以在化学反应中起到增强反应活性或改变反应产物选择性的作用。
例如,三氟甲氧基可以通过亲电取代反应引入到芳香化合物的芳香环上,从而改变其电子密度和亲核取代反应的速率。
此外,三氟甲氧基还可以作为活泼的氧化还原试剂,在一些氧化还原反应中发挥关键作用。
三氟甲氧基在药物合成、材料合成等领域中得到了广泛应用。
例如,在药物合成中,三氟甲氧基可以用于引入活性基团、改变药物分子的溶解性、增强活性或改善药物代谢性质等。
在材料合成中,三氟甲氧基可以作为改性试剂,改变材料的表面性质、增强其稳定性或改善材料界面等。
总而言之,三氟甲氧基是一种重要的有机化合物中的定位基团,具有较强的反应活性和应用潜力。
通过合适的合成方法和反应条件,可以将三氟甲氧基引入到目标分子中的特定位置上,从而实现取代或改变其物理化学性质。
氨基和甲基的定位能力

氨基和甲基的定位能力
氨基(NH2)是一种碱性基团,通常具有一定的亲电性,能与电子富集的反应物发生反应。
氨基团的存在大大改变了分子的化学性质和生物学性质,因为它能够在中性或者较低PH值下接受质子而产生正电荷。
氨基的位置对于分子的性质和活性有很大的影响,在分子设计和药物研究中,准确定位氨基位置以及调节其环境是非常重要的。
在有机合成中,氨基通常通过氨解反应、还原反应、胺加成等方法引入分子中。
在这些反应中,反应条件、催化剂的选择以及反应物之间的选择都会影响氨基的位置和定位。
例如,在胺加成反应中,选择合适的底物和反应条件可以使反应产物中氨基的定位更为准确。
而如果选择不合适的反应条件和底物,可能会出现对立异构体的产生,从而影响化合物性质和活性。
在分子设计中,氨基的定位也是非常重要的。
合适的氨基位置可以增强分子的亲和性和生物学活性,而不合适的位置则会对活性产生负面影响。
例如,在药物设计中,选择合适的氨基位置可以增强药物的亲和力、选择性和生物稳定性,从而提高药物的治疗效果和安全性。
甲基(CH3)是一种非极性或微极性基团,通常具有一定的疏水性。
甲基的存在可以增强分子的疏水性和极性,从而调节分子的溶解度、分配系数和生物利用度。
在分子设计和合成中,准确定位甲基的位置是非常关键的。
总结
氨基和甲基的定位能力在有机合成和分子设计中具有非常重要的作用。
准确定位氨基和甲基的位置可以调节分子的化学性质和生物学性质,从而实现分子设计和化合物优化。
在分子合成和设计中,选择合适的反应条件、催化剂和底物及正确地调节反应条件,可以有效地实现分子中氨基和甲基的定位,从而提高化合物的性质和活性。
以togni试剂作为三氟甲基源的反应机理

以togni试剂作为三氟甲基源的反应机理以Togni试剂是一种常见的烷酸衍生物,它的反应机理在最近的几十年里受到越来越多的关注。
以Togni试剂可以在弱基团环境中作为三氟甲基源,参与取代反应。
一般来说,三氟甲基源可以与氨基酸作用,以生成取代后的氨基酸,这反应机理是三氟甲基源和氨基酸之间形成亲核键而驱动的。
虽然以Togni试剂被用作三氟甲基源已经有多年了,但是其与氨基酸之间的反应机理仍然不是很明确。
有些研究表明,以Togni试剂中的烯烃基团可以和氨基酸的质子发生反应,从而构成三氟甲基取代的氨基酸反应产物。
这种反应机理被称为“烷烃基团质子接受者”,它允许烷烃基团与质子进行反应,使烷烃基团转化为三氟甲基取代的氨基酸反应产物。
此外,有些研究表明,以Togni试剂中的烯烃基团与氨基酸的树脂酸或脂肪酸发生反应,从而形成取代产物。
这种反应机理也被称为“烯烃基团树脂酸接受者反应”,它允许烷烃基团与树脂酸发生反应,使它们转化为三氟甲基取代的氨基酸反应产物。
而脂肪酸反应则是由烯烃基团与脂肪酸发生反应而构建出三氟甲基取代的氨基酸反应产物。
这两种反应机理都可以被用来解释以Togni试剂作为三氟甲基源的反应机理。
此外,也有一些研究表明,以Togni试剂也可以通过酶促反应形成取代基。
在这种情况下,以Togni试剂中的烷烃基团可以与酶发生反应,从而使烷烃基团被酶分解,并扮演一个促进反应的作用。
虽然这项研究还处于早期,但它表明以Togni试剂可以有效地在酶促反应中发挥作用,从而形成三氟甲基取代的氨基酸反应产物。
综上所述,以Togni试剂可以作为三氟甲基源,参与取代反应,与氨基酸的反应机理可以通过“烷烃基团质子接受者”和“烯烃基团树脂酸/脂肪酸受者反应”来概括。
此外,以Togni试剂也可以用作酶促反应形成三氟甲基取代的氨基酸反应产物。
因此,对以Togni试剂作为三氟甲基源,参与取代反应的机理进行研究,可以为未来开发更多新型取代反应和制备新型氨基酸提供宝贵的知识基础。
三氟甲基化有机胺类化合物

三氟甲基化有机胺类化合物
三氟甲基化有机胺类化合物是指在有机胺分子中引入三氟甲基基团的化合物。
三氟甲基基团由一个碳原子和三个氟原子组成,属于高度电负的基团,在有机合成中具有广泛的应用。
常见的三氟甲基化有机胺类化合物包括三氟甲基胺
(CF3NH2)、三氟甲基甲胺(CF3CH2NH2)、三氟甲基苯
胺(CF3C6H4NH2)等。
这些化合物常用于药物、农药、材
料等领域的研究和开发中。
三氟甲基化有机胺类化合物具有很高的化学稳定性,并且可以通过引入三氟甲基基团改变原有化合物的性质,如增加溶解性、改善生物利用度等。
三氟甲基化有机胺类化合物的合成方法有多种,常用的方法包括三氟甲基化反应、亲核取代反应等。
其中,三氟甲基化反应是通过引入三氟甲基化试剂(如三氟甲基化化合物、三氟甲基化试剂溶液)来实现的,具体反应条件和步骤根据具体化合物而定。
总体而言,三氟甲基化有机胺类化合物在有机化学领域中具有重要应用价值,不仅可以扩展化合物的化学性质,还可以用于新药物和新材料的合成。
《有机化学》(第四版)第五章芳烃(习题答案)
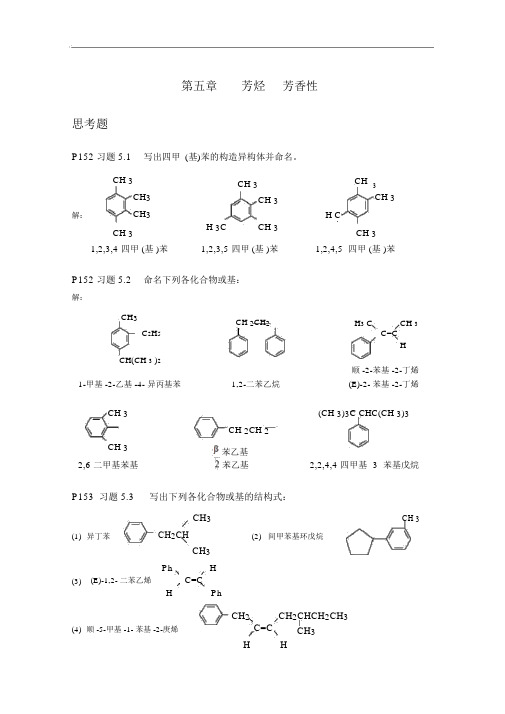
第五章芳烃芳香性思考题P152 习题 5.1写出四甲(基)苯的构造异构体并命名。
CH 3CH 3CH3 CH3CH 3CH 3解:CH3H CCH 3H 3C CH 33CH 31,2,3,4-四甲 (基 )苯1,2,3,5-四甲 (基 )苯1,2,4,5- 四甲 (基 )苯P152 习题 5.2命名下列各化合物或基:解:CH3CH 2CH2H3 C CH 3 C2H5C=CH CH(CH 3 )2顺 -2-苯基 -2-丁烯1-甲基 -2-乙基 -4- 异丙基苯1,2-二苯乙烷(E)-2- 苯基 -2-丁烯CH 3(CH 3)3C CHC(CH 3)3CH 2CH 2CH 3-苯乙基2,6-二甲基苯基2,2,4,4-四甲基 -3- 苯基戊烷-苯乙基P153 习题 5.3写出下列各化合物或基的结构式:CH3CH 3 (1)异丁苯CH2CH(2) 间甲苯基环戊烷CH3Ph H(3)(E)-1,2- 二苯乙烯C=CH Ph(4)顺 -5-甲基 -1- 苯基 -2-庚烯CH2C=CCH2CHCH2CH3CH3H H(5)二苯甲基 C 6H 5CH C 6H 5(6) 3- 苯基 -2-丙烯基CH 2 CH=CH C 6H 5P156 习题 5.4甲苯的沸点比苯高 30.5℃,而熔点低 ~100℃,为什么?解:甲苯的相对分子质量大于苯,分子间 色散力 大于苯,因比甲苯的沸点也高于苯;但苯分子的 对称性 好,晶格能大于甲苯,因此苯的熔点高于苯。
P161 习题 5.5写出乙苯与下列试剂作用的反应式 (括号内是催化剂 ):(1) Cl 2 (FeCl 3 )(2) 混酸 (3) 正丁醇 (BF 3)(4) 丙烯 (无水 AlCl 3 )(5) 丙酸酐 (CH 3CH 2CO)2O(无水 AlCl 3)(6) 丙酰氯 CH 3CH 2COCl( 无水 AlCl 3)解: (1) CH 3CH 2Cl 2CH 3CH 2CH 2CH 3FeCl 3Cl+ClCH 3CH 2 混酸CH 3CH 2CH 2CH 3(2)NO 2+NO 2CH 2CH 3C 2H 5+CH 2CH 3(3)CH 3(CH 2)3OHCHCH 2CHBF 33CHCH 2CH 3CH 3CH 3CH 2CH 3CH 2CH 3CH 2CH 3CH 2=CHCH 3(4)+无水 AlCl 3CH(CH 3)2CH(CH 3)2CH 2CH 3CH 2CH 3CH 2CH 3(CH 3CH 2CO)2O(5)+无水 AlCl 3COCH 2CH 3O CCH 2CH 3CH 2CH 3CH 2CH 3CH 3CH 2COClCH 2CH 3(6)无水 AlCl 3+COCH 2CH 3O CCH 2CH 3P161 习题 5.6由苯和必要的原料合成下列化合物:(1)H 2SO 4解:+ HO (或环己烯 )(2) 叔丁苯CH 3H 2SO 4CH 3 解:C CH 3 + CH 2=C CH 3CH 3(3) CH 2 (CH 2)5 CH 3解:OOAlCl 3C(CH) CH Zn-HgCH 2(CH 2)5CH 32 + CH 3(CH 2)5C Cl53HClO O (4)C CH 2CH 2C OHOOO解:+O AlCl 3C CH 2CH 2C OHOP164 习题 5.7 试以苯和必要的原料合成正丙苯。
定位效应的解释

同学们,大家好。
今天要讲的是定位效应的解释。
通过上节课的学习,我们已经知道,有些基团会使苯环的亲电取代反应活性增大,称为活化基;有些基团会使苯的亲电取代反应活性减小,称为钝化基;苯环上的基团还会影响取代位置,根据定位效果分为邻对位定位基和间位定位基。
苯环上原有基团为什么会影响亲电取代活性和取代位置呢?今天我们就来分析并解释这一问题。
大家都知道,苯亲电取代时,亲电试剂靠近苯环生成σ-络合物是整个反应的决速步骤。
同样,取代苯反应的决速步骤也生成σ-络合物,如图,决速步骤中苯与亲电试剂的成键能力与苯环上电子密度有关。
若原有基团是供电子基,苯环电子密度增大,容易受到亲电试剂的进攻,则亲电取代活性增大,该基团就是活化基。
若原有基团是吸电子基,会使苯环电子密度减小,吸引亲电试剂的能力减小,则反应活性减小,该基团是钝化基。
因此判断一个基团是活化基还是钝化基,只需要分析基团与苯环间的电子效应(包括诱导效应和共轭效应)来确定该基团是供电子基还是吸电子基即可。
那么如何分析判断一个基团是邻对位定位基还是间位定位基呢?从反应式可以看出,决速步骤中生成了三种σ-络合物:邻位、间位、对位,这三个平行反应的相对速度决定了最终产物的多少,即决定了取代位置。
这三个平行反应的相对速度可以从两个角度比较。
一方面可以从反应物中邻、间、对三个位置上碳的电子密度相对大小分析。
基团与苯环间的电子效应使邻间对位碳上电子密度不同,电子密度大的碳自然容易受到亲电试剂的进攻而表现出较大的反应活性。
另一方面也可以从三个σ-络合物的稳定性比较。
σ-络合物越稳定,能量越低,生成时经历的过渡态能量越低,反应的活化能越小,反应速度快,相应的σ-络合物生成的就多。
通过以上讲解,大家脑海中要有这样几个概念:第一,分析基团与苯环间的电子效应可以判断基团是供电子基还是吸电子基,从而来确定基团使苯环活化还是钝化;第二,分析基团与苯环间的电子效应可以比较邻间对位碳的电子密度大小,以此判断基团的定位效果;第三,分析σ-络合物的稳定性也可以判断基团的定位效果。
三氟甲氧基 定位基 -回复

三氟甲氧基定位基-回复什么是三氟甲氧基定位基?三氟甲氧基定位基是一种有机化学中常用的官能团,由一个氟原子和一个甲氧基(OCH3)组成。
它可以被引入到分子中的特定位置,以便在后续的有机合成过程中进行定向的化学反应。
三氟甲氧基定位基的引入和去除操作相对简单,因此在有机合成中被广泛应用。
三氟甲氧基定位基的引入方法可以分为两种:直接引入和氟化后引入。
直接引入三氟甲氧基的方法多数是通过两步反应来实现的。
首先,在反应溶剂中加入三氟甲基酮或三氟甲基酸酯,并加入亲电溴化剂(如溴或亚氯化亚铜),使其发生亲电取代反应,把三氟甲基引入目标分子。
然后,添加氢氧化钠或其他碱性试剂来负离子化三氟甲基,进而得到三氟甲氧基定位基。
氟化后引入三氟甲氧基的方法则是先将目标分子部分或全部氟化,然后再通过亲核取代反应引入甲氧基。
常用的氟化剂有氟化氢、三氟化锂等。
通过在反应中以氟化离子取代其他基团,将目标分子进行氟化,生成相应的氟代物。
然后再加入甲醇或甲醇锂等亲核试剂,使其与氟代物发生取代反应,从而引入三氟甲氧基。
三氟甲氧基定位基具有许多应用,如合成有机化合物、药物研究和杂环合成等领域。
在有机合成中,三氟甲氧基可以通过氢化反应或析出反应等去除,同时保持其他官能团的稳定性。
这使得它成为一种常用的定位基,用于合成复杂的有机分子。
除了引入和去除操作之外,定位基的选择也很重要。
三氟甲氧基是一种较为稳定的基团,与许多官能团可进行化学反应,而不易发生副反应。
此外,其引入和去除操作较为方便,使得三氟甲氧基定位基成为有机合成中的重要一环。
总结起来,三氟甲氧基定位基是一种在有机合成中常用的官能团,它可以被引入到分子的特定位置,以便在后续的有机合成过程中进行定向的化学反应。
其引入和去除操作相对简单,稳定性较高,并且使用广泛。
在有机合成中,合理选择和使用三氟甲氧基定位基将为合成有机化合物提供更多的可能性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
三氟甲基和氨基定位效应
三氟甲基和氨基都是常见的取代基团,它们在化学反应中都会产生定位效应。
1. 三氟甲基定位效应:三氟甲基基团是电子密度较高的取代基,通过共轭效应和电子吸引效应,可以影响邻位和对位的反应性。
三氟甲基常常会增加邻位的亲电性,使得邻位易于发生亲电取
代反应。
此外,三氟甲基还可以通过电子吸引效应,使对位的电荷密度降低,减少对位的亲电位。
因此,三氟甲基常常表现出较强的取向效应,使反应选择性增强。
2. 氨基定位效应:氨基(NH2)基团是亲核基团,通过共振效应和电子给体效应,可以影响邻
位和对位的反应性。
氨基基团可以提供一个孤对电子,通过这个电子对的共振,影响邻位的亲
电性。
此外,氨基基团还可以通过电子给体效应,提供电子密度,增加对位的亲电性。
因此,
氨基基团也可以表现出一定的取向效应,使反应具有一定的选择性。
总而言之,三氟甲基和氨基都能够通过共轭效应、电子吸引效应、共振效应和电子给体效应等
方式,对邻位和对位的反应进行定位效应的调控。
具体的反应定向规律会受到其他反应条件和
基团环境的影响,需要具体问题具体分析。
