11食品中元素含量的测定
食品中铅、镉、铬的测定

实验八:食品中铅、镉、铬的测定(原子吸收光谱法综合性试验)一、目的与要求1.通过实际试样,对食品中的多种限量金属成分,采用不同的光谱分析条件进行测定,以达到综合应用原子吸收光谱法的目的。
2.根据各元素的分析特性,试样的含量,基体组成及可能干扰选取合适的分析条件。
包括了试样的制备、预处理、标准溶液的配制及校正曲线的制作、分析条件的选择、操作方法、结果计算、数据处理及误差分析等。
二、实验原理与相关知识食品中有害金属元素铅、镉、铬的测定,目前国际上通用的方法均以石墨炉原子化法较为准确、快速。
该法检出限为5μg/kg,基于基态自由原子对特定波长光吸收的一种测量方法,它的基本原理是使光源辐射出的待测元素的特征光谱通过样品的蒸汽时,被蒸汽中待测元素的基态原子所吸收,在一定范围与条件下,入射光被吸收而减弱的程度与样品中待测元素的含量成正比关系,由此可得出样品中待测元素的含量。
食品中铅、镉、铬等元素的基态原子对空心阴极灯的共辐射都有选择性吸收,但是各元素具体的分析条件不同,例如铅的测定是氧化性气氛,但铬的测定却要求还原性气氛,并且要有高性能的空心阴极灯才能获得足够的灵敏度。
这些元素的灵敏度都有差别,因此配制标准序列时,浓度序列有所不同,但是它们在一定的浓度下,彼此不会干扰,因而可以把它们的标准溶液混合配在一起,方便操作。
三、仪器与试剂1.实验室提供的仪器与试剂(1)石墨炉原子吸收分光光度计(具氘灯扣背景装置)及其它配件;(2)氮气钢瓶;(3)铅、镉、铬等元素空心阴极灯。
(4)基准试剂:铅、镉、铬标准贮备液。
(5)基体改进试剂:①磷酸二氨铵溶液(20g/L);②盐酸溶液(1mol/L);③柠檬酸钠缓冲溶液(2mol/L);④双硫腙-乙酸丁酯溶液(0.1%);⑤二乙基二硫代氨基甲酸钠溶液(1%)2.由学生自配试剂(1) 铅、镉、铬系列标准使用溶液;(2) 样品消化及定容用试剂。
四、实验方案的设计提示1.测定各元素离子时样品的处理方案样品经消解(可选用干法灰化、压力消解法、常压湿法消化、微波消解法中的任何一种)后,制成供试样液,可参考表5-3-12.测定各元素离子的标准系列配制方案:可参考表表5-3-2或参考其他资料.3.测定铅、镉、铬的条件选择:由于仪器型号规格不同,测定条件有所差别,可根据仪器说明书选择最佳条件测试,可参考表5-3-3. 表5-3-1 食品中铅、镉、铬测定用样品的处理表5-3-2 金属离子标准溶液系列五、实验步骤(按设计的方案进行实验)(一) 样品处理(可参照表5-3-1 食品中铅、镉、铬测定用样品的处理) (二) 操作步骤参照仪器说明书,根据各自仪器性能及设计的方案调至最佳状态,简要步骤如下: 1. 安装待测元素空心阴极灯,对准位置,固定待测波长及狭缝宽度。
ECP-MS法测定饮用水、绿茶、大米中10种元素的含量

第 3 4卷第 6期
I C P — MS 法测定饮用水 、 绿茶 、 大米中1 0 种 元素的含量
董旭, 何绍 媛 , 杜杰 , 戴炳业 。 石楠 , 王硕
( 天津科 技大学 食 品工程 与生物技术学 院 , 食 品营养与安全教育部重点实验室 , 天津 3 0 0 4 5 7 )
摘 要: 建立湿法 消解一 电感耦合等 离子体质谱 法( I C P — MS ) 同时测定饮 用水 、 绿 茶和大米样 品 中钒 、 铬、 镍、 铜、 砷、
B i o t e c h n o l o g y , T i a n J i n U n i v e r s i t y o f S c i e n c e a n d T e c h n o l o g y , T i a n J i n 3 0 0 4 5 7, C h i n a )
测定水和植物样品 中 l 0种 元 素 的检 测 。
关键词 : 电感耦合等 离子体质谱 ; 元素 ; 饮 用水; 绿茶 ; 大米
De t e r mi na t i o n o f Te n Me t a l El e me nt s i n Dr i nk i ng Wa t e r,Gr e e n Te a a n d Ri c e by I CP-M S
Ab s t r a c t : A me t h o d f o r s i mu l t a n e o us l y d e t e c t i o n o f V,Cr ,Ni ,Cu,As ,S e ,Mo ,Cd, S b,P b i n d r i n k i n g wa t e r ,
原子吸收光谱法测定食品中锌的含量

移入马弗炉中在500±25℃下灰化8h后,取出坩埚 加入小量混合酸,以小火加热。反复处理至残渣 中无炭粒,加10mL(1+11)盐酸溶解后移入50mL容 量瓶,再用 (1+11)盐酸定容至刻度.
分别吸取奶粉样液0.00、1.25、2.5、5.00mL 于25mL容量瓶中并定容至刻度,待测(浓 度分别为0.00、0.20、0.40、0.80ug/mL)
走平后,点“自动调零” 。 ②.吸锌标液为0.00ug/ml(空白)溶液,待曲线走
平后,点“空白”进行数据的测定。 ③.吸锌标液,待曲线走平后,点“开始”,读完
数后,吸取一段时间的蒸馏水使曲线走平 ④.更换下一个浓度的标液,重复③至测定所有标
液
样品(葡萄糖酸锌)测定
1.待锌标准曲线绘制完并用蒸馏水调零后, 更换样品(葡萄糖酸锌),待曲线走平后, 点“开始”,读完数后,记录吸光值读数、 吸一段时间的蒸馏水并调零。
3.分别吸取0.00、0.20、0.40、0.80、1.60mL锌的标 准使用液于25mL容量瓶中,再以(1mol/L)HCL稀 释至刻度,待测。(浓度依次为:0.0、0.20、0.40、 0.80、1.60ug/mL)
预实验:
样品:(葡萄糖酸锌、奶粉、粒,所
锌标准溶液配制
1.锌的标准储备液:称取0.5000g锌粉溶于10mL盐 酸中,然后在水浴蒸发至干,在用小量水溶解后 移入1000mL容量瓶中,以水稀释至刻度。备用。 (浓度为0.5mg/mL)
2.锌的标准使用液:吸取2.5mL锌的标准贮备液于 50mL容量瓶中,以(0.1mol/L)盐酸稀释至刻 度.(浓度为25ug/mL).
食品中矿物质的测定

(3)仪器 原子吸收分光光度计、钙空心阴极灯 (4) 操作步骤 1. 样品制备 湿样(如蔬菜,水果,鲜鱼,鲜肉等)用水清洗干净
(4)操作步骤 消化:精确称取均匀样品干样0.5~1.5g(湿样2.0~4.0g,饮料 等液体样品5.0~10.0g)于250ml高型烧杯内,加混合酸消化液 20~30ml.上盖表皿.置于电热板或电沙浴上加热消化.如未消 化好而酸液过少时,再补加几毫升混合酸消化液,继续加热消化, 直至无色透明为止.
后,要用去离子水充分洗净.干粉类样品(如面粉,奶粉等)取 样后立即装容器密封保存,防止空气中的灰尘和水分污染. 2. 样品消化 精确称取均匀样品干样0.5~1.5g(湿样2.0~ 4.0g,饮料等液体样品5.0~10.0g)于250ml高型烧杯内,加 混合酸消化液20~30ml.上盖表皿.置于电热板或电沙浴上 加热消化.如未消化好而酸液过少时,再补加几毫升混合酸 消化液,继续加热消化,直至无色透明为止.
二、铁的测定—邻二氮菲法
1,原理: 在pH为2~9的溶液中,二价铁离子与邻二氮菲生成稳 定的橙红色配合物,在510nm有最大吸收,其吸光度与铁的含量成 正比,故可比色测定.
2,试剂 ①盐酸羟胺溶液:10% ②邻二氮菲水溶液(新鲜配 制):0.12% ③醋酸钠溶液:10% ④盐酸:1mol/L ⑤铁标准溶液
③ 柠檬酸铵溶液
④ 淀粉指示液
⑤ 二硫腙-三氯甲烷溶液 ⑥ 二硫腙使用液 ⑦ 铅标准溶液 ⑧ 铅标准使用液 3.仪器 分光光度计 4操作步骤 (1)样品预处理 在采样和制备过程中,注意样品不被污染。 粮食、水果、鱼类、肉类及蛋类等水分含量高的鲜样,用食品 加工机大成匀浆存于塑料瓶中,保存备用。 (2)样品消化(灰化法)
高效液相色谱法快速检测食品中12_种添加剂
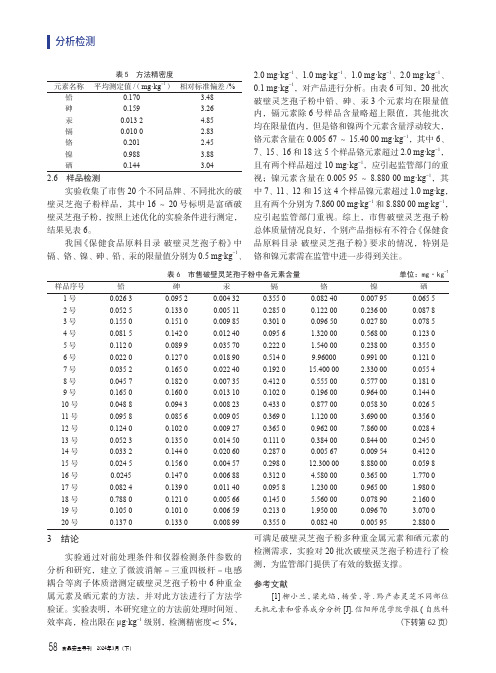
表5 方法精密度元素名称平均测定值/(mg·kg-1)相对标准偏差/%铅0.170 3.48砷0.159 3.26汞0.013 2 4.85镉0.010 0 2.83铬0.201 2.45镍0.988 3.88硒0.144 3.042.6 样品检测实验收集了市售20个不同品牌、不同批次的破壁灵芝孢子粉样品,其中16~20号标明是富硒破壁灵芝孢子粉,按照上述优化的实验条件进行测定,结果见表6。
我国《保健食品原料目录破壁灵芝孢子粉》中镉、铬、镍、砷、铅、汞的限量值分别为0.5 mg·kg-1、2.0 mg·kg-1、1.0 mg·kg-1、1.0 mg·kg-1、2.0 mg·kg-1、0.1 mg·kg-1,对产品进行分析。
由表6可知,20批次破壁灵芝孢子粉中铅、砷、汞3个元素均在限量值内,镉元素除6号样品含量略超上限值,其他批次均在限量值内,但是铬和镍两个元素含量浮动较大,铬元素含量在0.005 67~15.40 00 mg·kg-1,其中6、7、15、16和18这5个样品铬元素超过2.0 mg·kg-1,且有两个样品超过10 mg·kg-1,应引起监管部门的重视;镍元素含量在0.005 95~8.880 00 mg·kg-1,其中7、11、12和15这4个样品镍元素超过1.0 mg·kg,且有两个分别为7.860 00 mg·kg-1和8.880 00 mg·kg-1,应引起监管部门重视。
综上,市售破壁灵芝孢子粉总体质量情况良好,个别产品指标有不符合《保健食品原料目录破壁灵芝孢子粉》要求的情况,特别是铬和镍元素需在监管中进一步得到关注。
表6 市售破壁灵芝孢子粉中各元素含量 单位:mg·kg-1样品序号铅砷汞镉铬镍硒1号0.026 30.095 20.004 320.355 00.082 400.007 950.065 5 2号0.052 50.133 00.005 110.285 00.122 000.236 000.087 8 3号0.155 00.151 00.009 850.301 00.096 500.027 800.078 5 4号0.081 50.142 00.012 400.095 6 1.320 000.568 000.123 0 5号0.112 00.089 90.035 700.222 0 1.540 000.238 000.355 0 6号0.022 00.127 00.018 900.514 09.960000.991 000.121 0 7号0.035 20.165 00.022 400.192 015.400 00 2.330 000.055 4 8号0.045 70.182 00.007 350.412 00.555 000.577 000.181 0 9号0.165 00.160 00.013 100.102 00.196 000.964 000.144 0 10号0.048 80.094 30.008 230.433 00.877 000.058 300.026 5 11号0.095 80.085 60.009 050.369 0 1.120 00 3.690 000.356 0 12号0.124 00.102 00.009 270.365 00.962 007.860 000.028 4 13号0.052 30.135 00.014 500.111 00.384 000.844 000.245 0 14号0.033 20.144 00.020 600.287 00.005 670.009 540.412 0 15号0.024 50.156 00.004 570.298 012.300 008.880 000.059 8 16号0.02450.147 00.006 880.312 0 4.580 000.365 00 1.770 0 17号0.082 40.139 00.011 400.095 8 1.230 000.965 00 1.980 0 18号0.788 00.121 00.005 660.145 0 5.560 000.078 90 2.160 0 19号0.105 00.101 00.006 590.213 0 1.950 000.096 70 3.070 0 20号0.137 00.133 00.008 990.355 00.082 400.005 95 2.880 03 结论实验通过对前处理条件和仪器检测条件参数的分析和研究,建立了微波消解-三重四极杆-电感耦合等离子体质谱测定破壁灵芝孢子粉中6种重金属元素及硒元素的方法,并对此方法进行了方法学验证。
食品中微量元素的常规检验方法

食品中微量兀素的常规检验方法食品中微量兀素的常规检验方法摘要:现如今人们对食品安全问题越来越重视,对社会报道的食品安全事件较为关注,尤其是对于食品中微量元素的污染问题,逐渐成为人类健康的核心影响因素之一,对食品安全有严重的威胁。
因此,食品中微量元素的测定已成为当前食品安全检查中的核心工作内容。
但我国与发达国家的食品安全测定与问题分析相比较而言还存在较大的差距。
关键词:食品安全微量元素检验测定引言:随着国民经济的快速发展,食品安全问题已经成为我国发展过程中需要面临的重要难题和挑战,对于政府的食品安全检测部门和生产企业都是一个巨大的考验。
我国现有的食品中微量元素的检测方式已经不能满足现代社会发展的需要,迫切需要完善的检验方式,一门新兴的边缘化科学“生命科学中的微量元素”由此应运而生。
本文就当前常规的食品微量元素的检验方法及其测定的重要性进行分析探讨。
一、原子荧光光谱法每种元素的原子荧光强度都是特定的,根据此原理就可以检验出待测的元素含量。
这种方法的特点是检测的灵敏度较高,实施过程中的干扰比较少,具有较宽的线性范围,并且能够将较多的元素放在一起同时检测分析。
NaBH4与汞离子、SnCL2与汞离子都可以反应形成原子态的汞,在室温环境中能够被相互作用从而变成汞原子荧光,这种方式叫做冷原子荧光光谱法,也可以称作冷蒸汽法。
因为AFS的测定方法对检验汞的敏感程度较高,所以在分析样品汞含量的时候通常较多的运用冷原子荧光与无焰、有焰HG-AFG^几种测定方式。
如果想要检验大米当中的汞元素就可以使用原子荧光光谱法,它是通过微波加热的方式使样品在温度较高和压力较大的环境下消解样品。
同时也可以利用此方法检验错这一微量元素,它多存在于保健食品当中。
可以研究酸介质和氢氧化物等因素对检验所产生的影响。
把仪器最适宜的工作条件选定出来,用酒石酸来进行检验,不仅能够打破干扰因素共存离子,还能够增敏,可以适用于在室温原子化环境下检验错在保健食品中的痕量。
食品中重金属残留的检测方法

食品中重金属残留的检测方法随着人们对健康的重视程度逐渐提高,食品安全问题成为了人们关注的重点之一。
其中,食品中的重金属残留问题备受关注。
重金属是指比较密度较大,具有较强的毒性和生物积累性的元素,如铅、汞、镉、砷等。
食品中的重金属残留会对人体造成很大的危害,因此必须对食品中的重金属含量进行检测。
下面将介绍一些常见的食品中重金属残留的检测方法。
一、原子吸收光谱法(AAS)原子吸收光谱法是一种分析化学方法,可用于检测食品中的重金属残留。
该方法的基本原理是利用原子对吸收较明显的某种波长的光的量与元素浓度之间的关系来分析元素。
AAS法具有灵敏度高、专属性强、分析时间短、误差小等优点,但是该法的适用性和灵敏度仅限于特定元素,且样品处理方法较为繁琐。
二、电感耦合等离子体发射光谱法(ICP-OES)电感耦合等离子体发射光谱法是一种分析化学方法,用于分析食品中的重金属元素含量。
该方法的原理是利用样品在高温下气化,生成几千度高温下的等离子体,再用光电多道辐射计测定不同波长的辐射强度,进而分析样品中重金属元素的含量。
ICP-OES 法具有分析速度快、灵敏度高、准确度好等优点,但是设备较为昂贵,需要专业技术人员操作。
三、电感耦合等离子体质谱法(ICP-MS)电感耦合等离子体质谱法是一种高灵敏度的分析方法,可用于检测食品中的重金属元素含量。
该方法的原理是利用设备将样品中元素离子化成带正电荷的离子,并测定离子的质量和相对丰度,进而分析样品中重金属元素的含量。
ICP-MS法具有极高的灵敏度和准确度,但是设备价格昂贵,需要专业技术人员操作。
四、原子荧光光谱法(AFS)原子荧光光谱法是一种基于元素的原子荧光现象实现的分析技术,可用于检测食品中的重金属元素含量。
该方法的基本原理是通过激发样品中重金属元素的原子产生荧光,然后测定荧光的强度,从而确定元素的含量。
AFS法具有高准确性、精度高、测定速度快等特点,但是分析的元素种类相对较少,且需要较为严格的样品预处理。
检测食品成分实验报告(3篇)

第1篇一、实验目的本次实验旨在通过化学分析和仪器分析方法,检测食品中的主要成分,包括蛋白质、脂肪、碳水化合物、矿物质、维生素等,以了解食品的营养成分和卫生状况。
二、实验原理1. 蛋白质:采用双缩脲法测定蛋白质含量,原理为蛋白质中的肽键与双缩脲试剂发生反应,生成紫色络合物,其颜色深浅与蛋白质含量成正比。
2. 脂肪:采用索氏抽提法测定脂肪含量,原理为脂肪不溶于水,可被有机溶剂抽提,通过称量抽提出的脂肪量来计算脂肪含量。
3. 碳水化合物:采用苯酚-硫酸法测定碳水化合物含量,原理为碳水化合物与苯酚在硫酸作用下生成蓝绿色化合物,其颜色深浅与碳水化合物含量成正比。
4. 矿物质:采用原子吸收光谱法测定矿物质含量,原理为样品中的矿物质元素在特定波长下吸收特定波长的光,通过测定吸光度来计算元素含量。
5. 维生素:采用高效液相色谱法测定维生素含量,原理为维生素具有特定的紫外吸收峰,通过测定样品的紫外吸收光谱来计算维生素含量。
三、实验材料1. 样品:面粉、牛奶、鸡蛋、水果等。
2. 试剂:双缩脲试剂、苯酚、硫酸、盐酸、氢氧化钠、三氯化铁、氯化钠、硝酸、高氯酸、原子吸收光谱标准溶液、维生素标准溶液等。
3. 仪器:分光光度计、索氏抽提器、电子天平、原子吸收光谱仪、高效液相色谱仪等。
四、实验步骤1. 蛋白质含量测定(1)称取样品0.5g,加入5mL双缩脲试剂,充分混合,室温放置10min。
(2)以试剂空白为参比,在540nm波长下测定吸光度。
(3)根据标准曲线计算蛋白质含量。
2. 脂肪含量测定(1)称取样品5g,加入50mL石油醚,在索氏抽提器中抽提6h。
(2)将抽提液转移至锥形瓶中,挥去石油醚,加入5mL盐酸,加热至近干。
(3)加入5mL氢氧化钠溶液,充分混合,加入5mL三氯化铁溶液,静置10min。
(4)以试剂空白为参比,在520nm波长下测定吸光度。
(5)根据标准曲线计算脂肪含量。
3. 碳水化合物含量测定(1)称取样品5g,加入10mL苯酚溶液,充分混合。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
食品缶头马口铁焊锡中铅含量达40-60%,有时会 溶于食品中形成污染。会引起中毒。含铅“松花蛋”。
离地面1m处空气铅浓度是1.5m处的16倍,儿童 受害,2000年8月调查北京、广州城市儿童铅高率 达80%左右。验头发。
晶状粉末。可溶于三氯甲烷及四氯甲烷中,溶液呈绿 色。
(二)双硫腙与金属离子的反应 在酸性溶液中并有过量双硫腙存在时生成单取代
双硫腙盐,即1个双硫腙分子中有1个H原子被金属离子 所取代,二价金属离子则同时与2个双硫腙分子反应。
在碱性溶液中或双硫腙量不足时、生成 二代(双取代)双硫腙盐,即1个双硫腙分 子中有两个H原子同时被金属离子所取代。
国标的方法:石墨炉原子吸收光谱法
原理:
酸性溶液中,镉离子与碘离子形成络合物,并经 4-甲基戊酮—2萃取分离,导入原子吸收仪中,原子 化后,吸收228.8nm共振线,与标准系列比较定量。 镉标准溶液:用金属镉溶于HCL中加 HNO3+H2O稀 释。
4、汞的测定
汞多用于电气仪器及设备、电解食盐、农药等等。
2、锌的测定(Zn)
GB 5009.14-2017
锌用在电镀、造纸、机械和自来水的制造等工业 中应用,镀锌厂的废水,采用镀锌铁的容器包装食 品,特别是酸性饮料,易沾有锌。 金属锌本身无害。 锌化合物可引起急性肠炎、肾损害,特别是氯化 锌3-5g可导致死亡。
(1)双硫腙比色法
用二硫腙分别提取2次 用二硫腙提取1次
(2)原子吸收分光光度法(国标中第一法)
样品处理后,导入原子吸收分光光度计中, 原子化后,吸收213.8 nm共振线,其吸收量 与Zn量成正比。
3 、 镉 的测 定 ( Cd) GB 5009.15—2014
镉用于冶金、电镀、颜料、原子工业、农药等, 生活用水,因使用镀锌、塑料管中镉的污染经 消化道、呼吸道进入人体,损害人的肾、肝, 易引起“骨痛病”。
原理:在pH 4.5-5.0,锌离子与双硫腙生成红色络
合物,此络合物溶于CCl4 ,其它金属离子靠加入硫 代硫酸钠、盐酸羟胺溶液和pH值的控制。
•仪器:分光光度计
530nm处测定吸光度
•要领:
①锌标准曲线重现性差,平行作1-2份标准锌,以进 行校正。
②硫代硫酸钠不能任意增加,因为它也能络合锌。
③本法灵敏度较高,必须严格控制pH值,同时所用水 应为无锌水,经阴、阳离子交换树脂纯化。器皿也先 用硝酸溶液洗涤,然后再用无离子水冲洗干净。
另外还有: 1、栎精比色法(又叫栎皮黄素,一种天然染料) 2、二硫酚法 3、碘法 4、原子吸收分光光度法 灵敏度约为1ppm。
GB 5009.16—2014 《食品中锡的测定》
1. 氢化物原子荧光光谱法
2. 苯芴酮比色法
(二)铜的测定
GB 5009.13—2017 中第一法是石墨炉原子吸收光谱法
11 食品中元素含量的测定
第一节 概述 食物中各种元素对人体来说,分为:
必需元素
非必需元素 有毒元素
人体内矿物质大约占人体重量 6%,其中包 括常量元素、微量元素、有毒元素。
一 . 常 量 元 素 : K 、 Na 、 Ca 、 Mg 、 P 、 Cl 、 S 二.微量元素:
在肌体中起作用的浓度以ppm、ppb计。是 人体必需的、但过量又会中毒的元素,现有14 种。
主要仪器:
消化装置:上带冷凝管的平底烧瓶。
721型分光光度计
(2)测汞仪法(<1 mg/kg)又叫冷离子吸收法现
有590型测汞仪。 (3)甲基汞测定: 1、薄层层析分离 2、气相色谱法
另:分离测定痕量汞时要注意试剂、滤纸、 橡皮管上可能含有少量汞。
汞若洒在地上,应马上用吸尘器或用洗耳 球吸除干净,或用脱汞剂去除。 (1)硫磺粉 (2)20%FeCl2溶液 (3)矿物油+含有粉末硫、碘的水→乳浊液 (4)盐酸酸化的10%KMnO4溶液。
• 2、锰的测定(分光光度法)
原理:
样品经消化后,在酸性条件下二价锰被过 碘酸钾氧化成七价锰呈紫红色,与标准比较定 量。反应式如下: 2Mn2++5KIO4+3H2O→2MnO4-+5KIO3+6H+
一、双硫腙比色法测 Pb、Zn、Cd、Hg的含量
(一)双硫腙的结
② 铅:在体内半衰期为1460天。
在骨骼中为10年 ③ 镉在体内半衰期为16—31年。
北京部分 农产品含 砷量过高 可能导致 中毒!
04年网上 报道。
2.微量元素与有毒元素合称限量元素。
3. 这些物质进入人体的渠道有:水源、土壤、环 境、原料、辅料、添加剂、农药、化肥的使用、加 工、制造、运输等带入;容器本身不纯,金属带入 铅、锌;罐头中酸性锡的溶出;铜器带入过量铜; 另外,还有呼吸、皮肤。
铜在工业广泛应用,铜的化合物作为 杀虫剂、杀菌剂和消毒剂等。食品加工中 由于使用铜器而易于受污染,铜是人体所 必须的微量元素,但过量在人体积累中毒 可引起肝肾障碍,甚至死亡。经“食物链” 进入人体。
• 书中介绍:二乙胺基二硫代甲酸钠比色 法,常 用的方法,最低检出量为2.5 μg。
(三)铬的测定
铬用于印染、电镀、制革工业中。主要是6价 铬对人体造成危害。 测定方法
工业自动化越发展,汞的用量越大,环境污染就越
严重。污染严重的日本、瑞典40ug/人· 天摄入,其 它国家10 ug/人·天,
FAO/WHO规定34 ug/人·天,
中国食品汞允许量(mg/kg)
粮食 0.02 禽肉蛋 0.05
水产 0.3
牛乳 0.01
蔬菜水果 0.01 植物油 0.05
汞挥发性强,气态汞被人呼吸进入肺部,大部 分进入红血球中;进入消化道;接触或皮肤吸收进 入体内。
布不牢而溶锡,有机锡毒性很大,如锡化氢SnH4 1、苯芴酮比色法 样品消化后,在酸性介质中,4价锡离子与苯芴
酮生成的橙红色胶体颗粒络合物,在动物胶存在下 不聚集,可比色定量。
加抗坏血酸、酒石酸作掩蔽剂,排除铁离子干 扰。
仪器:分光光度计 490 nm处测吸光度 注意:天冷时,由于显色反应很慢,标准和样品分析 溶液加入显色剂后,可在37℃恒温箱放置30分钟,再 比色。
GB 5009.17—2014 《食品中总汞及有机汞的测定》 总汞的测定:
1. 原子荧光光谱法 2. 冷原子吸收光谱法 甲基汞的测定: 液相色谱-原子荧光光谱联用方法
二、其他比色法测定锡、铜、铬的含量
选用比双硫腙专用性更强的螯合剂进行测定。
(一)锡的测定
除了工业污染外,罐头食品中镀锡马口铁有时 被内容物侵蚀,产生了溶锡现象,还有的因焊锡涂
汞对中枢神经损害, 汞蒸汽中毒:兴奋亢进、易怒、健忘失眠。 汞急性中毒:恶心、呕吐、腹痛、肾损害、
死亡。 有机汞毒性更强,特别是甲基汞: 使人感官失调、视野缩小、头发损伤、各机 群间共济失调。
(1)比色法:(>1 mg/kg)
原理:双硫腙氯仿溶液与样品中汞离子在酸性条 件下生成双硫腙汞,在氯仿溶液中呈橙黄色,颜色深 浅与汞离子浓度成正比。
③如果样品中含Ca、Mg的磷酸盐时,不要加柠檬酸铵, 避免生成沉淀带走使铅损失。
④样品中含锡量>150mg时,要设法让其变成溴化锡, 而蒸发除去,以免产生偏锡酸而使铅丢失。
⑤测铅要用硬质玻璃皿,提前用1-10% HNO3浸泡,再 用水冲洗干净。
(2)原子吸收分光光度法 这是国标中第一方法。 灵敏度高,可用来测定含量> 0.01% 痕量铅。 GB 5009.12—2017 《食品中铅的测定》 1.石墨炉原子吸收光谱法 2.电感耦合等离子体质谱法 3.火焰原子吸收光谱法 4.二硫腙比色法
铅能与许多有机试剂生成带有颜色的化合物, 常用来比色测定的还是双硫腙。
(1)双硫腙法
原理:在碱性(pH值在9左右)溶剂中,Pb2+ 双硫腙形成红色络合物,溶于氯仿或CCl4中,红色 深浅与铅离子浓度成正比,比色测定。
测定前要加盐酸羟胺、氰化钾、柠檬酸铵来 掩蔽铁、铜、锡、镉等离子。
测定步骤: (1)用铅标准溶液(1ug/ml)标定双硫腙溶
• 日本,前几年流行含金食物,内含银、铜等杂质。 • 饮水、食品、茶叶、烟草、化妆品等都可能被污 染,环境污染已成为世界问题。
•食物链——水
鱼
农作物
食品
饲料
家畜
鸭子 人 肉制品
4.我国食品安全法对食品中有害元素含量 的规定。 生活饮用水卫生标准(GB 5749)。 联合国粮食卫生组织与世界卫生组织
对有些限量元素比中国规定的量大。
5.食品中限量元素的检测方法主要有:
(1)原子吸收分光光度法:选择性好、灵敏度高、 简便、快速、可同时测定多中元素。
(2)比色法:设备简单、价廉、灵敏度可满足要求。 (3)另外还有极谱法、离子选择电极法和荧光分光光度法。 (极谱法——光学分析的一种,让电流通过溶液,然后增加电压, 由电流变化情况来进行定量、定性分析。如:小型极谱仪,可用 来自动监测自来水中限量元素的含量,实验操作全都自动化,每 隔12min记录一次水样中Cu、Pb、Cd、Zn的含量。)
原理:
在pH为2~9的溶液中,Fe2+可与邻二氮 菲生成极稳定的橙红色络合物Fe(Phen)32+在 波长510nm处有最大吸收,其吸光度与铁含 量成正比,可用比色法测定。在显色之前, 可用盐酸羟胺把Fe3+还原为Fe2+ :
2 Fe3++2NH2OH·HCl→2 Fe2+ +N2↑+4H++2H2O+2Cl-
双硫腙盐的萃取性能,主要决定于水相 中的pH值和双硫腙试剂的浓度。
某些金属离子有氧化双硫腙的性质,在
水溶液中加入盐酸羟胺,可阻止氧化作用。
