〖含6套中考试卷〗中考化学复习第二部分专题六综合计算题试题
2020中考化学复习《化学的综合计算》专项检测题(包含答案)
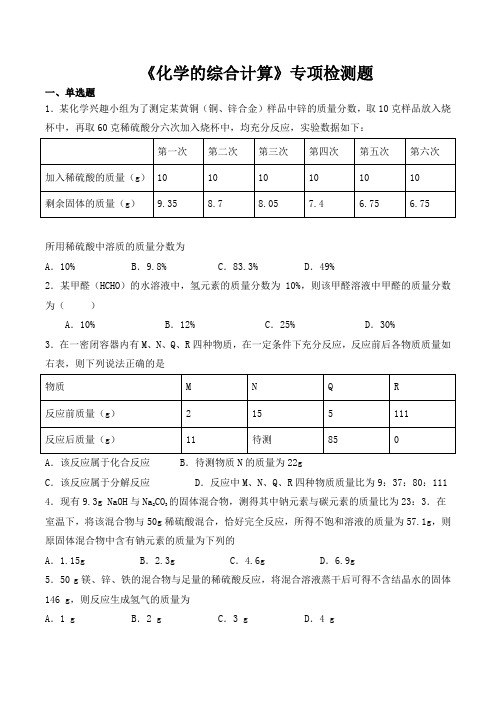
《化学的综合计算》专项检测题一、单选题1.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,均充分反应,实验数据如下:所用稀硫酸中溶质的质量分数为A.10% B.9.8% C.83.3% D.49%2.某甲醛(HCHO)的水溶液中,氢元素的质量分数为10%,则该甲醛溶液中甲醛的质量分数为()A.10% B.12% C.25% D.30%3.在一密闭容器内有M、N、Q、R四种物质,在一定条件下充分反应,反应前后各物质质量如右表,则下列说法正确的是A.该反应属于化合反应 B.待测物质N的质量为22gC.该反应属于分解反应 D.反应中M、N、Q、R四种物质质量比为9:37:80:1114.现有9.3g NaOH与Na2CO3的固体混合物,测得其中钠元素与碳元素的质量比为23:3.在室温下,将该混合物与50g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为57.1g,则原固体混合物中含有钠元素的质量为下列的A.1.15g B.2.3g C.4.6g D.6.9g5.50 g镁、锌、铁的混合物与足量的稀硫酸反应,将混合溶液蒸干后可得不含结晶水的固体146 g,则反应生成氢气的质量为A.1 g B.2 g C.3 g D.4 g6.氢氧化钠固体易吸收空气中的二氧化碳而变化。
取4.65g已部分变质的氢氧化钠固体跟36.5g10%的盐酸恰好完全反应后,将溶液蒸干,所得固体的质量是 ( )A.11.7g B.5.85g C.4.65g D.8.3g7.某固体混合物由Mg和MgO组成,取该混合物6.4g与一定量稀硫酸恰好完全反应(反应后溶液中无晶体析出),所得溶液中溶质的质量为24g,则原混合物中氧元素的质量为A.4.8g B.3.2g C.2.56g D.1.6g8.实验室测定菱铁矿主要成分的含量时,取29g含杂质的菱铁矿(杂质不溶于水也不与酸反应)加入到200g稀盐酸中,恰好完全反应,过滤得滤液214.4 g,则该菱铁矿主要成分的质量分数为A.75% B.80% C.85% D.90%9.现有一样品,经分析含氧化钙、碳酸钙两种物质。
人教版中考化学总复习 第二轮 重难专题研究 专题六 教材基础实验组合题练习

题练习第二轮重庆重难专题研究专题六教材基础实验组合题1. (xx葫芦岛改编)化学是一门以实验为基础的科学。
请回答。
第1题图(1)A实验:当蒸发皿中出现____________时,停止加热。
(2)B实验:硬质玻璃管中的现象是_______________________,反应的化学方程式为____________________________。
(3)C实验:稀释浓硫酸时,玻璃棒的作用____________________。
(4)D实验:证明水是由______________组成的。
2. (xx西宁改编)请结合下图所示实验回答问题:第2题图(1)实验一中铜片上的白磷燃烧红磷不燃烧,说明燃烧的条件之一是______________________。
题练习(2)实验二中活性炭具有________、过滤作用。
(3)实验三中玻璃棒不断搅拌的目的是______________________。
3. 下列A~D是初中化学中的四个实验,请按要求填空:(1)仪器a是________。
(2)B实验成功的关键是________(填序号)。
①装置气密性好②冷却后再打开止水夹③红磷过量或足量第3题图(3)B中发生反应的化学方程式为________________________。
(4)C中开水的作用为____________________。
(5)上述A~D四个实验中能达到实验目的且正确的是________(填字母)。
4. 根据下图回答问题:题练习第4题图(1)A是小明制作的简易净水器,其中小卵石、石英砂的作用是________。
(2)B中制备氧气的化学方程式是____________________________。
(3)若用C装置收集一瓶氢气,则气体应从____端进(填“a”或“b”)。
(4)小东用D组对比实验证明氢氧化钠溶液和二氧化碳发生了反应,但小丽告诉他并不能达到目的,原因是________________________。
2022年中考化学专题复习计算题(word版含答案)

2022中考化学专题复习 计算题 1. (2020·山东枣)人体所需的维生素C(化学式为C6H8O6)主要从蔬菜、水果中摄取,计算: (1)维生素C中碳、氢、氧三种元素质量的最简整数比为______________________。 (2)现有溶质质量分数为1%的维生素C的溶液300g,若配制成溶质质量分数为0.3%的维生素C的溶液,问需要加水的质量是多少。(写出计算过程)
2. (2020·辽宁营口)化学兴趣小组要测定制作叶脉书签所用氢氧化钠溶液的浓度。取40g该氢氧化钠溶液于锥形瓶中,加入数滴酚酞溶液后再滴加质量分数为10%的稀硫酸,当锥形瓶中液体由红色恰好变成无色时,消耗稀硫酸的质量为49g。试计算该氢氧化钠溶液中溶质的质量分数。
3. (2020·辽宁鞍山)赤铁矿石的主要成分为氧化铁。将10g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,再加入92g稀硫酸,恰好完全反应,过滤,得到滤液和2g滤渣。请计算:
(1)赤铁矿石样品中氧化铁的质量分数。 (2)反应后所得溶液中溶质质量分数。
4. (2020年黄冈市)“人工固氮”每年能生产11.9亿吨氨(NH3),反应原理为:N2+ 3H2
一定条件
2NH3。根据化学方程式计算:“人工固氮”每年固定氮气的质量是多少? 5. (2020·湖南湘西)向一定量的稀硫酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如图所示。求:
(1)此过程中产生氢气的最大质量是 克。 (2)锌粉中锌的质量分数为多少。(请写出计算过程) 6. (2021·辽宁朝阳)某小组同学进行了如图所示的实验,请计算: (1)生成氢气的质量是 g。 (2)反应后所得溶液中溶质的质量分数。(写出计算过程) 7. (2020年鄂州市)为了测定某纯碱样品中Na2CO3的质量分数。某化学兴趣小组的同学称取该纯碱样品11.0g,加入到足量的稀盐酸的烧杯中,充分反应后,称量烧杯内物质的总质量,发现比反应前物质的总质量减少了4.4g(纯碱样品中杂质不溶于水,不与酸反应)。求该纯碱样品中Na2CO3的质量分数(精确到0.1%)。 8. (2021·湖北省直辖县级单位)现有一包氯化镁与氯化钡的混合固体20g,为测定其组成,小明先将该混合固体全部溶于水中,形成混合溶液;再将60gNaOH溶液平均分4次加入到该混合溶液中,每次充分反应后过滤,所得沉淀质量与加入NaOH溶液质量的关系如下表。请回答∶
九年级下册化学中考第六单元复习试卷二

初三下册化学中考第六单元复习试卷二可能用到的相对原子质量: H 1 C 12 O 16 Cl-35.5 Ca 40 Cu 64 一、选择题(每小题只有一个选项符合题意,每小题2分,共40分)1.“低碳生活”指的是生活作息时所耗用的能量要尽量减少,特别是减少二氧化碳的排放量,减缓生态恶化,下列行为中不符合“低碳生活”的精神的是A.避免购买不需要的物品,少穿化纤材质的服装B. 使用手绢代替餐巾纸C.推广无纸化办公,使用再生纸且双面打印文印D. 夏天将空调开的很低2. 空气的成分中,能产生温室效应的是()A.氮气B.氧气C.稀有气体D.二氧化碳3.据报道:高考、中考临近时,个别不法商贩唯利是图,制造、销售假冒伪劣的"2B"铅笔,此类铅笔石墨含量低,光电阅读机读不出答案,会严重影响考生成绩,给家庭、社会带来危害。
用石墨制铅笔,除了颜色外主要是利用石墨的()A.质硬 B.吸附性 C. 还原性 D. 质软4.下列CO的性质中属于化学性质的是()A.常温下为无色气体 B.难溶于水C.没有气味 D.可以燃烧5.下列物质的性质与所对应的用途没有关系的是()A.氧气助燃——焊接金属B.稀有气体的性质稳定——作保护气C.石墨导电——可作电极D.二氧化碳能与水反应——人工降雨6.由同种元素组成的不同单质叫做同素异形体,如O2与O3。
下列各组物质属于同素异形体的是()A. CO和CO2B.金刚石与石墨C.铝条和铝粉D.生铁与钢7.下列四瓶气体存放方法正确的是()8. 镁带能在CO2气体中燃烧:2Mg+CO2点燃2MgO+C,该反应中的还原剂是()A.Mg B. CO2 C.MgO D.C9. 下列对一氧化碳的认识中,错误..的是()A.一氧化碳有可燃性,可用作燃料 B.一氧化碳有还原性,可用于冶炼金属C.室内放一盆水,能防止一氧化碳中毒D.分子的不断运动,能使一氧化碳向四周弥漫10.纳米材料被誉为21世纪最有前途的新型材料。
中考化学总复习试题专题六归纳推理类比解题思想的应用

专题六归纳、推理、类比解题思想的应用一、选择题1.(2018,重庆)蚕丝含有蛋白质,在灼烧时有烧焦羽毛的气味,下列物质燃烧时也会产生该气味的是( A ) A.猪皮 B.牛油 C.青椒 D.馒头2.(2018,百色)推理是一种重要的学习方法,下列推理正确的是( D )A.离子是带电的原子或原子团,所以带电的粒子就是离子B.化学变化都遵守质量守恒定律,所以质量不发生改变的变化就是化学变化C.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应D.化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物3.(2018,衡阳)下列分析推理正确的是( D )A.有机物一定含有碳元素,所以含有碳元素的化合物一定是有机物B.铝的化学性质比铁活泼,所以在空气中铝比铁更容易被锈蚀C.酸溶液显酸性,所以显酸性的溶液一定是酸溶液D.固体氢氧化钠具有吸水性,所以固体氢氧化钠可用作某些气体的干燥剂4.(2018,贵港)分析推理是一种重要的化学思想方法。
下列推理正确的是( B )A.分子、原子可以构成物质,所以物质一定是由分子、原子构成的B.碱性溶液能使酚酞试液变红色,所以能使酚酞试液变红色的溶液的pH一定大于7C.溶液的特征是均一、稳定,所以均一、稳定的液体一定是溶液D.稀有气体元素的原子最外层有8个(氦是2个)电子,所以微粒一定是稀有气体元素的原子5.“类推”是学习化学的常用方法,下列推理正确的是( A )A.酸和碱生成盐和水的反应属于中和反应,故盐酸和氢氧化钠溶液能发生中和反应B.酸的溶液pH<7,故pH<7的溶液一定是酸的溶液C.镁条在空气中燃烧生成白色固体,故铜片在空气中灼烧也生成白色固体D.碳可用于炼铁,故碳可用于冶炼所有的金属6.推理是化学学习的一种方法,以下推理正确的是( B )A.单质中只含有一种元素,因此只含有一种元素的物质一定是单质B.碱性溶液能使酚酞试液变红色,因此能使酚酞试液变红色的溶液的pH一定大于7C.在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,则非金属元素一定显负价D.稀有气体元素的原子最外层电子数为8(氦除外),因此微粒一定是稀有气体元素的原子7.(2018,巴中)“归纳”“总结”是学习化学常用的方法,下列说法错误的是( C )A.通常物质燃烧的条件是:物质具有可燃性、跟氧气接触、温度达到可燃物的着火点,当这三个条件同时具备时燃烧才能发生B.复分解反应的条件是:生成物有水、气体、沉淀,三个条件至少满足一个,复分解反应才能发生C.原子是由质子、中子、电子三种微粒构成的D.不同的物质构成它的基本微粒可能不同,分子、原子、离子都能构成物质89.下列归纳和推理,你认为不合理的是( B )A.冰和干冰,组成元素不同——物质分类相同B.纯碱和烧碱,组成元素不同——物质分类相同C.金刚石和石墨,组成元素相同,原子排列不同——物理性质不同D.一氧化碳和二氧化碳,组成元素相同,分子结构不同——化学性质不同10.比较推理是化学学习中常用的思维方法,下列推理正确的是( A )A.生铁比纯铁硬,故黄铜比纯铜硬B.烧碱属于碱,故纯碱也属于碱C.金刚石很硬,故石墨也很硬D.氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多11.(2018,广安)分析推理是化学学习常用的方法,下列分析推理正确的是( D )A.浓盐酸具有挥发性,所以浓硫酸也具有挥发性B.金刚石和石墨都是由碳原子构成,所以它们的性质相同C.离子是带电荷的粒子,所以带电荷的粒子一定是离子D.点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度二、填空题12.归纳总结是学习化学的重要方法,下面是某同学对有关知识的总结,请你填写空格:(1)逻辑关系:物质类属间存在着如下关系,其中酸和盐属于__并列__关系。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题六 综合计算题 1.(2016年山西)某同学用锌和稀硫酸做了如下实验,并进行相关的定量分析。将一定量的锌放入试管中,向其中加入98 g质量分数为10%的稀硫酸,恰好完全反应。 (1)请计算生成氢气的质量(写出计算过程)。
(2)通过已知数据还能求出的量有________(填字母,符合题意的选项都选)。 a.参加反应锌的质量 b.生成硫酸锌的质量 c.稀硫酸中水的质量 d.反应后溶液中溶质质量分数 2.(2014年广东)同学们做甲、乙两个中和反应实验的探究(见下图)。
(1)甲实验恰好中和,则该溶液中的溶质是____________(填化学式)。 (2)取乙反应后的溶液60.0 g,滴加质量分数26.5%的Na2CO3溶液(如图丙),溶液pH的变化如图丁,则与CaCl2反应的碳酸钠溶液的质量为____________g;请计算该溶液中CaCl2的溶质质量分数____________(写出计算过程,精确到0.1%)。
戊 (3)根据计算所得数据在图戊中画出产生沉淀的曲线。 (4)乙组的中和反应实验设计存在的不足是____________________________。 3.(2016年邵阳)某化学兴趣小组参观了一个石灰厂时,带回了一些石灰石样品,同学们利用这些石灰石样品做了如下实验:取样品10 g放入烧杯中,将50 g稀盐酸分5次加入,实验过程所得的数据如表所示(已知石灰石样品中的杂质不参与反应,也不溶于水),根据实验数据计算: 实验次数 加入稀盐酸的质量/g 剩余固体的质量/g 1 10 8 2 10 6 3 10 4 4 10 2 5 10 2 (1)第______次加入稀盐酸充分反应,CaCO3恰好完全反应。 (2)石灰石样品中CaCO3的质量分数=________。 (3)所用稀盐酸中溶质的质量分数(写出计算过程,结果精确到0.1%)。
4.(2016年南昌)小新用20 g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。操作过程如下:
请计算: (1)20 g样品中碳酸钠的质量为________g。 (2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200 g滤液浓缩成制作“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水________g。 5.(2015年揭阳)某铝制品的主要成分是Al和Cu,课外小组将200 g NaOH溶液不断地加到50 g铝制品中得到如下数据(已知金属铝既可以与强酸反应也可以与强碱反应,而金属铜不能与强碱反应,铝与NaOH溶液反应的化学方程式为:2Al+2NaOH+2H2O===2NaAlO2+3H2↑)。 实验次数 第一次 第二次 第三次 第四次 加入氢氧化钠溶液的质量/g 50 50 50 50 剩余固体的质量/g 36.5 23 9.5 9.5 请回答以下问题: (1)该50 g铝制品中含有____________g铜。 (2)求所用氢氧化钠溶液的溶质质量分数为多少?
6.(2015年茂名)某氢氧化钙粉末中含有碳酸钙杂质。现取样品15 g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示。 (1)生成二氧化碳的质量是____________g。 (2)加入60 g稀盐酸后所得溶液中含有的溶质是____________、____________(填化学式)。 (3)计算样品中碳酸钙的质量分数(写出计算过程,结果精确到0.1%)。 专题六 综合计算题 【演练·专项提升】 1.(1)98 g稀硫酸中含有硫酸的质量=98 g×10%=9.8 g。设生成氢气的质量为x。 Zn+H2SO4===ZnSO4+H2↑ 98 2 9.8 g x 989.8 g=2x x=0.2 g 答:生成氢气的质量为0.2 g。 (2)abcd 2.(1)CaCl2 (2)由图可知,丙实验中,加入的碳酸钠溶液先与HCl反应,再与CaCl2反应,与CaCl2反应消耗碳酸钠溶液的质量为70.0 g-30.0 g=40.0 g。设参加反应的CaCl2的质量为x,则 CaCl2+Na2CO3===CaCO3↓+2NaCl 111 106 x 40.0 g×26.5% 111106=x40.0 g×26.5% 解得x=11.1 g
该CaCl2溶液的溶质质量分数为:11.1 g60.0 g×100%≈18.5%。 (3)
(4)无法验证是否恰好中和 解析:(3)设滴加质量分数26.5%的Na2CO3溶液70.0 g时(此时与CaCl2溶液反应的Na2CO3溶液质量为40.0 g),生成沉淀的质量为y,则 CaCl2+Na2CO3===CaCO3↓+2NaCl 106 100 40.0 g×26.5% y 106100=40.0 g×26.5%y 解得y=10.0 g 由此可绘制生成沉淀的曲线图。 (4)乙组的中和反应实验中没有加酚酞试液,无法验证是否恰好中和。 3.(1)4 (2)80% (3)设盐酸的质量分数为x。 CaCO3+2HCl===CaCl2+H2O+CO2↑ 100 73 8 g 40 g×x 1008 g=7340 g×x x=14.6% 答:盐酸的质量分数为14.6%。 解析:(1)通过分析表中的数据可知,第4次和第5次所得剩余固体的质量相等,说明第4加入稀盐酸与CaCO3恰好完全反应;(2)石灰石中杂质的质量为2 g,则石灰石样品中CaCO3的质量分数为:10 g-2 g10 g×100%=80%。 4.(1)10.6 (2)设滤液中氢氧化钠的质量分数为x。 Na2CO3+Ca(OH)2===CaCO3↓+2NaOH 106 80 10.6 g 200 g×x 10610.6 g=80200 g×x x=4% 答:滤液中氢氧化钠的质量分数为4%。 (3)120 解析:(3)设需要蒸发水的质量为y。 200 g×4%=(200 g-y)×10% y=120 g 5.(1)9.5 (2)50 g氢氧化钠溶液消耗金属Al的质量为50 g-36.5 g=13.5 g。 设50 g氢氧化钠溶液的溶质质量为x。 2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 54 80 13.5 g x 5413.5 g=80x 解得x=20 g
则,所用氢氧化钠溶液的溶质质量分数为:20 g50 g×100%=40% 答:所用氢氧化钠溶液的溶质质量分数为40%。 6.(1)2.2 (2)CaCl2 HCl (3)设样品中碳酸钙的质量分数为x。 CaCO3+2HCl === CaCl2+H2O+CO2↑ 100 44 15 g×x 2.2 g 10015 g×x=442.2 g 解得 x=33.3%
答:样品中碳酸钙的质量分数为33.3%。 2020年中考化学模拟试卷 一、选择题 1.下列图象能正确反映其对应操作中各量变化关系的是( )
A.向一定质量的稀硫酸中滴加过量氯化钡溶液
B.稀释等质量的浓度分别为30%和10%的硫酸溶液 C.等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量 D.向一定量的CuSO4溶液中加入足量的铁粉 2.℃时,取四个各盛有50g水的烧杯,分别加入甲、乙、丙、丁四种物质各20g,充分溶解,其溶解情况如图所示。下列说法正确的是( )
A.t℃时四种溶液都是饱和溶液 B.甲溶液的溶质质量分数最大 C.t℃时四种物质溶解度最大的是丙 D.升高温度乙物质一定能继续溶解 3.除去下列各组物质中的少量杂质,所用的试剂和方法中,不正确的是( )
物质 杂质 除杂质的方法 A FeSO4溶液 CuSO4溶液 加入过量铁粉后过滤 B CaO固体 CaCO3固体 加足量水溶解后过滤 C H2 H2O、HCl 先后通过足量氢氧化钠溶液、浓硫酸 D 稀盐酸 稀硫酸 加入适量氯化钡溶液后过滤 A.A B.B C.C D.D 4.对下列事实的解释错误..的是( )
选项 事实 解释 A 用洗洁精洗去餐具上的油污 洗洁精具有乳化功能 B 用普通显微镜观察不到苯分子 分子很小 C 品红在热水中扩散比在冷水中快 水分子间有空隙 D 金刚石、石墨和的物理性质存在着明显差异 碳原子排列方式不同 A.A B.B C.C D.D 5.下列四个图象中,能正确表示对应变化关系的是( )
A B C D
向一定量稀盐酸中加水 20℃时,向一杯饱和KNO3溶液中加入KNO3晶体 室温时,向一定量的稀盐酸中加入少量镁条 用等质量、等浓度的双氧水分别制取氧气
A.A B.B C.C D.D 6.除去下列各组物质中的少量杂质,所用的试剂和方法都正确的是( )
物质 杂质 除杂质所用试剂和方法 A Cu CuO 加入过量稀硫酸、过滤 B CO2 HCl 通过足量的氢氧化钠溶液 C NaOH 溶液 Na2CO3 加入适量 CaCl2溶液、过滤 D NaNO3溶液 NaCl 加入过量 AgNO3溶液、过滤 A.A B.B C.C D.D 7.下列主题知识的归纳中,正确的一组是
A.物质俗名 B.安全常识
