氧化还原反应经典练习题
高考化学氧化还原反应综合经典题附答案

一、高中化学氧化还原反应练习题(含详细答案解析)1.某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Fe2+、Al3+、Ca2+和Mg2+等,且酸性较强。
为回收利用,通常采用如下流程处理:注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
氢氧化物Fe(OH)3Fe(OH)2Mg(OH)2Al(OH)3Cr(OH)3pH 3.79.611.189(>9溶解)(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________;已知钠离子交换树脂的原理:M n++nNaR→MR n+nNa+,此步操作被交换除去的杂质离子是__________。
A.Fe3+B.Al3+C.Ca2+D.Mg2+(3)还原过程中,每消耗0.8 mol Cr2O72-转移4.8 mol e-,该反应离子方程式为____________。
【答案】A AB CD 3S2O32— + 4Cr2O72— + 26H+ = 6SO42— + 8Cr3+ +13H2O【解析】【分析】某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,加双氧水把亚铁离子氧化为铁离子,同时Cr3+被氧化为Cr2O72-,加氢氧化钠调节pH=8,则Fe3+、Al3+转化为氢氧化铁和氢氧化铝沉淀,过滤,滤液中主要含有Cr2O72-、Ca2+和Mg2+等,通过钠离子交换树脂,除去Ca2+和Mg2+,然后加Na2S2O3把Cr2O72-还原为Cr3+,再调节pH得到Cr(OH)(H2O)5SO4;(1)加氧化剂主要目的是把亚铁离子氧化为铁离子,注意不能引入新的杂质;(2)根据表中数据判断;通过钠离子交换树脂,除去Ca2+和Mg2+;(3)每消耗0.8mol Cr2O72-转移4.8mol e-,则1molCr2O72-转移6mol电子,所以生成Cr3+,S2O32-被氧化为SO42-,结合得失电子守恒和原子守恒写出离子方程式。
氧化还原反应综合练习题

氧化还原反应综合练习题篇一:高中化学必修一氧化还原反应练习题(含答案)氧化还原反应一、选择题1、今有下列三个氧化还原反应:①2fecl3+2ki==2fecl2+2kcl+i2②2fecl2+cl2==2fecl3③2kmno4+16hcl==2kcl+2mncl2+8h2o+5cl2↑若某溶液中存有fe2+和i-并存,必须水解除去i-而又不影响fe2+和cl-,可以重新加入试剂就是()a.cl2b.kmno4c.fecl3d.hcl2、氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。
下列反应与2al+2naoh+2h2o=2naalo2+3h2↑相比较,水的作用相同的是()a.2na2o2+2h2o=4naoh+o2↑b.4fe(oh)2+o2+2h2o=4fe(oh)3c.2na+2h2o=2naoh+h2↑d.2f2+2h2o=4hf+o23、水解还原成反应的实质就是电子的迁移,以下关于水解还原成反应的描述恰当的就是a.在氧化还原反应中,有一种元素被氧化,肯定有另一种元素被还原b.11.2lcl2灌入足量的naoh溶液中,迁移的电子数为0.5nac.难失电子的原子,得电子的能力一定强d.元素由化合态变为游离态时,它可能将被水解,也可能将被还原成4、下列化学反应中,属于置换反应的是()a、naoh+hcl==nacl+h2ob、h2+cuocu+h2oc、fe2o3+3co2co25、下列反应中,水只作氧化剂的是a.2f2+2h2o===4hf+2fe+3co2d、2co+o2o2b.2na+2h2o===2naoh+h2↑c.2h2o2h2↑+o2↑d.na2o+h2o===2naoh6、用下列方法均可制得氧气:(1)2kclo32kcl+3o2↑(2)2na2o2+2h2o===4naoh+o2↑(3)2hgo(4)2kmno42hg+o2↑k2mno4+mno2+o2↑若要制得相同质量的氧气,反应中电子转移数目之比为a.3∶2∶1∶4b.1∶1∶1∶1c.2∶1∶2∶2d.1∶2∶1∶17、在以下转变中必须重新加入氧化剂就可以同时实现的就是 a.s→h2sb.cuso4→cuc.kclo3→o2d.c→co28、根据下列反应判断有关物质还原性由强到弱的顺序是h2so3+i2+h2o===2hi+h2so42fecl3+2hi===2fecl2+2hcl+i23fecl2+4hno3===2fecl3+no↑+2h2o+fe(no3)3a.h2so3>i->fe2+>nob.i->fe2+>h2so3>noc.fe2+>i->h2so3>nod.no>fe2+>h2so3>i-9、下列反应既是氧化还原反应又是离子反应的是a.钠在氯气中冷却b.二氧化碳通入澄清的石灰水中c.氯化钠溶液中滴提硝酸银溶液d.锌粒放入稀硫酸中10、未知kh和h2o反应分解成h2和koh,反应中1molkha.失去1mol电子b.得到1mol电子c.丧失2mol电子d.没电子利害11、下列反应中,既属于氧化还原反应,又属于离子反应的是a.铝片与稀盐酸的反应b.甲烷与氧气的反应c.灼热的炭与二氧化碳反应分解成一氧化碳d.氢氧化钠溶液与稀盐酸的反应12、以下描述中恰当的就是a.由x变为x2-的反应是氧化反应b.凡存有单质参予的化学反应,一定就是水解还原成反应c.含氧酸能发生氧化反应,无氧酸则不能d.反应中某元素的原子变成阳离子,则该元素的单质在反应中一定就是还原剂二、填空题三、13、四、五、六、(1)饮用水中的no对人类身心健康可以产生危害,为了减少饮用水中no的浓度,可以在碱性条件下以铝粉将no还原为n2,其化学方程式为:10al+2nano3+4naoh===10naalo2+3n2↑+2h2o。
氧化还原反应经典练习题(精品免费)

氧化还原反应练习题班级_________ 姓名___________ 学号___________一、选择题1.下列反应一定属于氧化还原反应的是( )A.化合反应B.分解反应C.置换反应D.复分解反应2.下列叙述正确的是( )A.氧化还原反应的本质是化合价发生变化B.有单质产生的分解反应一定是氧化还原反应C.氧化剂在同一反应中既可以是反应物,也可以是生成物D.还原剂在反应中发生还原反应3.某元素在化学反应中由化合态变为游离态,则该元素( )A.一定被氧化B.一定被还原C.既可能被氧化,也可能被还原D.以上都不是4.下列叙述中,正确的是( )A、含金属元素的离子一定是阳离子B、在氧化还原反应中,非金属单质一定是还原剂C、某元素从化合态变为游离态时,该元素一定被还原D、金属阳离子被还原不一定得到金属单质5.下列关于氧化还原反应说法正确的是()A.肯定一种元素被氧化,另一种元素被还原B.某元素从化合态变成游离态,该元素一定被还原C.在反应中不一定所有元素的化合价都发生变化D.在氧化还原反应中非金属单质一定是氧化剂6.下列变化过程属于还原反应的是( )A.HCl→MgCl2B.Na→Na+C.CO→CO2D. Fe3+→Fe7.下列反应属于氧化还原反应的是()8.下列变化需要加入氧化剂的是( )A S2-→HS- B.HCO3-→CO2 C.2 Cl-→Cl2 D. Cu2+→Cu9.下列物质不能做还原剂的是( )A. H2SB. Fe2+ C .Fe3+ D. SO210.下列各反应中,水只做氧化剂的是( )A. C+ H2O = CO+ H2B.2 H2O = 2 H2↑+ O2↑C. Na2O + H2O =2NaOHD.CuO+ H2= Cu+ H2O11.下列反应中,水作为还原剂的是()A、Cl2 + H2O = HCl + HClOB、2Na2O2 + 2H2O = 4NaOH + O2C、2F2 + 2H2O = 4HF + O2D、2Na + 4H2O = 2NaOH + H212.P单质在下列反应中4P+3KOH+3H2O=3KH2PO2+PH3的变化是( )A.被氧化B.被还原C.既被氧化又被还原D.既未被氧化又未被还原13.在H2SO3+2 H2S=3 H2O+3S反应中,被氧化与被还原元素的质量比为( )A.1:1B.2:1C.1:2D.3:214.实现下列变化需要加入氧化剂的是()15.下列粒子中,既具有氧化性,又具有还原性的是( )A.MgB. Zn2+C. Fe2+D.HCl16.在反应中,还原产物是()17.下列变化中,需要加入氧化剂的是()18.为了治理废水中Cr2O72-的污染,常先加入试剂使之变为Cr3+,该试剂为()A、NaOH溶液B、FeCl3溶液C、明矾D、Na2SO3和H2SO419.离子M2O7X-与S2-能在酸性溶液中发生如下反应:aM2O7X- +3S2- +cH+==2M3+ +eS +fH2O,则M2O7X-中M的化合价为()A、+4B、+5C、+6D、+720.对反应H-+NH3==H2+NH2-的不正确说法()A、是置换反应B、H-是还原剂C、NH3是氧化剂D、氧化产物和还原产物都是H221、黑火药爆炸反应为:S+2KNO3+3C=K2S+3CO2 +N2 。
氧化还原反应练习题

氧化还原反应练习题氧化还原反应是化学中常见的一类反应,也是我们需要掌握的重要知识点。
下面是一些氧化还原反应练习题,帮助大家巩固理论知识并提高解题能力。
题目一:1.化学方程式:Mg + 2HCl → MgCl2 + H2此反应中,哪个是还原剂?哪个是氧化剂?解析:在该化学方程式中,Mg被氯化氢(HCl)氧化生成氯化镁(MgCl2),因此Mg是氧化剂;氯化氢(HCl)则被Mg还原生成氢气(H2),因此HCl是还原剂。
题目二:2.化学方程式:2Fe + 3Cl2 → 2FeCl3此反应中,哪个是还原剂?哪个是氧化剂?解析:在该化学方程式中,氯气(Cl2)被铁(Fe)氧化生成三氯化铁(FeCl3),因此Cl2是氧化剂;铁(Fe)则被氯气(Cl2)还原,因此Fe是还原剂。
题目三:3.化学方程式:2H2S + O2 → 2H2O + 2S此反应中,哪个是还原剂?哪个是氧化剂?解析:在该化学方程式中,氧气(O2)被硫化氢(H2S)氧化生成水(H2O)和硫(S),因此O2是氧化剂;硫化氢(H2S)则被氧气(O2)还原,因此H2S是还原剂。
题目四:4.化学方程式:2KBr + Cl2 → 2KCl + Br2此反应中,哪个是还原剂?哪个是氧化剂?解析:在该化学方程式中,氯气(Cl2)被溴化钾(KBr)氧化生成氯化钾(KCl)和溴(Br2),因此Cl2是氧化剂;溴化钾(KBr)则被氯气(Cl2)还原,因此KBr是还原剂。
题目五:5.化学方程式:Fe2O3 + 3CO → 2Fe + 3CO2此反应中,哪个是还原剂?哪个是氧化剂?解析:在该化学方程式中,一氧化碳(CO)被三氧化二铁(Fe2O3)氧化生成铁(Fe)和二氧化碳(CO2),因此CO是氧化剂;三氧化二铁(Fe2O3)则被一氧化碳(CO)还原,因此Fe2O3是还原剂。
通过以上练习题,我们可以进一步理解氧化还原反应中的还原剂和氧化剂的概念,并掌握如何判断它们在化学方程式中的位置。
高三化学练习题:氧化还原反应

高三化学练习题:氧化还原反应一、选择题:1. 下列反应中,属于氧化还原反应的是:A) 2Na + Cl2 → 2NaClB) AgNO3 + NaCl → AgCl + NaNO3C) 2H2 + O2 → 2H2OD) CaCO3 → CaO + CO22. Na2S + H2O2 → Na2SO4 + H2O,在该反应中,H2O2的作用是:A) 氧化剂B) 还原剂C) 酸化剂D) 中和剂3. 在电化学池中,写出下列反应的氧化还原半反应方程式:Pb(s) + 2H+(aq) → Pb2+(aq) + H2(g)A) Pb2+(aq) + 2e- → Pb(s)B) 2H+(aq) + 2e- → H2(g)C) Pb2+(aq) + 4e- → Pb(s)D) 2H2O(l) + 2e- → H2(g) + 2OH-(aq)二、填空题:1. Cl2 + 2NaI → 2NaCl + I2,该反应中,Cl2被____________。
2. Fe2O3 + 2Al → 2Fe + Al2O3,该反应中,Al被____________。
3. 在下列反应中,化合态氧被还原的反应是:_______。
4. 在化学反应中,发生氧化反应的物质称为_____________。
三、解答题:1. 请解释氧化还原反应的定义和特征。
2. 在化学反应中,为了区分氧化剂和还原剂,有一条简单的判断准则,即:氧化剂是能够______________;而还原剂是能够______________。
请填上空缺,并解释原因。
3. 某化合物X能与氧气反应生成二氧化碳。
试判断该化合物X的氧化性。
四、实验题:假设实验室已经配好以下试剂:- 稀盐酸 (HCl)- 锌粉 (Zn)- 硫酸铜 (CuSO4)- 白磷 (P4)请写出合适的实验方案,以展示氧化还原反应。
说明所使用试剂的化学性质和反应过程。
注意:实验过程涉及化学试剂,请确保在有合适的实验条件和指导下进行。
氧化还原反应专项训练(最新整理)

氧化还原反应专项训练1.常温下,往H 2O 2溶液中滴加少量FeSO 4溶液,可发生如下两个反应:2Fe 2++H 2O 2+2H +=2Fe 3++2H 2O ,2Fe 3++H 2O 2=2Fe 2++O 2↑+H +,下列说法正确的是( )A .H 2O 2的氧化性比Fe 3+强,其还原性比Fe 2+弱B .在H 2O 2分解过程中,溶液的pH 逐渐下降C .在H 2O 2分解过程中, Fe 2+和Fe 3+的总量保持不变D .H 2O 2生产过程可以使用铁质容器2.某容器中发生了一个化学反应,反应过程中存在H 2O 、ClO -、CN -、HCO 3-、N 2、Cl -六种粒子,在反应过程中测得ClO -和N 2的物质的量随时间变化的曲线如图所示。
下列判断中正确的是( )A .还原剂是CN -,氧化产物只有N 2B .氧化剂是ClO -,还原产物是HCO 3-C .配平后氧化剂与还原剂的化学计量数之比为5∶2D .标准状况下若生成2.24 L N 2,则转移0.5 mol 电子3.(2014·温州八校联考)新型纳米材料MFe 2O x (3<x <4)中M 表示+2价的金属元素,且在反应中化合价不发生变化。
常温下,MFe 2O x 能使工业废气中的SO 2转化为S ,流程如下:MFe 2O x ――――→常温下SO 2MFe 2O y 则下列有关该反应的判断正确的是 ( )A .MFe 2O x 是氧化剂 B .SO 2被氧化,1 mol SO 2得4 mol 电子C .x <yD .MFe 2O y 是还原产物4.向21.6 g 铁粉和铜粉的混合物中加入1 L 1 mol·L -1硝酸溶液,充分反应,放出NO气体且金属有剩余。
则反应后溶液中c (NO )可能为( )。
-3A .0.45 mol·L -1 B .0.6 mol·L -1 C .0.75 mol·L -1 D .0.9 mol·L -15.为监测空气中汞蒸气是否超标,通过悬挂涂有CuI(白色)的滤纸,根据滤纸是否变色(亮黄色至暗红色)及变色所需时间来判断空气中的汞含量。
氧化还原反应练习题及答案

氧化还原反应可能用到的相对原子质量:H:1C:12N:14O:16S:32第I卷(选择题共48分)一、选择题(本题包括16小题,每小题3分,共48分。
每小题只有一个选项符合题意)1.下列操作过程中一定有氧化还原反应发生的是ABCD2.成语是中华民族灿烂文化中的瑰宝,许多成语中蕴含着丰富的化学原理,下列成语中涉及氧化还原反应的是A.3.XA.XC.X4.A.5.6.A.C.7.A.B.C.D.8.已知N元素的最低化合价是–3价,最高化合价是+5价,那么下列物质中的N元素只具有氧化性的是A.NH3B.N2C.NO2D.HNO39.下列各反应中,水作为还原剂的是A.2H2+O22H2OB.SO3+H2O===H2SO4C.2F2+2H2O===4HF+O2D.2Na+2H2O===2NaOH+H210.下列药品置于空气中很容易变质(括号内的物质是变质后的物质),其中不是因为氧化还原反应而变质的是A.Na2SO3(Na2SO4)B.FeCl2(FeCl3)C.KI(I2)D.NaOH(Na2CO3)11.下列反应中,氧化反应与还原反应在同一种元素中进行的是A.Zn+H2SO4===ZnSO4+H2B.2FeCl2+Cl2===2FeCl3C.2KClO32KCL+3O2D.Cl2+H2O===HClO+HCl12.下列关于氧化还原反应的叙述中正确的是A.失去电子的反应为还原反应B.含有氧元素的物质是氧化剂C.氧化剂得到电子的数目和还原剂失去的电子的数目一定相等SB.Na3-Y+H W+O⑶结合I、II实验现象可知,Fe、Cu、Ag的还原性顺序为。
18、(14分)某学生为了验证氢气还原氧化铜的产物,设计了下图所示的实验装置。
⑴写出编号仪器的名称:①;②;⑵浓H2SO4的作用是。
⑶本实验需要加热的装置为(填字母编号)。
⑷写出装置C、D中可观察到的现象:C,D。
⑸D中反应每生成1个水分子,转移的电子数为个。
19、(8分)对于实验室制取O2的反应:2KCLO32KCL+3O2,其电子转移的方向和数目的标法有以下几种,你认为正确的是(填序号)该反应中,是氧化剂,是还原剂,MnO2是剂。
高中化学《氧化还原反应》专项训练(附答案)
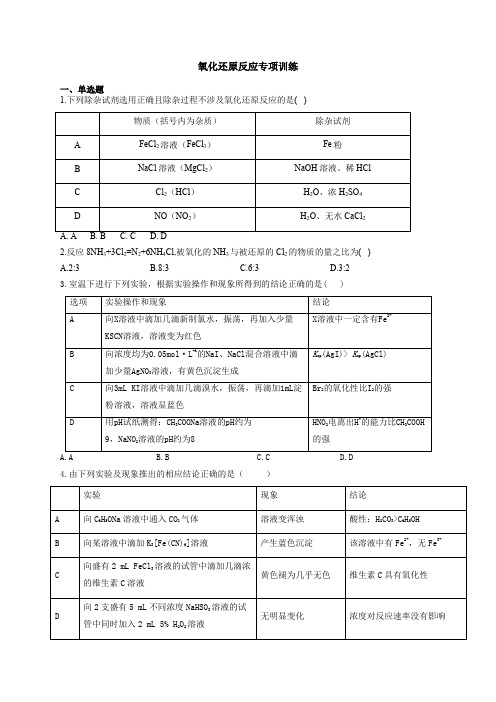
氧化还原反应专项训练一、单选题1.下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )2.反应8NH3+3Cl2=N2+6NH4Cl,被氧化的NH3与被还原的Cl2的物质的量之比为( )A.2:3B.8:3C.6:3D.3:23.室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )4.由下列实验及现象推出的相应结论正确的是()A. AB. BC. CD. D5.下列实验中的颜色变化,与氧化还原反应无关..的是 ( )6.某离子反应中涉及H2O、ClO-、4NH 、H+、N2、Cl-六种微粒,其中N2的物质的量随时间变化的曲线如图所示。
下列判断中正确的是( )A.该反应的还原剂是-Cl B.消耗1mol还原剂,转移6mol电子C.氧化剂与还原剂的物质的量之比为2:3D.反应后溶液的酸性明显增强7.含氰化物的废液乱倒或与酸混合,均易生成有剧毒且易挥发的氰化氢。
工业上常采用碱性氯化法来处理高浓度氰化物污水,发生的主要反应为:CN-+OH-+Cl2→CO2+N2+Cl-+H2O(未配平)。
下列说法错误的是(其中N A表示阿伏加德罗常数的值)()A.Cl2是氧化剂,CO2和N2是氧化产物B.上述离子方程式配平后,氧化剂、还原剂的化学计量数之比为2:5C.该反应中,若有1mol CN-发生反应,则有5N A电子发生转移D.若将该反应设计成原电池,则CN-在负极区发生反应8.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )A.洗气瓶中产生的沉淀中有碳酸钡B.在Z导管出来的气体中无二氧化碳C.洗气瓶中产生的沉淀是硫酸钡D.洗气瓶中无沉淀产生9.已知2HNO 在低温下较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH 的关系如下表。
下列有关说法错误的是( )A.碱性条件下, 2NaNO 与NaClO 反应的离子方程式为2NO ClO--+3NO Cl --+B.向冷的2NaNO 溶液中加入滴有淀粉的氢碘酸,溶液变蓝色C.向冷的2NaNO 溶液中加入稀硫酸可得到2HNOD.向冷的2NaNO 溶液中通入2CO 可得到2HNO 10.下列不涉及氧化还原反应的是( )A .补铁剂(有效成分为Fe 2+)与含维生素C 共服效果更佳B .雷雨肥庄稼——自然固氮C .灰肥相混损肥分——灰中含有碳酸钾,肥中含有铵盐D .从沙滩到用户——由二氧化硅制晶体硅11.下列实验现象与氧化还原反应无关的是( ) A. 氨气与氯化氢气体相遇产生白烟 B. 铜遇浓硝酸产生红棕色气体 C. 过氧化钠放置于空气中逐渐变白D. 一氧化氮遇空气变为红棕色参考答案1.答案:B解析:A.FeCl3与Fe反应生成FeCl2,2FeCl3+Fe=2FeCl2,此过程中Fe的化合价发生变化,涉及到了氧化还原法应,故A不符合题意;B.MgCl2与NaOH溶液发生复分解反应MgCl2+2NaOH=Mg(OH)2 +2NaCl,过量的NaOH溶液可用HCl除去HCl+NaOH=NaCl+H2O ,此过程中没有元素化合价发生变化,未涉及氧化还原反应,故B符合题意;C.部分氯气与H2O 发生反应生成氯化氢和次氯酸,反应过程中氯元素化合价变化,涉及到了氧化还原法应,故C不符合题意;D.NO2 与水反应生成硝酸和NO。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氧化还原反应经典练习题氧化还原反应练题
一、选择题
1.下列变化过程属于还原反应的是()
A。
HCl → MgCl2
B。
Na → Na+ C。
CO → CO2
D。
Fe3+ → Fe2+
2.下列反应属于氧化还原反应的是()
A。
2Na + 2H2O → 2NaOH + H2↑
B。
C + H2O → CO + H2
C。
Na2O + H2O → 2NaOH
D。
CuO + H2 → Cu + H2O
3.下列变化需要加入氧化剂的是()
A。
S2- → HS-
B。
HCO3- → CO2
C。
2Cl- → Cl2
D。
Cu2+ → Cu
4.下列各反应中,水只做氧化剂的是()
A。
C + H2O = CO + H2
B。
2H2O = 2H2↑ + O2↑
C。
Na2O + H2O = 2NaOH
D。
CuO + H2 = Cu + H2O
5.下列反应中,水作为还原剂的是()
A、Cl2 + H2O = HCl + HClO
B、2Na2O2 + 2H2O = 4NaOH + O2
C、2F2 + 2H2O = 4HF + O2
D、2Na + 4H2O = 2NaOH + H2
6.P单质在下列反应中4P + 3KOH + 3H2O = 3K2HPO4 + PH3的变化是()
A.被氧化
B.被还原
C.既被氧化又被还原
D.既未被氧化又未被还原
7.在H2SO3 + 2H2S = 3H2O + 3S反应中,被氧化与被还原元素的质量比为()
A.1:1
B.2:1
C.1:2
D.3:2
8.实现下列变化需要加入氧化剂的是()
A.2K + 2H2O = 2KOH + H2↑
B.2NaCl + F2 = 2NaF + Cl2
C.2Na + 2H2O = 2NaOH + H2↑
D.2HCl + Zn = ZnCl2 + H2↑
9.下列粒子中,既具有氧化性,又具有还原性的是()
A。
Mg
B。
Zn2+
C。
Fe2+
D。
HCl
10.在反应中,还原产物是()
A。
Fe2+
B。
Fe3+
C。
H2O
D。
O2
11.离子M2O7X-与S2-能在酸性溶液中发生如下反应:aM2O7X- + 3S2- + cH+ = 2M3+ + eS + fH2O,则M2O7X-中M 的化合价为()
A、+4
B、+5
C、+6
D、+7
12.对反应H- + NH3 = H2 + NH2-的不正确说法()
A、是置换反应
B、H-是还原剂
C、NH3是氧化剂
D、氧化产物和还原产物都是H2
13、黑火药爆炸反应为:S + 2KNO3 + 3C = K2S + 3CO2 + N2.在该反应中,氧化剂是()
①C ②S ③K2S ④KNO3 ⑤N2
A、①③⑤
B、②④
C、②④⑤
D、③④⑤
1.已知Ni+CuSO4=NiSO4+Cu,
Cu+2AgNO3=Cu(NO3)2+2Ag,则下列判断正确的是() A。
还原性: Ni>Cu>Ag
B。
氧化性: Ni2+>Cu2+>Ag+
C。
还原性: XXX<Cu<Ag
D。
氧化性: Ni2+<Cu2+<Ag+
2.已知X2、Y2、Z2、W2四种物质的氧化能力为:
W2>Z2>X2>Y2,下列氧化还原反应能发生的是()
A、2W-+ Z2=2Z-+W2
B、2X-+ Z2=2Z-+X2
C、2Y-+ W2=2W-+Y2
D、2Z-+ X2=2X-+Z2
填空题
1、油画的白色颜料含有PbSO4,久置后会变成PbS使油
画变黑,如果用双氧水擦拭则可恢复原貌。
试写出反应的方程式:
PbSO4 + H2O2 → Pb + H2SO4 + H2O
2、在反应中,某元素的化合价升高,该元素的原子失去
电子,被氧化;某元素的化合价降低,该元素的原子获得电子,被还原;该反应中,氧化剂是氧分子,还原剂是某元素。
3、分析下列变化过程,是氧化还是还原,再按要求填空:
1) Fe → FeCl2,需加入氯化剂,如HCl
2) CuO → Cu,需加入还原剂,如H2
3) HCl → H2,是还原反应,HCl是氧化剂
4、现有微粒:①S,②S2-,③Na+,④Fe2+,⑤H+,⑥Cu,
⑦O2,⑧HCl,⑨H2O,其中在反应中只能作还原剂的是Cu,既可作还原剂又可作氧化剂的是H+,只能作氧化剂的是O2.
5、有反应:RO3n- + 6I- + 6H+ = R- + 3I2 + 3H2O。
则
RO3n-中R化合价是n。
化学方程式:
1.2H2 + O2 = 2H2O。
还原剂是H2,氧化剂是O2,氧化
产物是H2O,还原产物是H2.
2.2H2O2 = 2H2O + O2.还原剂是H2O2,氧化剂是H2O2,氧化产物是O2,还原产物是H2O。
3.Cu + 2AgNO3 = Cu(NO3)2 + 2Ag。
还原剂是Cu,氧化
剂是AgNO3,氧化产物是Cu(NO3)2,还原产物是Ag。
4.2H2O2 = 2H2O + O2.还原剂是H2O2,氧化剂是H2O2,氧化产物是O2,还原产物是H2O。
5.2H2O = 2H2 + O2.还原剂是H2O,氧化剂是H2O,氧化产物是O2,还原产物是H2.
6、MnO2 + 4HCl = MnCl2 + 2H2O + Cl2.还原剂是HCl,
氧化剂是MnO2,氧化产物是Cl2,还原产物是H2O。
1.4HCl (浓) + MnO2 → MnCl2 + Cl2 ↑ + 2H2O
2.Cu + 4HNO3 (浓) → Cu(NO3)2 + 2NO2 ↑ + 2H2O
3.3Cu + 8HNO3 (稀) → 3Cu(NO3)2 + 2NO ↑ + 4H2O
4.用单线桥法分析以下氧化还原反应:
1.2Na + 2H2O → 2NaOH + H2 ↑
2.Fe + CuSO4 → FeSO4 + Cu
3.MnO2 + 4HCl (浓) → MnCl2 + Cl2 ↑ + 2H2O
4.Cu + 4HNO3 (浓) → Cu(NO3)2 + 2NO2 ↑ + 2H2O
改写后的文章:
下面是四个氧化还原反应,需要剔除格式错误并删除有问题的段落:
1.4HCl (浓) + MnO2 → MnCl2 + Cl2 ↑ + 2H2O
2.Cu + 4HNO3 (浓) → Cu(NO3)2 + 2NO2 ↑ + 2H2O
3.3Cu + 8HNO3 (稀) → 3Cu(NO3)2 + 2NO ↑ + 4H2O
4.用单线桥法分析以下氧化还原反应:
1.2Na + 2H2O → 2NaOH + H2 ↑
2.Fe + CuSO4 → FeSO4 + Cu
3.MnO2 + 4HCl (浓) → MnCl2 + Cl2 ↑ + 2H2O
4.Cu + 4HNO3 (浓) → Cu(NO3)2 + 2NO2 ↑ + 2H2O
以上是四个氧化还原反应,其中第四个需要用单线桥法进行分析。
第一个反应中,浓盐酸和二氧化锰反应生成氯气和氯化锰。
第二个反应中,浓硝酸和铜反应生成硝酸铜和二氧化氮。
第三个反应中,稀硝酸和铜反应生成硝酸铜和一氧化氮。
第四
个反应中,浓硝酸和铜反应生成硝酸铜和二氧化氮。
在单线桥法中,第一个反应中的氢气是还原剂,二氧化锰是氧化剂。
在第二个反应中,铜是还原剂,硝酸铜是氧化剂。
在第三个反应中,铜是还原剂,硝酸铜是氧化剂。
在第四个反应中,铜是还原剂,硝酸铜是氧化剂。
