【化学】化学氧化还原反应的专项培优 易错 难题练习题
【化学】化学 氧化还原反应的专项 培优 易错 难题练习题含详细答案

一、高中化学氧化还原反应练习题(含详细答案解析)1.阳极泥处理后的沉渣中含AgCl,工业上可用Na2SO3溶液作浸取剂浸出回收。
某小组在实验室模拟该过程。
已知:i.25o C时,部分物质的溶解度:AgCl 1.9×10–4 g;Ag2SO3 4.6×10–4 g;Ag2SO40.84 g。
ii.25o C时,亚硫酸钠溶液酸化过中含4S+微粒的物质的量分数随pH变化如图所示。
Ⅰ.浸出氯化银取AgCl固体,加入1 mol/L Na2SO3溶液作浸取剂,充分反应后过滤得到浸出液(pH=8),2SO- [Ag(SO3)2]3– + Cl–。
该过程中发生的反应为AgCl +23(1)用平衡移动原理解释AgCl溶解的原因是___。
Ⅱ. 酸化沉银(2)经检测,沉淀m为AgCl,则溶液m中含4S+微粒的主要存在形式是________。
(3)探究沉淀n的成分。
①甲同学认为沉淀n一定不含Ag2SO4,其依据是________。
②乙同学认为沉淀n可能含Ag2SO3,进行实验验证。
i. 本实验设计的依据是:Ag2SO3具有________性。
ii. 乙同学观察到________,得出结论“沉淀n不含Ag2SO3”。
③丙同学从溶液n的成分角度再次设计实验证明沉淀n不含Ag2SO3。
i. 本实验设计的依据是:若沉淀n含Ag2SO3,则溶液n中含1Ag+微粒的总物质的量___(填“>”、“=”或“<”)Cl–物质的量。
ii. 结合实验现象简述丙同学的推理过程:____。
Ⅲ.浸取剂再生(4)溶液m经处理后可再用于浸出AgCl,请简述该处理方法____。
【答案】AgCl(s)Ag+(aq)+ Cl-(aq) ,Ag+与SO 32- 结合生成[Ag(SO3)2]3–,促进AgCl的溶解平衡正向移动 HSO3- Ag2SO4的溶解度远大于AgCl或Ag2SO3,溶液中Ag+ 的浓度很小还原b.中清液的颜色与..,均为浅紫色溶液< e中无沉淀生成,说明清液中没有Cl-,则.......c.相同溶液n中加入稀硝酸使[Ag(SO3)2]3–全部转化为Ag+,Ag+将Cl–全部沉淀,由此可知溶液n中含Ag元素的微粒总物质的量不小于n(Cl–) 加NaOH溶液调节pH至9~10【解析】【分析】I、(1)利用平衡移动的知识答题即可;II、(2)生成沉淀m时,溶液m的pH为5,观察图像,可以得知HSO3-的物质的量分数占100%;(3)①溶液中Ag+的浓度很小,而Ag2SO4的溶解度较大,故不会形成Ag2SO4沉淀;②依据Ag2SO3的还原性答题;③e中无沉淀生成,说明清液中没有Cl-,则溶液n中加入稀硝酸使[Ag(SO3)2]3–全部转化为Ag+,Ag+将Cl–全部沉淀,由此可分析出溶液n中含Ag元素的微粒总物质的量不小于n(Cl–);III、(4)m溶液中的溶质为NaHSO3,浸取剂为Na2SO3溶液,需要加入NaOH溶液将NaHSO3转化为Na2SO3。
2020-2021【化学】化学氧化还原反应的专项培优 易错 难题练习题含答案

2020-2021【化学】化学氧化还原反应的专项培优易错难题练习题含答案一、高中化学氧化还原反应1.阳极泥处理后的沉渣中含AgCl,工业上可用Na2SO3溶液作浸取剂浸出回收。
某小组在实验室模拟该过程。
已知:i.25o C时,部分物质的溶解度:AgCl 1.9×10–4 g;Ag2SO3 4.6×10–4 g;Ag2SO40.84 g。
ii.25o C时,亚硫酸钠溶液酸化过中含4S+微粒的物质的量分数随pH变化如图所示。
Ⅰ.浸出氯化银取AgCl固体,加入1 mol/L Na2SO3溶液作浸取剂,充分反应后过滤得到浸出液(pH=8),2SO- [Ag(SO3)2]3– + Cl–。
该过程中发生的反应为AgCl +23(1)用平衡移动原理解释AgCl溶解的原因是___。
Ⅱ. 酸化沉银(2)经检测,沉淀m为AgCl,则溶液m中含4S+微粒的主要存在形式是________。
(3)探究沉淀n的成分。
①甲同学认为沉淀n一定不含Ag2SO4,其依据是________。
②乙同学认为沉淀n可能含Ag2SO3,进行实验验证。
i. 本实验设计的依据是:Ag2SO3具有________性。
ii. 乙同学观察到________,得出结论“沉淀n不含Ag2SO3”。
③丙同学从溶液n的成分角度再次设计实验证明沉淀n不含Ag2SO3。
i. 本实验设计的依据是:若沉淀n含Ag2SO3,则溶液n中含1Ag+微粒的总物质的量___(填“>”、“=”或“<”)Cl–物质的量。
ii. 结合实验现象简述丙同学的推理过程:____。
Ⅲ.浸取剂再生(4)溶液m经处理后可再用于浸出AgCl,请简述该处理方法____。
【答案】AgCl(s)Ag+(aq)+ Cl-(aq) ,Ag+与SO 32- 结合生成[Ag(SO3)2]3–,促进AgCl的溶解平衡正向移动 HSO3- Ag2SO4的溶解度远大于AgCl或Ag2SO3,溶液中Ag+ 的浓度很小还原b.中清液的颜色与..,均为浅紫色溶液< e中无沉淀生成,说明清液中没有Cl-,则.......c.相同溶液n中加入稀硝酸使[Ag(SO3)2]3–全部转化为Ag+,Ag+将Cl–全部沉淀,由此可知溶液n中含Ag元素的微粒总物质的量不小于n(Cl–) 加NaOH溶液调节pH至9~10【解析】【分析】I、(1)利用平衡移动的知识答题即可;II、(2)生成沉淀m时,溶液m的pH为5,观察图像,可以得知HSO3-的物质的量分数占100%;(3)①溶液中Ag+的浓度很小,而Ag2SO4的溶解度较大,故不会形成Ag2SO4沉淀;②依据Ag2SO3的还原性答题;③e中无沉淀生成,说明清液中没有Cl-,则溶液n中加入稀硝酸使[Ag(SO3)2]3–全部转化为Ag+,Ag+将Cl–全部沉淀,由此可分析出溶液n中含Ag元素的微粒总物质的量不小于n(Cl–);III、(4)m溶液中的溶质为NaHSO3,浸取剂为Na2SO3溶液,需要加入NaOH溶液将NaHSO3转化为Na2SO3。
培优 易错 难题氧化还原反应辅导专题训练附答案
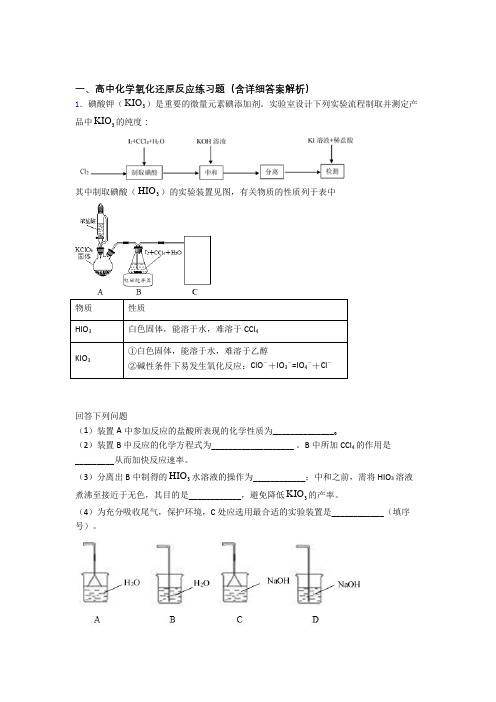
一、高中化学氧化还原反应练习题(含详细答案解析)1.碘酸钾(3KIO)是重要的微量元素碘添加剂。
实验室设计下列实验流程制取并测定产品中3KIO的纯度:其中制取碘酸(3HIO)的实验装置见图,有关物质的性质列于表中物质性质HIO3白色固体,能溶于水,难溶于CCl4KIO3①白色固体,能溶于水,难溶于乙醇②碱性条件下易发生氧化反应:ClO-+IO3-=IO4-+Cl-回答下列问题(1)装置A中参加反应的盐酸所表现的化学性质为______________。
(2)装置B中反应的化学方程式为___________________ 。
B中所加CCl4的作用是_________从而加快反应速率。
(3)分离出B中制得的3HIO水溶液的操作为____________;中和之前,需将HIO3溶液煮沸至接近于无色,其目的是____________,避免降低3KIO的产率。
(4)为充分吸收尾气,保护环境,C处应选用最合适的实验装置是____________(填序号)。
(5)为促使3KIO 晶体析出,应往中和所得的3KIO 溶液中加入适量的___________。
(6)取1.000g 3KIO 产品配成200.00mL 溶液,每次精确量取20.00mL 溶液置于锥形瓶中,加入足量KI 溶液和稀盐酸,加入淀粉作指示剂,用0.1004mol/L 223Na S O 溶液滴定。
滴定至终点时蓝色消失(2--2-22346I +2S O =2I +S O ),测得每次平均消耗223Na S O 溶液25.00mL 。
则产品中3KIO 的质量分数为___(结果保留三位有效数字)。
【答案】还原性、酸性 22235CI +I +6H O==2HIO +10HCl 充分溶解2I 和2Cl ,以增大反应物浓度 分液 除去2Cl (或-ClO ),防止氧化3KIO C 乙醇(或酒精) 89.5%。
【解析】【分析】装置A 用于制取Cl 2,发生的反应为:KClO 3+6HCl(浓)=KCl+3Cl 2↑+3H 2O ,装置B 中发生的是制取HIO 3的反应,装置C 为尾气处理装置,既要吸收尾气中的HCl 和Cl 2,还要防止倒吸。
【化学】化学氧化还原反应的专项培优 易错 难题练习题附详细答案

一、高中化学氧化还原反应练习题(含详细答案解析)1.工业上处理含苯酚废水的过程如下。
回答下列问题:Ⅰ.测定废水中苯酚的含量。
测定原理:+3Br 2→↓+3HBr 测定步骤:步骤1:准确量取25.00mL 待测废水于250mL 锥形瓶中。
步骤2:将5.00mL 1amol L -⋅浓溴水(量)迅速加入到锥形瓶中,塞紧瓶塞,振荡。
步骤3:打开瓶塞,向锥形瓶中迅速加入bmL 10.10mol L -⋅KI 溶液(过量),塞紧瓶塞,振荡。
步骤4:滴入2~3滴指示剂,再用10.010mol L -⋅223Na S O 标准溶液滴定至终点,消耗223Na S O 溶液1V mL (反应原理:2223246I 2Na S O 2NaI Na S O +=+)。
待测废水换为蒸馏水,重复上述步骤(即进行空白实验),消耗223Na S O 溶液2V mL 。
(1)“步骤1”量取待测废水所用仪器是________。
(2)为了防止溴的挥发,上述步骤中采取的措施包括迅速加入试剂和________。
(3)“步骤4”滴定终点的现象为________。
(4)该废水中苯酚的含量为________1mg L -⋅(用含1V 、2V 的代数式表示)。
如果空白实验中“步骤2”忘记塞紧瓶塞,则测得的废水中苯酚的含量________(填“偏高”“偏低”或“无影响”,下同);如果空白实验中“步骤4”滴定至终点时俯视读数,则测得的废水中苯酚的含量________。
Ⅱ.处理废水。
采用Ti 基2PbO 为阳极,不锈钢为阴极,含苯酚的废水为电解液,通过电解,阳极上产生羟基(·OH ),阴极上产生22H O 。
通过交排列的阴阳两极的协同作用,在各自区域将苯酚深度氧化为2CO 和2H O 。
(5)写出阳极的电极反应式:________。
(6)写出苯酚在阴极附近被22H O 深度氧化的化学方程式:________。
【答案】(酸式)滴定管 塞紧瓶塞 滴入一滴溶液后,锥形瓶内溶液蓝色恰好褪去,且半分钟不恢复原色 ()2194V -V 15偏低 偏低 2H O e OH H -+-=⋅+ 652222C H OH 14H O 6CO 17H O +=↑+【解析】【分析】向呈有待测废水加入浓溴水反应后得到三溴苯酚的沉淀,再加入KI 溶液与剩下的Br 2发生氧化还原反应得到I 2,方程式为Br 2+2I -===I 2+2Br -,再用Na 2S 2O 3标准溶液滴定I 2,可根据消耗的Na 2S 2O 3标准溶液的体积和浓度算出溶液中剩余的Br 2的物质的量,再设置一个空白实验测出浓溴水的物质的量,用Br 2总的物质的量-剩余Br 2的物质的量即可得出与苯酚反应的Br 2的物质的量,再结合反应方程式得到苯酚的物质的量,从而求出废水中苯酚的含量,结合实验基本操作及注意事项解答问题。
培优 易错 难题氧化还原反应辅导专题训练附详细答案

一、高中化学氧化还原反应练习题(含详细答案解析)1.224Na S O (连二亚硫酸钠)是易溶于水,不溶于甲醇的白色固体,在空气中极易被氧化,是一种还原性漂白剂。
制取224Na S O 的方法很多,(1)在碱性溶液中用4NaBH 还原3NaHSO 法制备224Na S O 的反应原理为:3222244NaBH NaHSO NaOH Na S O NaBO H O ++→++(未配平)反应装置如图所示:①实验开始及整个过程中均需通入2N ,其目的是__________________________________。
②制备过程中温度需控制在10~45℃,采用水浴加热的主要优点是______________________。
③为使3NaHSO 尽可能完全被还原,加入三口烧瓶中的反应液,应控制()()34n NaHSO n NaBH ______________。
(2)用HCOONa 还原2SO 制备224Na S O 的装置(夹持加热仪器略)如下:①装置a 烧瓶中发生反应的化学方程式为_________________________________。
②装置b 用于净化2SO ,适宜的试剂是______________________________。
③装置c 在70~83℃生成224Na S O 并析出,同时逸出2CO ,该反应的化学方程式为________________________,加入3CH OH 的目的是________________________;利用反应后的浊液分离提纯224Na S O 需经过的操作为_____________________________________________________。
【答案】排出装置内空气,使反应在无氧状况下进行 使反应液均匀受热 小于8:1(或<8) 2322Na SO 2HCl 2NaCl H O SO +=++↑ 饱和3NaHSO 溶液223224222HCOONa 4SO Na CO 2Na S O H O 3CO ++=++ 降低224Na S O 的溶解度 过滤、洗涤、重结晶、过滤、干燥【解析】【分析】(1)①224Na S O 在空气中极易被氧化,通入2N 其目的是排出装置内空气;②采用水浴加热的主要优点是使反应液均匀受热;③3222244NaBH NaHSO NaOH Na S O NaBO H O ++→++,根据得失电子守恒可知,()()34n NaHSO n NaBH =8; (2)①装置a 烧瓶中发生Na 2SO 3与盐酸反应生成SO 2的反应;②生成的SO 2气体中含有HCl 气体,根据性质选择除杂溶液;③装置c 在70~83℃HCOONa 和2SO 、23Na CO 反应生成224Na S O 并析出,同时逸出2CO ;224Na S O 不溶于甲醇,加入3CH OH 可降低224Na S O 的溶解度;利用反应后的浊液分离提纯224Na S O 需重结晶。
备战高考化学 氧化还原反应 培优 易错 难题练习(含答案)

备战高考化学 氧化还原反应 培优 易错 难题练习(含答案)一、高中化学氧化还原反应1.工业上处理含苯酚废水的过程如下。
回答下列问题:Ⅰ.测定废水中苯酚的含量。
测定原理:+3Br 2→↓+3HBr 测定步骤:步骤1:准确量取25.00mL 待测废水于250mL 锥形瓶中。
步骤2:将5.00mL 1amol L -⋅浓溴水(量)迅速加入到锥形瓶中,塞紧瓶塞,振荡。
步骤3:打开瓶塞,向锥形瓶中迅速加入bmL 10.10mol L -⋅KI 溶液(过量),塞紧瓶塞,振荡。
步骤4:滴入2~3滴指示剂,再用10.010mol L -⋅223Na S O 标准溶液滴定至终点,消耗223Na S O 溶液1V mL (反应原理:2223246I 2Na S O 2NaI Na S O +=+)。
待测废水换为蒸馏水,重复上述步骤(即进行空白实验),消耗223Na S O 溶液2V mL 。
(1)“步骤1”量取待测废水所用仪器是________。
(2)为了防止溴的挥发,上述步骤中采取的措施包括迅速加入试剂和________。
(3)“步骤4”滴定终点的现象为________。
(4)该废水中苯酚的含量为________1mg L -⋅(用含1V 、2V 的代数式表示)。
如果空白实验中“步骤2”忘记塞紧瓶塞,则测得的废水中苯酚的含量________(填“偏高”“偏低”或“无影响”,下同);如果空白实验中“步骤4”滴定至终点时俯视读数,则测得的废水中苯酚的含量________。
Ⅱ.处理废水。
采用Ti 基2PbO 为阳极,不锈钢为阴极,含苯酚的废水为电解液,通过电解,阳极上产生羟基(·OH ),阴极上产生22H O 。
通过交排列的阴阳两极的协同作用,在各自区域将苯酚深度氧化为2CO 和2H O 。
(5)写出阳极的电极反应式:________。
(6)写出苯酚在阴极附近被22H O 深度氧化的化学方程式:________。
化学氧化还原反应的专项培优 易错 难题练习题含答案

化学氧化还原反应的专项培优易错难题练习题含答案一、高中化学氧化还原反应1.某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:(一)制取氧化铜①往盛有一定量CuCl2溶液的烧杯中逐滴加入NaOH溶液,直至不再产生沉淀,然后将烧杯中的物质转移到蒸发皿中,加热至沉淀全部变为黑色。
②将步骤①所得的黑色沉淀过滤、洗涤,晾干后研细备用。
(1)在实验过程中,若未加入NaOH溶液,直接将CuCl2溶液转移到蒸发皿中加热,最后也能得到黑色沉淀,试分析其原因__________。
(2)写出检验步骤②中沉淀是否洗涤干净的操作__________________。
(二)为证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较,用下图装置进行实验,每次实验时均收集25ml气体,其他可能影响实验的因素均已忽略,实验数据见下表:实验序号KClO3质量其他物质质量待测数据③1.2g无其他物质a④1.2g CuO0.5g b⑤1.2g MnO20.5g c(3)写出氯酸钾分解反应的化学方程式,并用双线桥表示电子转移的方向和数目________。
(4)上述实验中的“待测数据”是指___________________。
(5)图中量气装置B由干燥管、乳胶管和50mL滴定管改造后组装面成,此处用滴定管是________(填“酸式”或“碱式”)滴定管。
(6)若实验证明氧化铜加快氯酸钾的分解效果比用二氧化锰差,请结合上表的实验效果数据,在坐标图中分别画出使用CuO、MnO2作催化剂时产生氧气的体积[V(O2)]随时间(t)变化的曲线(注明必要的标识)________。
【答案】CuCl2溶液中存在水解平衡CuCl2+2H2O Cu(OH)2+2HCl,加热时HCl逸出使平衡不断右移,同时得到的Cu(OH)2受热分解生成CuO 取2~3mL最后的洗涤液于试管中,滴入少量稀硝酸酸化,再滴入几滴硝酸银溶液,若无白色沉淀产生,则洗涤干净收集25mL气体所需的时间碱式【解析】【分析】【详解】(1)CuCl2是强酸弱碱盐会发生水解,CuCl2溶液中存在水解平衡CuCl2+2H 2O Cu(OH)2+2HCl,水解吸热,加热时HCl逸出使平衡不断右移,同时得到的Cu(OH)2受热分解生成CuO。
备战高考化学 氧化还原反应 培优 易错 难题练习(含答案)含答案

备战高考化学 氧化还原反应 培优 易错 难题练习(含答案)含答案一、高中化学氧化还原反应1.224Na S O (连二亚硫酸钠)是易溶于水,不溶于甲醇的白色固体,在空气中极易被氧化,是一种还原性漂白剂。
制取224Na S O 的方法很多,(1)在碱性溶液中用4NaBH 还原3NaHSO 法制备224Na S O 的反应原理为:3222244NaBH NaHSO NaOH Na S O NaBO H O ++→++(未配平)反应装置如图所示:①实验开始及整个过程中均需通入2N ,其目的是__________________________________。
②制备过程中温度需控制在10~45℃,采用水浴加热的主要优点是______________________。
③为使3NaHSO 尽可能完全被还原,加入三口烧瓶中的反应液,应控制()()34n NaHSO n NaBH ______________。
(2)用HCOONa 还原2SO 制备224Na S O 的装置(夹持加热仪器略)如下:①装置a 烧瓶中发生反应的化学方程式为_________________________________。
②装置b 用于净化2SO ,适宜的试剂是______________________________。
③装置c 在70~83℃生成224Na S O 并析出,同时逸出2CO ,该反应的化学方程式为________________________,加入3CH OH 的目的是________________________;利用反应后的浊液分离提纯224Na S O 需经过的操作为_____________________________________________________。
【答案】排出装置内空气,使反应在无氧状况下进行 使反应液均匀受热 小于8:1(或<8) 2322Na SO 2HCl 2NaCl H O SO +=++↑ 饱和3NaHSO 溶液223224222HCOONa 4SO Na CO 2Na S O H O 3CO ++=++ 降低224Na S O 的溶解度 过滤、洗涤、重结晶、过滤、干燥【解析】【分析】(1)①224Na S O 在空气中极易被氧化,通入2N 其目的是排出装置内空气;②采用水浴加热的主要优点是使反应液均匀受热;③3222244NaBH NaHSO NaOH Na S O NaBO H O ++→++,根据得失电子守恒可知,()()34n NaHSO n NaBH =8; (2)①装置a 烧瓶中发生Na 2SO 3与盐酸反应生成SO 2的反应;②生成的SO 2气体中含有HCl 气体,根据性质选择除杂溶液;③装置c 在70~83℃HCOONa 和2SO 、23Na CO 反应生成224Na S O 并析出,同时逸出2CO ;224Na S O 不溶于甲醇,加入3CH OH 可降低224Na S O 的溶解度;利用反应后的浊液分离提纯224Na S O 需重结晶。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、高中化学氧化还原反应练习题(含详细答案解析)1.高氯酸铵是一种常见的强氧化剂,常用作火箭发射的推进剂。
根据下列信息回答问题:已知:①高氯酸铵受热分解为N2、Cl2、O2和H2O;②Mg3N2易水解;③Cu与N2在酒精灯加热条件下不反应。
(1)写出高氯酸铵受热分解的化学反应方程式: _____________,Mg3N2的电子式为________。
(2)现有23.5g NH4ClO4分解,用下列装置设计实验,验证其分解产物并计算分解率。
(注:①装置中空气已除尽;②装置可重复使用;③B~F装置中的试剂均过量且能与相应物质反应完全。
)①用E装置质量的增加来验证生成的气体产物之一,则E中盛放的试剂是:_______。
②请按气流由左至右的方向连接装置:A →E→D →B→______→_____→_______→E (选择B~F 装置,并用B~F字母填空)。
③证明产物中有Cl2的实验现象:________。
④反应结束后,若C装置质量增加了2.38g,则NH4ClO4的分解率是:________%。
(3)样品中NH4ClO4的含量(杂质中不含NH4+)还可用蒸馏法测定(如图所示,加热和夹持装置已略去),实验步骤如下:步骤1:组装仪器,检查气密性;准确称取样品a g(不超过0.5g)于蒸馏烧瓶中,加入约150mL 水溶解。
步骤2:准确量取40.00mL 约0.1mol/L H2SO4于锥形瓶中。
步骤3:向蒸馏烧瓶中加入20mL 3mol/L NaOH溶液;加热蒸馏使NH3全部挥发。
步骤4:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤5:向锥形瓶中加2~3滴甲基橙,用c mol/L NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1 mL。
步骤6:重复实验2~3次。
回答下列问题:①步骤2中,准确量取40.00ml H2SO4溶液的玻璃仪器是: __________。
②为获得样品中NH4ClO4的含量,还需补充的实验是:______。
【答案】2NH4ClO 42O2↑+N2↑+Cl2↑+4H2O↑浓硫酸E F C D裝置中颜色由无色变为橙色 85.0或85 酸式滴定管或移液管用NaOH标准溶液标定硫酸溶液的浓度【解析】【分析】(1)根据得失电子守恒配平高氯酸铵受热分解的化学反应方程式;Mg3N2是离子化合物;(2)A是高氯酸铵受热分解的装置;B是氢氧化钠溶液,可以吸收氯气;C中盛放Mg 粉,可以检验氮气;D中溴化钾可以检验氯气;F中铜粉可以检验氧气;E中盛放液体,根据E装置质量的增加来验证生成的水,所以E中盛浓硫酸;(3)①根据硫酸体积的精度是0.01mL选择仪器;②要计算NH4ClO4的含量,需要知道硫酸溶液的浓度。
【详解】(1)根据得失电子守恒配平高氯酸铵受热分解的化学反应方程式为2NH4ClO 42O2↑+N2↑+Cl2↑+4H2O↑;Mg3N2是离子化合物,电子式是;(2)①A是高氯酸铵受热分解的装置;B是氢氧化钠溶液,可以吸收氯气;C中盛放Mg 粉,可以检验氮气;D中溴化钾可以检验氯气;F中铜粉可以检验氧气;E中盛放液体,根据E装置质量的增加来验证生成的水,所以E中盛浓硫酸;②根据以上分析,按气流由左至右的方向连接装置:A →E→D →B→E→F→C→E;③D中溴化钾可以与氯气反应,方程式是2KBr+Cl2=2KCl+Br2,溴水为橙色,所以D裝置中颜色由无色变为橙色可以证明产物中有Cl2;④C中盛放Mg粉,可以与氮气反应生成Mg3N2,若C装置质量增加了2.38g,说明反应生成氮气2.38g,则NH4ClO4的分解率是2.38100%85%1423.5117.5gg⨯=⨯;(3)①根据硫酸体积的精度是0.01mL,准确量取40.00mLH2SO4溶液的玻璃仪器是酸式滴定管;②为获得样品中NH4ClO4的含量,还需补充的实验是用NaOH标准溶液标定硫酸溶液的浓度。
2.某高中科研小组模拟工业尿素法生产肼(N2H4),具体方法:先将尿素、次氯酸钠和氢氧化钠溶液混合,然后在催化剂存在的条件下反应制得肼,利用氮气吹出混合物中的肼,并用硫酸吸收制备硫酸肼。
具体实验原理图如下:已知:①肼极易溶于水,长期暴露在空气中或短时间受高温作用会爆炸分解。
②硫酸肼(N2H4·H2SO4)是类似于NH4HSO4的盐类,白色固体,微溶于冷水,易溶于热水,不溶于乙醇和二氯乙烷等有机溶剂。
③密度:ρ硫酸肼>ρ二氯乙烷>ρ稀硫酸(1)盛装尿素溶液的装置名称为_____________________;硫酸肼的水溶液中含有多种阳离子,其中阳离子N2H5+的电子式为________________________。
(2)反应前应先通入一段时间氮气,其目的为________________________________。
(3)装置A中发生反应制备肼的离子方程式为_______________________________。
(4)装置B中二氯乙烷的作用为__________________________________________;使用冰水浴的作用__________________________________________________。
(5)装置B反应完全后需经过过滤、洗涤、干燥等操作得到硫酸肼,洗涤过程中最好选择下列那种洗涤剂________________(填字母)。
A.冷水 B.热水 C.无水乙醇 D.饱和食盐水(6)若实验中所用的NaClO和NaOH混合液中两溶质的浓度均为0.1mol·L−1,则此溶液中离子浓度的大小顺序为______________________________________。
【答案】三颈烧瓶赶走装置中的空气,避免空气与肼反应CO-+H2O 防倒吸,同时使产物硫酸肼脱离反应混合ClO−+2OH−+CO(NH2)2N2H4+Cl−+23液利于产物析出,同时降温防爆炸 C c(Na+)>c(OH−)>c(ClO−)>c(H+)【解析】【分析】(1)盛装尿素溶液的装置名称为三颈烧瓶;硫酸肼的水溶液中含有多种阳离子,其中阳离子N2H5+可以认为由N2H4与H+通过配位键结合,在N2H4中,每个N原子与两个H原子形成共价键,则两个N原子间还应形成一对共用电子。
(2)反应前应先通入一段时间氮气,其目的为排尽装置内的空气,防止空气与肼反应。
(3)装置A中,碱性溶液,ClO−在催化剂作用下,将CO(NH2)2氧化为N2H4,自身被还原为CO-和H2O。
Cl−,同时生成23(4)装置B中二氯乙烷的作用为防倒吸,同时使产物硫酸肼脱离反应混合液;使用冰水浴的作用是降低产物的溶解度,同时降温防爆。
(5)装置B反应完全后需经过滤、洗涤、干燥等操作得到硫酸肼,洗涤过程中尽可能减少产品的溶解损失,所以最好选择无水乙醇。
(6)若实验中所用的NaClO和NaOH混合液中两溶质的浓度均为0.1mol·L−1,c(Na+)=0.1mol·L−1,因水解c(ClO−)<0.1mol·L−1,c(OH−)>0.1mol·L−1,由此可确定溶液中离子浓度的大小。
【详解】(1)盛装尿素溶液的装置名称为三颈烧瓶;N2H5+可以认为由N2H4与H+通过配位键结合,在N2H4中,每个N原子与两个H原子形成共价键,则两个N原子间还应形成一对共用电子,电子式为。
答案为:三颈烧瓶;;(2)反应前应先通入一段时间氮气,其目的为排尽装置内的空气,防止空气与肼反应。
答案为:赶走装置中的空气,避免空气与肼反应;(3)装置A中,碱性溶液,ClO−在催化剂作用下,将CO(NH2)2氧化为N2H4,自身被还原为CO-和H2O,反应方程式为Cl−,同时生成23CO-+H2O。
答案为:ClO−+2OH−+CO(NH2)2N2H4+Cl−+23CO-+H2O;ClO−+2OH−+CO(NH2)2N2H4+Cl−+23(4)装置B中二氯乙烷的作用为防倒吸,同时使产物硫酸肼脱离反应混合液;使用冰水浴的作用是降低产物的溶解度,同时降温防爆。
答案为:防倒吸,同时使产物硫酸肼脱离反应混合液;利于产物析出,同时降温防爆炸;(5)装置B反应完全后需经过滤、洗涤、干燥等操作得到硫酸肼,洗涤过程中尽可能减少产品的溶解损失,所以最好选择无水乙醇。
答案为:C;(6)若实验中所用的NaClO和NaOH混合液中两溶质的浓度均为0.1mol·L−1,c(Na+)=0.1mol·L−1,因水解c(ClO−)<0.1mol·L−1,c(OH−)>0.1mol·L−1,由此可确定溶液中离子浓度的关系为:c(Na+)>c(OH−)>c(ClO−)>c(H+)。
答案为:c(Na+)>c(OH−)>c(ClO−)>c(H+)。
【点睛】在分析装置B中二氯乙烷的作用时,应借助信息“③密度:ρ硫酸肼>ρ二氯乙烷>ρ稀硫酸,且硫酸肼不溶于二氯乙烷”,则往二氯乙烷中通入肼后,肼逸出,在上层与稀硫酸反应生成硫酸肼,由于硫酸肼的密度比二氯乙烷大,且难溶于二氯乙烷,所以沉在二氯乙烷的底部,从而实现与反应混合液的分离。
3.现有一份含有FeCl3和FeCl2固体混合物,为测定各成分的含量进行如下两个实验:实验1:① 称取一定质量的样品,将样品溶解;② 向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;③ 将沉淀过滤、洗涤、干燥得到白色固体17.22 g。
实验2:① 称取与实验1中相同质量的样品,将样品溶解;② 向溶解后的溶液中通入足量的Cl2;③ 再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀;④ 将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4g。
回答下列问题:(1)溶解过程中所用到的玻璃仪器有___________________。
(2实验室保存FeCl2溶液时通常会向其中加入少量试剂_____________和_____________。
(3)实验2通入足量Cl2的目的是_____________;涉及的化学反应的离子方程式是____________________。
(4检述实验2的步骤④中沉淀已经洗涤干净的方法是_____________。
(5)加热FeCl3溶液,并将溶液蒸干时,通常不能得到FeCl3固体,请以平衡的观点解释其原因(方程式与文字相结合来说明)______________________。
(6)FeCl3溶液可以用于止血,主要是因为FeCl3溶液能使血液聚沉,这涉及胶体的特性。
以下关于胶体的说法不正确的是_____________。
