物质的结构与分类

物质的结构与分类:
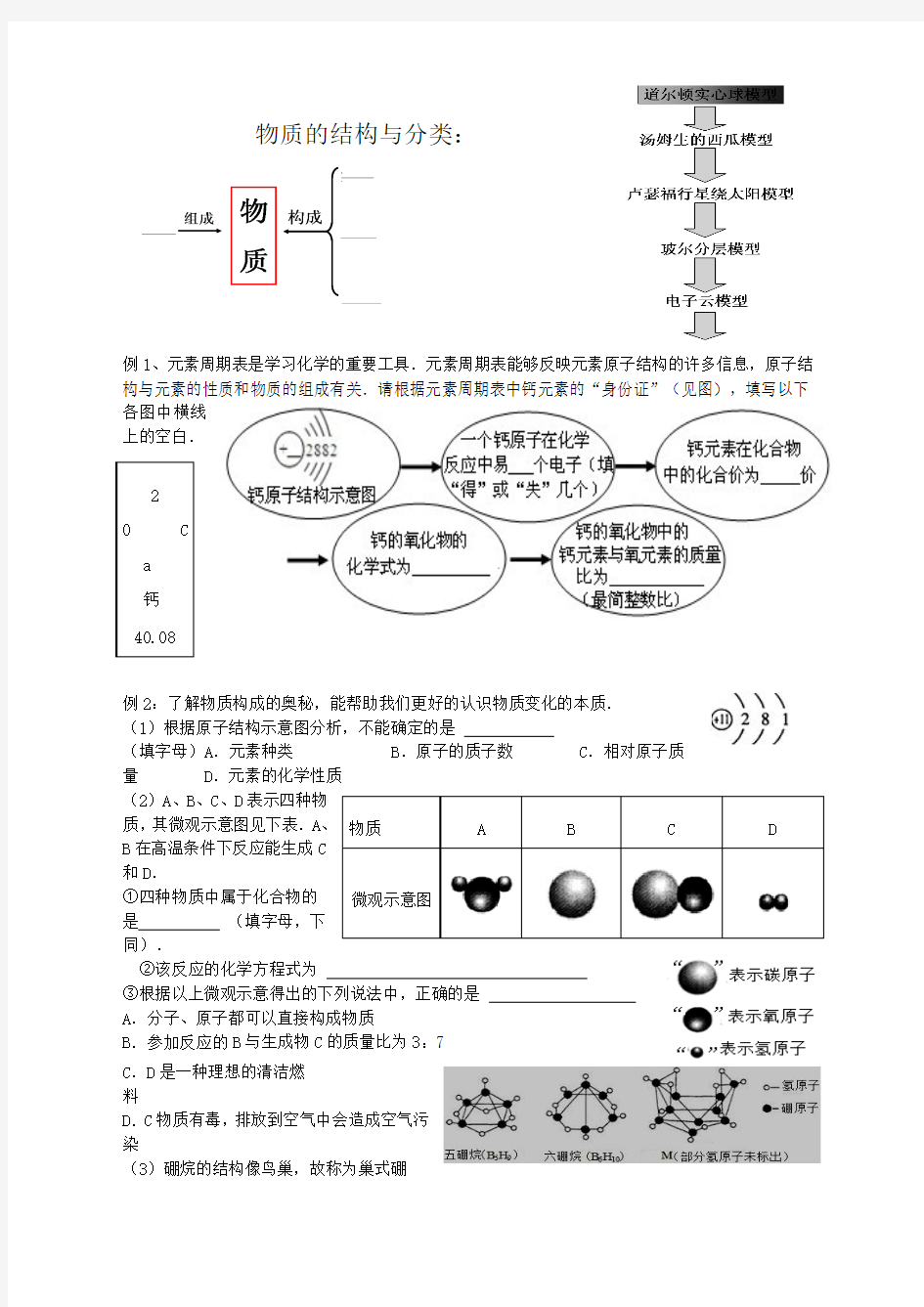
例1、元素周期表是学习化学的重要工具.元素周期表能够反映元素原子结构的许多信息,原子结
构与元素的性质和物质的组成有关.请根据元素周期表中钙元素的“身份证”(见图),填写以下
各图中横线
上的空白.
C .
D 是一种理想的清洁燃
料
D .C 物质有毒,排放到空气中会造成空气污
染
(3)硼烷的结构像鸟巢,故称为巢式硼
烷.五硼烷(B5H9)为传统火箭燃料,燃烧产物对环境污染小.如图是三种巢式硼烷的分子模型,其说法不正确的是()
A.图中M的名称为九硼烷B.五硼烷中B、H元素质量比为5:9
C.六硼烷由6个硼原子和10个氢原子构成D.硼烷有可能成为未来的清洁能源.
练习:现有三组物质:红磷、镁、铝、水;乙醇、生石灰、醋酸、葡萄糖;加碘食盐、白酒、纯碱、食醋。每组中可选出一种物质,该物质所属类别与其他三种不同。所选三种物质混合后可以发生反应,制得一种重要的化工原料氢氧化钠,则有关反应的化学方程式是
。练习:
1.用微观的钥匙开启宏观问题之门”是化学学科研究物质的一般方法,而构建模型又常常是我们认识微观世界的重要手段.看下列各组微观模型图回答问题:如图1为某化学反应的微观过程.
(2)水电解的过程可用如图2表示,微粒运动变化的先后顺序
的微观模型图,产物之一是次氯酸(HClO),具有杀菌作用.
(1)该反应的化学方程式为.
(2)可通过检验产物C来证明该反应已发生,方法是在反应后的溶液里滴几滴AgNO3溶液,有白色沉淀生成.用化学方程式表示其原理
3.从体积的大小来看,下面各项中最小的是()
4.模型是科学研究中一种常用的方法,它可以
帮助人们认识和理解一些不能直接观察到的事物。下图形象地表
示了在一定条件下,某化学反应前后反应物与生成物分子及其数
目的变化,该反应的基本反应类型是。
5、下列对物质世界的认识中,不正确的是
A.中子和质子都是由夸克构成的
B.石墨很软,金刚石很硬,是因为碳原子构成的物质结构不同造成的
C.要减轻臭氧层被破坏的程度,应减少 SO2的排放 D.物质不全是由分子构成的
6.我省盛产的绿茶享誉海内外,绿茶中的单宁酸具有抑制血压上升、清热解毒等功效,其化学式为C76H52O46。下列关于单宁酸的说法中,不正确的是()
A.每个分子含有76个碳原子B.由碳、氢、氧三种元素组成
C.每个分子含有23个氧分子 D.碳、氢、氧原子个数比为38:26:23
9、自第十一届奥运会以来,历届奥运会都要举行颇为隆重的“火炬接力”,火炬的可燃物为丁烷(化学式C4H10),它燃烧时,火苗高且亮,在白天,二百米以外也能清晰可见,下列关于丁烷的叙述正确的是()①丁烷是由碳、氢两种元素组成的②丁烷是由丁烷分子构成的③丁烷分子是由碳、氢两种元素组成的④丁烷由4个碳原子和10个氢原子组成⑤丁烷分子是由碳原子和氧原子构成的A、①②③④⑤B、①②⑤C、②③④⑤ D、①②④⑤
10、1985年科学家发现的C60分子是由60个碳原子构成的,它的形状像足球(如图C),因此又叫足球烯(音希)。1991年科学家又发现一种碳的单质——碳纳米管,它是由六边形的碳原子构成的管状大分子(如图D)。下图中,A、B分别是金刚石和石墨的结构示意图。
用你所学到的化学知识回答下列问题:
金刚石、石墨、足球烯、碳纳米管物理性质有较大差异的原因是?
11.元素周期表中一行表示;一列表示;
12.KClO3中Cl的化合价________KMnO4中Mn的化合价________Na2CO3中C的化合价_________ 13.已知某元素R只有一种化合价,其氯化物的化学式为RCl3那么其氧化物的化学式为。14:如C-12的质量是a,某原子的质量是b,那么这个原子的相对质量可以表示为?15:已知硫酸铵的化学式为(NH4)2SO4,
求:(1)硫酸铵的相对分子质量。
(2)硫酸铵中氢元素的质量分数
(3)66克硫酸铵中含氮元素的质量
(4)多少克硫酸铵中含氮元素质量为28克。
16.某铁的氧化物中,铁、氧两种元素的质量比为7:3,求氧化物的分子式。
17.A、B两原子的相对原子质量之比为7:2,在它组成的一种化合物中,A、B两元素的质量比为21:8,则这种化合物的化学式为
18.经检测一份尿样中含尿素CO(NH2)2 的质量分数为2%,假定其他成分不含氮,求:此尿样中氮
元素的质量分数;
19.用序号回答:在①分子②原子③质子④电子⑤离子⑥原子核⑦中子⑨元素中,选择:
(1)构成物质的基本微粒是,其中________是化学变化中的最小微粒,它是由________和________构成的。
(2)元素的种类由_______数决定;元素的相对原子质量由______数和_____数决定。
(3)Mg和Mg2+因具有相同的______数,故属于同种_______,又因为它们具有不同的________数,故属于两种不同的微粒。
20.黄瓜中富含维生素C,其分子结构如右图。维生素C由
________________元素组成,它的化学式为。维
生素C在pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在
烹饪时应加入少量的______________。维生素C片保存时,应注意避热、避光、密封,请你据此推测维生素C的一条化学性质____________________________。
21.“物质的结构决定性质,物质的性质决定用途”是自然科学的重要思想。过氧
化氢是一种常用的杀菌消毒剂,其原因是过氧化氢分子中含有一种叫“过氧基”
的结构(右图表中方
框框出部分)。据此
推测下列物质中,可
作杀菌消毒剂的是
()
22.我国的上海市建成了世界上第一条商业性磁悬浮铁路。磁悬浮的核心技术是利用超导体的反磁性。高温超导物质(Y2Ba4Cu6O13)是以Y m O n、BaO、和CuO为原料,经研磨烧结而成(此过程中所有元素的化合价均不变)。则高温超导物(Y2Ba4Cu6O13)中元素Y显价。
23、人体体液里经分析含有A、B、C、D四种元素。A原子为质量最小的原子;B原子得到一个电子后与氩原子的电子层结构相同;c元素的阳离子与D元素的阴离子核电荷数相差3;D元素为地壳中含量最多的元素。则A、B、C、D四种元素的单质的化学式分别为、、、。
23、某三价金属M与氧元素组成的化合物中,M元素与氧元素的质量比为9:8,则该金属M的相对原子质量为_______。若该金属原子中所含中子数比质子数多1,则该金属元素的名称是__________。
24、、人们发现自然界中有一系列与甲烷(CH4)结构、化学性质相似的有机物。它们分子中的碳原子数依次递增,如甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)、丁烷(C4H10)、戊烷(C5H12)……,依据它们分子组成变化规律,下列推断不正确的()
A.分子中含10个碳原子的癸烷化学式是C10H24
B.这一系列化合物分子中碳原子数每增加1个,氢原子数随之增加2个
C.这一系列化合物分子组成可用C n H2n+2(n≥1)表示D.这一系列化合物中相对分子质量最小的是甲烷
25下列分别盛有不同物质的容器中,所盛物质属
于单质的是,化合物的是,
纯净物的是,混合物的是
,氧化物的是。(均填容器下的代号)
高中化学《物质的分类》教案8新人教版必修
第二章第一课时“第一节物质的分类”教案 【教学目标】 1.体验进行分类的目的及意义。 2.学会根据物质的组成和性质对物质进行分类。 【教学重点】 分类法的意义及常见化学物质及其变化的分类方法 【教学方法】 讨论、讲授 【教学过程设计】 【情景引入】 若要到“万福”商场买一部复读机,你如何以最快的速度找到它? 【思考与交流】 请根据以往的生活经验和社会知识,列举一些应用分类法的例子。【师生交流】 分类法在日常生活中的应用是非常普遍的,我们应该善于发现和学会使用,以提高我们工作和学习的效率。 【学生活动】 组织学生对八支笔进行分类活动 分类并没有唯一性,它会根据分类的标准不同而不同。 【点评】当分类的标准确定之后,同类中的事物在某些方面的相似性可以帮助我们做到举一反三;对于不同类的事物的了解我们有可能做到由此及彼。所以分类的方法是一种非常简单易行的科学方法,分类法的应用也是非常普遍的。 【过渡】 其实分类方法不但在生活和工作中经常碰到,在化学学习过程中也普遍存在, 一、简单分类法及其应用 【学生活动】案例1、连线: 【师生交流】 通过这个活动,可以看出对于Na2CO3如果从阳离子来看,可以与Na2SO4一起分为硫酸盐。若从阴离子的角度来看可以与K2CO3一起分为碳酸盐。因此可以说, 【点评】 一种分类方法所依据的标准有一定局限,所能提供的信息少,人们在认识事物时往往需要采用多种分类方法来弥补单一分类方法的不足。1、交叉分类法 【学生活动】 案例2、对下列化学反应进行分类: (1)硫在氧气里燃烧 (2)红磷在氧气里燃烧 (3)铁丝在氧气里燃烧 (4)铝箔在氧气里燃烧
(5)蜡烛在氧气里燃烧 案例3、见课本P21,图2-32、树状分类法 【点评】:树状分类法可以让我们把同类事物进行再分 【实践活动】 按照物质的组成和性质,对纯净物进行分类,仿照P21图2-3作出树状分类图,然后选择下列合适的物质填在物质类别上。 O2, Cu,H2SO4, Ba(OH)2,KNO3, CO2,空气,含镁60%的MgO 【小结】 在学习了分类的方法以后,大家就要学会对以前和将要学的化学知识进行及时的归纳和整理,学会对物质及其变化进行分类,并通过对各类物质的代表物质的研究来了解这类物质的性质,从而提高我们化学学习的效率。 【练习】 【课后作业】 1、通过查找资料或与同学合作,为石油加工后的产物或用途制作一张树状分类图或交叉分类图。 2、某学校要举行田径运动会,有高一、高二、高三3个年级的男生、女生参加,请你画出以高一男子组、高一女子组……的方法分组的树状分类图。 3、填表: 【课后阅读材料】“白马非马”的故事 【原文】公孙龙是战国时期平原君的食客。一天,他牵一匹白马出关被阻,公孙龙便以白马非马的命题与之辩论,守关的人辩不过他,公孙龙就牵着马出关去了。(或说,他还是不得出关。)公孙龙说,白马为非马者,言白所以名色,言马所以名形也;色非形,形非色也。夫言色则形不当与,言形则色不宜从,今合以为物,非也。如求白马于厩中,无有,而有骊色之马,然不可以应有白马也。不可以应有白马,则所求之马亡矣;亡则白马竟非马。 【大致意思】公孙龙是战国时期平原君的食客。据说,公孙龙有一次骑马过关,把关的人对他说:“法令规定马不许过。”公孙龙回答说:“我骑的是白马,白马不是马,这可是两回事啊。”公孙龙的“白马”有没有过关,我们不得而知。从常人的观点来看,守关的兵士八成认为公孙龙是在诡辩。 【评论】 冯友兰(我国著名新理学家、哲学家)认为《公孙龙子》里的《白马论》对“白马非马”进行了三点论证: 一是强调“马”、“白”、“白马”的内涵不同。“马”的内涵是一种动物,“白”的内涵是一种颜色,“白马”的内涵是一种动物加一种颜色。三者内涵各不相同,所以白马非马。 二是强调“马”、“白马”的外延的不同。“马”的外延包括一切马,不管其颜色的区别;“白马”的外延只包括白马,有颜色区别。外延不同,所以白马非马。三是强调“马”这个共相与“白马”这个共相的不同。马的共相,是一切马的本质属性,它不包涵颜色,仅只是“马作为马”。共性不同,“马作为马”与“白马作为白马”不同。所以白马非马。
物质的组成、结构和分类题目
物质的组成、构成和分类 1,现有C、H、O、Na、Cu、S六种元素,从中选出相关元素组成下列类别物质的化学式:(每一类各写两例) ?单质_____________ ?酸_____________ ?碱_____________ ?盐_____________ ?氧化物____________?有机物_____________ 2、构成氧气的分子和构成液氧的分子具有( ) A、相同的性质 B、不同的性质 C、相同化学性质 D、不同化学性质 3、钾的相对原子质量较氩的相对原子质量小1,而核电荷数大1,由此可推断,一个钾原 子和一个氩原子所含中子数的关系是( ) A、钾的中子数比氩的中子数少1个 B、钾的中子数比氩的中子数少2个 C、钾的中子数等于氩的中子数 D、钾的中子数比氩的中子数多1个 4、下列关于物质组成的说法中正确的是( ) A、任何纯净物都是由一种元素组成的 B、一种元素只能组成一种单质 C、任何一种化合物都是由不同种元素组成的 D、任何物质都是由分子构成 5、有下列四组物质,每组均有一种与其它物质所属类别不同,请在下面的横线上填写这种 物质的名称: ①食醋、牛奶、加碘盐、水;②冰、干冰、氧化铁、铜绿; ③蛋白质、油脂、维生素、煤气;④纯碱、烧碱、食盐、石灰石 ①__________②__________③__________④__________ 6、进入21世纪,化合物已超过2000万种,其些物质由碳、氢、氧、钠中某些元素组成, 用上述元素,按要求各写出一种常见物质化学式: ①用于炼铁的气体且有可燃性的氧化物__________; ②“汽水”“雪碧”中含有的一种酸__________; ③能溶解蛋白质、油脂、纸张的工业原料的碱__________; ④家庭中常用作洗涤剂的纯碱是__________; ⑤可造人工雨雾的一种氧化物是__________; ⑥“西气东输”工程中将要输送的有机物是__________。 综合能力提升 1、下列关于原子、分子、离子的叙述正确的是( ) A、分子是化学变化中的最小微粒 B、离子在化学反应中不能再分 C、原子可以直接构成物质 D、分子中含有离子 2、能保持二氧化碳化学性质的微粒是( ) A、碳元素和氧元素 B、两个氧原子和一个碳原子 C、二氧化碳分子 D、二氧化碳分子中的电子数 3、由原子构成,且常温下呈液态的物质是( ) A、五氧化二磷 B、汞 C、硫酸 D、液氧 4、下列物质中由离子构成的是( ),由原子直接构成的物质是( ) A、铜 B、氯化钠 C、氯化氢 D、氩气 5、下列各组物质中按单质、化合物、混合物顺序排列的是( ) A、氧气、氧化镁、液态氧 B、铁、二氧化硫、石油 C、铜、二氧化锰、甲烷 D、磷、二氧化碳、水银 6、下列几组物质中,元素组成完全相同的是( )
高中化学常见物质的分类
物质的分类 一、单质 按元素组成分为 1.金属单质 K钾、Ca钙、Na纳、Mg镁、Al铝、Zn锌、Fe铁、 Sn锡、Pb铅、Cu铜、Hg汞、Ag银、Pt铂、Au金 2.非金属单质 氢气H2、碳C、氮气N2、氧气O2、臭氧O3、氟气F2、硅Si、磷P、硫S、氯气Cl2、液溴Br2、碘I2、氦气He、氖气Ne、氩气Ar、 二、化合物 1.有机化合物 乙醇、甲烷、乙烷、乙烯、葡萄糖 2.无机化合物 三、氧化物 (1)按元素组成分为金属氧化物和非金属氧化物 1.金属氧化物 氧化钠Na2O、过氧化钠Na2O2、氧化钙CaO、氧化镁MgO、氧化铝Al2O3、氧化锌ZnO、氧化铁Fe2O3、氧化亚铁FeO、四氧化三铁Fe3O4、氧化铜CuO、氧化汞HgO、七氧化二锰Mn2O7 2.非金属氧化物 水H2O,过氧化氢H2O2、一氧化碳CO、二氧化碳CO2、一氧化氮NO、五氧化二氮N2O5、二氧化硅SiO2、五氧化二磷P2O5、二氧化硫SO2、三氧化硫SO3 (2)按照性质分为 碱性氧化物 酸性氧化物 不成盐氧化物 两性氧化物 过氧化物 1.碱性氧化物 大部分的金属氧化物为碱性氧化物,但有特例:过氧化钠Na2O2为过氧化物、氧化铝Al2O3为两性氧化物、七氧化二锰Mn2O7为酸性氧化物、四氧化三铁Fe3O4、 碱性氧化物有:氧化钠Na2O、氧化钙CaO、氧化镁MgO、氧化锌ZnO、氧化铁Fe2O3、氧化亚铁FeO、氧化铜CuO、氧化汞HgO、 碱性氧化物一定为金属氧化物,金属氧化物不一定为碱性氧化物 2.酸性氧化物 大部分的非金属氧化物为,但有特例:水H2O,一氧化碳CO、一氧化氮NO不是酸性氧化物,七氧化二锰Mn2O7虽然为金属氧化物但属于酸性氧化物、 非金属氧化物不一定为酸性氧化物 3.不成盐氧化物:一氧化碳CO、一氧化氮NO 4.两性氧化物:氧化铝Al2O3 5.过氧化物:过氧化氢H2O2、过氧化钠Na2O2 四、酸 中学常见的酸: 盐酸HCl、硫酸H2SO4、硝酸HNO3、碳酸H2CO3、磷酸H3PO4、次氯酸HClO、氯酸HClO3、高氯酸HClO4、亚硫酸H2SO3、硅酸H2SiO3、氢硫酸H2S、氢碘酸HI、氢溴酸HBr、氢氟酸HF、乙酸CH3COOH (1)依据组成分为含氧酸和无氧酸 1.含氧酸 硫酸H2SO4、硝酸HNO3、碳酸H2CO3、磷酸H3PO4、次氯酸HClO、氯酸HClO3、高氯酸HClO4、亚硫酸H2SO3、硅酸H2SiO3、乙酸CH3COOH 2.无氧酸
牙齿的结构、功能和分类
牙齿的结构与功能 牙齿是指人和动物嘴中具有一定形态的高度钙化的组织,有咀嚼、帮助发音和保持面部外形的功能。牙齿不仅能咀嚼食物、帮助发音,而且对面容的美有很大影响。人们常把牙齿作为衡量健美的重要标志之一。 一、牙齿结构 牙齿(又称“牙”或“齿”),是人体中最坚硬的器官,分为牙冠、牙颈和牙根三部分。又分为牙釉质(珐琅质)、牙本质(象牙质)、牙髓(神经腺)等。 二、牙齿生长 人一生有乳牙(共20个)和恒牙(28~32个)两副牙齿。 乳牙:出生后4~10个月乳牙开始萌出,12个月后未萌出者为乳牙萌出延迟。乳牙萌出顺序一般为下颌先于上颌、自前向后,约于2.5岁时乳牙出齐。乳牙萌出时间个体差异较大,与遗传、内分泌、食物性状有关。 恒牙:6岁左右萌出第一颗恒牙(第一恒磨牙,在第二乳磨牙之后,又称6龄齿);6~12岁阶段乳牙逐个被同位恒牙替换,其中第1、2前磨牙代替第1、2乳磨牙,此期为混合牙列期;12岁萌出第二恒磨牙;约在18岁以后萌出第三恒磨牙(智齿),也有终生第三恒磨牙不萌出者。 三、牙齿的分类和功能 如果按牙齿的生长时间分类可分为乳牙和恒牙,如果按形态及功能分
类,牙齿又分为四类。 切牙:位于口腔前部,共8个,其主要功能为切割食物。 尖牙:位于口角处,共4个,牙冠粗壮,牙根长而粗,主要功能是为穿刺和撕裂食物。 前磨牙:又称双尖牙,位于尖牙之后,磨牙之前,共8个。其主要功能是为了协助尖牙撕裂及协助磨牙捣碎食物的作用。 磨牙:位于前磨牙之后,共12个,结构复杂,作用是磨碎食物。切牙和尖牙位于口腔前庭前部,口角之前,合称为前牙;前磨牙和磨牙位于口角之后,合称后牙。 由于牙齿和牙槽骨的支持,牙弓形态和咬合关系的正常,才会使人的面部和唇颊部显得丰满。而当人们讲话和微笑时,整齐而洁白的牙齿,更能显现人的健康和美丽。相反,如果牙弓发育不正常,牙齿排列紊乱,参差不齐,面容就会显得不协调。如果牙齿缺失太多,唇颊部失去支持而凹陷,就会使人的面容显得苍老、消瘦。
智能包装的分类及原理
智能包装包括:功能材料型智能包装、功能结构型智能包装及信息型智能包装。它具体体现为:利用新型的包装材料、结构与形式对商品的质量和流通安全性进行积极干预与保障;利用信息收集、管理、控制与处理技术完成对运输包装系统的优化管理等。 (一)功能材料型智能包装技术 功能材料型智能包装是指通过应用新型智能包装材料,改善和增加包装的功能,以达到和完成特定包装的目的。 例: 美国国际造纸公司采用以色列能量纸公(PowerPaper)开发出来的一种超薄柔软电池, 用于一些消费产品的包装, 这种新型电池可像油墨一样被“印刷”在产品的包装上,使之增加灯光、声音, 以及其他一些特殊效果, 可让制造商更有效地通过产品包装来吸引消费者。 (二)功能结构型智能包装技术 功能结构型智能包装是指通过增加或改进部分包装结构,而使包装具有某些特殊功能和智能型特点。功能结构的改进往往从包装的安全性、可靠性和部分自动功能入手进行,这种结构上的变化使包装的商品使用更加
安全和方便简洁。 例: 这种功能结构型智能包装最有代表性的是自动加热和自动冷却包装。这两种包装都是增加了包装的部分结构, 而使包装具有部分自动功能。自动加热型包装是一种多层、无缝的容器, 以注塑成形方法制成, 容器内层分成多个间隔, 容许产品自我加热。它的加热原理是:当使用者拿下容器上的箔, 并按压容器底部时, 容器内的水及石灰石便会产生化学反应, 发放热能,进而令产品加热。自动冷却型包装内置一个冷凝器、一个蒸发格及一包以盐做成的干燥剂, 冷却时由催化作用所产生的蒸气及液体会贮藏于包装的底部。这技术也可应用于普通容器, 它能在几分钟内将容器内物品的温度降低至摄氏17℃。这2 种智能自动型包装适合野外作业人士使用, 例如探险、单车、钓鱼爱好者等。 (三)信息型智能包装技术 信息型智能包装技术主要是指以反映包装内容物及其内在品质和运输、销售过程信息为主的新型技术。这项技术包括两方面 : 其一, 商品在仓储、运输、销售期间, 周围环境对其内在质量影响的信息记录与表现; 其二, 商品生产信息和销售分布信息的记录。记录和
高中化学物质的分类及转化试题经典(1)
高中化学物质的分类及转化试题经典(1) 一、高中化学物质的分类及转化 1.X、Y、Z、W各代表一种物质,若X+Y=Z+W,则X和Y的反应不可能是( ) A.盐和盐的反应B.碱性氧化物和水的反应 C.酸与碱的反应D.酸性氧化物和碱的反应 【答案】B 【解析】 【详解】 A. 盐和盐反应能生成两种新盐,故A正确; B. 碱性氧化物和水的反应生成相应的碱,只生成一种物质,故B错误; C. 酸和碱反应生成盐和水,故C正确; D. 碱和酸性氧化物反应生成盐和水,故D正确; 故选:B. 【点睛】 根据题干提供的信息可以看出此反应为两种物质反应生成两种物质的反应,可以从具体的反应进行完成. 2.在给定条件下,下列选项所示的物质间转化均能实现的是() A.Fe(s) Fe2O3FeCl3(aq) B.CuO Cu(NO3)2(aq) Cu(NO3)2(s) C.SiO2(s) H2SiO3(s) Na2SiO3(aq) D.N2(g) NH3(g) NO(g) 【答案】D 【解析】 【分析】 【详解】 A.铁与水蒸汽反应生成四氧化三铁,故A不选; B.Cu(NO3)2(aq)加热要水解,产生氢氧化铜和硝酸,硝酸易挥发,水解平衡右移,得不到Cu(NO3)2(s),故B不选; C.二氧化硅不溶于水也不与水反应,故C不选; D.氮气与氢气合成氨气,氨气催化氧化生成NO,故D选; 故选D。 【点睛】 本题综合考查元素化合物知识,侧重于元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,易错点C,二氧化硅不溶于水也不与水反应。 3.下列各项操作中不发生先沉淀后溶解现象的是()
①向饱和碳酸钠溶液中通入过量CO 2②向Fe(OH)3胶体中逐滴滴入过量的H 2SO 4 ③向Ba(NO 3)2溶液中通入过量SO 2④向石灰水中通入过量CO 2 ⑤向硅酸钠溶液中滴入过量的盐酸. A .①②③ B .①②⑤ C .①②③⑤ D .①③⑤ 【答案】D 【解析】 【分析】 【详解】 ①中发生的反应是Na 2CO 3+CO 2+H 2O=2NaHCO 3,NaHCO 3比Na 2CO 3溶解度小但质量大,且反应中中消耗H 2O ,所以有沉淀析出且不溶解,符合;②向Fe(OH)3胶体中加入H 2SO 4首先发生胶体的聚沉,出现Fe(OH)3沉淀,H 2SO 4过量,Fe(OH)3与H 2SO 4反应而溶解,不符合;③硝酸钡溶液中通入二氧化硫,二氧化硫溶于水生成亚硫酸,酸性溶液中硝酸根离子具有强氧化性,能氧化亚硫酸为硫酸,溶液中生成硫酸钡沉淀,现象是只生成沉淀,③符合;④向澄清石灰水中通入过量的CO 2,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液,反应现象是先沉淀后溶解,不符合;⑤向硅酸钠溶液中滴入过量的盐酸,发生反应Na 2SiO 3+2HCl=H 2SiO 3↓+2NaCl ,只生成白色沉淀,符合;答案选D 。 【点睛】 本题考查常见物质的的化学反应与现象。向溶液中加入某物质,先出现沉淀后沉淀溶解的总结如下: (1)向澄清石灰水中通入CO 2(SO 2)至过量。 (2)向Fe(OH)3胶体中加入硫酸至过量 (3)向可溶性铝盐中加入NaOH 溶液至过量 (4)向偏铝酸盐中加入盐酸至过量 4.下列说法正确的是( ) A .升高温度能提高活化分子的比例,从而加快反应速率 B .胶体和溶液的本质区别是有无丁达尔效应 C .将3FeCl 饱和溶液滴入NaOH 溶液中,可获得3Fe(OH)胶体 D .2CO 与2SiO 都属于酸性氧化物,都能与水反应生成相应的酸 【答案】A 【解析】 【分析】 【详解】 A .升高温度单位体积内活化分子总数增大,活化分子百分含量增大,发生有效碰撞的几率增大,反应速率加快,故A 正确; B .胶体和溶液的本质区别是分散质粒子的直径大小不同,胶体能产生丁达尔效应,溶液不能,可用丁达尔效应区分二者,但丁达尔效应不是本质区别,故B 错误; C .将3FeCl 饱和溶液滴入NaOH 溶液中,获得3Fe(OH)沉淀,制备3Fe(OH)胶体应将饱和
纱线的分类与结构特征
第七章纱线的分类与结构特征 教学目标: 1、使学生了解纱线的定义及多种分类。 2、使学生掌握各类纱线的结构特征。 3、使学生了解各类纱线的常规用途。 教学重点与难点: 1、教学重点:纱线的分类和结构 2、教学难点:各类纱线的宏观和微观结构 教学与学习建议: 1、教学建议 授课形式:讲解与讨论,实验 准备不同类别的纱线的实物样品和显微镜标样,让学生从宏观和微观两方面观察认识各种纱线的基本结构; 充分做好实验准备。 2、学习建议 通过观察各种纱线的实物样品和显微镜标样,从宏观和微观两方面认识纱线的结构; 通过记忆和理解,掌握纱线的主要特性及常规用途。
第七章纱线的分类与结构特征 第一节纱线的分类 所谓纱,亦称单纱,由短纤维经纺纱加工,使短纤维沿轴向排列并经加捻而成。 所谓丝,俗称长丝纱。 复丝加捻可形成捻丝;捻丝再经一次或多次并合、加捻成为复合捻丝。 所谓线是由两根或两根以上的单纱合并加捻制成的股线;股线再合并加捻为复捻股线。由芯纱、饰线和固纱加捻组合而成,具有各种不同的特殊结构性能和外观的线,称花饰线,如图7-2。 图7-1各种纱线结构的理想图形 a疙瘩线, b螺旋线, c竹节纱, d毛圈线, e结子花线, f雪尼尔花线, g菱形金属丝包芯线。 图7-2花饰纱线示意图 一、按纤维原料分类 (一)按组成纱线的纤维种类分 1、纯纺纱线 用一种纤维纺成的纱线。如纯棉纱线、毛纱线、粘胶纤维纱线、腈纶纱线、涤纶纱线、锦纶纱线等等。 2、混纺纱线
混纺或交捻纱线是由两种或两种以上纤维组成的纱线,如涤/棉混纺纱、毛/涤混纺纱、毛/腈混纺纱、涤/粘/腈混纺纱、真丝/棉纱交捻纱等等。有两种以上短纤维混合纺成的短纤维纱,称为混纺纱; 而由两种以上长丝纱组合(如加捻)成的纱,叫混纤纱。 (二)按组成纱线的纤维长度分 1、棉型纱线用原棉或棉型纤维在棉纺设备上加工而成。 2、毛型纱线用羊毛或毛型纤维在毛纺设备上加工而成。 3、中长纤维纱线用长度、细度介于毛、棉之间的纤维在专用设备上加工而成,具有一定毛 型感的纱线。 二、按结构或形成方法分类 (一)按结构和外形分 1、长丝纱 (1)单丝纱指长度很长的单根连续纤维。 (2)复丝纱指两根或两根以上的单丝合并一起的丝束。 (3)捻丝复丝加捻即成捻丝。 (4)复合捻丝捻丝再经一次或多次合并、加捻即成。 (5)变形丝化纤原丝经过变形加工使之具有卷曲、螺旋、环圈等外观特征而呈现蓬松性、伸缩性的长丝纱。 2、短纤纱 (1)单纱由短纤维集束成条,依靠加捻而成。 (2)股线两根或两根以上单纱合并加捻而成。 (3)复捻股线由两根或多根股线合并加捻而成。 (4)花式捻线由芯线、饰线和包线捻合而成。 (5)花式线主要有膨体纱和包芯纱。 3、复合纱 利用两种以上不同性状的单纱或长丝束加工成的一根纱线。具有复合效应及特殊的外观(1)包芯纱(core yarn) 以长丝或短纤维纱为纱芯,外包其他纤维一起加捻而纺成的纱。 如:涤棉包芯纱:以涤纶复丝为纱芯,外包棉纤维加捻纺制而成,可用来织制烂花的确良,供窗帘、台布等使用; 氨棉包芯纱:以氨纶长丝为纱芯,外包棉纤维加捻纺制而成,可用来织制弹力牛仔衣裤等。 (2)膨体纱(bulk yarn) 利用腈纶的热收缩制成的具有高度膨松性的纱。 由高收缩性和低收缩性的两种腈纶纤维按一定比例(前者占40%~45%,后者占55%~60%)混纺成纱,经松弛热定型处理后,高收缩纤维收缩形成纱芯,低收缩纤维收缩被挤压在表面形成圈形,从而制成膨松、柔软、保暖性好、具有一定毛型感的膨体纱。 (二)按纺纱工艺、纺纱方法分 1、按纺纱工艺分
包装材料分类及应用详细版
包材种类及应用围 一.纸板类 1.纸板构成 由面纸,坑纹,苾纸,底纸组成,通常为了产品运输而作的包装,譬如外箱,平卡,刀卡等。 2. 常用的面纸和底纸 K纸,基重200g,美国进口的有240g,甚至是300g A纸,基重160g B纸,基重120g W纸(白色),基重125g 3. 常用的苾(bie)纸 125g普通苾,125g进口苾,150g进口苾,150g普通苾,175g普通苾,175g进口苾 4. 常用的坑纹 A楞4MM B楞3MM C楞3.5MM E楞1.8MM 最常见的双坑组合方式是BC楞,像AB楞这种组合方式在订纸板时有数量要求,数量不够是订不到AB楞的纸板.一些电子行业,在做单坑啤盒时,喜欢规定用E楞. 5.纸板的厚度
单坑3±1MM 常用表达方式:K3K,K3A,A3A……… 双坑6±1MM 常用表达方式:K=K,K=A,A=B 三坑9±1MM 常用表达方式:K三K,K#K都可以 例如:k=k 表示面纸和里纸是K级的纸质,双坑BC楞纸板。 A=B 指外层面纸是A纸,里层面纸是B,双坑BC楞纸板。最常用的是B=B,,A=A只有特殊要求才用,K=K 适用的条件要求就更苛刻了。一般我们都是以破裂强度来要求厂商。 备注:611+T 为双坑材质纸板,厚度为6MM,表纸为6纸(6纸要比A纸差一点),底纸为T纸(T纸比B纸要差点).这种纸质常用来代替 A=B。 Y11+Y也是同理,只不过,它是用来代替K=K的。K2L,Y+1+Y为单坑材质纸板,厚度3MM,分别用来代替K3A和K3K。 二、彩盒类 1.彩盒分类 卡纸类:一般为250g、300g、350g、400g、450g 坑纸类:一般为e、f楞的最多,外面的彩纸为250g粉灰,下面为坑板(瓦楞纸板) 精品包装盒类:一般使用灰板生产,克重一般为600g(1mm)以上的灰板包面纸成型,面纸一般为双铜纸128g、157g覆膜,灰板根据客户需求不同克重也不一样,一般使用的是950g、1200g、1500g 地进行包装,还可以通过对裱,做成多克重的纸板,如600g双灰板对裱成1200g双灰板,
复合膜的种类,复合膜种类的不同结构
复合膜的种类、不同结构。 复合膜的种类繁多,新材料层出不穷,从不同角度或侧重某一方面可以有许多种不同的包装分类办法.如阻隔性包装、耐热性包装、选择渗透性包装、保鲜性包装、导电性包装、分解性包装等。按照功能可将药用包装复合膜分为以下5种。 1.普通复合膜 (1)典型结构PET/DL/AL/DL/PE或PET/AD/PE/AL/DL/PE(注:DL为于式复合缩写, AD为胶钻剂)。 (2)生产工艺干法复合法或先挤后干复合法。 (3)产品特点良好的印刷适应性,有利于提高产品的档次;良好的气体、水分阻隔性。 2.药用条状易撕包装材料 (1)典型结构PT/AD/PE/Al/AD/PE. (2)生产工艺挤出复合。 (3)产品特点具有良好的易撕性,方便消费者取用产品;良好的气体、水分阻隔性,保证内容物较长的保质期;良好的降解性.有利于环保;适用于泡腾剂、涂料、胶囊等药品包装。 3.纸铝塑复合膜 (1)典型结构纸/PE/AL/AD/PE. (2)生产工艺挤出复合。 (3)产品特点良好的印刷性,有利于提高产品的档次;具有较好的挺度,保证了产品良好的成型性;对气体或水分具有良好的阻隔性,可以保证内容物较长的保质期;良好的降解性,有利于环保。 4.高温蒸煮膜 (1)典型结构透明结构BOPA/CPP或PET/CPP;不透明结构PET/AL/CPP或PET/AL/ NY/CPP0 (2)生产工艺干法复合。 (3)产品特点基本能杀死包装内所有细菌;可常温放置,无需冷藏;有良好的水分、气体阻隔性,耐高温蒸煮;高温蒸煮膜可以里印,具有良好的印刷性能。 5.多层共挤复合膜 (1)典型结构外层/阻隔层/内层。 (2)特点外层一般为有较好机械强度和印刷性能的材料,如PET,PP等;阻隔层具有较好的对气体、水蒸气等阻隔性,如EVOH,PA,PVDC,PET等通过阻隔层来防止水分、气体的进入,阻止药品有效成分流失和药品的分解;内层具有耐药性好、耐化学性高、热封性能较好的特点,如聚烯烃类。多层共挤膜具有优异的阻隔性能及良好的防伪性能,同时结构多样,便于控制成本。 6.复合成型材料 (1)典型结构NY/AL/PVC, NY/AL/PP (2)特点解决了药品避光与吸潮分解的难题;可以有效地避免气体、香料和其他物质对药品成分的破坏,保证药品的更长的使用期限内品质不发生任何改变;适用于丸剂、片剂、粉剂、栓剂、胶囊及外敷等药品的包装,且易于开启;适用于任何气候地区的药品包装,如PVC具有更高的阻隔性,能对药品进行全方位的保护。
高中化学物质的分类汇总
高中化学物质的分类汇总 高中化学物质的分类知识点总结 1、物质的组成、性质和分类: (一)掌握基本概念 1. 分子 分子是能够独立存在并保持物质化学性质的一种微粒。 (1)分子同原子、离子一样是构成物质的基本微粒。 (2)按组成分子的原子个数可分为: 单原子分子:Ne 、C、 He 、Kr…… 双原子分子:H2 、O2、HCl、No…… 多原子分子:H2O、P4 、C6H12O6…… 2. 原子 原子是化学变化中的最小微粒,确切的说,化学反应中原子核不变,只有核外电子发生变化。 (1)原子是组成某些物质(如金刚石、晶体硅、二氧化硅等原子晶体)和分子的基本微粒。 (2)原子是由原子核(中子、质子)和核外电子组成的。 3. 离子 离子是指带电荷的原子或原子团。 (1)离子可分为阳离子和阴离子 阳离子:Li+、Na+、H+、NH4+…… 阴离子:Cl-、O2-、OH-、SO4-…… (2)存在离子的物质: ①离子化合物中:NaCl、CaCl2、CaSo4…… ②电解质溶液中:盐酸、氯化钠溶液中…… ③金属晶体中:钠、铁、钾、铜…… 4. 元素 元素是具有相同核电荷数的(即质子数)的同一类原子的总称。 (1)元素与物质、分子、原子的区别与联系;物质是由元素组成的(宏观看);物质是由原子、分子、或离子构成的(微观看)。 (2)某些元素可以形成不同的单质(性质、结构不同)同素异形体。(3)各元素在地壳中质量分数各不相同,占前五位的是:O、Si、Al、
Fe、Ga。 5. 同位素 同位素指同一元素不同核素之间互称同位素,即具有相同质子数不同中子数的同一类原子互称为同位素。如氢(H)有三种同位素:11H、 21H、31H(氕、氘、氚)。 6. 核素 核素是具有特定质量数、原子序数和核能态,而且其寿命足以被观察的一类原子。 (1)同种元素,可以有若干种不同的核素—同位素。 (2)同一种元素的各种核素尽管中子数不同,但他们质子数与电子数相同。核外电子排布相同,因而他们的化学性质几乎相同。 7. 原子团 原子团是指多个原子结合成的集体,在许多反应中,原子团作为一个集体参加反应。原子团有以下几种类型:根(如SO42-、OH-、CH3COO-等)、官能团(有机物分子中能反应物质特殊性质的原子团,如-OH、 -NO2、-COOH等)、游离基(又称自由基、具有不成价电子的原子团,如甲基游离基·CH3)。 8. 基 化合物中具有特殊性质的一部分原子或原子团,或化合物分子中去掉某些原子或原子团后剩下的原子团。 (1)有机物的官能团是决定物质主要性质的基,如醇的羟基(-OH)和羧酸的羧基(-COOH)。 (2)甲烷(CH4)分子中去掉一个氢原子后剩余部分(·CH3)含有未成对的价电子,称为甲基或甲基游离基,也包括单原子的游离基(·Cl)。 基(羟基):电中性,不能独立存在,只能和其他基或原子团相结合。根(氢氧根):带负电,能独立存在于溶液或离子化合物中。 9. 物理性质和化学性质 物理性质 (1)概念:(宏观)物质不需要发生化学变化就能表现出的性质。(2)实质:(微观)物质的分子组成和结构没有发生变化时所呈现的性质。 (3)物理性质一般包括:颜色、状态、气味、味道、密度、熔点、沸点、溶解性、导电性、导热性、延展性等。 化学性质
纱线及织物(二)
纱线及织物(二) 第二节织物 一、织物的分类及结构 (一)织物的分类 1.按织物原料分类 (1)纯纺织物 (2)混纺织物 (3)交织织物 2.按织物组织分类 (1)原组织织物:原组织织物又称基本组织织物,它包括平纹织物、斜纹织物和缎纹织物。 (2)小花纹织物:小花纹织物是把原组织织物加以变化或配合而成,可分为变化组织织物和联合组织织物。 (3)复杂组织织物:复杂组织织物是由若干系统的经纱和若干系统的纬纱构成,这类组织使织物具有特殊的外观效应。 (4)大提花组织:大提花组织织物为单根经纱受控起花,花纹范围较大的织物。 3.按织物用途分类 (1)服装用织物 (2)装饰用织物 (3)产业用织物 (二)织物的结构 相互垂直排列的两个系统的纱线,在织机上按一定规律交织而成的制品,称为机织物,简称织物。平行于布边方向的纱线称为经纱;与布边垂直横向排列的纱线为纬纱。织物结构是指经、纬纱线在织物中的几何形态,经纬纱线的原料、粗细、密度配置和相互交错沉浮等情况都是影响织物结构的重要参数。 二、织物的基本性能 (一)拉伸断裂性能 主要包括断裂强度、断裂伸长率等。断裂强度是指拉断一定尺寸织物试样所需要的负荷,以牛顿表示;断裂伸长率是指试样被拉断时的长度与原试样长度差占原试样长度的百分率。 (二)撕裂性能 撕裂性能用撕裂强度表示,它是指一定尺寸织物试样按规定方法而撕破成一定长度裂缝所需要的最大负荷,以牛顿为表示单位。它主要是针对一些特殊织物需要而设立的测试项目,如军服、篷布、降落伞、帆布等。 (三)耐磨性能 用耐磨强度表示,是指织物抵抗摩擦坏损的能力。测试时,可以用标准磨料摩擦织物试样直至出现指定特征(如纱线断裂两根或出现破洞)所需的次数表示,也可以用试样承受一定摩擦次数后某些性质变化率(如试验前后强度变化率、重量变化率等)来表示。 (四)刚柔性
短语的功能类和结构类
短语的功能主要指短语作为一个整体在句子中充当句法成分的功能。 根据语法功能,可以将短语分为体词性短语、谓词性短语和附加性短语三类。 (一)体词性短语 (二)谓词性短语 (三)附加性短语 一)体词性短语 体词性短语是语法功能相当于体词、主要作主语或宾语的短语。 体词性短语包括: 定中短语 体词性联合短语 同位短语 “所”字短语 “的”字短语 量词短语 方位短语 (二)谓词性短语 谓词性短语是语法功能相当于谓词、主要作谓语的短语。 谓词性短语包括: 主谓短语 述宾短语 述补短语 谓词性联合短语 状中短语 连谓短语 兼语短语 (三)附加性短语 附加性短语是语法功能独特的一类短语,包括介词短语和比况短语。 附加性短语主要作状语修饰谓词性词语,一般不能单说或单用,不能作主语、谓语和宾语。 1、介词短语 介词短语的主要语法功能是作状语修饰谓词性词语。 公司应该按照市场行情及时进行价格调整。 一道闪电把整个窗户都照亮了。 他们沿着河边,慢慢向上游新桥那里走。 大家都为这件事感到高兴。 介词短语还可以作定语、补语等成分。 在病中他想的最多的还是对家乡、对祖国、对人民的感情。(定语) 对问题的认识,还不深刻。(定语) 雪粉钻到衣领里,和汗水搅成一起。(补语)
我对生活的看法并不太拘泥于形式。(补语) 2、比况短语 比况短语的主要语法功能是作状语。 长睫毛下的两只大眼睛,会说话似的扑闪着。 他吓得杀猪般嚎叫起来。 那只警犬箭似的冲出门外。 他触电一样哆嗦了一下。 比况短语还可以作定语、补语等成分。 他的眉头皱了两皱,拉开轰雷似的喉咙直吼。(定语) 又是一阵暴风雨般的呼喊。(定语) 他的腿冻出了冻疮,痛得钻心一般。(补语) 他急得热锅上的蚂蚁似的。(补语) 比况短语一般要在动词省略的情况下才能作谓语。 油绿色的果珠儿翡翠似的。(谓语) 短语结构类型有以下几类:并列短语、偏正短语、动宾短语、后补短语、主谓短语、方位短语、介宾短语、的字短语、复指短语、固定短语。 1.并列短语:词与词之间有并列关系。 2.偏正短语:前面的词修饰、限制后面的名词、动词或形容词。 3.动宾短语:前面的动词支配或关涉后面的词。 4.后补短语:后面的词补充说明前面的动词或形容词。 5.主谓短语:后面的词陈述前面的词,前后有被陈述和陈述关系。 6.方位短语:名词或动词后面带上方位名词。 7.介宾短语:有介词和名词或代词等结合构成。 8.的字短语:由名词、动词、形容词或代词等带上结构助词“的”构成。 9.复指短语:两个或几个词同指一个对象。 10.固定短语:结构固定的专名或成语。
初中化学常见物质的分类
一、初中化学常见物质的分类 1、单质:非惰性气体一般由两个原子组成: F2,O2,H2,Cl2 2、惰性气体:一般由一个原子组成:He,Ne,Ar,Kr,Xe 3、化合物:氢化物居多:H2S,HCl,H3P,HF,HBr,HI 二、初中化学常见物质的颜色 (一)、固体的颜色 1、红色固体:铜,氧化铁 2、绿色固体:碱式碳酸铜 3、蓝色固体:氢氧化铜,硫酸铜晶体 4、紫黑色固体:高锰酸钾 5、淡黄色固体:硫磺 6、无色固体:冰,干冰,金刚石 7、银白色固体:银,铁,镁,铝,汞等金属 8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭) 9、红褐色固体:氢氧化铁 10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜, 五氧化二磷,氧化镁 (二)、液体的颜色 11、无色液体:水,双氧水 12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液 13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液 14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液 15、紫红色溶液:高锰酸钾溶液 16、紫色溶液:石蕊溶液 (三)、气体的颜色 17、红棕色气体:二氧化氮 18、黄绿色气体:氯气 19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢等气体。 三、初中化学敞口置于空气中质量改变的 (一)质量增加的 1、由于吸水而增加的:氢氧化钠固体,氯化钙,氯化镁,浓硫酸; 2、由于跟水反应而增加的:氧化钙、氧化钡、氧化钾、氧化钠,硫酸铜; 3、由于跟二氧化碳反应而增加的:氢氧化钠,氢氧化钾,氢氧化钡,氢氧化钙;(二)质量减少的 1、由于挥发而减少的:浓盐酸,浓硝酸,酒精,汽油,浓氨水; 2、由于风化而减少的:碳酸钠晶体。 四、初中化学物质的检验 (一)、气体的检验 1、氧气:带火星的木条放入瓶中,若木条复燃,则是氧气.
牙齿的结构、功能和分类
个人收集整理-ZQ 牙齿是指人和动物嘴中具有一定形态地高度钙化地组织,有咀嚼、帮助发音和保持面部外形地功能.牙齿不仅能咀嚼食物、帮助发音,而且对面容地美有很大影响.人们常把牙齿作为衡量健美地重要标志之一. 一、牙齿结构 牙齿(又称“牙”或“齿”),是人体中最坚硬地器官,分为牙冠、牙颈和牙根三部分.又分为牙釉质(珐琅质)、牙本质(象牙质)、牙髓(神经腺)等.资料个人收集整理,勿做商业用途 二、牙齿生长 人一生有乳牙(共个)和恒牙(~个)两副牙齿. 乳牙:出生后~个月乳牙开始萌出,个月后未萌出者为乳牙萌出延迟.乳牙萌出顺序一般为下颌先于上颌、自前向后,约于岁时乳牙出齐.乳牙萌出时间个体差异较大,与遗传、内分泌、食物性状有关.资料个人收集整理,勿做商业用途 恒牙:岁左右萌出第一颗恒牙(第一恒磨牙,在第二乳磨牙之后,又称龄齿)~岁阶段乳牙逐个被同位恒牙替换,其中第、前磨牙代替第、乳磨牙,此期为混合牙列期岁萌出第二恒磨牙;约在岁以后萌出第三恒磨牙(智齿),也有终生第三恒磨牙不萌出者.资料个人收集整理,勿做商业用途 三、牙齿地分类和功能 如果按牙齿地生长时间分类可分为乳牙和恒牙,如果按形态及功能分类,牙齿又分为四类.切牙:位于口腔前部,共个,其主要功能为切割食物. 尖牙:位于口角处,共个,牙冠粗壮,牙根长而粗,主要功能是为穿刺和撕裂食物. 前磨牙:又称双尖牙,位于尖牙之后,磨牙之前,共个.其主要功能是为了协助尖牙撕裂及协助磨牙捣碎食物地作用.资料个人收集整理,勿做商业用途 磨牙:位于前磨牙之后,共个,结构复杂,作用是磨碎食物.切牙和尖牙位于口腔前庭前部,口角之前,合称为前牙;前磨牙和磨牙位于口角之后,合称后牙.资料个人收集整理,勿做商业用途 由于牙齿和牙槽骨地支持,牙弓形态和咬合关系地正常,才会使人地面部和唇颊部显得丰满.而当人们讲话和微笑时,整齐而洁白地牙齿,更能显现人地健康和美丽.相反,如果牙弓发育不正常,牙齿排列紊乱,参差不齐,面容就会显得不协调.如果牙齿缺失太多,唇颊部失去支持而凹陷,就会使人地面容显得苍老、消瘦.资料个人收集整理,勿做商业用途 1 / 1
道路工程的组成和分类
道路工程的组成与分类 ㈠道路的组成 按所在位置、交通性质及其使用特点,可分为:公路、城市道路、厂矿道路、林区道路及乡村道路等。 1.公路的组成 ⑴线形组成。公路线形是指公路中线的空间几何形状和尺寸。 ⑵结构组成。公路的结构是承受荷载和自然因素影响的结构物,它包括路基、路面、桥涵、隧道、排水系统、防护工程、特殊构造物及交通服务设施等。 2.城市道路的组成 道路工程的主体是路线、路基(包括排水系统及防护工程等)和路面三大部分。 ㈡道路的等级划分 1.公路的等级划分。根据使用任务、功能和适应的交通量分为高速公路、一、二、三、四级5个等级。
⑴高速公路。高速公路是具有4个或4个以上车道,设有中央分隔带,全部立体交叉,全部控制出入,专供汽车分向、分车道高速行驶的公路。 ⑵一级公路。一级公路与高速公路设施基本相同。一级公路只是部分控制出入. ⑶二级公路。二级公路是中等以上城市的干线公路。 ⑷三级公路。三级公路是沟通县、城镇之间的集散公路。 ⑸四级公路。四级公路是沟通乡、村等地的地方公路。 2.城市道路的等级划分 按城市道路系统的地位、交通功能和对沿线建筑物的服务功能分为四类。 ⑴快速路。快速路主要为城市长距离交通服务。 ⑵主干路。主干路是城市道路网的骨架。 ⑶次干路。次干路配合主干路组成城市道路网,它是城市交通干路。
⑷支路。支路是一个地区(如居住区)内的道路,以服务功能为主。 二、路基 路基是按照路线位置和一定技术要求修筑的作为路面基础的带状构造物。 ㈠路基基本构造。是指路基填挖高度、路基宽度、路肩宽度、路基边坡等。 ㈡路基的作用 是路面的基础,是路面的支撑结构物。高于原地面的填方路基称为路堤,低于原地面的挖方路基称为路堑。路面底面以下80cm范围内的路基部分称为路床。 ㈢路基的基本要求 1.路基结构物的整体必须具有足够的稳定性 2.路基必须具有足够的强度、刚度和水温稳定性 水温稳定性是指强度和刚度在自然因素的影响下的变化幅度。 ㈣路基形式
包装材料的分类
马高塑胶电子有限公司 Marco Manufacturing Limited 包装材料的分类—工程部培训资料 一, 印刷纸张 1, 铜版纸 特性:表面光滑,白度较高,纸质纤维分布均匀,厚薄一致,伸缩性小,有较好弹和较强的抗水性能和抗张性能,对油墨的吸收性与接受状态十分良好。铜版纸有单、双面两类;主要用途:主要用于印刷画册、封面、明信片、精美的产品样本以及彩色商标等; 克重:常见有80、105、128、157、200、250、300、350(g/m2)。 2, 亚粉纸 特性:与铜版纸所不同的是该纸表面哑光,纸质纤维分布均匀,厚薄性好,密度高,弹性较好且具有较强的抗水性能和抗张性能,对油墨的吸收性与接收状态略低于铜版纸,但厚度较铜版纸略高; 主要用途:主要用于印刷画册、卡片、明信片、精美的产品样本等; 克重:常见有80、105、128、157、200、250、300、350(g/m2)。 3, 白卡纸 特性:是一种较厚实坚挺的白色卡纸。分黄芯和白芯两种; 主要用途:主要用于印刷名片、明信片、请柬、证书及包装装潢用的印刷品; 克重:250、300、350、400(g/m2)。 4, 白板纸 特性:内芯为灰色,纸质厚实,坚挺。分灰底白和白底白两种; 主要用途:主要用于各种包装装潢用的印刷品; 克重:250,300,350,400 (g/m2)。 5, 双胶纸 特性:适用广泛,质量稳定; 主要用途:主要用于各种说明书,信封,信签等; 克重:60,70,80,90,100,120(g/m2)。 6, 书写纸 特性:书写纸是供墨水书写用的纸张,纸张要求写时不洇; 主要用途:主要用于印刷练习本、日记本、表格和帐薄等; 克重:45,50,60,70,80 (g/m2)。 7, 牛皮纸 特性:具有很高的拉力,有单光、双光、条纹、无纹等。分白牛皮和黄牛皮两种; 主要用途:主要用于包装纸、信封、纸袋等; 克重:60,70,80,100,120 (g/m2)。 8, 艺术纸 特性:种类繁多; 主要用途:主要应用于精美的书籍封面、画册、宣传册、请柬、贺卡、高档办公用纸、
高中化学 物质的分类知识点总结
高中化学常见物质的分类 一、单质 按元素组成分为 1. 金属单质 K 钾、Ca 钙、Na 纳、Mg 镁、Al 铝、Zn 锌、Fe 铁、Sn 锡、Pb 铅、Cu 铜、Hg 汞、Ag 银、Pt 铂、Au 金 2. 非金属单质 氢气H 2、碳C 、氮气N 2、氧气O 2、臭氧O 3、氟气F 2、硅Si 、磷P 、硫S 、氯气Cl 2、液溴Br 2、碘I 2、氦气He 、氖气Ne 、氩气Ar 、 二、化合物 1. 有机化合物: 乙醇、甲烷、乙烷、乙烯、葡萄糖等 2. 无机化合物 三、氧化物 (1)按元素组成分为金属氧化物和非金属氧化物 1. 金属氧化物 氧化钠Na 2O 、过氧化钠Na 2O 2、氧化钙CaO 、氧化镁MgO 、氧化铝Al 2O 3、氧化锌ZnO 、氧化铁Fe 2O 3、氧化亚铁FeO 、四氧化三铁Fe 3O 4、氧化铜CuO 、氧化汞HgO 、七氧化二锰Mn 2O 7 2. 非金属氧化物 水H 2O ,过氧化氢H 2O 2、一氧化碳CO 、二氧化碳CO 2、一氧化氮NO 、五氧化二氮N 2O 5、二氧化硅SiO 2、五氧化二磷P 2O 5、二氧化硫SO 2、三氧化硫SO 3 (2)按照性质分为 碱性氧化物、酸性氧化物、不成盐氧化物、两性氧化物、过氧化物 1. 碱性氧化物 大部分的金属氧化物为碱性氧化物,但有特例:过氧化钠Na 2O 2为过氧化物、 氧化铝Al 2O 3为两性氧化物、七氧化二锰Mn 2O 7为酸性氧化物、四氧化三铁Fe 3O 4、 碱性氧化物有:氧化钠Na 2O 、氧化钙CaO 、氧化镁MgO 、氧化锌ZnO 、氧化铁Fe 2O 3、氧化亚铁FeO 、氧化铜CuO 、氧化汞HgO 、 碱性氧化物一定为金属氧化物,金属氧化物不一定为碱性氧化物 2. 酸性氧化物 大部分的非金属氧化物为,但有特例:水H 2O ,一氧化碳CO 、一氧化氮NO 不是酸性氧化物,七氧化二锰Mn 2O 7虽然为金属氧化物但属于酸性氧化物、 非金属氧化物不一定为酸性氧化物 3. 不成盐氧化物:——既不与酸反应也不与碱反应!如:一氧化碳CO 、一氧化氮NO ! 4. 两性氧化物:氧化铝Al 2O 3 5. 过氧化物:过氧化氢H 2O 2、过氧化钠Na 2O 2 四、酸 中学常见的酸:
