人IL-8试剂盒说明书
幽门螺杆菌感染后儿童与成人胃黏膜免疫状态差异

幽门螺杆菌感染后儿童与成人胃黏膜免疫状态差异目的探讨幽门螺杆菌(Hp)感染后儿童与成人胃黏膜免疫状态差异情况。
方法选取2009年1月~2012年2月因上腹部症状就诊于西安市儿童医院(以下简称“我院”)的120例儿童作为儿童组,同时选取同期我院收治的有上腹部症状的成人患者120例作为成人组,根据Hp检测结果,将儿童组分为Hp阳性组90例和Hp阴性组30例,成人组分为Hp阳性组90例和Hp阴性组30例。
分别检测各组患者胃黏膜组织中的免疫相关指标。
结果成人与儿童Hp阴性组的环氧化酶-2(COX-2)、核因子-κB (NF-κB)、过氧化物酶体增殖物活化受体-γ mRNA (PPAR-γ mRNA)、白介素-8(IL-8)及白介素-2(IL-2)表达比较,差异均无统计学意义(χ2=0.71、0.53,t=0.73、0.85、1.10,均P > 0.05)。
成人Hp阳性组COX-2 、NF-κB、PPAR-γ mRNA、IL-8及IL-2表达均高于Hp阴性组,差异均有统计学意义(χ2=128.00、114.40,t=5.63、17.86、18.82,P 0.05),具有可比性。
根据Hp诊断标准,将儿童组分为Hp阳性90例和Hp阴性30例,成人组分为Hp阳性90例和Hp阴性30例。
1.2 方法1.2.1 Hp感染阳性判定两组研究对象通过胃黏膜姬姆萨染色、13C呼气试验和快速尿素酶试验,三种方法均诊断为阳性患者,判断为Hp感染阳性病例。
1.2.2 COX-2和NF-κB的测定COX-2和NF-κB采用免疫组化分析过氧化酶标记的链霉卵白素法(SP法)染色定性,试剂盒来自上海华研生物科技有限公司。
Western印迹法半定量检测COX-2、NF-κB的表达。
COX-2蛋白表达结果判断[5-6]:以细胞浆染呈黄色至棕褐色为阳性细胞,无着色为阴性。
分别观察腺体和炎症细胞染色强度及阳性细胞比例。
采用定量积分法,每张切片至少观察10个高倍视野,每个视野下计数100个细胞,并根据每张切片阳性细胞比例及着色深浅计分,着色比例:30%以下为1分,30%~60%为2分,60%以上为3分;着色程度:无着色为0分(阴性),浅黄色为1分(弱阳性),棕黄色为2分(阳性),棕褐色为3分(强阳性)。
本试剂仅供研究使用

本试剂仅供研究使用人抗增殖细胞核抗原抗体(PCNA)elisa试剂盒使用说明书试剂盒组成:48孔配置/96孔配置说明书:1份封板膜:2片(48)/2片(96)密封袋:1个目的:【人抗增殖细胞核抗原抗体(PCNA)elisa试剂盒说明书】本试剂盒用于测定人血清,血浆及相关液体样本中介素2(IL-2)的含量。
服务承诺:供货期:款到发货。
工作时间内免费的技术咨询和指导。
请来电咨询为客户提供来样检测服务,最大限度实验结果的有效性(免费代测)。
试剂盒性能:1.样品线性回归与预期浓度相关系数R值为0.95以上。
2.批内与批见应分别小于9%和11%保存条件及有效期:1.试剂盒保存:2-8℃。
2.有效期:6个月检测范围:0.2IU/L - 6IU/L实验原理:【人抗增殖细胞核抗原抗体(PCNA)elisa试剂盒说明书】本试剂盒应用双抗体夹心法测定标本中人抗增殖细胞核抗原抗体(PCNA)水平。
用纯化的人抗增殖细胞核抗原抗体(PCNA)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入介素2(IL-2),再与HRP标记的介素2(IL-2)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的介素2(IL-2)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD 值),通过标准曲线计算样品中人抗增殖细胞核抗原抗体(PCNA)浓度。
样本处理及要求:1. 血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
2. 血浆:应根据标本的要求选择EDTA或柠檬酸钠作为抗凝剂,混合10-20分钟后,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应该再次离心。
3. 尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。
达科为IL-2 ELISA试剂盒说明书

6. 实验操作中请使用一次性的吸头,避免交叉污染。 7. 使用前检查试剂盒内各种试剂;试剂稀释、加样和中止反应
充分混匀或者摇匀对实验结果尤为重要,最好使用低速频 率振荡器或者反应过程中每 15 分钟手工摇匀一次。 8. 实验板孔加入试剂的顺序应一致,以保证所有反应孔的孵育 时间一致。 9. 使用洁净的塑料容器盛装洗涤液。
即用型
即用型
*:96/48 Tests
4、 需要实验者自行准备的试剂与仪器:
1. 酶标仪(建议参考仪器使用说明提前预热) 2. 微量加液器及吸头:P10,P50,P100,P200,P1000 3. 蒸馏水或去离子水 4. 全新滤纸 5. 旋涡振荡器和磁力搅拌器 6. 37℃温箱
-2-
5、 注意事项:
-3-
10. 洗涤过程中反应孔中残留的洗涤液应在滤纸上充分拍干,滤 纸上看不到水印。勿将滤纸直接放入反应孔中吸水。
11. TMB 对光敏感,避免长时间暴露于光下,避免金属接触影 响结果。有毒,避免用手接触!准备使用的 TMB 若变为蓝 色,表明 TMB 已经污染,请丢弃。请在终止反应后 10 分 钟内读取 OD 值。
-8-
8、结果分析:
1. 有两种设定空白对照的方案: 1) 将 TMB 空白显色孔设为对照。所有的标准品和样品的 吸光值减去空白孔的吸光值后,在坐标纸上画出曲线,以吸 光值作为纵坐标,以浓度作为横坐标。 2) 将零孔设为对照。得到的数据可以直接在坐标纸上画出 曲线。
2. 根据样品的吸光值在坐标上找出对应的浓度。用户也可以使 用各种应用软件来计算。若样品 OD 值高于标准曲线上限,应 适当稀释后重测,计算浓度时应乘以稀释倍数。
怎样使用人白介素17(IL-17)
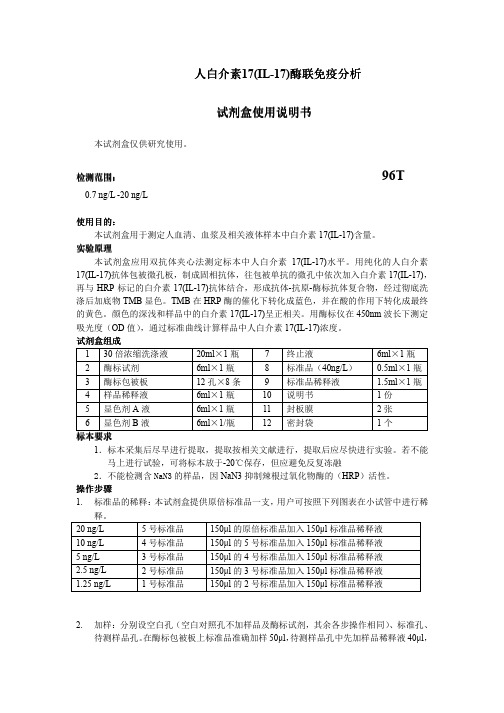
人白介素17(IL-17)酶联免疫酶联免疫分析分析分析试剂试剂盒使用说明书盒使用说明书盒使用说明书本试剂盒仅供研究使用。
检测范围检测范围:: 96T0.7 ng/L -20 ng/L使用目的使用目的::本试剂盒用于测定人血清、血浆及相关液体样本中白介素17(IL-17)含量。
实验原理本试剂盒应用双抗体夹心法测定标本中人白介素17(IL-17)水平。
用纯化的人白介素17(IL-17)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入白介素17(IL-17),再与HRP 标记的白介素17(IL-17)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB 显色。
TMB 在HRP 酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的白介素17(IL-17)呈正相关。
用酶标仪在450nm 波长下测定吸光度(OD 值),通过标准曲线计算样品中人白介素17(IL-17)浓度。
试剂盒组成 1 30倍浓缩洗涤液 20ml ×1瓶 7 终止液6ml ×1瓶 2 酶标试剂 6ml ×1瓶 8 标准品(40ng/L ) 0.5ml ×1瓶 3 酶标包被板 12孔×8条 9 标准品稀释液 1.5ml ×1瓶 4 样品稀释液 6ml ×1瓶 10 说明书 1份 5 显色剂A 液 6ml ×1瓶 11 封板膜 2张 6显色剂B 液6ml ×1/瓶12密封袋1个标本标本要求要求1.标本采集后尽早进行提取,提取按相关文献进行,提取后应尽快进行实验。
若不能马上进行试验,可将标本放于-20℃保存,但应避免反复冻融2.不能检测含NaN3的样品,因NaN3抑制辣根过氧化物酶的(HRP )活性。
操作步骤1. 标准品的稀释:本试剂盒提供原倍标准品一支,用户可按照下列图表在小试管中进行稀释。
20 ng/L 5号标准品 150µl 的原倍标准品加入150µl 标准品稀释液 10 ng/L 4号标准品 150µl 的5号标准品加入150µl 标准品稀释液 5 ng/L 3号标准品 150µl 的4号标准品加入150µl 标准品稀释液 2.5 ng/L 2号标准品 150µl 的3号标准品加入150µl 标准品稀释液 1.25 ng/L1号标准品150µl 的2号标准品加入150µl 标准品稀释液2. 加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、标准孔、待测样品孔。
重建人类表皮模型医疗器械体外皮肤刺激试验中白细胞介素-1α和白细胞介素-8的表达变化

•18•实用临床医药杂志Journal of Clinical Medicine in Practice2022,26(11):18-21,33.重建人类表皮模型医疗器械体外皮肤刺激试验中白细胞介素和白细胞介素的表达变化刘佳,范春光,孙立魁,赵增琳(山东省医疗器械和药品包装检验研究院/国家药品监督管理局材料器械安全性评价重点实验室/山东省医疗器械生物学评价重点实验室,山东济南,250101)摘要:目的探讨以体外皮肤刺激试验作为家兔皮肤刺激的替代试验,检测皮肤刺激性,分析试验模型相关分子标记物。
方法选取2种医疗器械产品,通过重建人类表皮模型(RhE模型)体外皮肤刺激试验检测皮肤刺激性。
收集皮肤组织培养基,采用酶联免疫吸附法(ELISA)测定培养基中白细胞介素(IL)-laJL-8含量。
结果组织病理学显示,使用4%乳酸处理,上皮细胞萎缩,角质层脱落;采用其他方式处理的上皮组织未见明显异常。
氯化钠注射液配制的1%的十二烷基硫酸钠(SDS)极性阳性对照和芝麻油制备1%的SDS非极性阳性对照中,上皮细胞变性坏死。
EUSA结果显示,培养基中IL-la表达与皮肤刺激指数呈正相关,IL£与皮肤刺激指数呈负相关。
结论IL-la可作为RhE模型体外皮肤刺激试验的分子标记物,以分析医疗器械产品的皮肤刺激性。
关键词:重建人类表皮模型;白细胞介素-la;白细胞介素皮肤刺激;医疗器械;分子标记物中图分类号:R197.39;Q81文献标志码:A文章编号:1672-2353(2022)11-018-04D0I:10.7619/jcmp.20214815Expression changes of interleukin-la and interleukin-8in vitro skin stimulation test of medical devicesfor medical devices with reconstructed humanepidermis modelLIU Jia,FAN Chunguang9SUN Likui,ZHAO Zenglin(Shandong Institute of Medical Device and Pharmaceutical Packaging Inspection,NationalMedical Products Administration Key Laboratory far Safety Evaluation of Biomaterials andMedical Devices,Shandong Key Laboratory of Biological Evaluation for Medical Devices,Jinan Shandong,250101)Abstract:Objective To explore the skin irritation test in vitro as a substitute test for rabbit skin irritation to detect skin irritation,and to analyze the molecular markers related to the test model. Methods Two kinds of medical devices were selected,and skin irritation was detected by reconstructing human epidermis(RhE)model in vitro skin stimulation test.Skin tissue substrates were collected,and the contents of interleukin(IL)-la and IL-8in the substrate were determined by enzyme-linked immunosorbent assay(ELISA).Results The histopathology showed that the epithelial cells with4%lactate were atrophied and the cuticle was exfoliated;there was no obvious abnormality in epithelial tissue by other methods.Epithelial cells were degenerate and necrotic in1%sodium dodecyl sulfate(SDS)polar positive control with sodium chloride injection and1%non-polar nonpolar positive control with sesame oil.ELISA results showed that IL-la expression in substrate was positively correlated with skin irritation index,but IL-8was negatively correlated with skin irritation index. Conclusion IL-la can be used as a molecular marker for RhE model skin irritation test in vitro to analyze skin irritation of medical devices.Key words:reconstruction of human epidermis model;interleukin-1a;interleukin-8;skin irritation;medical device;molecular marker收稿日期:2021-12-07基金项目:国家重点研发计划(2016YFC1103205);山东省医疗器械产品质量检验中心内部课题基金资助项目(ZX201801)表面接触医疗器械使用过程中与人体皮肤接触,其材料本身和(或)其可沥滤物可能会导致皮肤产生刺激反应。
联胺对人脐静脉内皮细胞中IL-8表达及NF-κB蛋白活化的影响

、
材 料
M19 新生 牛血 清 、 aD A 聚 合酶 、L 8 L S 9、 Tq N I-E IA
试 剂盒 、 谷氨 酰胺 、 N - 3 克 隆 鼠抗人 抗体 、 1 抗 Fv 单 3
S P法 免疫组 化试剂 盒 、 l o d 、 ML A O i (T)M- V、VL。 g
【 摘要】 目的 探 讨联胺对培养的人脐静脉 内皮细胞表达 I- L8及核 因子一B活化 的影响 。方 法 . c
I- 蛋 白的表达 , 转录聚合 酶链 反应 法检测 I -mRNA的表 达 , L8 逆 L8 细胞 免疫化 学法观 察 NF ̄ -B的活化 。结果
1 mo L 可诱导 I - 0 i ) / L 8在蛋 白及 rR n NA水平表达 , 与对照组差异有显著性意义 ( P<O 0 )且 与联胺呈浓度依赖性 。联胺 ( .5 , 5 “ lL 作用人脐静脉 内皮细胞 3 n mo ) / 0mi 后发现 NFK _B从胞质 向胞核转移 ,0mi 6 n达高峰 , 持续到 10ri。结论 2 n a
导 I- 在 蛋 白及 mRN 水 平 表 达 ,其 机 制 可 能 是 通 过 N -B活 化 实 现 的 。 L8 A FJ c
【 关键词】 白细胞介素蛋 白一 ; 因子一B 联胺 ; 8核 ; 人脐静脉 内皮细胞
研 究发 现 , I - 因序 列 的启 动子 区域有 核 在 L 8基 因子一B的结 合位 点 , x 因此 活 化 的 NF _B可 能 参 与 调控 I - 基 因转 录 。联 胺 可 诱 导 人 脐 静 脉 内皮 细 L8
mi 别收 集细胞 爬 片观察 NF n分 _B的活 化 。 2酶 联 免疫 吸附 法 收集 培 养基 上 清 液后 , . 操
白介素1β,IL-1βELISA试剂盒说明书
白介素1β,IL-1βELISA试剂盒说明书白介素1β,IL-1βELISA试剂盒说明书kit规格:48孔配置/96孔配置标准品稀释液:1.5ml×1瓶酶标试剂:3ml×1瓶(48)/6ml×1瓶(96)【白介素1β,IL-1βELISA试剂盒说明书】本试剂仅供研究使用计算:以标准物的浓度为横坐标,OD值为纵坐标,在坐标纸上绘出标准曲线,根据样品的OD值由标准曲线查出相应的浓度;再乘以稀释倍数;或用标准物的浓度与OD 值计算出标准曲线的直线回归方程式,将样品的OD值代入方程式,计算出样品浓度,再乘以稀释倍数,即为样品的实际浓度。
试剂盒组成:封板膜:2片(48)/2片(96)说明书:1份密封袋:1个标准品:2700ng/L 0.5ml×1瓶0.5ml×1瓶2-8℃保存酶标包被板: 1×48 1×96 2-8℃保存样品稀释液: 3ml×1瓶 6 ml×1瓶2-8℃保存显色剂A液: 3ml×1瓶 6 ml×1瓶2-8℃保存显色剂B液: 3ml×1瓶 6 ml×1瓶2-8℃保存终止液: 3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液:(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存【白介素1β,IL-1βELISA试剂盒说明书】实验原理:本试剂盒应用双抗体夹心法测定标本中人铁蛋白(FE) 水平。
用纯化的人铁蛋白(FE) 抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入铁蛋白(FE) ,再与HRP标记的铁蛋白(FE) 抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的铁蛋白(FE) 呈正相关。
人白细胞介素23(IL-23)说明书
人白细胞介素23(IL-23)酶联免疫分析(ELISA)试剂盒使用说明书本试剂仅供研究使用目的:本试剂盒用于测定人血清,血浆及相关液体样本中白细胞介素23(IL-23)的含量。
实验原理:本试剂盒应用双抗体夹心法测定标本中人白细胞介素23(IL-23)水平。
用纯化的人白细胞介素23(IL-23)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入白细胞介素23(IL-23),再与HRP标记的白细胞介素23(IL-23)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的白细胞介素23(IL-23)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中人白细胞介素23(IL-23)浓度。
试剂盒组成:试剂盒组成48孔配置96孔配置保存说明书1份1份封板膜2片(48)2片(96)密封袋1个1个酶标包被板1×481×962-8℃保存标准品:450ng/L0.5ml×1瓶0.5ml×1瓶2-8℃保存标准品稀释液 1.5ml×1瓶 1.5ml×1瓶2-8℃保存酶标试剂3ml×1瓶6ml×1瓶2-8℃保存样品稀释液3ml×1瓶6ml×1瓶2-8℃保存显色剂A液3ml×1瓶6ml×1瓶2-8℃保存显色剂B液3ml×1瓶6ml×1瓶2-8℃保存终止液3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存样本处理及要求:1.血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
人IFN-γ检测试剂盒ELISA法说明书
人IFN-γ检测试剂盒(ELISA法)说明书【产品名称】人IFN-γ检测试剂盒(ELISA法)【包装规格】96 T/盒【预期用途】本试剂仅供科研使用,不适合用于临床检测。
用于测定人血清、人血浆、细胞上清液及相关液体样本中IFN-γ的含量。
【IFN-γ简介】20世纪30年代,许多病毒学家在研究两种病毒感染同一宿主细胞时,发现普遍存在两种病毒相互拮抗的现象,由此产生了病毒间干扰现象的概念。
1957年发现细胞与病毒一起培养后能产生一种可溶性因子,该因子能“干扰”病毒感染新的细胞,此因子被称为“干扰素”。
此后证明干扰素(interferon,IFN)是由一族分泌蛋白质组成,对同种病毒具有广谱抗病毒活性,它存在于各种脊椎动物体内,平时细胞内含量很低,经病毒或其它干扰素诱导剂诱导后产量可以提高。
IFN蛋白家族基于它们的基因序列、染色体定位和受体特异性分为3型,即I型、II型和III型干扰素。
I型包括IFN-α、β、ω、ε、κ、δ、τ、ζ等;II型干扰素由单基因家族IFN-γ构成,又称为免疫干扰素;III型干扰素是一种新发现的细胞因子,与I型干扰素关系密切,称为IFN-λ。
γ-干扰素主要是由抗原、有丝分裂素等刺激、活化的CD4+Th1、CD8+T细胞及NK细胞所分泌的一类可溶性糖蛋白。
抗原、T细胞促分裂素(PHA、ConA)、细胞因子(IL-2、IL-12、IL-18、bFGF、PDGF、EGF)、葡萄球菌肠毒素B,均会诱导γ-干扰素的合成。
【检验原理】人IFN-γ检测试剂盒的检验原理是双抗体夹心ELISA(酶联免疫吸附试验)法,预先用抗人IFN-γ捕获抗体包被微孔板,加样时,标准品或样本和检测抗体(HRP标记的抗人IFN-γ抗体)同时加入微孔板中,人IFN-γ上的2个抗原决定簇分别与捕获抗体和检测抗体结合,形成“捕获抗体-人IFN-γ-检测抗体”的免疫复合物而附着在酶标板上,游离的成分则通过洗涤过程被除去。
人白细胞介素27 (IL-27)说明书
人白细胞介素27 (IL-27)酶联免疫分析(ELISA)试剂盒使用说明书本试剂仅供研究使用目的:本试剂盒用于测定人血清,血浆,组织及相关液体样本中白细胞介素27 (IL-27)的含量。
实验原理:本试剂盒应用夹心法测定标本中白细胞介素27 (IL-27)水平。
用纯化的人白细胞介素27 (IL-27)抗体包被微孔板,往微孔中依次加入白细胞介素27 (IL-27),再与HRP标记的白细胞介素27 (IL-27)抗体结合,形成免疫复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP 酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的白细胞介素27 (IL-27)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中白细胞介素27 (IL-27)浓度。
试剂盒组成:样本处理及要求:1. 血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
2. 血浆:应根据标本的要求选择EDTA或柠檬酸钠作为抗凝剂,混合10-20分钟后,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应该再次离心。
3. 尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应再次离心。
胸腹水、脑脊液参照实行。
4. 细胞培养上清:检测分泌性的成份时,用无菌管收集。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
检测细胞内的成份时,用PBS(PH7.2-7.4)稀释细胞悬液,细胞浓度达到100万/ml左右。
通过反复冻融,以使细胞破坏并放出细胞内成份。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
保存过程中如有沉淀形成,应再次离心。
5. 组织标本:切割标本后,称取重量。
加入一定量的PBS,PH7.4。
用液氮迅速冷冻保存备用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
552592
Eotaxin
555175
GM-CSF
555126
IFN-γ
555142
IL-1β Set II
557953
IL-2
555190
IL-2 sRα
559104
IL-3
558979
IL-4
555194
IL-5
555202
IL-6
555220
IL-8
555244
IL-10
555157
IL-12 p40
Unless otherwise specified, all products are for Research Use Only. Not for use in diagnostic or therapeutic procedures. Not for resale.
US Orders: 877.232.8995
Cat. No. 550499 550947 557965 550612 557966 550611 550614 550799 550999 550613 551116 559258 559017 550610
Mouse IFN-γ Kit II IL-6 Kit TNF Kit II
558258 550950 559732
Limit of Detection. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 12 Recovery. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 12 Linearity. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 12 Specificity. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13 Precision. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13 Intra-assay. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13 Inter-assay. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13 Standardization. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 13 Experimental Results . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14 Serum . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14 Plasma. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14 Cell Culture Supernatant. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14 Troubleshooting. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 14 References . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 15 Plate Templates . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 16
555171
IL-12 p70
555183
IL-15
559268
IP-10
550926
LT-α (TNF-β)
550995
MCP-1
555179
BD OptEIA ELISA Sets continued
Human
Cat. No.
MIG
550998
sFAS
555224
sICAM-1
551424
TGF-β1 TNF
Table of Contents
Introduction. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5 Principle of the Test. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5 Reagents Provided. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 6 Materials Required but not Provided. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 6 Storage Information. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 6 Warnings and Precautions. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 7 Specimen Collection and Handling . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 7 Reagent Preparation. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 8 Assay Procedure. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9 Assay Procedure Summary. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 10 Calculation of Results . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 10 Typical Data. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 11 Limitations of the Procedure. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 11 Performance. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 12
TNF (Mono/Poly)
555167 555138 551866 555248 552576 550347 559603 555148 555228 555232 555236 555240 555252 555165 555256 555260 555268
558874
Rat IFN-γ IL-4 IL-6 IL-10 MCP-1 TNF
BD OptEIA™
Human IL-8 ELISA Kit II
Instruction Manual
Cat. No. 550999
BD flow cytometers are class I (1) laser products © 2007 Becton, Dickinson and Company. All rights reserved. No part of this publication may be reproduced, transmitted, transcribed, stored in retrieval systems, or translated into any language or computer language, in any form or by any means: electronic, mechanical, magnetic, optical, chemical, manual, or otherwise, without prior written permission from BD Biosciences. For research use only. Not for use in diagnostic or therapeutic procedures. Purchase does not include or carry any right to resell or transfer this product either as a stand-alone product or as a component of another product. Any use of this product other than the permitted use without the express written authorization of Becton Dickinson and Company is strictly prohibited. BD, BD Logo and all other trademarks are property of Becton, Dickinson and Company. © 2007 BD
