2019年高考化学基础课程(江苏版)课后练习 第53讲 物质的检验与鉴别
2019年高考化学基础课程(江苏版)课后练习 第48讲 氨基酸、蛋白质和核酸
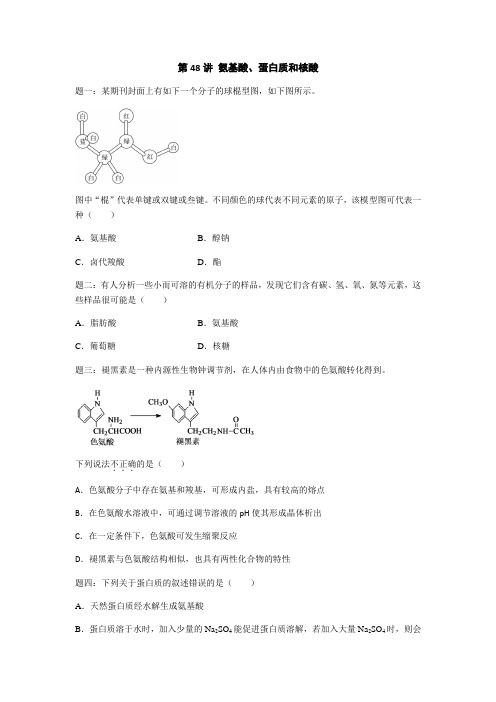
第48讲氨基酸、蛋白质和核酸题一:某期刊封面上有如下一个分子的球棍型图,如下图所示。
图中“棍”代表单键或双键或叁键。
不同颜色的球代表不同元素的原子,该模型图可代表一种()A.氨基酸B.醇钠C.卤代羧酸D.酯题二:有人分析一些小而可溶的有机分子的样品,发现它们含有碳、氢、氧、氮等元素,这些样品很可能是()A.脂肪酸B.氨基酸C.葡萄糖D.核糖题三:褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到。
下列说法不正确...的是()A.色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点B.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出C.在一定条件下,色氨酸可发生缩聚反应D.褪黑素与色氨酸结构相似,也具有两性化合物的特性题四:下列关于蛋白质的叙述错误的是()A.天然蛋白质经水解生成氨基酸B.蛋白质溶于水时,加入少量的Na2SO4能促进蛋白质溶解,若加入大量Na2SO4时,则会使蛋白质溶解度降低C.蛋白质溶液中加入甲醛可以使蛋白质从溶液中析出,加水又溶解D.酶是一种蛋白质题五:下列叙述正确的是()A.酶具有很强的催化作用,胃蛋白酶只能催化蛋白质的水解,348 K时活性更强B.医疗上的血液透析利用了胶体的性质,而土壤保肥与胶体的性质无关C.银制品久置干燥空气中因电化学腐蚀使表面变暗D.C60是由60个碳原子构成的形似足球的分子,结构对称,稳定性好题六:下图是某有机物分子中C、H、O、N四种原子的成键方式示意图。
下列关于该有机物的说法正确的是()A.在一定条件下,可以通过聚合反应生成高分子化合物B.分子式为C3H7NO2C.不能和盐酸溶液反应D.不能和NaHCO3溶液反应生成CO2题七:2004年诺贝尔化学奖授予两名以色列科学家和一名美国科学家。
他们突破性地发现人类细胞如何控制某种蛋白质的过程,具体地说,人类细胞对无用蛋白质的“废物处理”就是对其进行降解的过程,也可认为蛋白质发生了()A.酯化反应B.水解反应C.加聚反应D.缩聚反应题八:2004年度诺贝尔化学奖授予以色列Aaron Ciechanover和Avram Hershko以及美国的Irwin Rose三名科学家。
高考化学真题2019江苏

高考化学真题2019江苏
2019年江苏高考化学试题
2019年江苏高考化学试题近期发布,备受广大考生关注。
下面将为大家详细介绍这份试题的内容及相关知识点,希望能对大家的学习有所帮助。
一、单选题
1. 下列金属中是k字符号的元素是()
A. 镁
B. 铁
C. 铝
D. 铅
答案:B
2. 不能从光谱中得到的信息是()
A. 光的颜色
B. 物质的成分
C. 光的波长
D. 光的振动方向
答案:B
3. 已知两种气体A、B,A气体熔点高于B气体,如何判断A,B 的分子量?()
A. A气体的分子量大
B. A气体的分子量小
C. B气体的分子量大
D. B气体的分子量小
答案:A
二、填空题
1. 一物质的分子4g,含有1g的元素X,X的相对原子质量是()。
答案:32
2. 空气中氮气和氧气的质量比约为()。
答案:7:3
3. 在锌与二氧化碳气体通电生成碳酸锌的实验中,辅助电解的氧气来源于()。
答案:水
三、简答题
1. 请解释一下阴极和阳极的概念。
答:阴极是电子流向的电极,是电池、电解池中原子、离子还电子形成原子或离子的部分。
阳极是电子从原子或离子脱离的电极,一般法向电极。
2. 什么是化学计量?
答:分子中化学计量简称为配数。
是分子中元素的相互华丽比共同的比例,是裂解合一个化学本领所需要的多种基础、最根本的不妙基础。
本文为您介绍了2019年江苏高考化学试题,通过对试题内容的解析,相信对大家学习化学知识有所帮助。
祝愿大家取得优异的成绩,实现自己的理想和目标!。
2019年高考化学基础课程(江苏版)课后练习 第33讲 Al及其重要化合物

第33讲Al及其重要化合物题一:把铝粉和氧化亚铁粉配成铝热剂,分成两等份,一份在高温下恰好完全反应后,再与足量盐酸反应,另一份直接放入足量的烧碱溶液中充分反应;前后两种情况下生成的气体质量比是()A.3∶2 B.2∶3C.1∶1 D.28∶9题二:将等物质的量的镁和铝相混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是()A.3mol/LHCl B.4mol/LHNO3C.8mol/LNaOH D.18mol/LH2SO4题三:含有M金属(不超过0.5g)的铁5.6g,与足量稀硫酸反应,得到氢气0.23g,则金属M 可能是()A.Mg B.Al C.Zn D.Cu题四:等体积等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5∶6,则甲、乙两烧杯中的反应情况可能分别是()A.甲、乙中都是铝过量B.甲中铝过量、乙中碱过量C.甲中酸过量、乙中铝过量D.甲中酸过量、乙中碱过量题五:下列有关金属铝及其化合物的叙述正确的是()A.铝在常温下不能与氧气反应B.铝不能与氯气反应C.铝既能溶于酸,又能溶于碱D.氧化铝只能与酸反应,不能与碱反应题六:有关Al与少量NaOH溶液的反应的说法中,正确的是()A.铝是还原剂,其氧化产物是Al(OH)3B.NaOH是氧化剂,其还原产物是H2C.铝是还原剂,H2O和NaOH都是氧化剂D.H2O是氧化剂,Al被氧化题七:有氧化镁、氧化铝粉末18.2g将它溶于500mL4mol/L的盐酸里,若要使沉淀的质量达到最大值,则需加入2mol/L的氢氧化钠溶液的体积为()A.1000mL B.500mL C.100mL D.1500mL题八:甲、乙两烧杯中各盛有100mL3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为()A.5.4g B.3.6g C.2.7g D.1.6g题九:下列各组离子在溶液中可以大量共存,且加入氨水后也不产生沉淀的是()A.Na+ Ba2+ Cl- SO42-B.K+ AlO2- NO3- OH-C.H+ NH4+ Al3+ SO42-D.H+ Cl- CH3COO- NO3-题十:在前一种分散系中慢慢滴加后一种试剂,能观察到先生成沉淀后变澄清的是()①氯化铝溶液中滴加氢氧化钠溶液②偏铝酸钠溶液中加盐酸③氢氧化钠溶液中滴加氯化铝溶液④氯化铝溶液中滴加氨水⑤硝酸银溶液中滴加氨水⑥氢氧化铁胶体中滴加硫酸A.①②⑤⑥B.②③④⑥C.①②④⑤D.③④⑤⑥。
2019年高考化学基础课程(江苏版)课后练习 第31讲 金属的化学性质

第31讲金属的化学性质题一:金属钠分别在过量的O2和Cl2中燃烧,产生的现象相同点是()A.都产生白烟B.都产生黄色火焰C.都发光发热D.都生成白色固体题二:在烧杯中加水和苯(密度:0.88 g/cm3)各50 mL。
将一小粒金属钠(密度:0.97g/cm3)投入烧杯中。
观察到的现象可能是()。
A.钠在水层中反应并四处游动B.钠停留在苯层中不发生反应C.钠在苯的液面上反应并四处游动D.钠在苯与水的界面处反应并可能上、下跳动题三:铝分别与足量的稀盐酸和足量氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH的物质的量之比为()A.1∶1B.2∶1C.3∶1D.1∶3题四:把一质量为2.3 g的钠用一铝箔(上面用针刺有许多小孔)包好,放入到足量水中,理论上可收集到氢气(标准状况下)()A.1.12 L B.2.24 LC.略大于1.12 L D.略小于1.12 L题五:将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是()A.表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠B.“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液C.最后变成碳酸钠粉末D.该过程的所有化学反应均为氧化还原反应题六:有一块表面被氧化成氧化钠的金属钠,质量是10.8 g。
将它投入到100 g水中完全反应后,收集到0.2 g氢气(已知Na2O+H2O===2NaOH),试计算:未被氧化的金属钠的质量是多少克?题七:若1.8 g某金属跟足量盐酸充分反应,放出2.24 L(标准状况)氢气,则该金属是()A.Al B.Mg C.Fe D.Zn题八:将11.5 g钠、9 g铝、28 g铁分别投入200 mL 1 mol/L的盐酸中,下列分析结果正确的是()A.钠与盐酸反应最剧烈,产生的气体最多B.铝与盐酸反应的速率仅次于钠,但产生的气体最多C.铁与盐酸反应产生的气体比钠多D.反应结束时产生的气体一样多题九:有人设计了如图所示的实验装置。
2019年高考化学基础课程(江苏版)课后练习 第9讲 原子结构

第9讲原子结构题一:在化学变化过程中,原子中的下列粒子数可能发生改变的是()A.质子数B.中子数C.质量数D.电子数题二:某课外兴趣小组通过实验发现钾和钠的性质相似,下列说法中能最好地解释这个事实的是()A.都是金属元素B.原子半径相差不大C.最外层电子数相同D.最高化合价相同题三:已知元素的原子序数,可以推断元素原子的()①质子数②核电荷数③核外电子数④离子所带电荷数A.①③B.②③C.①②③D.②③④题四:决定核素种类的是()A.质子数B.中子数C.原子的最外层电子数D.质子数和中子数Rn),从而对人体产生伤害。
请回答:题五:据报道,某些花岗岩会产生放射性的氡(22286(1)该原子的质量数是________,质子数是________,中子数是________。
(2)请将以下Rn的原子结构示意图补全。
(3)请根据Rn的原子结构预测氡气的化学性质:A.非常活泼,容易与氧气等非金属单质反应B .比较活泼,能与钠等金属反应C .不太活泼,与氮气性质相似D .很难与其他物质发生反应你选择________选项,理由是________________________________________。
题六: 下列关于指定粒子构成的几种描述中,不正确的是( )A .37Cl 与39K 具有相同的中子数B .第114号元素的一种核素298114X 与207 82Pb 具有相同的最外层电子数C .H 3O +与OH -具有相同的质子数和电子数D .O 2-2与S 2-具有相同的质子数和电子数 题七: 已知X 元素的某种同位素的氯化物XCl n 为离子化合物,在该化合物中X 元素的微粒的核内中子数为m ,核外电子数为y ,则该同位素的符号是( )A .m y XB .y +m y XC .m +y +n y +n XD .y +m -n y +n X题八: 按要求填空:(1)A Z X 原子的中子数:N =________。
2019年高考化学基础课程江苏版课后练习 第33讲 Al及其

第33讲Al及其重要化合物题一:把铝粉和氧化亚铁粉配成铝热剂,分成两等份,一份在高温下恰好完全反应后,再与足量盐酸反应,另一份直接放入足量的烧碱溶液中充分反应;前后两种情况下生成的气体质量比是()A.3∶2 B.2∶3C.1∶1 D.28∶9题二:将等物质的量的镁和铝相混合,取等质量该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是()A.3mol/LHCl B.4mol/LHNO3C.8mol/LNaOH D.18mol/LH2SO4题三:含有M金属(不超过0.5g)的铁5.6g,与足量稀硫酸反应,得到氢气0.23g,则金属M 可能是()A.MgB.Al C.Zn D.Cu题四:等体积等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5∶6,则甲、乙两烧杯中的反应情况可能分别是()A.甲、乙中都是铝过量B.甲中铝过量、乙中碱过量C.甲中酸过量、乙中铝过量D.甲中酸过量、乙中碱过量题五:下列有关金属铝及其化合物的叙述正确的是()A.铝在常温下不能与氧气反应B.铝不能与氯气反应C.铝既能溶于酸,又能溶于碱D.氧化铝只能与酸反应,不能与碱反应题六:有关Al与少量NaOH溶液的反应的说法中,正确的是()A.铝是还原剂,其氧化产物是Al(OH)3B.NaOH是氧化剂,其还原产物是H2C.铝是还原剂,H2O和NaOH都是氧化剂D.H2O是氧化剂,Al被氧化题七:有氧化镁、氧化铝粉末18.2g将它溶于500mL4mol/L的盐酸里,若要使沉淀的质量达到最大值,则需加入2mol/L的氢氧化钠溶液的体积为()A.1000mL B.500mL C.100mL D.1500mL题八:甲、乙两烧杯中各盛有100mL3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为()A.5.4g B.3.6g C.2.7g D.1.6g题九:下列各组离子在溶液中可以大量共存,且加入氨水后也不产生沉淀的是()A.Na+ Ba2+ Cl- SO42-B.K+ AlO2- NO3- OH-C.H+ NH4+ Al3+ SO42-D.H+ Cl- CH3COO- NO3-题十:在前一种分散系中慢慢滴加后一种试剂,能观察到先生成沉淀后变澄清的是()①氯化铝溶液中滴加氢氧化钠溶液②偏铝酸钠溶液中加盐酸③氢氧化钠溶液中滴加氯化铝溶液④氯化铝溶液中滴加氨水⑤硝酸银溶液中滴加氨水⑥氢氧化铁胶体中滴加硫酸A.①②⑤⑥B.②③④⑥C.①②④⑤D.③④⑤⑥。
2019年江苏卷化学高考真题(原卷 答案)
绝密★启用前2019年普通高等学校招生全国统一考试(江苏卷)化 学本试卷共21题,共120分。
考试结束后,将本试卷和答题卡一并交回。
注意事项:1.答题前,考生先将自己的姓名、准考证号码填写清楚,将条形码准确粘贴在条形码区域内。
2.答题时请按要求用笔。
3.请按照题号顺序在答题卡各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试卷上答题无效。
4.作图可先使用铅笔画出,确定后必须用黑色字迹的签字笔描黑。
5.保持卡面清洁,不要折叠、不要弄破、弄皱,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量: H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35. 5 K 39 Ca 40 Cr 52 Fe 56 Cu 64 Ag 108 I 127选 择 题单项选择题:本题包括10 小题,每小题2 分,共计20 分。
每小题只有一个....选项符合题意。
1.糖类是人体所需的重要营养物质。
淀粉分子中不含的元素是 A .氢 B .碳 C .氮 D .氧 2.反应NH 4Cl+NaNO 2NaCl+N 2↑+2H 2O 放热且产生气体,可用于冬天石油开采。
下列表示反应中相关微粒的化学用语正确的是 A .中子数为18的氯原子:1817Cl B .N 2的结构式:N=NC .Na +的结构示意图:D .H 2O 的电子式:3.下列有关物质的性质与用途具有对应关系的是 A .NH 4HCO 3受热易分解,可用作化肥 B .稀硫酸具有酸性,可用于除去铁锈 C .SO 2具有氧化性,可用于纸浆漂白 D .Al 2O 3具有两性,可用于电解冶炼铝4.室温下,下列各组离子在指定溶液中能大量共存的是 A .0.1 mol·L −1NaOH 溶液:Na +、K +、23CO −、2AlO −B .0.1 mol·L −1FeCl 2溶液:K +、Mg 2+、24SO −、4MnO −C .0.1 mol·L −1K 2CO 3溶液:Na +、Ba 2+、Cl −、OH −D .0.1 mol·L −1H 2SO 4溶液:K +、4NH +、3NO −、3HSO −5.下列实验操作能达到实验目的的是A .用经水湿润的pH 试纸测量溶液的pHB .将4.0 g NaOH 固体置于100 mL 容量瓶中,加水至刻度,配制1.000 mol·L −1NaOH 溶液C .用装置甲蒸干AlCl 3溶液制无水AlCl 3固体D .用装置乙除去实验室所制乙烯中的少量SO 2 6.下列有关化学反应的叙述正确的是 A .Fe 在稀硝酸中发生钝化 B .MnO 2和稀盐酸反应制取Cl 2 C .SO 2与过量氨水反应生成(NH 4)2SO 3 D .室温下Na 与空气中O 2反应制取Na 2O 2 7.下列指定反应的离子方程式正确的是A .室温下用稀NaOH 溶液吸收Cl 2:Cl 2+2OH −ClO −+Cl −+H 2OB .用铝粉和NaOH 溶液反应制取少量H 2:Al+2OH −2AlO −+H 2↑ C .室温下用稀HNO 3溶解铜:Cu+23NO −+2H +Cu 2++2NO 2↑+H 2OD .向Na 2SiO 3溶液中滴加稀盐酸:Na 2SiO 3+2H +H 2SiO 3↓+2Na +8.短周期主族元素X 、Y 、Z 、W 的原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层有2个电子,Z 的单质晶体是应用最广泛的半导体材料,W 与X 位于同一主族。
2019年江苏省高考化学试卷解析版
2019年江苏省高考化学试卷解析版参考答案与试题解析一、单项选择题:本题包括10小题,每小题2分,共计20分。
每小题只有一个选项符合题意1.(2分)糖类是人体所需的重要营养物质。
淀粉分子中不含的元素是( )A .氢B .碳C .氮D .氧【考点】45:分子式;K3:淀粉的性质和用途.【分析】淀粉属于多糖,属于烃的含氧衍生物,含有C 、H 、O 元素,据此分析解答。
【解答】解:糖类物质属于烃的含氧衍生物,都含有C 、H 、O 元素,淀粉属于多糖,所以含有C 、H 、O 元素,但不含N 元素;蛋白质中含有C 、H 、O 、N 元素,部分蛋白质还含有S 、P 等元素,故选:C 。
【点评】本题考查淀粉中元素判断,属于基础题,明确人类所需营养物质中所含元素是解本题关键,注意基础知识的归纳总结,题目难度不大。
2.(2分)反应NH 4Cl+NaNO 2═NaCl+N 2↑+2H 2O 放热且产生气体,可用于冬天石油开采。
下列表示反应中相关微粒的化学用语正确的是( )A .中子数为18的氯原子:Cl1817B .N 2的结构式:N ═NC .Na +的结构示意图:D .H 2O 的电子式: 【考点】4J :电子式、化学式或化学符号及名称的综合.【分析】A .质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;B .氮气分子中含有的是氮氮三键;C .钠离子的核外电子总数为10,最外层达到8电子稳定结构;D .水分子为共价化合物,含有2个O ﹣H 键。
【解答】解:A .中子数为18的氯原子的质量数为18+17=35,该氯原子正确的表示方法为1735Cl,故A错误;B.分子中含有1个氮氮三键,其正确的结构式为N≡N,故B错误;C.为钠原子结构示意图,钠离子最外层含有8个电子,其离子结构示意图为,故C错误;D.水分子属于共价化合物,其电子式为,故D正确;故选:D。
【点评】本题考查常见化学用语的表示方法,题目难度不大,涉及电子式、原子结构示意图和离子结构示意图、结构式等知识,明确常见化学用语的书写原则即可解答,试题侧重考查学生的规范答题能力。
2019年高考江苏卷化学真题试题(Word版,含答案与解析)
2019年高考化学真题试卷(江苏卷)原卷+解析一、单选题1.(2019•江苏)糖类是人体所需的重要营养物质。
淀粉分子中不含的元素是()A. 氢B. 碳C. 氮D. 氧【答案】 C【考点】淀粉的性质和用途【解析】【解答】淀粉的化学式为(C6H10O5)n,故淀粉中含有碳元素、氢元素和氧元素,不含有氮元素,C符合题意;故答案为:C【分析】根据淀粉的化学式确定淀粉中所含和不含的元素。
2.(2019•江苏)反应NH4Cl+NaNO2=NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。
下列表示反应中相关微粒的化学用语正确的是()A. 中子数为18的氯原子:B. N2的结构式:N=NC. Na+的结构示意图:D. H2O的电子式:【答案】 D【考点】原子中的数量关系,电子式、化学式或化学符号及名称的综合【解析】【解答】A、中子数为18的氯原子,其质量数=质子数+中子数=17+18=35,因此该原子的表示方法为:, A不符合题意;B、N2的结构式为N≡N,B不符合题意;C、Na的最外层电子数为11,失去一个电子后形成Na+,其离子结构示意图为, C不符合题意;D、H2O中存在两个氢氧共价键,其电子式为, D符合题意;故答案为:D【分析】A、标在元素符号左上角的数字表示的是质量数,质量数=质子数+中子数;B、N2分子中存在N≡N;C、Na+是在Na原子的基础上失去最外层一个电子形成的;D、H2O中存在着氢氧共价键;3.(2019•江苏)下列有关物质的性质与用途具有对应关系的是()A. NH4HCO3受热易分解,可用作化肥B. 稀硫酸具有酸性,可用于除去铁锈C. SO2具有氧化性,可用于纸浆漂白D. Al2O3具有两性,可用于电解冶炼铝【答案】 B【考点】镁、铝的重要化合物,化肥、农药及其合理利用,二氧化硫的漂白作用【解析】【解答】A、NH4HCO3中含有氮元素,可作氮肥,做氮肥与其受热易分解的性质无关,A不符合题意;B、铁锈的主要成分是Fe2O3,属于金属氧化物,金属氧化物能与酸反应,二者具有对应关系,B 符合题意;C、SO2漂白纸浆的过程,是与纸浆中的有色物质发生化合反应形成无色物质,过程中没有涉及氧化还原反应,不体现SO2的氧化性,该过程体现了SO2的漂白性,C不符合题意;D、Al2O3具有两性,既能与强酸溶液反应,也能与强碱溶液反应,该性质与电解冶炼铝的用途无关,D不符合题意;故答案为:B【分析】A、受热易分解与做化肥无关;B、金属氧化物能与酸反应;C、SO2漂白纸浆体现了SO2的漂白性;D、Al2O3具有两性,既能与强酸溶液反应,也能与强碱溶液反应;4.(2019•江苏)室温下,下列各组离子在指定溶液中能大量共存的是()A. 0.1 mol·L−1NaOH溶液:Na+、K+、、B. 0.1 mol·L−1FeCl2溶液:K+、Mg2+、、C. 0.1 mol·L−1K2CO3溶液:Na+、Ba2+、Cl−、OH−D. 0.1 mol·L−1H2SO4溶液:K+、、、【答案】 A【考点】离子共存问题【解析】【解答】A、溶液中各离子相互间不形成难溶物(或微溶物)、不形成弱电解质、不形成易挥发性物质、不发生络合反应和氧化还原反应,可大量共存,A符合题意;B、溶液中的MnO4-具有氧化性,Fe2+具有还原性,二者可发生氧化还原反应,不可大量共存,B不符合题意;C、溶液中的Ba2+能与CO32-形成BaCO3沉淀,不可大量共存,C不符合题意;D、溶液中NO3-在酸性条件下具有氧化性,能将HSO3-氧化成SO42-,同时H+能与HSO3-反应生成SO2和H2O,不可大量共存,D不符合题意;故答案为:A【分析】A、溶液中各离子相互间不发生反应;B、MnO4-具有氧化性,可将Fe2+氧化;C、Ba2+能与CO32-形成BaCO3沉淀;D、H+能与HSO3-反应形成SO2和H2O,NO3-在酸性条件下具有氧化性;5.(2019•江苏)下列实验操作能达到实验目的的是()A. 用经水湿润的pH试纸测量溶液的pHB. 将4.0 g NaOH固体置于100 mL容量瓶中,加水至刻度,配制1.000 mol·L−1NaOH溶液C. 用装置甲蒸干AlCl3溶液制无水AlCl3固体D. 用装置乙除去实验室所制乙烯中的少量SO2【答案】 D【考点】配制一定溶质质量分数、物质的量浓度溶液的方法,溶液酸碱性的判断及相关计算,二氧化硫的性质,蒸发和结晶、重结晶【解析】【解答】A、测溶液的pH值时,应用干燥洁净的玻璃棒蘸取待测液滴在pH试纸上,显色后与标准比色卡对照,得出溶液的pH值;若pH试纸润湿,则相当于对溶液进行了稀释操作,对于酸性溶液,会使得结果偏大,对于碱性溶液,会的结果偏小,对于中性溶液,则无影响,A不符合题意;B、配制一定物质的量浓度的溶液时,应先将固体在烧杯中溶解,恢复至室温后,再转移到容量瓶中,不可在容量瓶内进行溶解操作,B不符合题意;C、AlCl3在水中易水解,产生Al(OH)3和具有挥发性的HCl,直接加热蒸发AlCl3溶液,最终得到的是Al(OH)3,欲得到AlCl3晶体,应在HCl气流中加热蒸发,以抑制AlCl3的水解,C不符合题意;D、SO2能与NaOH溶液反应,乙烯不能,故将混合气体通过NaOH溶液,可除去乙烯中混有的SO2,D符合题意;故答案为:D【分析】A、根据测溶液pH的实验操作分析;B、不能在容量瓶内进行溶解;C、AlCl3在水中易水解,产生Al(OH)3和具有挥发性的HCl;D、SO2能与NaOH溶液反应,乙烯不能;6.(2019•江苏)下列有关化学反应的叙述正确的是()A. Fe在稀硝酸中发生钝化B. MnO2和稀盐酸反应制取Cl2C. SO2与过量氨水反应生成(NH4)2SO3D. 室温下Na与空气中O2反应制取Na2O2【答案】 C【考点】氯气的实验室制法,硝酸的化学性质,二氧化硫的性质,钠的化学性质【解析】【解答】A、常温下,浓硝酸能使铁钝化,稀硝酸不能使铁钝化,A不符合题意;B、实验室制取Cl2所用的试剂为MnO2和浓盐酸,MnO2与稀盐酸不反应,B不符合题意;C、氨水过量,则SO2反应,反应生成(NH4)2SO3, C符合题意;D、室温下,Na与空气中的O2反应生成Na2O,在加热条件下,反应生成Na2O2, D不符合题意;故答案为:C【分析】A、常温下,浓硝酸能使铁钝化;B、根据实验室制取Cl2的原理分析;C、氨水过量,则SO2少量,反应生成SO32-;D、室温下, Na与O2反应生成Na2O;7.(2019•江苏)下列指定反应的离子方程式正确的是()A. 室温下用稀NaOH溶液吸收Cl2:Cl2+2OH−=ClO−+Cl−+H2OB. 用铝粉和NaOH溶液反应制取少量H2:Al+2OH−= +H2↑C. 室温下用稀HNO3溶解铜:Cu+2+2H+=Cu2++2NO2↑+H2OD. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+【答案】 A【考点】离子方程式的书写【解析】【解答】A、Cl2与NaOH溶液反应生成NaCl、NaClO和H2O,该反应的离子方程式为:Cl2+2OH−=ClO−+Cl−+H2O,A符合题意;B、Al与NaOH溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,B不符合题意;C、铜与稀硝酸反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,C不符合题意;D、盐酸与Na2SiO3溶液反应的离子方程式为:SiO32-+2H+=H2SiO3↓,D不符合题意;故答案为:A【分析】A、Cl2与NaOH溶液反应生成NaCl、NaClO和H2O;B、不满足电荷守恒;C、左右两边电荷不守恒;D、Na2SiO3是可溶性盐,在离子方程式中可以拆解成离子形式;8.(2019•江苏)短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素,Y 原子的最外层有2个电子,Z的单质晶体是应用最广泛的半导体材料,W与X位于同一主族。
2019年高考化学基础课程(江苏版)课后练习 第23讲 弱电解质的电离
第23讲弱电解质的电离题一:下列物质分类组合正确的是()题二:按照混合物、纯净物、强电解质、弱电解质、非电解质的顺序排列正确的一组是()A.盐酸、氯气、BaSO 4、CO2、SO2B.硫酸、氨水、醋酸、乙醇、NO 2C.漂白粉、胆矾、NH 4Cl、CH3COOH、CO2D.干冰、氯水、HCl、HClO、CO题三:下列溶液中加入少量NaOH固体导电能力变化不大的是()A.盐酸B.CH3COOH C.NH3·H2O D.H2O题四:如图所示的图像是在一定温度下,向不同电解质溶液中加入新物质时溶液的导电性发生变化,其电流强度(I)随加入量(m)的变化曲线。
①向Ba(OH)2溶液中滴入H2SO4溶液至过量②向醋酸溶液中滴入NH3·H2O溶液至过量③向澄清石灰水中通入CO2至过量④向NH4Cl溶液中逐渐加入适量NaOH固体⑤向盐酸中通入适量氨气⑥向氢氧化钠溶液中加入适量冰醋酸其中与A的变化趋势一致的是_______,与B的变化趋势一致的是________,与C的变化趋势一致的是________。
题五:相同体积、相同氢离子浓度的强酸溶液和弱酸溶液分别跟足量的镁完全反应,下列说法正确的是()A.弱酸溶液产生较多的氢气B.强酸溶液产生较多的氢气C.两者产生等量的氢气D.无法比较两者产生氢气的量题六:体积跟浓度都相同的的某一元弱酸溶液①和某一元强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是()题七:在0.1 mol/L CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+对于该平衡,下列叙述正确的是()A.加入水时,平衡向逆反应方向移动B.加入少量NaOH固体,平衡正向移动C.加入少量0.1 mol/L HCl溶液,溶液中c(H+)减小D.加入少量CH3COONa固体,平衡正向移动题八:在100mL0.1mol/L醋酸溶液中加入以下物质中的一种,醋酸溶液pH变小。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第53讲物质的检验与鉴别
题一:对于某些物质的检验及结论正确的是()
A.取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体,说明没有变质
B.淀粉溶液和稀H2SO4混合加热一段时间,冷却后,加入少量新制的Cu(OH)2,再加热至沸腾,无红色沉淀生成,说明淀粉尚未水解
-C.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液中可能有SO2
4
-D.加入氢氧化钙溶液产生白色沉淀,再加盐酸白色沉淀消失,原溶液中一定有CO2
3
题二:下列有关物质检验的实验结论正确的是()
题三:下列依据相关实验得出的结论正确的是()
A.用激光笔照射淀粉溶液和葡萄糖溶液,能产生光亮的“通路”的是淀粉溶液
B.将某气体通入淀粉碘化钾溶液中,溶液变蓝色,该气体一定是Cl2
C.某无色溶液中加入银氨溶液,加热后产生银镜,该溶液中含有醛类物质
-D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO2
3
题四:进行下列实验,由实验现象得出的结论错误的是()
题五:下列与实验操作对应的实验现象、离子方程式都正确的是()
题六:下列与实验操作对应的实验现象、离子方程式都正确的是()
题七:硫代硫酸钠是一种重要的化工产品。
某兴趣小组拟制备硫代硫酸钠晶体
(Na2S2O3·5H2O)。
Ⅰ.【查阅资料】
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3,所得产品常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀盐酸。
Ⅱ.【制备产品】
实验装置如图所示(省略夹持装置):
实验步骤:
(1)检查装置气密性,如图示加入试剂。
仪器a的名称是________;E中的试剂是________(选填下列字母编号)。
A.稀H2SO4
B.NaOH溶液
C.饱和NaHSO3溶液
(2)先向C中烧瓶加入Na2S和Na2CO3的混合溶液,再向A中烧瓶滴加浓H2SO4。
(3)待Na2S和Na2CO3完全消耗后,结束反应。
过滤C中的混合物,滤液经________(填写操作名称)、结晶、过滤、洗涤、干燥、得到产品。
Ⅲ.【探究与反思】
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。
(所需试剂从稀HNO3、稀H2SO4、稀盐酸、蒸馏水中选择)取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_______________
_________________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤进行了改进,改进后的操作是_________________________。
题八:三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。
某校一化学实验小组通过实验来探究红色粉末是Fe2O3、Cu2O或二者混合物。
探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN 试液。
(1)若假设1成立,则实验现象是__________。
(2)若滴加KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。
你认为这种说法合理吗?__________,简述你的理由(不需写出反应的方程
式)__________________。
(3)若固体粉末完全溶解无固体存在,滴加KSCN 试液时,溶液不变红色,则证明原固体粉末是__________,写出发生反应的离子方程式:
_____________________________________。
题九:从下列事实所得出的相应结论肯定正确的是()
题十:下列实验的现象与对应结论均正确的是()
题十一:下述实验能达到预期目的的是()
题十二:下列实验操作不能达到预期实验目的的是()。
