进口兽药质量标准
中国与美国、日本、欧盟和国际食品法典委员会关于禽类产品中兽药最大残留限量标准的对比
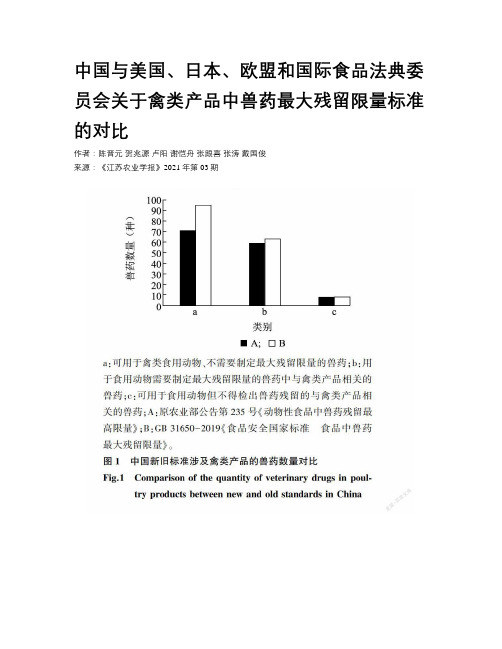
中国与美国、日本、欧盟和国际食品法典委员会关于禽类产品中兽药最大残留限量标准的对比作者:陈晋元贺兆源卢阳谢恺舟张跟喜张涛戴国俊来源:《江苏农业学报》2021年第03期摘要:旨在對中国关于禽类产品中兽药最大残留限量的新旧标准进行对比并将新标准与美国、日本等发达国家以及国际组织关于禽类产品中兽药最大残留限量标准进行对比。
结果表明,中国禽类产品中兽药的最大残留限量新标准与旧标准相比,内容上已经更为完善,与国外的差距逐渐缩小。
通过对比研究发现了中国标准的不足之处,并提出相关建议,以期为进一步完善中国禽类产品中兽药的最大残留限量标准提供参考。
关键词:兽药;最大残留限量标准;禽类产品中图分类号: S859.84 文献标识码: A 文章编号: 1000-4440(2021)03-0754-09Comparison of the standards about the maximum residue limit of veterinary drugs in poultry products between China and USA, Japan, European Union and Codex Alimentarius CommissionCHEN Jin-yuan1,2, HE Zhao-yuan1,2, LU Yang1,2, XIE Kai-zhou1,2, ZHANG Gen-xi1,2, ZHANG Tao1,2,DAI Guo-jun1,2(1.College of Animal Science and Technology, Yangzhou University, Yangzhou 225009,China;2.Joint International Research Laboratory of Agriculture & Agri-Product Safety, Ministry of Education, Yangzhou 225009, China)Abstract: The aim of this study is to compare the old and new domestic standards about the maximum residue limit of veterinary drugs in poultry products, and to compare the maximum veterinary drug residue limit in poultry products between the new standard and the standards of the United States, Japan and other developed countries and international organizations. The results showed that, the content of the Chinese new standard about the maximum residue limit of veterinary drugs in poultry products was improved compared with the old standard, and the gap between Chinese new standard and foreign standards gradually narrowed. Deficiencies of the domestic standard were found through comparative study, and relevant suggestions were proposed to providereference for further improvement of the domestic standard about the maximum residue limit of veterinary drugs in poultry products.Key words: veterinary drug;maximum residue limits (MRLs) standard;poultry products兽药的使用会使畜禽产品中存在兽药原形及其代谢产物的残留,而食用含有残留兽药的畜禽产品会产生许多不良影响,危害人们的身体健康[1-4],如引起体内菌群失调、胃肠道感染[5]、过敏反应和变态反应等[6-8],并能产生致癌、致畸、致突变等作用[9-14]。
兽药GMP新验收评定标准

作出“不推荐”结论 ≥1
﹥15%
主要变化
一、在上版?标准?根底上,新?标准?对文字作 了 进一步标准。
二、新?标准?对厂房设施等硬件方面的条款进展了 调整,增加了管理方面的条款,突出了对管理方 面的检查。
三、对一个条款中涉及多项内容的,进展拆分,尽 量使每一条款只涉及一个方面的内容。
四、对内容明显重复的条款进展了合并。根据?标准? 增加了局部条款。结合实际工作需要增加了对人 员现场考核的要求。
• 企业应制定年度的人员培训方案,明确培训的要 求、方式和内容,并应根据实际情况调整培训内 容。
• 增加了并应根据实际情况调整培训内容。
机构与人员章节增加了以下条款:
• 013 人员的现场考核结果应符合要求 • 014 企业负责人应承受有关法律法规培训,提高
法律意识和质量意识。
015
• 703:从事高生物活性、高毒性等有特殊要求的生 产、检验人员,应经相应专业的技术培训和生产 平安防护培训。
• 生产中涉及易燃、易爆、强腐蚀物品时应设置相 应的危险品仓库。毒、易制毒、麻、精神药品应 按国家有关规定保存。
• 增加为关键项,增加为“易制毒〞
*077
• *3301:生产企业应具备与所生产产品相适应的生 产和检验设备;主要生产和检验设备的技术参数、 性能应能够满足生产、检验的需要。
• 生产企业应具备与所生产产品相适应的生产和检 验设备。
五、对涉及生产管理、质量管理内容的条款,进展 了拆分、细化,到达提高权重、加强日常管理的 目的。
新老条款的比照
• 新条款有142条是在老条款的根底上变动 • 新条款有13条涉及老条款的合并 • 新条款有25条涉及老条款的拆分 • 新条款有12条新增条款
兽药GMP检查验收评定标准(新)232条

兽药GMP检查验收评定标准(新)232条兽药GMP检查验收评定标准(化药、中药等)1、根据《兽药生产质量管理规范》(以下简称兽药GMP)及其附录,制定兽药GMP检查验收评定标准。
2、兽药GMP检查验收项目共232项,其中关键项目(条款号前加“*”)65项,一般项目167项。
检查项目分布状况(关键项/检查项):机构与人员6/17;厂房与设施11/59;设备5/23;物料11/24;卫生1/19;验证7/12;文件3/10;生产管理12/36;质量管理6/20;产品销售与收回1/6;投诉与不良反应报告1/3;自检1/3。
3、兽药GMP检查验收应以申请验收范围确定相应的检查项目。
现场检查时,应对所列项目及其涵盖内容进行全面检查,并逐项作出评定。
4、评定方式:评定结果分为“N”、“Yˉ”和“Y”三档。
凡某项得分在75分以上的,判定为符合要求,评定结果标为“Y”;凡某项得分在50-75分之间的,判定为基本符合要求,评定结果标为“Yˉ”;凡某项得分在50分以下,判定为不符合要求,评定结果标为“N”。
5、通过分别计算关键项目不符合项数、关键项目基本符合项数和一般项目不符合率作出最终评定结论,并在验收报告中用文字说明。
2序号章节条款内容结果*001机构与人企业应建立生产和质量管理机构,各类机构设置应合理,岗位的职责应明确。
002管理人员和技术人员的专业知识和生产经验及人员数量应与生产相适应。
00 3 企业主管生产和质量管理的负责人应具有兽医、药学等相关专业大专以上学历,并具有兽药生产和质量管理经验。
* 004 兽药生产管理部门的负责人和质量管理部门的负责人应具有兽医、药学等相关专业大专以上学历,有生产、质量管理经验。
含中药制剂生产企业,生产3员管理和质量管理的负责人应具有中医药专业学历或经过中药专业知识的培训。
*005生产管理和质量管理部门负责人应由专职人员担任,并不得互相兼职。
006直接从事生产人员应具有高中以上文化程度并经本岗位技术培训。
30项兽药GSP质量管理制度

兰坪群兴牧业公司兽药经营组织机构设置图 (2)兰坪群兴牧业公司兽药经营企业质量管理机构职能图 (3)兽药经营质量方针、目标和承诺 (4)兽药经营质量管理制度 (5)兽药GSP质量责任制度 (8)首营企业与首营品种审核管理制度 (9)兽药采购管理制度 (11)兽药验收管理制度 (12)兽药质量验收、养护、外观质量检查项目 (14)兽药入库管理制度 (15)兽药陈列管理制度 (16)兽药储存与养护制度 (17)兽药运输管理制度 (19)兽药销售管理制度 (20)兽药出库检查管理制度 (21)环境及人员卫生管理制度 (23)兽药不良反应报告制度 (24)退回与不合格兽药管理制度 (26)兽药质量事故、质量投诉管理制度 (27)兽药经营记录、资料档案管理制度 (29)质量管理培训、考核管理制度 (30)总经理岗位职责 (31)质量管理负责人岗位职责 (32)兽药仓库管理人员岗位职责 (34)兽药销售人员岗位职责 (35)兽医处方审核岗位职责 (36)兽药质量检查验收程序 (37)兽药养护程序 (39)不合格兽药控制程序 (41)兽药拆零销售程序 (43)1兽药经营组织机构设置图2兽药经营企业质量管理机构职能图3兽药经营质量方针、目标和承诺1.目的:强化全员质量意识,提高兽药经营质量管理水平2.适用范围:公司全体员工3.责任人:公司全体员工4.内容:本公司坚持“质量第一”的原则,全面贯彻落实《兽药管理条例》、《兽药经营质量管理规范》、《云南省兽药经营质量管理规范实施细则》等法律法规,加强基础管理,完善各项质量管理制度,确保各项质量管理制度的有效实施,强化全员的质量意识,提高员工素质,不断提高兽药经营质量管理水平。
企业质量管理方针为:“管理规范、品质保证、服务周到、信誉优良”。
企业质量目标如下:①确保企业经营行为的规范性、合法性;②确保所经营兽药质量的安全有效;③确保质量管理体系的有效运行及持续改进;④不断提升公司的质量信誉及品牌效益;⑤最大限度地满足客户的需求。
兽药生产质量管理规定(3篇)

兽药生产质量管理规定是指对于兽药生产过程中的各个环节,从原料采购到成品装箱,都需要严格遵守的管理规定,以确保兽药产品的质量安全。
以下是一般性的兽药生产质量管理规定的主要内容:1. 原料采购:兽药生产企业应从合法、可靠的渠道采购原料,严格按照国家相关标准进行检验,并有相应的采购记录。
2. 原材料质量控制:兽药生产企业应对采购的原料进行质量控制,包括对原料进行鉴定、检验和评价,并建立相应的质量档案。
3. 生产设备和场所管理:兽药生产企业应严格管理生产设备和生产场所,确保设备的完好无损、洁净卫生,并定期进行维护和清洁。
4. 生产工艺控制:兽药生产企业应建立科学合理的生产工艺流程,明确工艺参数和操作要求,并进行严格的记录和控制。
5. 中间和成品质量控制:兽药生产企业应对生产过程中的中间产物和成品进行质量控制,包括进行检验、评价和记录,确保产品的质量符合标准要求。
6. 储存和运输管理:兽药生产企业应建立合适的储存和运输管理制度,对成品进行妥善保管,确保产品质量不受损失。
7. 质量管理体系:兽药生产企业应建立完善的质量管理体系,包括制定相应的质量管理制度、培训员工的质量意识和技能,进行内部审核和不断的改进。
8. 不良事件报告和处理:兽药生产企业应建立不良事件的报告和处理制度,对发生的不良事件进行及时报告,并采取相应的纠正和预防措施。
以上是兽药生产质量管理规定的一些主要内容,具体要求可能根据不同国家和地区的法规和标准而有所差异。
兽药生产企业需根据实际情况制定相应的质量管理制度,并确保其有效实施。
兽药生产质量管理规定(2)兽药是用于预防和治疗动物疾病的药物。
兽药的生产质量管理是确保兽药安全性和有效性的重要环节。
为了保障兽药的质量,相关的国家和地区都制定了严格的兽药生产质量管理规定。
本文将对兽药生产质量管理规定进行详细介绍。
一、兽药生产许可证要求兽药生产企业在申请兽药生产许可证时,必须符合一定的要求。
首先,企业必须具备一定的技术和人员条件。
创制中兽药的质量标准

创制中兽药的质量标准创制中兽药的质量标准涉及多个方面,包括但不限于以下内容:1.安全性标准:中兽药的安全性是兽药质量控制的首要考虑因素之一。
安全性标准包括对毒性、副作用、残留物等进行评价,确保中兽药使用不会对动物的健康和环境造成不良影响。
2.有效性标准:中兽药的有效性是其质量标准的重要组成部分。
有效性标准包括对药效、治疗速度、治愈率等指标进行评价,以确保中兽药能够有效地治疗动物的疾病,提高动物的健康水平。
3.稳定性标准:中兽药的稳定性对其质量具有重要影响。
稳定性标准包括对中兽药的化学成分、物理性质、微生物指标等进行检测和评价,以确保中兽药在存储和使用过程中不会发生变质或降低其有效性。
4.原料药标准:原料药是中兽药的主要成分之一,其质量直接影响到中兽药的质量。
原料药标准包括对原料药的来源、质量、纯度、安全性等方面进行严格控制,以确保原料药的质量符合要求。
5.生产工艺标准:生产工艺是影响中兽药质量的另一个重要因素。
生产工艺标准包括对生产过程中的各个环节进行严格控制,确保生产工艺的稳定性和可靠性,以保证中兽药的质量和有效性。
6.包装标准:中兽药的包装对其质量也有重要影响。
包装标准包括对包装材料的质量、安全性、环保性等方面进行控制,以确保中兽药的包装符合要求,能够保证中兽药的储存和使用安全有效。
7.贮存和运输标准:中兽药的贮存和运输过程中也需要进行严格控制。
贮存和运输标准包括对中兽药的贮存环境、运输方式、温度和湿度等进行控制,以确保中兽药的储存和使用安全有效。
总之,创制中兽药的质量标准是一个全面而复杂的过程,需要从多个方面进行控制和管理。
只有符合质量标准的中兽药才能够保证其安全性和有效性,从而为动物的健康提供有力保障。
绿色食品 兽药使用准则
绿色食品兽药使用准则1、范围。
本标准规定了绿色食品生产中兽药使用的术语和定义、基本原则、生产AA级和A级绿色食品的兽药使用原则。
本标准适用于绿色食品畜禽及其产品的生产与管理。
2、规范性引用文件。
下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 19630.1 有机产品第1部分:生产NY/T 391 绿色食品产地环境质量中华人民共和国动物防疫法兽药管理条例畜禽标识和养殖档案管理办法中华人民共和国农业部中华人民共和国兽药典中华人民共和国农业部兽药质量标准中华人民共和国农业部兽用生物制品质量标准中华人民共和国农业部进口兽药质量标准中华人民共和国农业部公告第235号动物性食品中兽药最高残留限量中华人民共和国农业部公告第278号兽药停药期规定3、术语和定义。
下列术语和定义适用于本文件。
3.1 AA级绿色食品。
产地环境质量符合NY/T 391的要求, 遵照绿色食品生产标准生产,生产过程中遵循自然规律和生态学原理,协调种植业和养殖业的平衡,不使用化学合成的肥料、农药、兽药、渔药、添加剂等物质,产品质量符合绿色食品产品标准,经专门机构许可使用绿色食品标志的产品。
3.2 A级绿色食品。
产地环境质量符合NY/T 391的要求, 遵照绿色食品生产标准生产,生产过程中遵循自然规律和生态学原理,协调种植业和养殖业的平衡,限量使用限定的化学合成生产资料,产品质量符合绿色食品产品标准,经专门机构许可使用绿色食品标志的产品。
3.3 兽药。
用于预防、治疗、诊断动物疾病,或者有目的地调节动物生理机能的物质。
包括化学药品、抗生素、中药材、中成药、生化药品、血清制品、疫苗、诊断制品、微生态制剂、放射性药品、外用杀虫剂和消毒剂等。
3.4 微生态制剂。
运用微生态学原理,利用对宿主有益的微生物及其代谢产物,经特殊工艺将一种或多种微生物制成的制剂。
兽药生产质量管理规范
物料管理要求
兽药生产所需物料应符合质量标准,有检验报告或合格证明文件。 物料应按照规定的贮存条件进行储存,确保物料质量稳定。 物料应按照生产计划和需求进行发放,并做好记录。 生产过程中应对物料进行监控,确保物料使用符合规定。
生产过程管理要求
兽药生产应严格执行 生产工艺规程,并按 照工艺规程的先后顺 序进行生产操作。
推进兽药生产技术创新和升级,提高生产效率和产品质量。
提升方向
完善生产流程:优化兽药生产过程中的各个环节,确保生产过程的规范化和高效化。
加强质量监管:建立健全兽药质量管理体系,加强质量检验和监控,确保兽药产品质量安全可靠。
提高人员素质:加强员工培训和教育,提高员工的专业技能和素质水平,确保生产过程中的操作规范和质量控制。
兽药生产质量管理规范
目录
兽药生产质量管理规范概述 兽药生产质量管理规范要求 兽药生产质量管理规范实施 兽药生产质量管理规范监督与检查 兽药生产质量管理规范改进与提升
定义和目的
定义:兽药生产质量管理规范是指导兽药生产和质量管理的法规,确 保兽药的安全、有效和质量的可控性。
目的:规范兽药生产过程,确保兽药的安全、有效和质量可控,保障 动物健康和公共卫生安全。
添加标题
添加标题
文件资料检查:对兽药生产企业的 相关文件、记录、报告等进行审查 和核实。
投诉处理:对消费者和相关部门的 投诉进行调查和处理,以确保兽药 产品的安全性和有效性。
改进措施
完善兽药生产质量管理体系,加强生产过程控制和监督。
加强兽药生产人员的培训和管理,提高生产人员的素质和技能水平。
建立兽药生产质量信息反馈机制,及时收集和分析生产过程中出现的质量问题, 采取有效措施进行改进。
兽药GMP检查验收评定标准
兽药GMP检查验收评定标准(生物制品)
一、兽药GMP检查验收评定标准说明
(一)本标准根据《兽药生产质量管理规范》(以下简称兽药GMP)及其附录制定。
(二)兽药GMP检查验收项目共224项,其中关键项目(条款号前加“*”)25项,一般项目199项。
检查项目分布状况(关键项/检查项):机构与人员3/14;厂房与设施7/62;设备1/22;物料5/25;卫生0/16;验证1/14;文件1/14;生产管理2/20;质量管理3/21;产品销售与收回1/6;投诉与不良反应报告0/4;自检1/6。
(三)在组织兽药GMP检查验收时,须根据申请验收的范围,按照兽药GMP检查验收项目确定相应的检查项目,并进行全面检查和评定。
(四)现场检查中发现不符合要求的项目统称为“缺陷项目”。
其中,关键项目不符合要求者称为“严重缺陷”,一般项目不符合要求者称为“一般缺陷”。
(五)在检查过程中,企业隐瞒有关情况或提供虚假材料的,按严重缺陷处理。
检查验收组应调查取证并详细记录。
(六)结果评定1.未发现严重缺陷,且一般缺陷≤20%的,现场做出“推荐”结论。
2.发现严重缺陷或一般缺陷>20%的,现场做出“不推荐”结论。
农业部公告第2513号――《兽药质量标准》(2017年版)
农业部公告第2513号――《兽药质量标准》(2017年版)
【法规类别】兽医兽药
【发文字号】农业部公告第2513号
【发布部门】农业部
【发布日期】2017.04.07
【实施日期】2017.11.01
【时效性】现行有效
【效力级别】部门规范性文件
农业部公告
(第2513号)
为加强兽药国家标准管理,我部对2010年12月31日前发布的、未列入《中国兽药典》(2015年版)的兽药质量标准进行了修订,编纂为《兽药质量标准》(2017年版),并制定了配套的说明书范本,现予发布,自2017年11月1日起施行。
现就有关事宜公告如下。
一、《兽药质量标准》(2017年版)包括化学药品卷、中药卷和生物制品卷等三个部分。
二、自2017年11月1日起,除《中国兽药典》(2015年版)和《兽药质量标准》(2017年版)收载品种的兽药质量标准外,2010年12月31日前(含31日)各版《中
国兽药典》《兽药国家标准》《兽用生物制品质量标准》《兽用生物制品规程》以及农业部公告发布的同品种兽药质量标准同时废止。
凡《兽药质量标准》(2017年版)品种项下未收载的制剂规格(已明令废止的除外),其质量标准按《兽药质量标准》(2017年版)同品种相关要求执行,规格项按原批准证明文件执行。
三、自2017年11月1日起,申报《兽药质量标准》(20。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
进口兽药质量标准
来源:作者:加入时间:2004-12-20 14:15:35 阅读次数:823
第一部分化学药品
1.三氯苯唑
2.三氯苯唑混悬液
3.马杜霉素铵预混剂
4.牛至油溶液
5.牛至油预混剂
6.长效土霉素注射液
7.长效盐酸土霉素注射液
8.双甲脒溶液
9.双甲脒项圈
10.北里霉素
11.北里霉素预混剂
12.戊二醛溶液
13.右旋糖酐铁注射液
14.甲基吡啶磷
15.甲基吡啶磷可湿性粉10
16.甲基吡啶磷可湿性粉50
17.甲基吡啶磷颗粒诱饵
18.甲基盐霉素预混剂
19.甲基盐霉素、尼卡巴嗪预混剂
20.尼卡巴嗪预混剂
21.尼卡巴嗪、乙氧酰胺苯甲酯预混剂
22.头孢氨苄混悬液
23.亚甲基水杨酸杆菌肽可溶性粉
24.地克珠利预混剂
25.伊维菌素注射液
26.伊维菌素预混剂
27.妥曲珠利溶液
28.杆菌肽锌
29.杆菌肽锌预混剂
30.杆菌肽锌、硫酸粘杆菌素预混剂
31.呋喃苯烯酸钠
32.呋喃苯烯酸钠粉
33.邻氯青霉素、氨苄青霉素乳剂(停乳期)
34.邻氯青霉素、氨苄青霉素乳剂(泌乳期)
35.延胡索酸泰妙菌素
36.延胡索酸泰妙菌素可溶性粉
37.延胡索酸泰妙菌素预混剂
38.辛硫磷浇泼溶液
39.环丙氨嗪
40.环丙氨嗪可溶性粉
41.环丙氨嗪可溶性颗粒
42.环丙氨嗪预混剂(l%)
43.环丙氨嗪预混剂(10%)
44.拉沙洛西钠
45.拉沙洛西钠预混剂(15%)
46.拉沙洛西钠预混剂(45%)
47.注射用头孢噻呋钠
48.氢溴酸常山酮预混剂
49.氟甲喹可溶性粉
50.氟苯咪唑
51.氟苯咪唑预混剂
52.氟氯苯氰菊酯条
53.氟胺氰菊酯条
54.癸甲溴铵溶液
55.复方二甲硝咪唑可溶性粉
56.复方布他磷注射液
57.复方促性腺激素释放激素类似物注射液58.复方盐酸氨丙啉可溶性粉
59.复方氯羟吡啶粉
60.复方氯羟吡啶预混剂
61.复方黄体酮缓释圈
62.复方硝基酸钠预混剂
63.复方煤焦油酸溶液
64.复方磺胺氯哒嗪钠粉
65.复方磺胺喹恶啉钠可溶性粉
66.复方磺胺嘧啶预混剂
67.复方磺胺嘧啶混悬液
68.复合碘溶液
69.盐酸壮观霉素可溶性粉
70.盐酸林可霉素(饲料级)
71.盐酸林可霉素可溶性粉
72.盐酸林可霉素预混剂
73.盐酸林可霉素、硫酸壮观霉素可溶性粉74.盐酸林可霉素、硫酸壮观霉素预混剂75.盐酸氨丙啉可溶性粉
76.盐酸氨丙啉、乙氧酰胺苯甲酯预混剂
77.盐霉素钠
78.盐霉素钠预混剂(l06)
79.氨苄青霉素可溶性粉
80.氨苄青霉素钠注射液
81.氨基丁三醇前列腺素F2α注射液82.恩拉霉素(饲料级)
83.恩拉霉素预混剂
84.恩诺沙星溶液
85.恩诺沙星注射液
86.莫能菌素预混剂
87.酒石酸北里霉素可溶性粉
88.酒石酸泰乐菌素
89.酒石酸泰乐菌素可溶性粉
90.泰乐菌素注射液
91.诺氟沙星溶液
92.烟酸诺氟沙星
93.烟酸诺氟沙星注射液
94.黄霉素预混剂
95.越霉素A预混剂
96.曼泰普林溶液
97.维吉尼亚霉素
98.维吉尼亚霉素预混剂
99.硫氰酸红霉素可溶性粉
100.硫酸壮观霉素
101.硫酸阿普拉霉素预混剂
102.硫酸阿普拉霉素可溶性粉
103.硫酸粘杆菌素
104.硫酸粘杆菌素(饲料级Ⅰ)
105.硫酸粘杆菌素(饲料级Ⅱ)106.硫酸粘杆菌素可溶性粉
107.硫酸粘杆菌素预混剂
108.硫酸新霉素(饲料级)109.硫酸新霉素可溶性粉(IM)110.硫酸新霉素预混剂111.硫酸新霉素、甲溴东莨菪碱溶液112.硝碘酚腈注射液
113.氯化氮氨菲啶盐酸盐
114.氯芬新片Ⅱ(151
115.氯芬新片Ⅲ
116.氯芬新片Ⅳ
117.氯芬新混悬液
118.氯氰碘柳胺钠
119.氯氰碘柳胺钠片
120.氯氰碘柳胺钠注射液
121.氯氰碘柳胺钠混悬液
122.恶喹酸
123.恶喹酸散
124.恶喹酸混悬液
125.恶喹酸溶液
126.碘酸混合液
127.溴氰菊酯溶液(169
128.溴酚磷
129.溴酚磷片
130.溴酚磷粉
131.溴螨酯纸条
132.稳定化二嗪农
133.二嗪农溶液250
134.二嗪农溶液600
135.二嗪农项圈
136.赛杜霉素预混剂
137.赛地卡霉素
138.赛地卡霉素预混剂
139.醋酸促性腺激素释放激素注射液
140.潮霉素B预混剂
141.磺胺间甲氧嘧啶
142.磺胺间甲氧嘧啶钠
143.磺胺氯吡嗪钠可溶性粉
144.磷酸泰乐菌素预混剂
145.磷酸泰乐菌素、磺胺二甲嘧啶预混剂
146.露它净溶液
第二部分生物制品
一般检验
1.物理性状检验
2.无菌检验或纯粹检验
3.杂菌计数和病原性鉴定
4.支原体污染检验
5.禽用活疫苗外源病毒检验
灭活疫苗
6.鸡新城疫灭活疫苗
7.鸡传染性法氏囊病灭活疫苗
8.鸡减蛋综合征灭活疫苗
9.鸡病毒性关节炎灭活疫苗
10.鸡新城疫-传染性支气管炎二联灭活疫苗
11.鸡新城疫-传染性法氏囊病二联灭活疫苗
12.鸡新城疫-减蛋综合征二联灭活疫苗
13.鸡新城疫-支气管炎-法氏囊炎三联灭活疫苗
14.鸡新城疫-支气管炎-减蛋综合征三联灭活疫苗
15.鸡新城疫-法氏囊炎-减蛋综合征三联灭活疫苗16.鸡新城疫-支气管炎-法氏囊炎-病毒性关节炎四联灭活疫苗17.鸡传染性鼻炎A型灭活疫苗
18.鸡传染性鼻炎A型、C型二价灭活疫苗19.鸡传染性鼻炎A型、B型、C型三价灭活疫苗20.禽多杀性巴氏杆菌病灭活疫苗
21.狂犬病灭活疫苗
活疫苗
22.鸡新城疫低毒力株活疫苗
23.鸡马立克氏病活疫苗
24.鸡马立克氏病火鸡疱疹病毒活疫苗25.鸡马立克氏病(Ⅱ型、Ⅲ型)双价活疫苗26.鸡传染性支气管炎活疫苗
27.鸡传染性法氏囊病活疫苗
28.鸡传染性喉气管炎活疫苗
29.鸡病毒性关节炎活疫苗
30.禽痘活疫苗
31.禽脑脊髓炎活疫苗
32.禽脑脊髓炎-禽痘二联活疫苗33.鸡新城疫-传染性支气管炎二联活疫苗34.鸡毒支原体活疫苗(TS-11株)。
